HIT เฉียบพลัน
จำนวนเกล็ดเลือด: ต่ำ
การทดสอบการทำงาน (SRA): บวก
การตรวจทางภูมิคุ้มกัน (ELISA): บวก
ช่วงที่มีความเสี่ยงสูงที่สุด หยุดเฮปารินทั้งหมดทันทีและเปลี่ยนไปใช้ยาต้านการแข็งตัวของเลือดที่ไม่ใช่เฮปาริน

ภาวะเกล็ดเลือดต่ำจากการใช้เฮปาริน (Heparin-Induced Thrombocytopenia; HIT) เป็นปฏิกิริยาที่เกิดจากภูมิคุ้มกันต่อการให้เฮปาริน มีการสร้างแอนติบอดี IgG ต่อสารเชิงซ้อนของปัจจัยเกล็ดเลือดที่ 4 (PF4) และเฮปาริน ซึ่งกระตุ้นการทำงานของเกล็ดเลือด ส่งผลให้จำนวนเกล็ดเลือดลดลงอย่างขัดแย้งในขณะที่เลือดมีภาวะแข็งตัวมากเกินไป
HIT แบ่งเป็นชนิดที่ 1 และ 2 HIT ชนิดที่ 1 เป็นภาวะเกล็ดเลือดต่ำชั่วคราวที่หายได้เอง HIT ชนิดที่ 2 เป็นภาวะที่เกิดจากแอนติบอดี ร่วมกับภาวะแทรกซ้อนลิ่มเลือดอุดตันที่รุนแรง 1)
ภาวะแทรกซ้อนทางตาจะเกิดขึ้นเมื่อลิ่มเลือดและเลือดออกที่เกี่ยวข้องกับ HIT ส่งผลต่อระบบหลอดเลือดของตา จำเป็นต้องจัดการทางตาควบคู่ไปกับการจัดการ HIT ทั่วร่างกาย
ในผู้ป่วยที่ได้รับ UFH อุบัติการณ์สูงถึง 5% ในผู้ป่วยที่ได้รับ LMWH ประมาณ 1 ใน 10 ของนั้น หลังการผ่าตัดหัวใจ อุบัติการณ์ 0.1–3% สูงกว่าประชากรทั่วไป และอัตราการเสียชีวิตสูงถึง 10% 2)
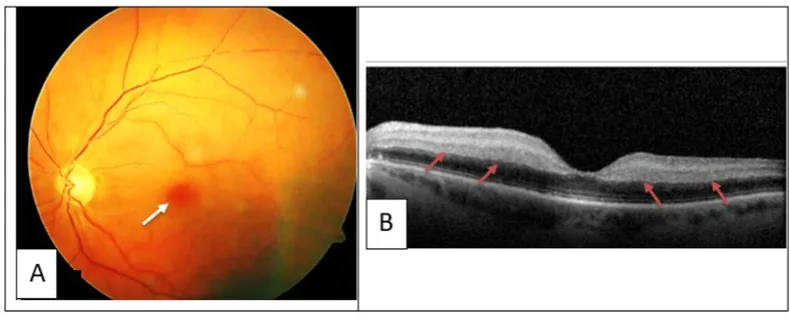
อาการทางตาขึ้นอยู่กับตำแหน่งที่เกิดลิ่มเลือดหรือเลือดออก
สาเหตุของ HIT คือปฏิกิริยาทางภูมิคุ้มกันต่อการให้เฮปาริน ปัจจัยเสี่ยงหลักได้แก่:
HIT สามารถเกิดขึ้นได้กับ LMWH เช่นกัน แต่อุบัติการณ์ต่ำกว่าประมาณ 1/10 เมื่อเทียบกับ UFH การตรวจติดตามเกล็ดเลือดไม่สามารถละเว้นได้เพียงเพราะความเสี่ยงต่ำ
HIT เป็นการวินิจฉัยแบบแยกออก (exclusion diagnosis) สงสัยเมื่อมีลิ่มเลือดอุดตันและเกล็ดเลือดต่ำภายใน 5-14 วันหลังให้เฮปาริน หลังจากแยกสาเหตุอื่นออกแล้ว
คะแนน 4T เป็นคะแนนความน่าจะเป็นทางคลินิกที่ประกอบด้วยเกณฑ์สี่ข้อ (Thrombocytopenia, Timing, Thrombosis, oTher causes) แต่ละเกณฑ์ให้คะแนน 0-2 คะแนนรวมจำแนกความน่าจะเป็น
| คะแนนรวม | การจำแนกความน่าจะเป็น |
|---|---|
| 6-8 คะแนน | ความน่าจะเป็นสูง |
| 4–5 คะแนน | ปานกลาง |
| 0–3 คะแนน | ความน่าจะเป็นต่ำ |
ค่าทำนายผลบวกของคะแนน 4T คือประมาณ 10% สำหรับคะแนนปานกลาง 4 คะแนน และประมาณ 80% สำหรับคะแนนสูง 8 คะแนน 4)
ในผู้ป่วยผ่าตัดหัวใจ จำนวนเกล็ดเลือดมักลดลง 30–50% หลัง CPB และหากพบรูปแบบสองเฟส (การลดลงของเกล็ดเลือดแบบสองเฟส) ถือเป็นลักษณะเฉพาะของ HIT 3)1)}
การตรวจหาแอนติบอดีต่อ PF4/เฮปาริน (anti-PF4 ELISA) และการทดสอบการปลดปล่อยเซโรโทนิน (SRA) เป็นวิธีการตรวจวินิจฉัยหลัก
แนวทางของ ASH แนะนำให้ตรวจ anti-PF4 ELISA ในผู้ป่วยที่มีคะแนน 4T ระดับปานกลางขึ้นไป และหากผลเป็นบวก ให้ยืนยันด้วย SRA 2)
มีรายงานกรณีที่พบความแตกต่างที่หาได้ยากซึ่งผล anti-PF4 ELISA เป็นลบแต่ SRA เป็นบวก (16 รายจาก 8,546 ราย คิดเป็น 0.2%) หากสงสัยทางคลินิกอย่างมากว่าเป็น HIT ควรให้ความสนใจกับความแตกต่างของผลการตรวจ 2)
กลยุทธ์การจัดการ HIT แตกต่างกันไปตามระยะ 3)
HIT เฉียบพลัน
จำนวนเกล็ดเลือด: ต่ำ
การทดสอบการทำงาน (SRA): บวก
การตรวจทางภูมิคุ้มกัน (ELISA): บวก
ช่วงที่มีความเสี่ยงสูงที่สุด หยุดเฮปารินทั้งหมดทันทีและเปลี่ยนไปใช้ยาต้านการแข็งตัวของเลือดที่ไม่ใช่เฮปาริน
HIT กึ่งเฉียบพลัน A
จำนวนเกล็ดเลือด: ปกติ
การตรวจการทำงาน (SRA): บวก
การตรวจทางภูมิคุ้มกัน (ELISA): บวก
จำนวนเกล็ดเลือดกลับมาเป็นปกติแล้ว แต่การตรวจการทำงานยังให้ผลบวก ควรเลื่อนการผ่าตัดหัวใจหากเป็นไปได้
HIT กึ่งเฉียบพลัน B
จำนวนเกล็ดเลือด: ปกติ
การตรวจการทำงาน (SRA): ลบ (เปลี่ยนเป็นลบที่ค่ามัธยฐาน 50 วัน)
การตรวจทางภูมิคุ้มกัน (ELISA): บวก
การสัมผัสเฮปารินระยะสั้นระหว่างผ่าตัดมีความเสี่ยงต่ำ หลีกเลี่ยงเฮปารินต่อหลังผ่าตัด
HIT ระยะไกล
จำนวนเกล็ดเลือด: ปกติ
การตรวจการทำงาน (SRA): ผลลบ
การตรวจทางภูมิคุ้มกัน (ELISA): ผลลบ (แอนติบอดี PF4/H หายไปในค่ามัธยฐาน 85 วัน)
ภาวะที่สามารถให้เฮปารินระยะสั้นเมื่อมีการสัมผัสซ้ำได้
ในผู้ป่วยที่มีอาการทางตาที่เกิดจาก HIT ควรซักประวัติและตรวจร่างกายอย่างละเอียดเพื่อดูว่ามีอาการทางระบบอื่นๆ ร่วมด้วยหรือไม่
เป็นคะแนนที่ประเมินความน่าจะเป็นทางคลินิกของ HIT โดยใช้เกณฑ์ 4 ข้อ ได้แก่ ระดับของเกล็ดเลือดต่ำ (Thrombocytopenia) ช่วงเวลาที่เกิด (Timing) การมีลิ่มเลือดอุดตัน (Thrombosis) และการแยกสาเหตุอื่น (oTher causes) คะแนนรวม 0–8 คะแนน โดย ≥6 คะแนนถือว่ามีความน่าจะเป็นสูง
เมื่อวินิจฉัยหรือสงสัยอย่างมากว่าเป็น HIT ให้ดำเนินการดังต่อไปนี้ทันที:
อาร์กาทรอแบน
การจัดกลุ่ม: ยายับยั้งทรอมบินโดยตรง
ครึ่งชีวิต: 39–51 นาที (การทำงานของตับปกติ), ขยายถึง 181 นาทีในกรณีตับบกพร่อง
การเผาผลาญ: ขับออกทางตับ มีข้อดีในกรณีไตบกพร่อง
ไบวาลิรูดิน
การจำแนกประเภท: ยายับยั้งทรอมบินโดยตรง
ครึ่งชีวิต: 25 นาที (การทำงานของไตปกติถึงบกพร่องเล็กน้อย)
ขนาดยาสำหรับ PCI: 0.75 มก./กก. โบลัส + 1.75 มก./กก./ชม.
ขนาดยา CPB: 1 มก./กก. โบลัส + 2.5 มก./กก./ชม. (เพิ่ม 50 มก. ในน้ำยาปรับสภาพ) 3)
แนวทางปฏิบัติของ ASH 2018 แนะนำให้ใช้ bivalirudin สำหรับ PCI ใน 52 รายที่ใช้ PCI มีรายงานอัตราความสำเร็จของหัตถการ 98% และภาวะเลือดออกรุนแรง 1.9% 3)
ใน HIT ที่ดื้อต่อการรักษาซึ่งลิ่มเลือดดำเนินไปแม้จะได้รับการรักษาด้วยยาต้านการแข็งตัวของเลือดที่ไม่ใช่เฮปารินอย่างเหมาะสม ให้พิจารณาสิ่งต่อไปนี้ 5)
หากผู้ป่วย HIT ชนิดเฉียบพลัน/กึ่งเฉียบพลัน A จำเป็นต้องผ่าตัดหัวใจ ให้พิจารณาทางเลือกสามทางต่อไปนี้ 3)
การอุดตันของหลอดเลือดจอตาและเลือดออกในเบ้าตาได้รับการจัดการทางจักษุควบคู่ไปกับการจัดการ HIT ทั่วร่างกาย
เปลี่ยนไปใช้ยาที่ยับยั้งทรอมบินโดยตรง เช่น อาร์กาโทรแบน หรือ ไบวาลิรูดิน ยาทั้งสองชนิดยับยั้งทรอมบินโดยตรงด้วยกลไกที่แตกต่างจากเฮปาริน จึงไม่ได้รับผลกระทบจากแอนติบอดีของ HIT การเลือกใช้ยาขึ้นอยู่กับการทำงานของตับ การทำงานของไต และสภาพทางคลินิก
การเกิด HIT ดำเนินไปตามขั้นตอนต่อไปนี้
ขั้นตอนที่ 1: การสร้างสารเชิงซ้อนและการผลิตแอนติบอดี
PF4 (ปัจจัยเกล็ดเลือดที่ 4) เป็นคีโมไคน์ที่มีประจุบวกซึ่งมาจากเมกะคาริโอไซต์ และถูกเก็บไว้ในแกรนูลอัลฟาของเกล็ดเลือด PF4 สร้างสารเชิงซ้อนกับเฮปารานซัลเฟตที่มีประจุลบ (GAG บนผิวเยื่อบุหลอดเลือด) หรือ LPS (เยื่อหุ้มชั้นนอกของแบคทีเรียแกรมลบ) สารเชิงซ้อนเหล่านี้ทำหน้าที่เป็น “สัญญาณอันตราย” ทำให้สามารถผลิตแอนติบอดี IgG ได้อย่างรวดเร็ว
ขั้นตอนที่ 2: การสร้างสารเชิงซ้อน PF4-เฮปาริน
การให้เฮปารินทำให้เกิดสารเชิงซ้อน PF4-เฮปาริน เนื่องจากเฮปารินมีโครงสร้างโมเลกุลคล้ายกับ LPS และเฮปารานซัลเฟต IgG ที่มีอยู่ก่อนจึงจับกัน
ขั้นตอนที่ 3: การกระตุ้นเกล็ดเลือดและการแข็งตัวของเลือดมากเกินไป
สารเชิงซ้อน IgG-PF4-เฮปารินจับกับตัวรับ FcγRII (FcγRIIa) บนเกล็ดเลือด กระตุ้นเกล็ดเลือด วิถีภายในของกระบวนการแข็งตัวของเลือดเริ่มต้นขึ้น ทำให้เกิดลิ่มเลือดอุดตันอย่างกว้างขวางและเกล็ดเลือดต่ำจากการบริโภคเกล็ดเลือดพร้อมกัน นี่คือแก่นแท้ของพยาธิสรีรวิทยา “ที่ขัดแย้ง” ของ HIT
นอกจาก PF4 ทั่วไปแล้ว แอนติบอดีที่กำหนดเป้าหมาย IL-8 โปรตามีน และ NAP-2 ยังตรวจพบได้ในน้อยกว่า 1% ของกรณีที่ตรวจสอบหา HIT 2) นอกจากนี้ แอนติบอดีต่อต้าน PF4 ที่กระตุ้นเกล็ดเลือดในกรณีที่ไม่มีเฮปาริน (แอนติบอดี HIT ที่ไม่ขึ้นกับเฮปาริน) อาจเกี่ยวข้องกับการเกิดโรคของ HIT ที่ดื้อต่อการรักษาและ HIT ภูมิต้านตนเอง 5)
หลัง CPB การเปลี่ยนสภาพซีรั่มของแอนติบอดี PF4/H เกิดขึ้นในผู้ป่วยมากถึง 50% แต่มีเพียง 1-2% เท่านั้นที่พัฒนาเป็น HIT ทางคลินิก 1) การให้ UFH ขนาดสูงระหว่าง CPB การปล่อยปัจจัยเนื้อเยื่อ และการอักเสบ เชื่อว่าส่งเสริมการผลิตแอนติบอดี HIT 3)
การเตรียมจากแอนติบอดีโมโนโคลนอลของหนูชนิด IgG2b ที่ต่อต้าน PF4/H KKO ซึ่งถูกตัดหมู่ไกลโคซิล ยับยั้งการกระตุ้นเกล็ดเลือดและการกระตุ้นคอมพลีเมนต์โดยการปิดกั้นการจับที่อาศัย FcγRIIa
ในแบบจำลองหนู มีรายงานว่าช่วยปรับปรุงภาวะเกล็ดเลือดต่ำและลดขนาดลิ่มเลือด5) ขั้นตอนนี้จำเป็นต้องมีการประเมินในการทดลองทางคลินิกในอนาคต
กำลังมีการศึกษากลยุทธ์การให้เฮปารินซ้ำระหว่างการทำ CPB โดยใช้ยาคังเกรเลอร์ซึ่งเป็นสารยับยั้ง P2Y12
ในการรวบรวมผู้ป่วย 10 ราย ปรับขนาดยาโดยใช้ VerifyNow P2Y12 PRU และไม่มีรายงานภาวะแทรกซ้อนจากลิ่มเลือด5) ยังไม่มีการกำหนดแนวทางปฏิบัติที่ชัดเจน.
แม้ว่าประสิทธิภาพของ TPE จะเป็นที่ยอมรับ แต่ยังไม่มีการกำหนดแนวทางปฏิบัติที่เป็นมาตรฐานเดียวกัน
การทบทวนวรรณกรรมอย่างเป็นระบบ (30 ราย) รายงานค่าเฉลี่ยการทำ TPE 4 ครั้ง ปริมาณการแลกเปลี่ยนพลาสมา 1.3 PV แต่ระดับหลักฐานยังต่ำ จำเป็นต้องมีการศึกษาไปข้างหน้าในอนาคต 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.