HIT aguda
Recuento de plaquetas: Disminuido
Prueba funcional (SRA): Positivo
Inmunoensayo (ELISA): Positivo
Período de mayor riesgo. Suspenda toda heparina inmediatamente y cambie a un anticoagulante no heparínico.

La trombocitopenia inducida por heparina (HIT) es una reacción inmunomediada a la administración de heparina. Se producen anticuerpos IgG contra el complejo del factor 4 plaquetario (PF4) y la heparina, lo que provoca la activación plaquetaria. Esto resulta paradójicamente en una disminución del recuento de plaquetas mientras la sangre se vuelve hipercoagulable.
La HIT se clasifica en tipo I y tipo II. La HIT tipo I es una trombocitopenia transitoria que se resuelve espontáneamente. La HIT tipo II es mediada por anticuerpos y una afección grave con complicaciones tromboembólicas. 1)
Las complicaciones oftálmicas ocurren cuando la trombosis o hemorragia asociada a HIT afecta el sistema vascular ocular. Se requiere manejo oftálmico en paralelo con el manejo sistémico de la HIT.
En pacientes que reciben UFH, la incidencia es de hasta el 5%, y en aquellos que reciben LMWH, es aproximadamente una décima parte de esa cifra. Después de cirugía cardíaca, la incidencia es del 0,1 al 3%, más alta que en la población general, y la tasa de mortalidad puede alcanzar hasta el 10%. 2)
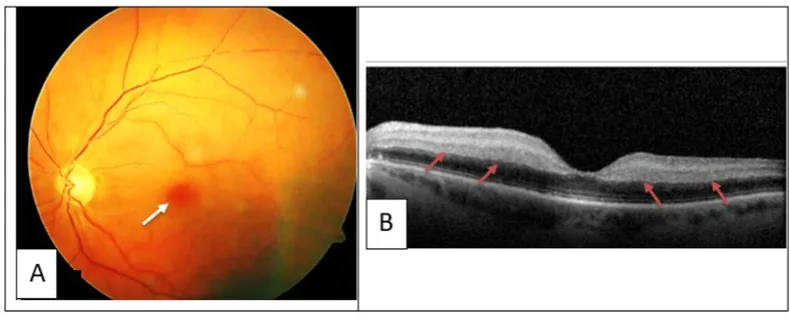
Los síntomas oculares varían según la ubicación de la trombosis o hemorragia.
La causa de la HIT es una reacción inmunomediada a la administración de heparina. Los principales factores de riesgo son los siguientes.
La HIT también puede ocurrir con HBPM, pero la incidencia es aproximadamente 1/10 de la de HNF. Aunque el riesgo es menor, no se puede omitir la monitorización de plaquetas.
La HIT es un diagnóstico de exclusión. Se sospecha cuando se presenta trombosis y trombocitopenia entre 5 y 14 días después de la administración de heparina y se descartan otras causas.
La puntuación 4T es una puntuación de probabilidad clínica que consta de cuatro criterios: Trombocitopenia, Momento, Trombosis y Otras causas. Cada criterio se puntúa de 0 a 2 puntos, y la puntuación total clasifica la probabilidad.
| Puntuación total | Clasificación de probabilidad |
|---|---|
| 6–8 puntos | Alta probabilidad |
| 4–5 puntos | Moderado |
| 0–3 puntos | Baja probabilidad |
El valor predictivo positivo de la puntuación 4T es aproximadamente del 10% para una puntuación moderada de 4 puntos y aproximadamente del 80% para una puntuación de alta probabilidad de 8 puntos. 4)
En pacientes de cirugía cardíaca, el recuento de plaquetas suele disminuir entre un 30 y un 50% después de la CPB, y si se observa un patrón bifásico de trombocitopenia, se considera un hallazgo característico de HIT. 3)1)
Las principales pruebas diagnósticas son la detección de anticuerpos anti-PF4/heparina (ELISA anti-PF4) y la prueba de liberación de serotonina (SRA).
Las guías ASH recomiendan ELISA anti-PF4 para pacientes con puntuación 4T moderada o alta, y si es positivo, confirmar con SRA. 2)
Se han reportado raros casos discordantes de ELISA anti-PF4 negativo y SRA positivo (16 de 8,546 casos, 0.2%); se debe tener precaución cuando se sospecha fuertemente HIT clínicamente. 2)
La estrategia de manejo de HIT difiere según la fase. 3)
HIT aguda
Recuento de plaquetas: Disminuido
Prueba funcional (SRA): Positivo
Inmunoensayo (ELISA): Positivo
Período de mayor riesgo. Suspenda toda heparina inmediatamente y cambie a un anticoagulante no heparínico.
HIT A subaguda
Recuento de plaquetas: Normalizado
Prueba funcional (SRA): Positiva
Inmunoensayo (ELISA): Positivo
El recuento de plaquetas se ha recuperado pero la prueba funcional es positiva. La cirugía cardíaca debe posponerse si es posible.
HIT B subaguda
Recuento de plaquetas: Normal
Prueba funcional (SRA): Negativa (mediana de 50 días para la seroconversión)
Inmunoensayo (ELISA): Positivo
La exposición breve a heparina intraoperatoria es de bajo riesgo. Continuar evitando la heparina después de la cirugía.
HIT remota
Recuento de plaquetas: Normal
Prueba funcional (SRA): Negativa
Inmunoensayo (ELISA): Negativo (los anticuerpos PF4/H desaparecen en una mediana de 85 días)
Es posible la administración de heparina de corta duración durante la reexposición.
En pacientes con síntomas oculares secundarios a HIT, se debe realizar una anamnesis exhaustiva y un examen físico para detectar otros síntomas sistémicos.
Esta puntuación evalúa la probabilidad clínica de HIT basándose en cuatro criterios: grado de trombocitopenia, momento de aparición, presencia de trombosis y exclusión de otras causas. La puntuación total oscila entre 0 y 8, considerándose alta probabilidad una puntuación de 6 o más.
Cuando se diagnostica o se sospecha fuertemente HIT, se deben implementar inmediatamente las siguientes medidas.
Argatrobán
Clasificación: Inhibidor directo de la trombina
Vida media: 39–51 minutos (función hepática normal), hasta 181 minutos con insuficiencia hepática
Metabolismo: Excreción hepática. Ventajoso en pacientes con insuficiencia renal.
Bivalirudina
Clasificación: Inhibidor directo de la trombina
Vida media: 25 minutos (función renal normal a deterioro leve)
Dosis para ICP: 0,75 mg/kg en bolo + 1,75 mg/kg/h
Dosis para CEC: 1 mg/kg en bolo + 2,5 mg/kg/h (añadir 50 mg a la solución de cebado)3)
Las guías ASH 2018 recomiendan bivalirudina para ICP. En 52 casos de uso en ICP, se ha informado una tasa de éxito del procedimiento del 98% y hemorragia mayor del 1,9%.3)
Para la HIT refractaria en la que la trombosis progresa a pesar de la anticoagulación adecuada sin heparina, considere lo siguiente. 5)
Si un paciente con HIT aguda/HIT subaguda A requiere cirugía cardíaca, considere las siguientes tres opciones. 3)
La oclusión vascular retiniana y la hemorragia orbitaria se manejan oftalmológicamente en paralelo con el manejo sistémico de la HIT.
Cambiar a un inhibidor directo de la trombina como argatrobán o bivalirudina. Ambos inhiben directamente la trombina mediante un mecanismo diferente al de la heparina y no se ven afectados por los anticuerpos HIT. La elección del fármaco depende de la función hepática, la función renal y la situación clínica.
El inicio del HIT progresa a través de las siguientes etapas.
Paso 1: Formación de complejos y producción de anticuerpos
El PF4 (factor plaquetario 4) es una quimiocina con carga positiva derivada de los megacariocitos y almacenada en los gránulos alfa de las plaquetas. El PF4 forma complejos con el heparán sulfato con carga negativa (GAG en la superficie endotelial vascular) o con LPS (membrana externa de bacterias gramnegativas). Estos complejos actúan como “señales de peligro” y permiten la producción rápida de anticuerpos IgG.
Paso 2: Formación de complejos PF4-heparina
La administración de heparina conduce a la formación de complejos PF4-heparina. Debido a que la heparina tiene una estructura molecular similar al LPS y al heparán sulfato, la IgG preexistente se une a ella.
Paso 3: Activación plaquetaria e hipercoagulabilidad
El complejo IgG-PF4-heparina se une a los receptores FcγRII (FcγRIIa) en las plaquetas, activándolas. Se inicia la vía intrínseca de la cascada de coagulación, lo que provoca trombosis generalizada y trombocitopenia por consumo de plaquetas. Esta es la esencia de la fisiopatología “paradójica” de la HIT.
Además de la PF4 normal, se detectan anticuerpos dirigidos contra IL-8, protamina y NAP-2 en menos del 1% de los casos de estudio de HIT. 2) Además, los anticuerpos anti-PF4 que activan las plaquetas incluso en ausencia de heparina (anticuerpos HIT independientes de heparina) pueden estar involucrados en la fisiopatología de la HIT refractaria y la HIT autoinmune. 5)
Después de la CPB, hasta el 50% de los pacientes presentan seroconversión de anticuerpos PF4/H, pero solo el 1-2% desarrolla HIT clínica. 1) Se cree que la administración de UFH en dosis altas durante la CPB, la liberación de factor tisular y la inflamación promueven la producción de anticuerpos HIT. 3)
Esta es una formulación desglicosilada del anticuerpo monoclonal de ratón IgG2b anti-PF4/H KKO. Al bloquear la unión mediada por FcγRIIa, suprime la activación plaquetaria y la activación del complemento.
En modelos de ratón, se ha informado que mejora la trombocitopenia y reduce el tamaño del trombo. 5) Esta es una etapa que requiere evaluación en futuros ensayos clínicos.
Se está investigando una estrategia de readministración de heparina durante la CEC utilizando el inhibidor de P2Y12 cangrelor.
En una serie de 10 casos, se ajustó la dosis mediante VerifyNow P2Y12 PRU y no se reportaron complicaciones trombóticas. 5) No se ha establecido un protocolo estandarizado.
Aunque se reconoce la eficacia de la TPE, no se ha establecido un protocolo unificado.
Una revisión sistemática (30 casos) reportó un promedio de 4 sesiones de TPE y un volumen de intercambio plasmático de 1.3 PV, pero el nivel de evidencia es bajo y se necesitan estudios prospectivos futuros. 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.