HIT cấp tính
Số lượng tiểu cầu: Thấp
Xét nghiệm chức năng (SRA): Dương tính
Xét nghiệm miễn dịch (ELISA): Dương tính
Giai đoạn nguy cơ cao nhất. Ngừng ngay lập tức tất cả heparin và chuyển sang thuốc chống đông không phải heparin.

Giảm tiểu cầu do heparin (Heparin-Induced Thrombocytopenia; HIT) là một phản ứng qua trung gian miễn dịch xảy ra khi dùng heparin. Các kháng thể IgG được sản xuất chống lại phức hợp yếu tố tiểu cầu 4 (PF4) và heparin, gây hoạt hóa tiểu cầu. Kết quả là số lượng tiểu cầu giảm một cách nghịch lý trong khi máu trở nên tăng đông.
HIT được phân loại thành type I và type II. HIT type I là giảm tiểu cầu thoáng qua và tự hồi phục. HIT type II là tình trạng qua trung gian kháng thể, kèm theo các biến chứng tắc mạch huyết khối nghiêm trọng. 1)
Biến chứng nhãn khoa xảy ra khi huyết khối và xuất huyết liên quan đến HIT ảnh hưởng đến hệ thống mạch máu của mắt. Cần xử trí nhãn khoa song song với quản lý toàn thân HIT.
Ở bệnh nhân dùng UFH, tỷ lệ mắc lên tới 5%; ở bệnh nhân dùng LMWH, khoảng 1/10 con số đó. Sau phẫu thuật tim, tỷ lệ là 0,1–3%, cao hơn dân số chung, và tỷ lệ tử vong lên tới 10%. 2)
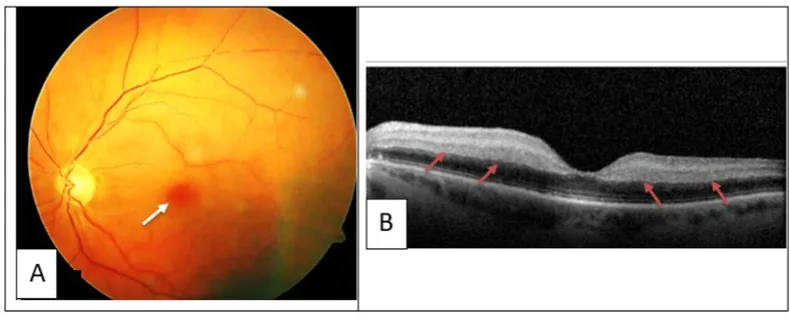
Triệu chứng mắt khác nhau tùy theo vị trí huyết khối hoặc xuất huyết.
Nguyên nhân của HIT là phản ứng qua trung gian miễn dịch đối với việc dùng heparin. Các yếu tố nguy cơ chính bao gồm:
HIT cũng có thể xảy ra với LMWH, nhưng tỷ lệ mắc thấp hơn khoảng 1/10 so với UFH. Không thể bỏ qua việc theo dõi tiểu cầu chỉ vì nguy cơ thấp.
HIT là chẩn đoán loại trừ. Nghi ngờ khi có huyết khối và giảm tiểu cầu từ 5-14 ngày sau khi dùng heparin, sau khi loại trừ các nguyên nhân khác.
Điểm 4T là thang điểm xác suất lâm sàng gồm bốn tiêu chí (Giảm tiểu cầu, Thời điểm, Huyết khối, Nguyên nhân khác). Mỗi tiêu chí được chấm 0-2 điểm, tổng điểm phân loại xác suất.
| Tổng điểm | Phân loại xác suất |
|---|---|
| 6-8 điểm | Xác suất cao |
| 4–5 điểm | Trung bình |
| 0–3 điểm | Xác suất thấp |
Giá trị dự báo dương tính của thang điểm 4T là khoảng 10% đối với điểm trung bình 4 và khoảng 80% đối với điểm cao 8. 4)
Ở bệnh nhân phẫu thuật tim, số lượng tiểu cầu thường giảm 30–50% sau CPB, và nếu thấy mô hình hai pha (giảm tiểu cầu hai pha) thì được coi là dấu hiệu đặc trưng của HIT. 3)1)
Xét nghiệm kháng thể kháng PF4/heparin (ELISA kháng PF4) và xét nghiệm giải phóng serotonin (SRA) là các phương pháp xét nghiệm chính.
Hướng dẫn của ASH khuyến nghị xét nghiệm anti-PF4 ELISA cho bệnh nhân có điểm 4T từ trung bình trở lên, nếu dương tính thì xác nhận bằng SRA. 2)
Các trường hợp hiếm gặp có sự khác biệt giữa kết quả anti-PF4 ELISA âm tính và SRA dương tính (16 trong số 8.546 trường hợp, 0,2%) cũng đã được báo cáo. Nếu nghi ngờ lâm sàng mạnh mẽ về HIT, cần chú ý đến sự khác biệt trong kết quả xét nghiệm. 2)
Chiến lược quản lý HIT khác nhau tùy theo giai đoạn. 3)
HIT cấp tính
Số lượng tiểu cầu: Thấp
Xét nghiệm chức năng (SRA): Dương tính
Xét nghiệm miễn dịch (ELISA): Dương tính
Giai đoạn nguy cơ cao nhất. Ngừng ngay lập tức tất cả heparin và chuyển sang thuốc chống đông không phải heparin.
HIT bán cấp A
Số lượng tiểu cầu: Bình thường hóa
Xét nghiệm chức năng (SRA): Dương tính
Xét nghiệm miễn dịch (ELISA): Dương tính
Số lượng tiểu cầu đã hồi phục nhưng xét nghiệm chức năng dương tính. Phẫu thuật tim nên hoãn lại nếu có thể.
HIT bán cấp B
Số lượng tiểu cầu: Bình thường
Xét nghiệm chức năng (SRA): Âm tính (chuyển âm tính sau trung bình 50 ngày)
Xét nghiệm miễn dịch (ELISA): Dương tính
Tiếp xúc heparin ngắn trong phẫu thuật có nguy cơ thấp. Tiếp tục tránh heparin sau phẫu thuật.
HIT từ xa
Số lượng tiểu cầu: Bình thường
Xét nghiệm chức năng (SRA): Âm tính
Xét nghiệm miễn dịch (ELISA): Âm tính (kháng thể PF4/H biến mất ở trung vị 85 ngày)
Tình trạng có thể dùng heparin trong thời gian ngắn khi tái phơi nhiễm.
Ở bệnh nhân có triệu chứng mắt thứ phát do HIT, cần khai thác bệnh sử kỹ lưỡng và khám thực thể để loại trừ các triệu chứng toàn thân khác.
Đây là thang điểm đánh giá xác suất lâm sàng của HIT dựa trên 4 tiêu chí: mức độ giảm tiểu cầu (Thrombocytopenia), thời điểm khởi phát (Timing), sự hiện diện của huyết khối (Thrombosis) và loại trừ các nguyên nhân khác (oTher causes). Tổng điểm từ 0 đến 8, với ≥6 được coi là xác suất cao.
Khi HIT được chẩn đoán hoặc nghi ngờ mạnh, cần thực hiện ngay những điều sau:
Argatroban
Phân loại: Thuốc ức chế trực tiếp thrombin
Thời gian bán thải: 39–51 phút (chức năng gan bình thường), kéo dài đến 181 phút khi suy gan
Chuyển hóa: Bài tiết qua gan. Có lợi trong trường hợp suy thận.
Bivalirudin
Phân loại: Thuốc ức chế thrombin trực tiếp
Thời gian bán thải: 25 phút (chức năng thận bình thường đến suy thận nhẹ)
Liều PCI: 0,75 mg/kg bolus + 1,75 mg/kg/giờ
Liều CPB: 1 mg/kg bolus + 2,5 mg/kg/giờ (thêm 50 mg vào dung dịch priming) 3)
Hướng dẫn ASH 2018 khuyến cáo sử dụng bivalirudin cho PCI. Trong 52 trường hợp sử dụng PCI, tỷ lệ thành công thủ thuật là 98% và chảy máu nặng là 1,9% đã được báo cáo. 3)
Trong HIT kháng trị, nơi huyết khối tiến triển mặc dù đã dùng thuốc chống đông không phải heparin thích hợp, hãy xem xét những điều sau. 5)
Nếu bệnh nhân HIT cấp tính/bán cấp loại A cần phẫu thuật tim, hãy xem xét ba lựa chọn sau. 3)
Tắc mạch máu võng mạc và xuất huyết hốc mắt được xử trí nhãn khoa song song với quản lý toàn thân HIT.
Chuyển sang dùng thuốc ức chế thrombin trực tiếp như argatroban hoặc bivalirudin. Cả hai đều ức chế thrombin trực tiếp theo cơ chế khác với heparin, do đó không bị ảnh hưởng bởi kháng thể HIT. Việc lựa chọn thuốc phụ thuộc vào chức năng gan, chức năng thận và tình trạng lâm sàng.
Sự phát triển của HIT tiến triển qua các giai đoạn sau.
Bước 1: Hình thành phức hợp và sản xuất kháng thể
PF4 (yếu tố tiểu cầu 4) là một chemokine mang điện tích dương có nguồn gốc từ megakaryocyte, được lưu trữ trong các hạt alpha của tiểu cầu. PF4 tạo phức hợp với heparan sulfate mang điện tích âm (GAG trên bề mặt nội mô) hoặc LPS (màng ngoài của vi khuẩn Gram âm). Các phức hợp này hoạt động như “tín hiệu nguy hiểm”, cho phép sản xuất nhanh kháng thể IgG.
Bước 2: Hình thành phức hợp PF4-heparin
Việc dùng heparin dẫn đến hình thành phức hợp PF4-heparin. Do heparin có cấu trúc phân tử tương tự LPS và heparan sulfate, IgG có sẵn sẽ gắn kết.
Bước 3: Hoạt hóa tiểu cầu và tăng đông máu
Phức hợp IgG-PF4-heparin gắn kết với thụ thể FcγRII (FcγRIIa) trên tiểu cầu, kích hoạt tiểu cầu. Con đường nội sinh của dòng thác đông máu được khởi động, dẫn đến huyết khối lan rộng và giảm tiểu cầu do tiêu thụ tiểu cầu đồng thời. Đây là bản chất của cơ chế bệnh sinh “nghịch lý” của HIT.
Ngoài PF4 thông thường, kháng thể nhắm vào IL-8, protamine và NAP-2 được phát hiện trong dưới 1% các trường hợp được xét nghiệm HIT. 2) Ngoài ra, kháng thể anti-PF4 kích hoạt tiểu cầu khi không có heparin (kháng thể HIT không phụ thuộc heparin) có thể tham gia vào cơ chế bệnh sinh của HIT kháng trị và HIT tự miễn. 5)
Sau CPB, chuyển đổi huyết thanh kháng thể PF4/H xảy ra ở tới 50% bệnh nhân, nhưng chỉ 1-2% tiến triển thành HIT lâm sàng. 1) Việc dùng UFH liều cao trong CPB, giải phóng yếu tố mô và viêm được cho là thúc đẩy sản xuất kháng thể HIT. 3)
Chế phẩm kháng thể đơn dòng chuột IgG2b kháng PF4/H KKO đã được khử glycosyl. Ức chế hoạt hóa tiểu cầu và hoạt hóa bổ thể bằng cách ngăn chặn liên kết qua trung gian FcγRIIa.
Trên mô hình chuột, đã được báo cáo cải thiện giảm tiểu cầu và giảm kích thước huyết khối.5) Giai đoạn này cần được đánh giá trong các thử nghiệm lâm sàng trong tương lai.
Chiến lược tái sử dụng heparin trong CPB bằng thuốc ức chế P2Y12, cangrelor, đang được nghiên cứu.
Trong một loạt 10 ca, liều được điều chỉnh bằng VerifyNow P2Y12 PRU và không có biến chứng huyết khối nào được báo cáo.5) Chưa có phác đồ chuẩn nào được thiết lập.
Mặc dù hiệu quả của TPE đã được công nhận, nhưng một quy trình thống nhất vẫn chưa được thiết lập.
Một đánh giá hệ thống (30 ca) báo cáo trung bình 4 lần TPE và thể tích trao đổi huyết tương 1,3 PV, nhưng mức độ bằng chứng thấp, cần các nghiên cứu tiến cứu trong tương lai. 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.