HIT حاد
تعداد پلاکت: کاهش
آزمایش عملکردی (SRA): مثبت
آزمایش ایمنی (ELISA): مثبت
پرریسکترین دوره. تمام هپارینها را فوراً قطع کرده و به داروهای ضد انعقاد غیرهپارینی تغییر دهید.

ترومبوسیتوپنی ناشی از هپارین (HIT) یک واکنش ایمنی-واسطه به تجویز هپارین است. آنتیبادیهای IgG علیه کمپلکس فاکتور 4 پلاکتی (PF4) و هپارین تولید شده و باعث فعالسازی پلاکتها میشوند. در نتیجه، به طور متناقضی تعداد پلاکتها کاهش یافته و خون در حالت انعقادپذیری بالا قرار میگیرد.
HIT به دو نوع I و II تقسیم میشود. نوع I HIT یک ترومبوسیتوپنی گذرا است که خودبهخود بهبود مییابد. نوع II HIT یک وضعیت آنتیبادی-واسطه و شدید همراه با عوارض ترومبوآمبولی است. 1)
عوارض چشمی زمانی رخ میدهد که ترومبوز یا خونریزی ناشی از HIT به عروق چشم گسترش یابد. مدیریت چشمی همزمان با مدیریت سیستمیک HIT ضروری است.
در بیماران دریافتکننده UFH تا 5% و در بیماران دریافتکننده LMWH حدود یک دهم آن میزان گزارش شده است. پس از جراحی قلب، میزان بروز 0.1 تا 3% است که از جمعیت عمومی بیشتر بوده و میزان مرگومیر تا 10% میرسد. 2)
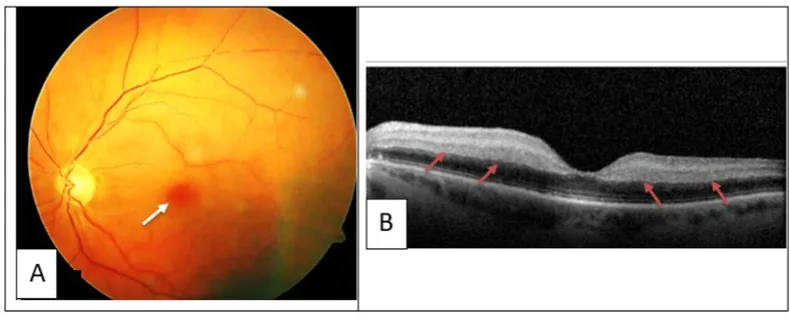
علائم چشمی بسته به محل ترومبوز یا خونریزی متفاوت است.
علت HIT یک واکنش ایمنیمحور به تجویز هپارین است. عوامل خطر اصلی عبارتند از:
HIT میتواند با LMWH نیز رخ دهد، اگرچه میزان بروز آن حدود یک دهم UFH است. با وجود خطر کمتر، نمیتوان از نظارت بر پلاکت صرف نظر کرد.
HIT یک تشخیص افتراقی است. در صورت مشاهده ترومبوز و ترومبوسیتوپنی 5 تا 14 روز پس از تجویز هپارین و رد سایر علل، به آن مشکوک شوید.
نمره 4T یک نمره احتمال بالینی است که از چهار معیار (ترومبوسیتوپنی، زمانبندی، ترومبوز، سایر علل) تشکیل شده است. هر معیار 0 تا 2 امتیاز دارد و مجموع امتیازات احتمال را طبقهبندی میکند.
| مجموع امتیاز | طبقهبندی احتمال |
|---|---|
| 6-8 امتیاز | احتمال بالا |
| ۴ تا ۵ امتیاز | متوسط |
| ۰ تا ۳ امتیاز | احتمال کم |
مثبت کاذب ۴T اسکور برای امتیاز متوسط ۴ حدود ۱۰٪ و برای امتیاز بالا ۸ حدود ۸۰٪ است. 4)
در بیماران جراحی قلب، کاهش پلاکت ۳۰ تا ۵۰٪ پس از CPB طبیعی است و در صورت وجود الگوی دو فازی (biphasic pattern) کاهش پلاکت، به عنوان یافته مشخصه HIT در نظر گرفته میشود. 3)1)
آزمایشهای اصلی شامل آنتیبادی ضد PF4/هپارین (anti-PF4 ELISA) و آزمایش آزادسازی سروتونین (SRA) هستند.
دستورالعمل ASH برای بیمارانی با نمره 4T متوسط یا بالاتر، آزمایش anti-PF4 ELISA را توصیه میکند و در صورت مثبت بودن، تأیید با SRA را مشخص میکند.2)
موارد نادر واگرایی (16 مورد از 8546 مورد، 0.2%) با anti-PF4 ELISA منفی و SRA مثبت نیز گزارش شده است و در صورت شک بالینی قوی به HIT، باید به واگرایی آزمایشها توجه کرد.2)
استراتژی مدیریت HIT بسته به فاز متفاوت است. 3)
HIT حاد
تعداد پلاکت: کاهش
آزمایش عملکردی (SRA): مثبت
آزمایش ایمنی (ELISA): مثبت
پرریسکترین دوره. تمام هپارینها را فوراً قطع کرده و به داروهای ضد انعقاد غیرهپارینی تغییر دهید.
HIT تحت حاد A
تعداد پلاکت: نرمال
آزمایش عملکردی (SRA): مثبت
آزمایش ایمنی (ELISA): مثبت
تعداد پلاکت بهبود یافته اما آزمایش عملکردی مثبت است. در صورت امکان جراحی قلب به تعویق بیفتد.
HIT تحت حاد B
تعداد پلاکت: طبیعی
آزمایش عملکردی (SRA): منفی (میانگین 50 روز تا منفی شدن)
ایمونواسی (ELISA): مثبت
قرار گرفتن کوتاه مدت در معرض هپارین حین عمل، کمخطر است. پس از عمل، اجتناب از هپارین ادامه مییابد.
HIT از راه دور
تعداد پلاکت: طبیعی
آزمایش عملکردی (SRA): منفی
اندازهگیری ایمنی (ELISA): منفی (آنتیبادی PF4/H پس از 85 روز به طور متوسط ناپدید میشود)
وضعیتی که در صورت مواجهه مجدد، تجویز کوتاه مدت هپارین امکانپذیر است.
در بیمارانی که علائم چشمی ثانویه به HIT دارند، باید سابقه پزشکی کامل و معاینه فیزیکی برای بررسی سایر علائم سیستمیک انجام شود.
این امتیاز برای ارزیابی احتمال بالینی HIT بر اساس چهار معیار است: شدت ترومبوسیتوپنی، زمان شروع، وجود ترومبوز و رد سایر علل. مجموع امتیاز ۰ تا ۸ است و امتیاز ۶ یا بیشتر به عنوان احتمال بالا در نظر گرفته میشود.
هنگامی که HIT تشخیص داده میشود یا به شدت مشکوک است، موارد زیر بلافاصله انجام میشود:
آرگاتروبان
طبقهبندی: مهارکننده مستقیم ترومبین
نیمهعمر: ۳۹ تا ۵۱ دقیقه (عملکرد طبیعی کبد)، در نارسایی کبد تا ۱۸۱ دقیقه افزایش مییابد
متابولیسم: دفع کبدی. برای استفاده در بیماران مبتلا به نارسایی کلیوی مفید است.
بیوالیرودین
طبقهبندی: مهارکننده مستقیم ترومبین
نیمهعمر: ۲۵ دقیقه (عملکرد طبیعی تا اختلال خفیف کلیوی)
دوز PCI: بولوس ۰.۷۵ میلیگرم/کیلوگرم + ۱.۷۵ میلیگرم/کیلوگرم/ساعت
دوز CPB: بولوس ۱ میلیگرم/کیلوگرم + ۲.۵ میلیگرم/کیلوگرم/ساعت (اضافه کردن ۵۰ میلیگرم به مایع پریماژ)3)
راهنمای ASH 2018 بیوالیرودین را برای PCI توصیه میکند. در ۵۲ مورد استفاده در PCI، میزان موفقیت روش ۹۸٪ و خونریزی عمده ۱.۹٪ گزارش شده است.3)
در HIT مقاوم به درمان که با وجود ضد انعقاد مناسب غیر هپارینی ترومبوز پیشرفت میکند، موارد زیر را بررسی کنید. 5)
اگر بیمار مبتلا به HIT حاد/تحت حاد A نیاز به جراحی قلب داشته باشد، سه گزینه زیر را در نظر بگیرید. 3)
انسداد عروق شبکیه و خونریزی اربیتال باید همزمان با مدیریت سیستمیک HIT به صورت چشمی درمان شوند.
به داروهای مهارکننده مستقیم ترومبین مانند آرگاتروبان یا بیوالیرودین تغییر داده میشود. هر دو با مکانیسمی متفاوت از هپارین، ترومبین را مستقیماً مهار میکنند و تحت تأثیر آنتیبادیهای HIT قرار نمیگیرند. انتخاب دارو بر اساس عملکرد کبد، عملکرد کلیه و شرایط بالینی تعیین میشود.
ایجاد HIT در مراحل زیر پیشرفت میکند.
مرحله ۱: تشکیل کمپلکس و تولید آنتیبادی
PF4 (فاکتور ۴ پلاکتی) یک کموکاین با بار مثبت است که از مگاکاریوسیتها منشأ گرفته و در گرانولهای آلفای پلاکت ذخیره میشود. PF4 با هپاران سولفات با بار منفی (GAG روی سطح اندوتلیال عروق) یا LPS (غشای خارجی باکتریهای گرممنفی) کمپلکس تشکیل میدهد. این کمپلکسها به عنوان «سیگنال خطر» عمل کرده و تولید سریع آنتیبادی IgG را ممکن میسازند.
مرحله ۲: تشکیل کمپلکس PF4-هپارین
با تجویز هپارین، کمپلکس PF4-هپارین تشکیل میشود. از آنجا که هپارین از نظر ساختار مولکولی مشابه LPS و هپاران سولفات است، IgG موجود به آن متصل میشود.
مرحله ۳: فعالسازی پلاکت و افزایش انعقاد
کمپلکس IgG-PF4-هپارین به گیرنده FcγRII (FcγRIIa) روی پلاکتها متصل شده و پلاکتها را فعال میکند. مسیر درونزاد آبشار انعقادی آغاز میشود و همزمان ترومبوز گسترده و ترومبوسیتوپنی ناشی از مصرف پلاکت رخ میدهد. این جوهر پاتوفیزیولوژی «متناقض» HIT است.
علاوه بر PF4 معمولی، آنتیبادیهای هدفگیرنده IL-8، پروتامین و NAP-2 در کمتر از 1% موارد بررسیشده HIT شناسایی میشوند. 2) همچنین، آنتیبادیهای ضد PF4 که پلاکتها را در غیاب هپارین فعال میکنند (آنتیبادی HIT مستقل از هپارین) ممکن است در پاتوفیزیولوژی HIT مقاوم و HIT خودایمن نقش داشته باشند. 5)
پس از CPB، تا 50% بیماران دچار سروکانورژن آنتیبادی PF4/H میشوند، اما تنها 1-2% به HIT بالینی مبتلا میشوند. 1) تجویز دوز بالای UFH در حین CPB، آزادسازی فاکتور بافتی و التهاب تصور میشود که تولید آنتیبادی HIT را تقویت میکند. 3)
این دارو یک فرم دگلیکوزیله از آنتیبادی مونوکلونال موشی IgG2b ضد PF4/H به نام KKO است. با مسدود کردن اتصال با واسطه FcγRIIa، فعالسازی پلاکت و فعالسازی کمپلمان را مهار میکند.
در مدلهای موشی، بهبود ترومبوسیتوپنی و کاهش اندازه لخته گزارش شده است.5) این مرحله نیاز به ارزیابی در کارآزماییهای بالینی آینده دارد.
استراتژی تجویز مجدد هپارین در حین گردش خون برونپیکری (CPB) با استفاده از کانگرلور، یک مهارکننده P2Y12، در حال بررسی است.
در یک مجموعه ۱۰ موردی، دوز بر اساس VerifyNow P2Y12 PRU تنظیم شد و هیچ عارضه ترومبوتیک گزارش نشد.5) با این حال، یک پروتکل استاندارد هنوز ایجاد نشده است.
اگرچه اثربخشی تبادل پلاسما (TPE) شناخته شده است، اما یک پروتکل یکپارچه هنوز ایجاد نشده است.
یک مرور سیستماتیک (۳۰ مورد) میانگین ۴ جلسه TPE و حجم تبادل پلاسما ۱.۳ برابر حجم پلاسما را گزارش کرده است، اما سطح شواهد پایین است و مطالعات آیندهنگر مورد نیاز است.5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.