तीव्र HIT
प्लेटलेट गणना : कम
कार्यात्मक परीक्षण (SRA) : सकारात्मक
प्रतिरक्षा माप (ELISA) : सकारात्मक
सबसे अधिक जोखिम वाला समय। सभी हेपरिन को तुरंत बंद करें और गैर-हेपरिन एंटीकोआगुलेंट पर स्विच करें।

हेपरिन-प्रेरित थ्रोम्बोसाइटोपेनिया (HIT) हेपरिन प्रशासन के प्रति एक प्रतिरक्षा-मध्यस्थ प्रतिक्रिया है। प्लेटलेट फैक्टर 4 (PF4) और हेपरिन के कॉम्प्लेक्स के विरुद्ध IgG एंटीबॉडी उत्पन्न होते हैं, जो प्लेटलेट सक्रियण का कारण बनते हैं। इसके परिणामस्वरूप, विरोधाभासी रूप से प्लेटलेट संख्या कम हो जाती है जबकि रक्त हाइपरकोएग्युलेबल अवस्था में आ जाता है।
HIT को प्रकार I और II में वर्गीकृत किया जाता है। HIT प्रकार I एक क्षणिक थ्रोम्बोसाइटोपेनिया है जो स्वतः ठीक हो जाता है। HIT प्रकार II एंटीबॉडी-मध्यस्थ है और थ्रोम्बोएम्बोलिक जटिलताओं के साथ एक गंभीर स्थिति है। 1)
नेत्र संबंधी जटिलताएं तब उत्पन्न होती हैं जब HIT से जुड़े थ्रोम्बस या रक्तस्राव आंखों के संवहनी तंत्र में फैल जाते हैं। HIT के प्रणालीगत प्रबंधन के समानांतर नेत्र संबंधी देखभाल की आवश्यकता होती है।
UFH प्राप्त करने वाले रोगियों में 5% तक और LMWH प्राप्त करने वाले रोगियों में लगभग 1/10 घटना दर बताई गई है। हृदय शल्य चिकित्सा के बाद यह 0.1-3% होती है, जो सामान्य जनसंख्या से अधिक है, और मृत्यु दर 10% तक पहुँच सकती है। 2)
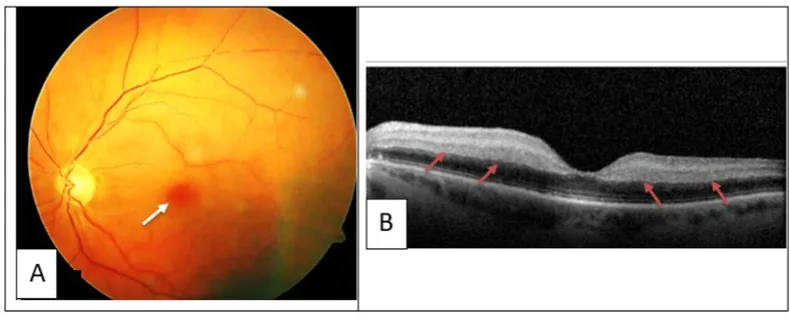
नेत्र लक्षण थ्रोम्बस या रक्तस्राव के स्थान के अनुसार भिन्न होते हैं।
HIT का कारण हेपरिन प्रशासन के प्रति प्रतिरक्षा-मध्यस्थ प्रतिक्रिया है। मुख्य जोखिम कारक निम्नलिखित हैं।
LMWH से भी HIT हो सकता है, लेकिन इसकी घटना दर UFH की तुलना में लगभग 1/10 कम है। कम जोखिम के बावजूद प्लेटलेट निगरानी को छोड़ा नहीं जा सकता।
HIT एक बहिष्करण निदान है। हेपरिन देने के 5-14 दिनों के भीतर थ्रोम्बोसिस और थ्रोम्बोसाइटोपेनिया होने पर, अन्य कारणों को खारिज करने के बाद इसका संदेह किया जाता है।
4T स्कोर चार मानदंडों (थ्रोम्बोसाइटोपेनिया, समय, थ्रोम्बोसिस, अन्य कारण) पर आधारित एक नैदानिक संभाव्यता स्कोर है। प्रत्येक मानदंड 0-2 अंकों पर स्कोर किया जाता है, और कुल अंक संभाव्यता को वर्गीकृत करते हैं।
| कुल अंक | संभाव्यता वर्गीकरण |
|---|---|
| 6–8 अंक | उच्च संभाव्यता |
| 4-5 अंक | मध्यम |
| 0-3 अंक | कम संभावना |
4T स्कोर की सकारात्मक भविष्यवाणी मूल्य मध्यम स्कोर 4 अंकों पर लगभग 10% और उच्च संभावना स्कोर 8 अंकों पर लगभग 80% है। 4)
हृदय शल्य चिकित्सा के रोगियों में CPB के बाद प्लेटलेट काउंट में 30-50% की कमी सामान्य है, और द्विफेज़िक पैटर्न (द्विफेज़िक प्लेटलेट कमी) देखा जाना HIT की विशेषता माना जाता है। 3)1)
एंटी-PF4/हेपरिन एंटीबॉडी (एंटी-PF4 ELISA) और सेरोटोनिन रिलीज परीक्षण (SRA) मुख्य परीक्षण विधियाँ हैं।
ASH दिशानिर्देश 4T स्कोर मध्यम या उच्च वाले रोगियों में एंटी-PF4 ELISA की सिफारिश करते हैं, और सकारात्मक होने पर SRA द्वारा पुष्टि करने की प्रक्रिया बताते हैं। 2)
एंटी-PF4 ELISA नकारात्मक और SRA सकारात्मक के दुर्लभ विचलन मामले (8,546 में से 16, 0.2%) भी रिपोर्ट किए गए हैं, और नैदानिक रूप से HIT का दृढ़ संदेह होने पर परीक्षण विचलन पर ध्यान देना आवश्यक है। 2)
HIT का प्रबंधन दृष्टिकोण चरण के अनुसार भिन्न होता है। 3)
तीव्र HIT
प्लेटलेट गणना : कम
कार्यात्मक परीक्षण (SRA) : सकारात्मक
प्रतिरक्षा माप (ELISA) : सकारात्मक
सबसे अधिक जोखिम वाला समय। सभी हेपरिन को तुरंत बंद करें और गैर-हेपरिन एंटीकोआगुलेंट पर स्विच करें।
सबस्यूट HIT A
प्लेटलेट काउंट : सामान्य
कार्यात्मक परीक्षण (SRA) : सकारात्मक
इम्यूनोएसे (ELISA) : सकारात्मक
प्लेटलेट काउंट सामान्य हो गया है लेकिन कार्यात्मक परीक्षण सकारात्मक है। हृदय शल्य चिकित्सा यदि संभव हो तो स्थगित करें।
उपतीव्र HIT B
प्लेटलेट गणना : सामान्य
कार्यात्मक परीक्षण (SRA) : नकारात्मक (माध्य 50 दिनों में नकारात्मक होना)
प्रतिरक्षा मापन (ELISA) : सकारात्मक
शल्यक्रिया के दौरान अल्पकालिक हेपरिन जोखिम कम जोखिम है। शल्यक्रिया के बाद हेपरिन से बचना जारी रखें।
दूरस्थ HIT
प्लेटलेट गणना : सामान्य
कार्यात्मक परीक्षण (SRA) : नकारात्मक
प्रतिरक्षा मापन (ELISA) : नकारात्मक (माध्य 85 दिनों में PF4/H एंटीबॉडी गायब हो जाते हैं)
पुनः संपर्क पर अल्पकालिक हेपरिन प्रशासन संभव है।
HIT के बाद नेत्र लक्षण वाले रोगियों में, अन्य प्रणालीगत लक्षणों के लिए गहन इतिहास और शारीरिक परीक्षण किया जाना चाहिए।
यह एक स्कोर है जो HIT की नैदानिक संभावना का मूल्यांकन चार मानदंडों के आधार पर करता है: थ्रोम्बोसाइटोपेनिया की डिग्री, घटना का समय, थ्रोम्बोसिस की उपस्थिति या अनुपस्थिति, और अन्य कारणों का बहिष्कार। कुल स्कोर 0 से 8 तक होता है, और 6 या उससे अधिक को उच्च संभावना माना जाता है।
जब HIT का निदान हो या दृढ़ता से संदेह हो, तो निम्नलिखित तुरंत किया जाना चाहिए।
अर्गाट्रोबान
वर्गीकरण : प्रत्यक्ष थ्रोम्बिन अवरोधक
अर्धायु : 39-51 मिनट (सामान्य यकृत कार्य), यकृत विकार में 181 मिनट तक बढ़ जाती है
चयापचय : यकृत उत्सर्जन प्रकार। गुर्दे की विकार वाले रोगियों में उपयोग के लिए लाभदायक।
बिवालिरुडिन
वर्गीकरण : प्रत्यक्ष थ्रोम्बिन अवरोधक
अर्ध-आयु : 25 मिनट (सामान्य से हल्की गुर्दे की हानि)
PCI खुराक : 0.75 mg/kg बोलस + 1.75 mg/kg/h
CPB खुराक : 1 mg/kg बोलस + 2.5 mg/kg/h (प्राइमिंग द्रव में 50 mg जोड़ें) 3)
ASH 2018 दिशानिर्देश PCI के लिए बिवालिरुडिन की सिफारिश करते हैं। PCI में 52 मामलों के उपयोग में 98% प्रक्रिया सफलता और 1.9% प्रमुख रक्तस्राव की सूचना दी गई है। 3)
उपयुक्त गैर-हेपरिन एंटीकोआगुलेंट के बावजूद थ्रोम्बस बढ़ने वाले दुर्दम्य HIT में निम्नलिखित पर विचार करें। 5)
तीव्र/उपतीव्र HIT A रोगी को हृदय शल्य चिकित्सा की आवश्यकता होने पर निम्नलिखित 3 विकल्पों पर विचार करें। 3)
रेटिना संवहनी अवरोध और कक्षीय रक्तस्राव का नेत्र संबंधी उपचार एचआईटी के प्रणालीगत प्रबंधन के समानांतर किया जाता है।
आर्गाट्रोबैन या बिवालिरुडिन जैसे प्रत्यक्ष थ्रोम्बिन अवरोधकों पर स्विच करें। ये दोनों हेपरिन से भिन्न तंत्र द्वारा थ्रोम्बिन को सीधे रोकते हैं, इसलिए HIT एंटीबॉडी से प्रभावित नहीं होते। दवा का चयन यकृत कार्य, गुर्दे के कार्य और नैदानिक स्थिति पर निर्भर करता है।
HIT का विकास निम्नलिखित चरणों में होता है।
चरण 1: कॉम्प्लेक्स निर्माण और एंटीबॉडी उत्पादन
PF4 (प्लेटलेट फैक्टर 4) एक धनात्मक आवेशित केमोकाइन है जो मेगाकैरियोसाइट्स से उत्पन्न होता है और प्लेटलेट अल्फा ग्रैन्यूल्स में संग्रहीत होता है। PF4 ऋणात्मक आवेशित हेपरान सल्फेट (संवहनी एंडोथेलियल सतह पर GAG) और LPS (ग्राम-नेगेटिव बैक्टीरिया की बाहरी झिल्ली) के साथ कॉम्प्लेक्स बनाता है। ये कॉम्प्लेक्स ‘खतरे के संकेत’ के रूप में कार्य करते हैं और IgG एंटीबॉडी के तेजी से उत्पादन को सक्षम बनाते हैं।
चरण 2: PF4-हेपरिन कॉम्प्लेक्स का निर्माण
हेपरिन प्रशासन से PF4-हेपरिन कॉम्प्लेक्स बनता है। हेपरिन की आणविक संरचना LPS और हेपरान सल्फेट के समान होती है, इसलिए मौजूदा IgG इससे जुड़ जाते हैं।
चरण 3: प्लेटलेट सक्रियण और हाइपरकोएग्युलेबिलिटी
IgG-PF4-हेपरिन कॉम्प्लेक्स प्लेटलेट्स पर FcγRII रिसेप्टर (FcγRIIa) से जुड़ता है और प्लेटलेट्स को सक्रिय करता है। जमावट कैस्केड का आंतरिक मार्ग शुरू होता है, जिससे व्यापक थ्रोम्बोसिस और प्लेटलेट खपत के कारण थ्रोम्बोसाइटोपेनिया एक साथ होते हैं। यह HIT की ‘विरोधाभासी’ रोग स्थिति का सार है।
सामान्य PF4 के अलावा, IL-8, प्रोटामाइन और NAP-2 को लक्ष्य करने वाले एंटीबॉडी HIT जांच के 1% से कम मामलों में पाए जाते हैं। 2) इसके अलावा, हेपरिन की अनुपस्थिति में भी प्लेटलेट्स को सक्रिय करने वाले एंटी-PF4 एंटीबॉडी (हेपरिन-स्वतंत्र HIT एंटीबॉडी) दुर्दम्य HIT और ऑटोइम्यून HIT की रोग प्रक्रिया में शामिल हो सकते हैं। 5)
CPB के बाद 50% तक रोगियों में PF4/H एंटीबॉडी का सेरोकनवर्जन होता है, लेकिन केवल 1-2% में नैदानिक HIT विकसित होता है। 1) CPB के दौरान UFH की उच्च खुराक, ऊतक कारक का स्राव और सूजन HIT एंटीबॉडी उत्पादन को बढ़ावा देते हैं। 3)
यह एक डीग्लाइकोसिलेटेड माउस मोनोक्लोनल IgG2b प्रकार का एंटी-PF4/H एंटीबॉडी KKO तैयारी है। FcγRIIa-मध्यस्थ बंधन को अवरुद्ध करके, यह प्लेटलेट सक्रियण और पूरक सक्रियण को दबाता है।
माउस मॉडल में प्लेटलेट की कमी में सुधार और थ्रोम्बस के आकार में कमी की सूचना दी गई है। 5) यह भविष्य के नैदानिक परीक्षणों में मूल्यांकन के चरण में है।
P2Y12 अवरोधक कैंग्रेलोर का उपयोग करके CPB के दौरान हेपरिन को पुनः प्रशासित करने की रणनीति पर विचार किया जा रहा है।
10 मामलों की श्रृंखला में, VerifyNow P2Y12 PRU द्वारा खुराक समायोजित की गई और कोई थ्रोम्बोटिक जटिलता रिपोर्ट नहीं हुई।5) कोई स्थापित प्रोटोकॉल अभी तक विकसित नहीं हुआ है।
TPE की प्रभावशीलता को मान्यता दी गई है, लेकिन कोई एकीकृत प्रोटोकॉल स्थापित नहीं किया गया है।
एक व्यवस्थित समीक्षा (30 मामलों) में TPE के औसत 4 सत्र और प्लाज्मा विनिमय मात्रा 1.3 PV की रिपोर्ट की गई है, लेकिन साक्ष्य का स्तर कम है, और भविष्य में आगे के अध्ययन की आवश्यकता है। 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.