HIT الحاد
عدد الصفائح الدموية: منخفض
الاختبار الوظيفي (SRA): إيجابي
القياس المناعي (ELISA): إيجابي
الفترة الأعلى خطورة. أوقف جميع أنواع الهيبارين فورًا وانتقل إلى مضادات التخثر غير الهيبارينية.

قلة الصفيحات المحدثة بالهيبارين (HIT) هي تفاعل مناعي يحدث عند إعطاء الهيبارين. يتم إنتاج أجسام مضادة من نوع IgG ضد معقد العامل الصفيحي 4 (PF4) والهيبارين، مما يؤدي إلى تنشيط الصفيحات. ونتيجة لذلك، ينخفض عدد الصفيحات بشكل متناقض بينما يصبح الدم في حالة فرط تخثر.
يصنف HIT إلى نوعين: النوع الأول (HIT I) هو نقص صفيحات عابر يتحسن تلقائيًا. النوع الثاني (HIT II) هو حالة بوساطة الأجسام المضادة، وهي حالة خطيرة مصحوبة بمضاعفات انصمام خثاري. 1)
تحدث المضاعفات العينية عندما تؤثر الخثارات والنزيف المرتبط بـ HIT على الأوعية الدموية للعين. يلزم التعامل العيني بالتزامن مع الإدارة العامة لـ HIT.
يُقدر معدل الإصابة بما يصل إلى 5% في المرضى الذين يتلقون الهيبارين غير المجزأ (UFH)، وحوالي عُشر ذلك في المرضى الذين يتلقون الهيبارين منخفض الوزن الجزيئي (LMWH). بعد جراحة القلب، يتراوح المعدل بين 0.1% و3%، وهو أعلى من عامة السكان، ويصل معدل الوفيات إلى 10%. 2)
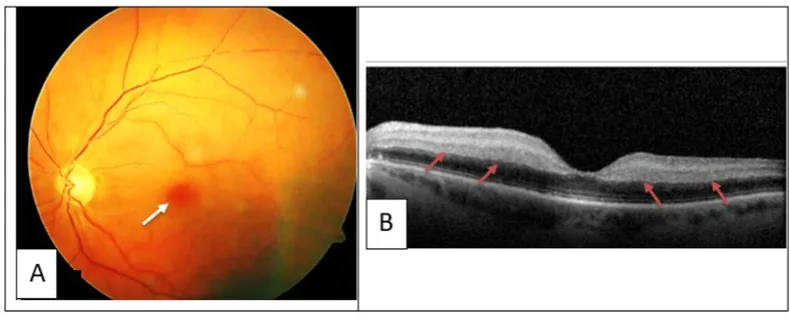
تختلف الأعراض العينية حسب موقع الجلطة أو النزيف.
سبب HIT هو تفاعل مناعي ضد إعطاء الهيبارين. عوامل الخطر الرئيسية هي:
يمكن أن يحدث HIT مع LMWH أيضًا، لكن معدل حدوثه أقل بحوالي 10 مرات مقارنة بـ UFH. لا يمكن تخطي مراقبة الصفائح الدموية لمجرد أن الخطر منخفض.
HIT هو تشخيص استبعادي. يُشتبه به عند حدوث تخثر دموي ونقص الصفيحات بعد 5-14 يومًا من إعطاء الهيبارين، مع استبعاد الأسباب الأخرى.
درجة 4T هي درجة احتمالية سريرية تتكون من أربعة معايير (نقص الصفيحات، التوقيت، التخثر، الأسباب الأخرى). يتم تسجيل كل معيار من 0 إلى 2 نقطة، وتصنف النتيجة الإجمالية الاحتمال.
| النتيجة الإجمالية | تصنيف الاحتمال |
|---|---|
| 6-8 نقاط | احتمال مرتفع |
| 4-5 نقاط | متوسط |
| 0-3 نقاط | احتمال منخفض |
القيمة التنبؤية الإيجابية لدرجة 4T هي حوالي 10% لدرجة متوسطة 4 نقاط وحوالي 80% لدرجة عالية 8 نقاط. 4)
في مرضى جراحة القلب، ينخفض عدد الصفائح الدموية عادة بنسبة 30-50% بعد المجازة القلبية الرئاسية، وإذا لوحظ نمط ثنائي الطور (انخفاض صفائحي ثنائي الطور) فإنه يعتبر علامة مميزة لـ HIT. 3)1)
اختبار الأجسام المضادة لـ PF4/الهيبارين (مقايسة الممتز المناعي المرتبط بالإنزيم المضاد لـ PF4) واختبار إطلاق السيروتونين هما الطريقتان الرئيسيتان للتشخيص.
توصي إرشادات ASH بإجراء اختبار anti-PF4 ELISA للمرضى الذين لديهم درجة 4T متوسطة أو أعلى، وإذا كانت النتيجة إيجابية، يتم التأكيد باستخدام اختبار SRA. 2)
تم الإبلاغ عن حالات نادرة من التباين حيث تكون نتيجة اختبار anti-PF4 ELISA سلبية ونتيجة اختبار SRA إيجابية (16 حالة من أصل 8,546 حالة، أي 0.2%)، وإذا كان هناك اشتباه سريري قوي في HIT، يجب الانتباه إلى هذا التباين في نتائج الاختبارات. 2)
تختلف استراتيجية إدارة HIT حسب المرحلة. 3)
HIT الحاد
عدد الصفائح الدموية: منخفض
الاختبار الوظيفي (SRA): إيجابي
القياس المناعي (ELISA): إيجابي
الفترة الأعلى خطورة. أوقف جميع أنواع الهيبارين فورًا وانتقل إلى مضادات التخثر غير الهيبارينية.
HIT تحت الحاد A
عدد الصفائح الدموية: طبيعي
الاختبار الوظيفي (SRA): إيجابي
القياس المناعي (ELISA): إيجابي
عدد الصفائح الدموية قد تعافى ولكن الاختبار الوظيفي إيجابي. يُفضل تأجيل جراحة القلب إن أمكن.
HIT تحت الحاد B
عدد الصفائح الدموية: طبيعي
الاختبار الوظيفي (SRA): سلبي (يتحول إلى سلبي في متوسط 50 يومًا)
القياس المناعي (ELISA): إيجابي
التعرض القصير للهيبارين أثناء الجراحة منخفض المخاطر. استمر في تجنب الهيبارين بعد الجراحة.
HIT عن بعد
عدد الصفائح الدموية: طبيعي
الاختبار الوظيفي (SRA): سلبي
اختبار المناعة (ELISA): سلبي (اختفاء الأجسام المضادة لـ PF4/H في متوسط 85 يومًا)
حالة يمكن فيها إعطاء الهيبارين لفترة قصيرة عند التعرض مرة أخرى.
بالنسبة للمرضى الذين يعانون من أعراض عينية ثانوية لـ HIT، يجب إجراء تاريخ مرضي شامل وفحص بدني دقيق للتحقق من عدم وجود أعراض جهازية أخرى.
هي درجة تقيم الاحتمال السريري لـ HIT بناءً على أربعة معايير: شدة نقص الصفيحات (Thrombocytopenia)، توقيت ظهوره (Timing)، وجود تجلط الدم (Thrombosis)، ونفي الأسباب الأخرى (oTher causes). المجموع من 0 إلى 8 نقاط، وتعتبر 6 نقاط أو أكثر احتمالية عالية.
عند تشخيص أو الاشتباه القوي بـ HIT، يجب تنفيذ ما يلي فورًا:
أرغاتروبان
التصنيف: مثبط الثرومبين المباشر
عمر النصف: 39-51 دقيقة (وظيفة الكبد الطبيعية)، يصل إلى 181 دقيقة في حالة ضعف الكبد
الاستقلاب: إفراز كبدي. مفيد في حالات القصور الكلوي.
بيفاليرودين
التصنيف: مثبط الثرومبين المباشر
عمر النصف: 25 دقيقة (وظائف الكلى طبيعية إلى ضعف خفيف)
جرعة القسطرة القلبية التداخلية (PCI): 0.75 مغ/كغ بلعة + 1.75 مغ/كغ/ساعة
جرعة CPB: 1 ملغم/كغم بلعة + 2.5 ملغم/كغم/ساعة (إضافة 50 ملغم إلى سائل البدء) 3)
توصي إرشادات ASH 2018 باستخدام البيفاليرودين في التدخل التاجي عن طريق الجلد (PCI). تم الإبلاغ عن معدل نجاح الإجراء بنسبة 98% ونزيف كبير بنسبة 1.9% في 52 حالة استخدام في PCI. 3)
في حالات HIT المقاومة للعلاج والتي يتقدم فيها التخثر على الرغم من مضادات التخثر غير الهيبارينية المناسبة، يجب النظر في الخيارات التالية. 5)
إذا كان المريض المصاب بـ HIT الحاد أو تحت الحاد من النوع A يحتاج إلى جراحة قلب، فيجب النظر في الخيارات الثلاثة التالية. 3)
يتم التعامل مع انسداد الأوعية الدموية الشبكية والنزيف المداري بالتوازي مع الإدارة الجهازية لـ HIT.
يتم التحول إلى مثبطات الثرومبين المباشرة مثل الأرغاتروبان أو البيفاليرودين. كلاهما يثبط الثرومبين مباشرة بآلية مختلفة عن الهيبارين، وبالتالي لا يتأثران بأجسام HIT المضادة. يعتمد اختيار الدواء على وظائف الكبد والكلى والحالة السريرية.
يحدث تطور HIT عبر المراحل التالية.
الخطوة 1: تكوين المعقد وإنتاج الأجسام المضادة
PF4 (العامل الصفائحي الرابع) هو كيموكين موجب الشحنة مشتق من الخلايا النواءية، ويُخزن في حبيبات ألفا الصفائحية. يشكل PF4 معقدات مع الهيباران سلفات سالب الشحنة (GAG على سطح البطانة الوعائية) أو LPS (الغشاء الخارجي للبكتيريا سالبة الجرام). تعمل هذه المعقدات كـ”إشارات خطر”، مما يتيح إنتاجًا سريعًا للأجسام المضادة IgG.
الخطوة 2: تكوين معقد PF4-هيبارين
يؤدي إعطاء الهيبارين إلى تكوين معقد PF4-هيبارين. نظرًا لتشابه الهيبارين الجزيئي مع LPS والهيباران سلفات، ترتبط الأجسام المضادة IgG الموجودة مسبقًا به.
الخطوة 3: تنشيط الصفائح الدموية وفرط التخثر
يرتبط مركب IgG-PF4-هيبارين بمستقبل FcγRII (FcγRIIa) على الصفائح الدموية، مما ينشطها. يبدأ المسار الداخلي لسلسلة التخثر، مما يؤدي إلى حدوث تخثر واسع النطاق ونقص الصفيحات الناتج عن استهلاك الصفائح الدموية في وقت واحد. هذا هو جوهر الحالة المتناقضة لـ HIT.
بالإضافة إلى PF4 المعتاد، يتم الكشف عن الأجسام المضادة التي تستهدف IL-8 والبروتامين وNAP-2 في أقل من 1% من حالات فحص HIT. 2) كما أن الأجسام المضادة لـ PF4 التي تنشط الصفائح الدموية في غياب الهيبارين (أجسام مضادة لـ HIT غير معتمدة على الهيبارين) قد تشارك في التسبب في HIT المقاوم للعلاج وHIT المناعي الذاتي. 5)
بعد المجازة القلبية الرئوية، يحدث تحول مصلي للأجسام المضادة لـ PF4/H لدى ما يصل إلى 50% من المرضى، لكن 1-2% فقط يتطور لديهم HIT سريري. 1) يُعتقد أن الجرعات العالية من الهيبارين غير المجزأ أثناء المجازة القلبية الرئوية، وإطلاق العامل النسيجي، والالتهاب تعزز إنتاج الأجسام المضادة لـ HIT. 3)
مستحضر مشتق من إزالة الغليكوزيل من الجسم المضاد وحيد النسيلة الفأري KKO من النوع IgG2b المضاد لـ PF4/H. يثبط تنشيط الصفائح الدموية وتنشيط المتممة عن طريق منع الارتباط الوسيط بـ FcγRIIa.
تم الإبلاغ عن تحسين نقص الصفيحات وتقليل حجم الجلطة في نموذج الفأر.5) هذه المرحلة تتطلب تقييمًا في التجارب السريرية المستقبلية.
يتم دراسة استراتيجية إعادة إعطاء الهيبارين أثناء المجازة القلبية الرئوية باستخدام عقار كانغريلور، وهو مثبط P2Y12.
في تجميع 10 حالات، تم تعديل الجرعة باستخدام VerifyNow P2Y12 PRU، ولم تُبلغ عن مضاعفات تخثرية.5) لم يتم التوصل إلى بروتوكول محدد.
على الرغم من الاعتراف بفعالية تبادل البلازما العلاجي (TPE)، إلا أنه لم يتم وضع بروتوكول موحد له.
أظهرت مراجعة منهجية (30 حالة) أن متوسط عدد جلسات تبادل البلازما العلاجي هو 4 جلسات، وحجم تبادل البلازما 1.3 من حجم البلازما، لكن مستوى الأدلة منخفض، وهناك حاجة لدراسات مستقبلية. 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.