Akute HIT
Thrombozytenzahl : erniedrigt
Funktioneller Test (SRA) : positiv
Immunassay (ELISA) : positiv
Zeitraum mit höchstem Risiko. Sofort alle Heparine absetzen und auf ein Nicht-Heparin-Antikoagulans umstellen.

Die Heparin-induzierte Thrombozytopenie (HIT) ist eine immunvermittelte Reaktion auf die Gabe von Heparin. Es werden IgG-Antikörper gegen den Komplex aus Thrombozytenfaktor 4 (PF4) und Heparin gebildet, was zur Thrombozytenaktivierung führt. Paradoxerweise kommt es dabei zu einem Abfall der Thrombozytenzahl bei gleichzeitigem hyperkoagulablem Zustand des Blutes.
Die HIT wird in Typ I und II unterteilt. HIT Typ I ist eine vorübergehende Thrombozytopenie, die spontan abklingt. HIT Typ II ist antikörpervermittelt und eine schwerwiegende Erkrankung mit thromboembolischen Komplikationen. 1)
Augenkomplikationen treten auf, wenn die mit HIT verbundene Thrombose oder Blutung auf das Gefäßsystem des Auges übergreift. Eine augenärztliche Behandlung parallel zur systemischen Behandlung der HIT ist erforderlich.
Bei Patienten, die UFH erhalten, beträgt die Inzidenz bis zu 5 %, bei Patienten, die LMWH erhalten, etwa 1/10 davon. Nach Herzoperationen liegt die Inzidenz mit 0,1–3 % höher als in der Allgemeinbevölkerung, und die Letalität kann bis zu 10 % betragen. 2)
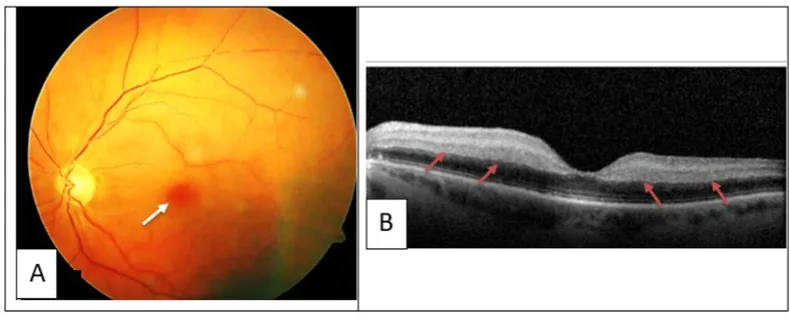
Die Augensymptome variieren je nach Ort des Thrombus oder der Blutung.
Die Ursache der HIT ist eine immunvermittelte Reaktion auf die Heparinverabreichung. Die wichtigsten Risikofaktoren sind die folgenden.
Auch NMH kann eine HIT auslösen, jedoch ist die Inzidenz etwa 1/10 im Vergleich zu UFH. Das geringere Risiko rechtfertigt keine Unterlassung der Thrombozytenüberwachung.
HIT ist eine Ausschlussdiagnose. Sie wird vermutet, wenn 5–14 Tage nach Heparingabe eine Thrombose und Thrombozytopenie auftreten und andere Ursachen ausgeschlossen wurden.
Der 4T-Score ist ein klinischer Wahrscheinlichkeitsscore, der auf vier Kriterien basiert (Thrombozytopenie, Zeitpunkt, Thrombose, andere Ursachen). Jedes Kriterium wird mit 0–2 Punkten bewertet, die Gesamtpunktzahl klassifiziert die Wahrscheinlichkeit.
| Gesamtpunktzahl | Wahrscheinlichkeitsklassifikation |
|---|---|
| 6–8 Punkte | Hohe Wahrscheinlichkeit |
| 4–5 Punkte | Mäßig |
| 0–3 Punkte | Niedrige Wahrscheinlichkeit |
Der positive Vorhersagewert des 4T-Scores beträgt bei einem mäßigen Score von 4 Punkten etwa 10 % und bei einem hohen Score von 8 Punkten etwa 80 %. 4)
Bei herzchirurgischen Patienten ist ein Abfall der Thrombozytenzahl um 30–50 % nach CPB normal, und ein zusätzliches biphasisches Muster (biphasische Thrombozytopenie) wird als charakteristisch für HIT angesehen. 3)1)
Die wichtigsten Testmethoden sind der Anti-PF4/Heparin-Antikörper (Anti-PF4-ELISA) und der Serotonin-Freisetzungstest (SRA).
Die ASH-Leitlinien empfehlen den Anti-PF4-ELISA für Patienten mit mittlerem bis hohem 4T-Score und bei Positivität eine Bestätigung durch SRA. 2)
Seltene Diskrepanzfälle (Anti-PF4-ELISA negativ und SRA positiv) wurden berichtet (16 von 8.546 Fällen, 0,2 %), und bei starkem klinischem Verdacht auf HIT ist auf Testdiskordanzen zu achten. 2)
Das Management der HIT unterscheidet sich je nach Phase. 3)
Akute HIT
Thrombozytenzahl : erniedrigt
Funktioneller Test (SRA) : positiv
Immunassay (ELISA) : positiv
Zeitraum mit höchstem Risiko. Sofort alle Heparine absetzen und auf ein Nicht-Heparin-Antikoagulans umstellen.
Subakute HIT A
Thrombozytenzahl : normalisiert
Funktioneller Test (SRA) : positiv
Immunassay (ELISA) : positiv
Die Thrombozytenzahl hat sich normalisiert, aber der funktionelle Test ist positiv. Herzoperationen sollten wenn möglich verschoben werden.
Subakute HIT B
Thrombozytenzahl: normal
Funktioneller Test (SRA): negativ (Negativierung im Median nach 50 Tagen)
Immunassay (ELISA): positiv
Die kurze intraoperative Heparinexposition ist mit einem geringen Risiko verbunden. Postoperativ Heparin weiterhin vermeiden.
Remote HIT
Thrombozytenzahl: normal
Funktioneller Test (SRA): negativ
Immunassay (ELISA): negativ (PF4/H-Antikörper verschwinden im Median nach 85 Tagen)
Zustand, der eine kurzzeitige Heparingabe bei erneuter Exposition ermöglicht.
Bei Patienten mit Augensymptomen nach HIT sollten eine gründliche Anamnese und körperliche Untersuchung auf andere systemische Symptome erfolgen.
Dies ist ein Score, der die klinische Wahrscheinlichkeit einer HIT anhand von vier Kriterien bewertet: Schweregrad der Thrombozytopenie, Zeitpunkt des Auftretens, Vorhandensein oder Fehlen einer Thrombose und Ausschluss anderer Ursachen. Die Gesamtpunktzahl reicht von 0 bis 8, wobei 6 oder mehr Punkte als hohe Wahrscheinlichkeit gelten.
Sobald die Diagnose einer HIT gestellt oder stark vermutet wird, sind folgende Maßnahmen sofort durchzuführen.
Argatroban
Klassifikation : Direkter Thrombininhibitor
Halbwertszeit : 39–51 Minuten (normale Leberfunktion), bei Leberfunktionsstörung bis zu 181 Minuten verlängert
Stoffwechsel : Hepatische Ausscheidung. Vorteilhaft bei Nierenfunktionsstörung.
Bivalirudin
Klassifikation : Direkter Thrombininhibitor
Halbwertszeit : 25 Minuten (normale bis leichte Nierenfunktionsstörung)
PCI-Dosis : 0,75 mg/kg Bolus + 1,75 mg/kg/h
CPB-Dosis : 1 mg/kg Bolus + 2,5 mg/kg/h (50 mg zur Priminglösung hinzufügen) 3)
Die ASH 2018-Leitlinie empfiehlt Bivalirudin für die PCI. Bei 52 PCI-Anwendungen wurde eine Verfahrenserfolgsrate von 98 % und eine schwere Blutung von 1,9 % berichtet. 3)
Bei refraktärer HIT mit fortschreitender Thrombose trotz geeigneter Nicht-Heparin-Antikoagulation sind folgende Maßnahmen zu erwägen. 5)
Wenn bei einem Patienten mit akuter/subakuter HIT A eine Herzoperation erforderlich ist, sind die folgenden 3 Optionen zu erwägen. 3)
Netzhautgefäßverschluss und Orbitablutung werden ophthalmologisch parallel zur systemischen Behandlung der HIT behandelt.
Wechseln Sie zu einem direkten Thrombininhibitor wie Argatroban oder Bivalirudin. Beide hemmen Thrombin direkt über einen anderen Mechanismus als Heparin und werden daher nicht von HIT-Antikörpern beeinflusst. Die Wahl des Medikaments richtet sich nach Leberfunktion, Nierenfunktion und klinischer Situation.
Die Entwicklung der HIT verläuft in den folgenden Schritten.
Schritt 1: Komplexbildung und Antikörperproduktion
PF4 (Plättchenfaktor 4) ist ein positiv geladenes Chemokin, das von Megakaryozyten stammt und in den Alpha-Granula der Thrombozyten gespeichert wird. PF4 bildet Komplexe mit negativ geladenem Heparansulfat (GAG auf der vaskulären Endotheloberfläche) und LPS (äußere Membran gramnegativer Bakterien). Diese Komplexe fungieren als „Gefahrensignale“ und ermöglichen die schnelle Produktion von IgG-Antikörpern.
Schritt 2: Bildung des PF4-Heparin-Komplexes
Die Verabreichung von Heparin führt zur Bildung von PF4-Heparin-Komplexen. Da Heparin eine ähnliche Molekülstruktur wie LPS und Heparansulfat aufweist, binden vorhandene IgG daran.
Schritt 3: Thrombozytenaktivierung und Hyperkoagulabilität
Der IgG-PF4-Heparin-Komplex bindet an den FcγRII-Rezeptor (FcγRIIa) auf Thrombozyten und aktiviert diese. Der intrinsische Weg der Gerinnungskaskade wird eingeleitet, was gleichzeitig zu ausgedehnter Thrombose und Thrombozytopenie durch Thrombozytenverbrauch führt. Dies ist das Wesen der „paradoxen“ Pathophysiologie der HIT.
Neben dem üblichen PF4 werden bei weniger als 1 % der HIT-Abklärungsfälle Antikörper gegen IL-8, Protamin und NAP-2 nachgewiesen. 2) Darüber hinaus könnten Anti-PF4-Antikörper, die Thrombozyten auch ohne Heparin aktivieren (heparinunabhängige HIT-Antikörper), an der Pathogenese der refraktären HIT und der Autoimmun-HIT beteiligt sein. 5)
Nach CPB kommt es bei bis zu 50 % der Patienten zu einer Serokonversion von PF4/H-Antikörpern, aber nur 1–2 % entwickeln eine klinische HIT. 1) Die hohe Dosis von UFH während CPB, die Freisetzung von Gewebefaktor und Entzündung fördern vermutlich die HIT-Antikörperproduktion. 3)
Es handelt sich um ein deglykosyliertes Präparat des murinen monoklonalen IgG2b-Anti-PF4/H-Antikörpers KKO. Durch Blockierung der FcγRIIa-vermittelten Bindung hemmt es die Thrombozytenaktivierung und die Komplementaktivierung.
In Mausmodellen wurde eine Verbesserung der Thrombozytopenie und eine Verkleinerung der Thrombusgröße berichtet. 5) Dieses Stadium erfordert eine Bewertung in zukünftigen klinischen Studien.
Eine Strategie zur erneuten Heparingabe während der CPB unter Verwendung des P2Y12-Inhibitors Cangrelor wird untersucht.
In einer Serie von 10 Fällen wurde die Dosis mittels VerifyNow P2Y12 PRU angepasst, und es wurden keine thrombotischen Komplikationen berichtet.5) Ein etabliertes Protokoll wurde noch nicht erreicht.
Obwohl die Wirksamkeit der TPE anerkannt ist, wurde kein einheitliches Protokoll etabliert.
Eine systematische Übersichtsarbeit (30 Fälle) berichtet über durchschnittlich 4 TPE-Sitzungen mit einem Plasmaaustauschvolumen von 1,3 PV, aber die Evidenz ist gering, und zukünftige prospektive Studien sind erforderlich. 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.