급성 HIT
혈소판 수: 감소
기능 검사(SRA): 양성
면역 측정(ELISA): 양성
가장 위험이 높은 시기입니다. 모든 헤파린을 즉시 중단하고 비헤파린계 항응고제로 전환합니다.

헤파린 유발 혈소판감소증(HIT)은 헤파린 투여에 대한 면역 매개 반응입니다. 혈소판 인자 4(PF4)와 헤파린의 복합체에 대한 IgG 항체가 생성되어 혈소판 활성화를 유발합니다. 이로 인해 역설적으로 혈소판 수가 감소하면서 혈액이 과응고 상태가 됩니다.
HIT는 I형과 II형으로 분류됩니다. HIT I형은 일시적인 혈소판감소증으로 자연 회복됩니다. HIT II형은 항체 매개성이며 혈전색전증 합병증을 동반한 중증 질환입니다. 1)
안과적 합병증은 HIT에 따른 혈전·출혈이 눈의 혈관계에 파급될 때 발생합니다. HIT의 전신 관리와 병행한 안과적 대응이 필요합니다.
UFH 투여 환자에서는 최대 5%, LMWH 투여 환자에서는 그 약 1/10의 발병률로 보고됩니다. 심장 수술 후에는 0.1~3%로 일반 인구보다 높으며, 사망률은 최대 10%에 이릅니다. 2)
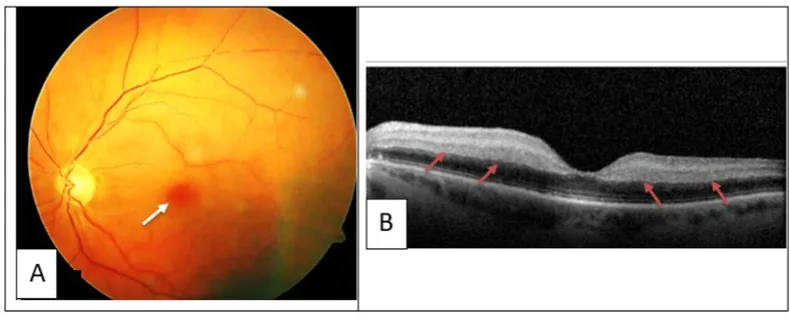
안구 증상은 혈전 또는 출혈 발생 부위에 따라 다릅니다.
HIT의 원인은 헤파린 투여에 대한 면역 매개 반응입니다. 주요 위험 인자는 다음과 같습니다.
LMWH로도 HIT가 발생할 수 있습니다. 다만 발생률은 UFH에 비해 약 1/10로 낮습니다. 위험이 낮다고 해서 혈소판 모니터링을 생략할 수는 없습니다.
HIT는 제외 진단입니다. 헤파린 투여 후 5~14일째 혈전증 및 혈소판 감소증이 나타나고 다른 원인이 배제된 경우 의심합니다.
4T 점수는 4가지 기준(혈소판 감소증, 시기, 혈전증, 기타 원인)으로 구성된 임상 확률 점수입니다. 각 기준은 0~2점으로 채점되며, 총점으로 확률을 분류합니다.
| 총점 | 확률 분류 |
|---|---|
| 6~8점 | 고확률 |
| 4~5점 | 중등도 |
| 0~3점 | 낮은 확률 |
4T 점수의 양성 예측도는 중등도 점수 4점에서 약 10%, 높은 확률 점수 8점에서 약 80%입니다. 4)
심장 수술 환자에서 CPB 후 혈소판 수가 30~50% 감소하는 것이 일반적이며, 이중성 혈소판 감소증(biphasic pattern)이 나타나는 경우 HIT의 특징적인 소견으로 고려합니다. 3)1)
주요 검사법은 항PF4/헤파린 항체 검사(anti-PF4 ELISA)와 세로토닌 방출 검사(SRA)입니다.
ASH 가이드라인은 4T 점수가 중등도 이상인 환자에게 anti-PF4 ELISA를 권장하며, 양성 시 SRA로 확인하는 절차를 제시합니다. 2)
anti-PF4 ELISA 음성이고 SRA 양성인 드문 불일치 사례(8,546례 중 16례, 0.2%)도 보고되어 있으며, 임상적으로 HIT가 강력히 의심되는 경우 검사 불일치에 주의해야 합니다. 2)
HIT의 관리 방침은 단계에 따라 다릅니다. 3)
급성 HIT
혈소판 수: 감소
기능 검사(SRA): 양성
면역 측정(ELISA): 양성
가장 위험이 높은 시기입니다. 모든 헤파린을 즉시 중단하고 비헤파린계 항응고제로 전환합니다.
아급성 HIT A
혈소판 수: 정상화
기능 검사(SRA): 양성
면역 측정(ELISA): 양성
혈소판 수는 회복되었으나 기능 검사가 양성입니다. 심장 수술은 가능하면 연기합니다.
아급성 HIT B
혈소판 수: 정상
기능 검사(SRA): 음성(중앙값 50일 후 음전)
면역 측정(ELISA): 양성
수술 중 단시간 헤파린 노출은 저위험. 수술 후 헤파린 회피를 지속한다.
원격 HIT
혈소판 수: 정상
기능 검사(SRA): 음성
면역 측정(ELISA): 음성 (PF4/H 항체 중앙값 85일 소실)
재노출 시 단시간 헤파린 투여가 가능한 상태.
HIT에 이차적인 안구 증상을 보이는 환자에서는 다른 전신 증상이 없는지 철저한 병력 청취와 신체 검진을 시행한다.
HIT로 진단되거나 강력히 의심될 때 즉시 다음을 시행합니다.
아르가트로반
분류: 직접 트롬빈 억제제
반감기: 39~51분(정상 간 기능), 간 장애 시 181분까지 연장
대사: 간 배설형. 신장애 환자에서 사용에 유리함.
비발리루딘
분류: 직접 트롬빈 억제제
반감기: 25분 (정상~경도 신장애)
PCI 용량: 0.75 mg/kg 볼루스 + 1.75 mg/kg/h
CPB 용량: 1 mg/kg 볼루스 + 2.5 mg/kg/h (프라이밍 용액에 50 mg 추가)3)
ASH 2018 가이드라인은 PCI에서 비발리루딘을 권장합니다. PCI 사용 52례에서 시술 성공률 98%, 주요 출혈 1.9%가 보고되었습니다.3)
적절한 비헤파린 항응고에도 불구하고 혈전이 진행되는 불응성 HIT에서는 다음을 고려한다. 5)
급성 HIT/아급성 HIT A 환자가 심장 수술이 필요한 경우 다음 세 가지 선택지를 고려한다. 3)
망막 혈관 폐쇄 및 안와 출혈은 HIT의 전신 관리와 병행하여 안과적으로 대응합니다.
아가트로반 또는 비발리루딘과 같은 직접 트롬빈 억제제로 전환합니다. 두 약물 모두 헤파린과 다른 기전으로 트롬빈을 직접 억제하므로 HIT 항체의 영향을 받지 않습니다. 약물 선택은 간 기능, 신장 기능 및 임상 상황에 따라 결정됩니다.
HIT의 발병은 다음 단계를 통해 진행됩니다.
1단계: 복합체 형성 및 항체 생성
PF4(혈소판 제4인자)는 거핵세포 유래의 양전하를 띤 케모카인으로, 혈소판 알파 과립에 저장됩니다. PF4는 음전하를 띤 헤파란 황산염(혈관 내피 표면의 GAG) 또는 LPS(그람 음성균 외막)와 복합체를 형성합니다. 이러한 복합체는 ‘위험 신호’로 작용하여 IgG 항체의 신속한 생성을 가능하게 합니다.
2단계: PF4-헤파린 복합체 형성
헤파린 투여로 PF4-헤파린 복합체가 형성됩니다. 헤파린은 LPS 및 헤파란 황산염과 분자 구조가 유사하므로 기존 IgG가 결합합니다.
3단계: 혈소판 활성화 및 응고 항진
IgG-PF4-헤파린 복합체가 혈소판의 FcγRII 수용체(FcγRIIa)에 결합하여 혈소판을 활성화합니다. 응고 캐스케이드의 내인성 경로가 시작되어 광범위한 혈전증과 혈소판 소모로 인한 혈소판 감소증이 동시에 발생합니다. 이것이 HIT의 ‘역설적’ 병태생리의 본질입니다.
일반 PF4 외에도 IL-8, 프로타민, NAP-2를 표적으로 하는 항체가 HIT 정밀 검사 사례의 1% 미만에서 검출됩니다. 2) 또한 헤파린이 없어도 혈소판을 활성화하는 항PF4 항체(헤파린 비의존성 HIT 항체)가 난치성 HIT 및 자가면역 HIT의 병태생리에 관여할 가능성이 있습니다. 5)
CPB 후 최대 50%의 환자에서 PF4/H 항체의 혈청전환이 발생하지만, 임상적 HIT로 진행되는 경우는 1~2%에 불과합니다. 1) CPB 중 고용량 UFH 투여, 조직인자 방출 및 염증이 HIT 항체 생성을 촉진하는 것으로 생각됩니다. 3)
이는 마우스 단클론 IgG2b형 항-PF4/H 항체 KKO를 탈글리코실화한 제제입니다. FcγRIIa 매개 결합을 차단하여 혈소판 활성화와 보체 활성화를 억제합니다.
마우스 모델에서 혈소판 감소증을 개선하고 혈전 크기를 줄인 것으로 보고되었습니다. 5) 향후 임상 시험에서 평가가 필요한 단계입니다.
P2Y12 억제제인 cangrelor를 사용하여 CPB 중 헤파린을 재투여하는 전략이 검토되고 있습니다.
10례의 증례 집적에서 VerifyNow P2Y12 PRU로 용량을 조절하면서 시행하였고, 혈전 합병증은 보고되지 않았습니다. 5) 확립된 프로토콜에는 이르지 못했습니다.
TPE의 유효성은 인식되고 있지만, 통일된 프로토콜은 확립되지 않았습니다.
체계적 문헌고찰(30례)에서는 TPE 평균 4회 시행, 혈장교환량 1.3 PV가 보고되었지만, 근거 수준은 낮으며 향후 전향적 연구가 필요합니다. 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.