急性HIT
血小板計數:降低
功能性檢測(SRA):陽性
免疫測定(ELISA):陽性
風險最高的時期。立即停用所有肝素,並改用非肝素類抗凝血藥。

肝素誘導的血小板減少症(HIT)是對肝素給藥產生的免疫介導反應。針對血小板因子4(PF4)與肝素複合物的IgG抗體被產生,導致血小板活化。這矛盾地導致血小板計數減少,同時血液處於高凝狀態。
HIT分為I型和II型。HIT I型是暫時性血小板減少,可自行緩解。HIT II型是抗體介導的,伴有血栓栓塞併發症的嚴重疾病。1)
眼部併發症發生在HIT相關的血栓或出血波及眼部血管時。需要與HIT全身管理並行進行眼科處理。
接受UFH治療的患者中發生率高達5%,接受LMWH治療的患者約為其1/10。心臟手術後發生率為0.1%~3%,高於一般人群,死亡率最高可達10%。2)
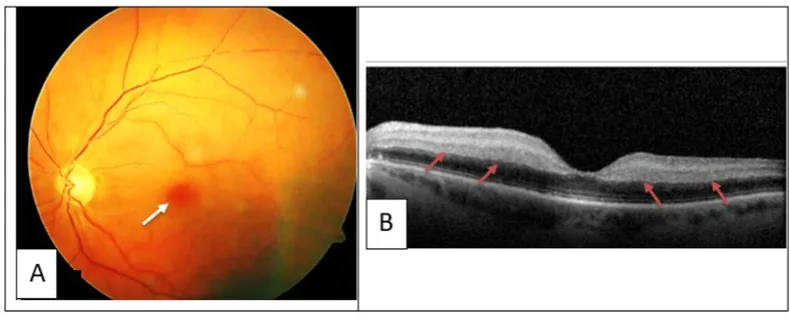
眼部症狀因血栓或出血的發生部位而異。
HIT的原因是針對肝素給藥的免疫介導反應。主要風險因素如下。
低分子肝素也可能引起HIT,但發生率約為普通肝素的1/10。即使風險較低,也不能省略血小板監測。
HIT是一種排除性診斷。當肝素給藥後5-14天出現血栓和血小板減少,且排除其他原因時,應懷疑HIT。
4T評分由四個標準(血小板減少、時間、血栓形成、其他原因)組成的臨床機率評分。每個標準評分0-2分,總分用於分類機率。
| 總分 | 機率分類 |
|---|---|
| 6-8分 | 高機率 |
| 4~5分 | 中度 |
| 0~3分 | 低機率 |
4T評分的陽性預測值:中度評分4分時約為10%,高機率評分8分時約為80%。4)
心臟手術患者CPB後血小板計數通常下降30%~50%,若出現雙相血小板減少,則視為HIT的特徵性表現。3)1)
主要檢查方法為抗PF4/肝素抗體檢測(anti-PF4 ELISA)和血清素釋放試驗(SRA)。
ASH指南建議對4T評分中度及以上的患者進行anti-PF4 ELISA檢測,陽性者用SRA確認。2)
有報告罕見的anti-PF4 ELISA陰性而SRA陽性的不一致病例(8,546例中16例,0.2%),臨床高度懷疑HIT時需注意檢查結果的不一致。2)
HIT的管理策略因階段而異。3)
急性HIT
血小板計數:降低
功能性檢測(SRA):陽性
免疫測定(ELISA):陽性
風險最高的時期。立即停用所有肝素,並改用非肝素類抗凝血藥。
亞急性HIT A
血小板計數:恢復正常
功能性檢測(SRA):陽性
免疫測定(ELISA):陽性
血小板計數已恢復,但功能性檢測陽性。心臟手術如可能應延期。
亞急性HIT B
血小板計數:正常
功能檢測(SRA):陰性(中位數50天轉陰)
免疫測定(ELISA):陽性
術中短時間肝素暴露風險低。術後繼續避免使用肝素。
遠端HIT
血小板計數:正常
功能檢測(SRA):陰性
免疫測定(ELISA):陰性(PF4/H抗體中位消失時間85天)
再次暴露時可短期使用肝素。
對於出現HIT繼發眼部症狀的患者,應進行徹底的病史詢問和身體檢查,以排除其他全身症狀。
此評分根據血小板減少程度、發生時間、有無血栓形成及其他原因排除等四項標準評估HIT的臨床機率。總分0-8分,6分以上為高機率。
當診斷或高度懷疑HIT時,應立即執行以下措施。
阿加曲班
分類:直接凝血酶抑制劑
半衰期:39~51分鐘(肝功能正常),肝功能不全時延長至181分鐘
代謝:肝臟排泄型。適用於腎功能不全患者。
比伐盧定
分類:直接凝血酶抑制劑
半衰期:25分鐘(正常至輕度腎功能不全)
PCI劑量:0.75 mg/kg 推注 + 1.75 mg/kg/h
CPB劑量:1 mg/kg 推注 + 2.5 mg/kg/h(預充液中加入50 mg)3)
ASH 2018指引建議在PCI中使用比伐盧定。在52例PCI使用中,報告手術成功率98%,重大出血1.9%。3)
對於儘管使用適當的非肝素抗凝治療但血栓仍進展的難治性HIT,考慮以下措施。5)
如果急性HIT/亞急性HIT A患者需要心臟手術,考慮以下三種選擇。3)
視網膜血管閉塞和眼眶出血需在HIT全身管理的同時進行眼科處理。
改用直接凝血酶抑制劑,如阿加曲班或比伐盧定。兩者均通過與肝素不同的機制直接抑制凝血酶,不受HIT抗體影響。藥物選擇取決於肝功能、腎功能和臨床情況。
HIT的發病經由以下階段進展。
步驟1:複合物形成與抗體產生
PF4(血小板第4因子)是一種來源於巨核細胞、帶正電荷的趨化因子,儲存於血小板α顆粒中。PF4與帶負電荷的硫酸乙醯肝素(血管內皮表面的GAG)或LPS(革蘭氏陰性菌外膜)形成複合物。這些複合物作為「危險信號」,促使IgG抗體快速產生。
步驟2:PF4-肝素複合物的形成
肝素給藥導致PF4-肝素複合物的形成。由於肝素與LPS和硫酸乙醯肝素的分子結構相似,既有的IgG會與之結合。
步驟3:血小板活化與高凝血狀態
IgG-PF4-肝素複合物與血小板上的FcγRII受體(FcγRIIa)結合,活化血小板。凝血級聯反應的內源性途徑被啟動,導致廣泛的血栓形成和因血小板消耗引起的血小板減少。這就是HIT「矛盾性」病理生理學的本質。
除常規PF4外,針對IL-8、魚精蛋白和NAP-2的抗體在HIT檢查病例中檢出率低於1%。2) 此外,即使在無肝素存在下也能活化血小板的抗PF4抗體(肝素非依賴性HIT抗體)可能參與難治性HIT和自體免疫性HIT的病理生理過程。5)
CPB後,多達50%的患者出現PF4/H抗體血清轉化,但僅1-2%發展為臨床HIT。1) CPB期間高劑量UFH給藥、組織因子釋放和炎症被認為促進HIT抗體產生。3)
這是一種去糖基化的小鼠單株IgG2b型抗PF4/H抗體KKO製劑。通過阻斷FcγRIIa介導的結合,抑制血小板活化和補體活化。
在小鼠模型中,已報告可改善血小板減少並縮小血栓大小。5) 目前處於需要在未來臨床試驗中評估的階段。
正在研究使用P2Y12抑制劑坎格瑞洛在CPB期間重新給予肝素的策略。
在10例病例系列中,透過VerifyNow P2Y12 PRU調整劑量,未報告血栓併發症。5) 尚未建立標準方案。
雖然TPE的有效性已得到認可,但尚未建立統一的方案。
一項系統性回顧(30例)報告平均進行4次TPE,血漿交換量為1.3 PV,但證據等級較低,需要未來的前瞻性研究。5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.