HIT aigu
Numération plaquettaire : diminuée
Test fonctionnel (SRA) : positif
Test immunologique (ELISA) : positif
Période à plus haut risque. Arrêter immédiatement toute héparine et passer à un anticoagulant non héparinique.

La thrombopénie induite par l’héparine (HIT) est une réaction immunitaire survenant après administration d’héparine. Des anticorps IgG sont produits contre le complexe formé par le facteur plaquettaire 4 (PF4) et l’héparine, entraînant une activation plaquettaire. Il en résulte paradoxalement une diminution du nombre de plaquettes tout en créant un état d’hypercoagulabilité.
La HIT est classée en types I et II. Le type I est une thrombopénie transitoire qui se résout spontanément. Le type II est médié par des anticorps et constitue une pathologie grave avec complications thromboemboliques. 1)
Les complications ophtalmiques surviennent lorsque la thrombose ou l’hémorragie associée à la HIT se propage au système vasculaire oculaire. Une prise en charge ophtalmique parallèle à la gestion systémique de la HIT est nécessaire.
Chez les patients recevant de l’UFH, l’incidence peut atteindre 5 %, et chez ceux recevant de la LMWH, elle est environ 10 fois plus faible. Après une chirurgie cardiaque, l’incidence est de 0,1 à 3 %, plus élevée que dans la population générale, et le taux de mortalité peut atteindre 10 %. 2)
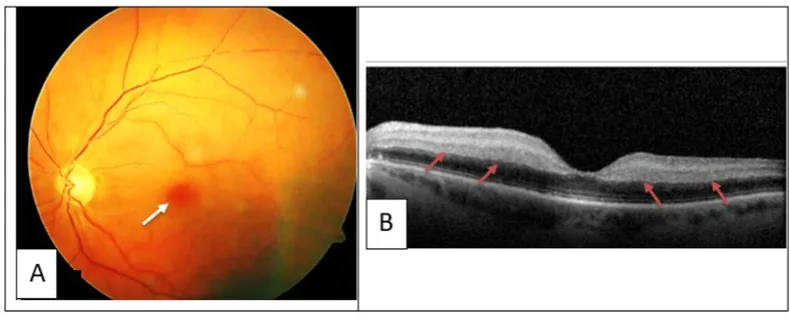
Les symptômes oculaires varient selon le site de la thrombose ou de l’hémorragie.
La cause du HIT est une réaction immunitaire médiée par l’administration d’héparine. Les principaux facteurs de risque sont les suivants.
La TIH peut également survenir avec l’HBPM, mais l’incidence est environ 10 fois plus faible qu’avec l’HNF. Le risque plus faible ne permet pas de supprimer la surveillance plaquettaire.
Le HIT est un diagnostic d’exclusion. Il est suspecté en cas de thrombose et thrombocytopénie survenant 5 à 14 jours après l’administration d’héparine, après exclusion des autres causes.
Le score 4T est un score de probabilité clinique basé sur quatre critères (Thrombocytopénie, Timing, Thrombose, autres causes). Chaque critère est noté de 0 à 2 points, et le total classe la probabilité.
| Score total | Classification de probabilité |
|---|---|
| 6–8 points | Haute probabilité |
| 4 à 5 points | Modéré |
| 0 à 3 points | Faible probabilité |
La valeur prédictive positive du score 4T est d’environ 10 % pour un score modéré de 4 points et d’environ 80 % pour un score élevé de 8 points. 4)
Chez les patients en chirurgie cardiaque, une diminution de 30 à 50 % du nombre de plaquettes après CEC est normale, et un motif biphasique (thrombocytopénie biphasique) supplémentaire est considéré comme une caractéristique de la HIT. 3)1)
Les principaux tests sont le dosage des anticorps anti-PF4/héparine (anti-PF4 ELISA) et le test de libération de sérotonine (SRA).
Les directives de l’ASH recommandent l’anti-PF4 ELISA pour les patients avec un score 4T modéré à élevé, et une confirmation par SRA en cas de positivité. 2)
De rares cas de discordance (anti-PF4 ELISA négatif et SRA positif) ont été rapportés (16 cas sur 8 546, soit 0,2 %), nécessitant une attention en cas de forte suspicion clinique de HIT. 2)
La stratégie de prise en charge du HIT varie selon la phase. 3)
HIT aigu
Numération plaquettaire : diminuée
Test fonctionnel (SRA) : positif
Test immunologique (ELISA) : positif
Période à plus haut risque. Arrêter immédiatement toute héparine et passer à un anticoagulant non héparinique.
HIT subaiguë A
Numération plaquettaire : normalisée
Test fonctionnel (SRA) : positif
Dosage immunologique (ELISA) : positif
La numération plaquettaire est rétablie mais le test fonctionnel est positif. La chirurgie cardiaque doit être reportée si possible.
HIT subaigu B
Numération plaquettaire : normale
Test fonctionnel (SRA) : négatif (négativation médiane à 50 jours)
Dosage immunologique (ELISA) : positif
L’exposition peropératoire brève à l’héparine est à faible risque. En postopératoire, continuer à éviter l’héparine.
HIT à distance
Numération plaquettaire : normale
Test fonctionnel (SRA) : négatif
Dosage immunologique (ELISA) : négatif (disparition des anticorps PF4/H en médiane 85 jours)
État permettant une administration brève d’héparine en cas de réexposition.
Chez les patients présentant des symptômes oculaires secondaires à un HIT, un interrogatoire approfondi et un examen physique doivent être réalisés pour rechercher d’autres symptômes systémiques.
Il s’agit d’un score qui évalue la probabilité clinique de HIT selon quatre critères : le degré de thrombocytopénie, le moment de l’apparition, la présence ou non de thrombose, et l’exclusion d’autres causes. Le score total va de 0 à 8, un score de 6 ou plus étant considéré comme une forte probabilité.
Dès que le diagnostic de HIT est posé ou fortement suspecté, les mesures suivantes doivent être prises immédiatement.
Argatroban
Classification : Inhibiteur direct de la thrombine
Demi-vie : 39 à 51 minutes (fonction hépatique normale), prolongée jusqu’à 181 minutes en cas d’insuffisance hépatique
Métabolisme : Élimination hépatique. Avantageux en cas d’insuffisance rénale.
Bivalirudine
Classification : Inhibiteur direct de la thrombine
Demi-vie : 25 minutes (fonction rénale normale à légèrement altérée)
Dose pour ICP : 0,75 mg/kg en bolus + 1,75 mg/kg/h
Dose pour CEC : 1 mg/kg en bolus + 2,5 mg/kg/h (ajouter 50 mg dans le liquide d’amorçage) 3)
Les recommandations ASH 2018 recommandent la bivalirudine pour l’ICP. Dans 52 cas d’utilisation en ICP, un taux de succès de la procédure de 98 % et un taux d’hémorragie majeure de 1,9 % ont été rapportés. 3)
Dans la HIT réfractaire où la thrombose progresse malgré une anticoagulation non héparinique appropriée, envisager les éléments suivants. 5)
Si une chirurgie cardiaque est nécessaire chez un patient atteint de HIT aiguë/subaiguë A, envisager les 3 options suivantes. 3)
L’occlusion vasculaire rétinienne et l’hémorragie orbitaire sont traitées sur le plan ophtalmologique en parallèle de la prise en charge systémique du THI.
Passer à un inhibiteur direct de la thrombine tel que l’argatroban ou le bivalirudine. Ces deux médicaments inhibent directement la thrombine par un mécanisme différent de celui de l’héparine, et ne sont donc pas affectés par les anticorps HIT. Le choix du médicament dépend de la fonction hépatique, de la fonction rénale et de la situation clinique.
Le développement de la HIT progresse par les étapes suivantes.
Étape 1 : Formation du complexe et production d’anticorps
Le PF4 (facteur plaquettaire 4) est une chimiokine chargée positivement dérivée des mégacaryocytes, stockée dans les granules alpha des plaquettes. Le PF4 forme des complexes avec l’héparane sulfate chargé négativement (GAG à la surface endothéliale vasculaire) et le LPS (membrane externe des bactéries Gram-négatives). Ces complexes agissent comme des « signaux de danger » permettant la production rapide d’anticorps IgG.
Étape 2 : Formation du complexe PF4-héparine
L’administration d’héparine conduit à la formation de complexes PF4-héparine. Comme l’héparine a une structure moléculaire similaire au LPS et à l’héparane sulfate, les IgG préexistants s’y lient.
Étape 3 : Activation plaquettaire et hypercoagulabilité
Le complexe IgG-PF4-héparine se lie au récepteur FcγRII (FcγRIIa) sur les plaquettes, activant ainsi les plaquettes. La voie intrinsèque de la cascade de coagulation est initiée, entraînant simultanément une thrombose étendue et une thrombopénie due à la consommation de plaquettes. C’est l’essence de la pathologie « paradoxale » du HIT.
En dehors du PF4 habituel, des anticorps ciblant l’IL-8, la protamine et le NAP-2 sont détectés dans moins de 1 % des cas de suspicion de TIH. 2) De plus, les anticorps anti-PF4 activant les plaquettes même en l’absence d’héparine (anticorps TIH indépendants de l’héparine) pourraient être impliqués dans la pathogénie de la TIH réfractaire et de la TIH auto-immune. 5)
Après une CEC, jusqu’à 50 % des patients développent une séroconversion des anticorps PF4/H, mais seulement 1 à 2 % évoluent vers un HIT clinique. 1) L’administration de doses élevées d’UFH pendant la CEC, la libération de facteur tissulaire et l’inflammation sont considérées comme favorisant la production d’anticorps HIT. 3)
Il s’agit d’une préparation d’anticorps monoclonal murin IgG2b anti-PF4/H KKO déglycosylé. En bloquant la liaison médiée par FcγRIIa, il inhibe l’activation plaquettaire et l’activation du complément.
Des études sur des modèles murins ont rapporté une amélioration de la thrombocytopénie et une réduction de la taille des caillots. 5) Cette étape nécessite une évaluation dans le cadre d’essais cliniques futurs.
Une stratégie de réadministration d’héparine pendant la CEC utilisant le cangrélor, un inhibiteur du P2Y12, est à l’étude.
Dans une série de 10 cas, la dose a été ajustée à l’aide du VerifyNow P2Y12 PRU, et aucune complication thrombotique n’a été rapportée.5) Aucun protocole établi n’a encore été atteint.
Bien que l’efficacité de la TPE soit reconnue, aucun protocole standardisé n’a été établi.
Une revue systématique (30 cas) rapporte une moyenne de 4 séances de TPE avec un volume d’échange plasmatique de 1,3 PV, mais le niveau de preuve est faible, et des études prospectives futures sont nécessaires. 5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.