نوع کریبریفرم
فراوانی: شایعترین (39.8%)
ویژگیها: ساختار لوبولار با حوضچههای دایرهای موسین. ظاهر «پنیر سوئیسی». پیشآگهی متوسط.

کارسینوم آدنوئید کیستیک (ACC) یک تومور بدخیم نادر است که از غدد ترشحی منشأ میگیرد و بروز جهانی آن 3-4 مورد در هر میلیون نفر جمعیت گزارش شده است1). حدود 1٪ از کل سرطانهای سر و گردن را تشکیل میدهد و هنگامی که در غده اشکی ایجاد شود، کارسینوم آدنوئید کیستیک غده اشکی نامیده میشود1).
کارسینوم آدنوئید کیستیک غده اشکی حدود 1.6٪ از کل تومورهای اربیت را تشکیل میدهد3)5) و شایعترین تومور بدخیم اپیتلیال غده اشکی است که 13-40٪ از سرطانهای غده اشکی را شامل میشود5). تومورهای غده اشکی حدود 10٪ از ضایعات فضاگیر اربیت را تشکیل میدهند، حدود 20٪ از تومورهای جامد غده اشکی منشأ اپیتلیال دارند، حدود 45٪ از آنها بدخیم هستند و حدود 60٪ از تومورهای بدخیم اپیتلیال غده اشکی کارسینوم آدنوئید کیستیک هستند.
کارسینوم آدنوئید کیستیک غده اشکی اولین بار توسط تئودور بیلروث توصیف شد و به دلیل ویژگیهای بافتشناسی، در ابتدا «cylindroma» نامیده شد5).
ویژگیهای اپیدمیولوژیک به شرح زیر است:
حدود 1.6٪ از کل تومورهای اربیت را تشکیل میدهد و بروز جهانی کارسینوم آدنوئید کیستیک 3 تا 4 مورد در هر میلیون نفر جمعیت است که بسیار نادر است1)5). این شایعترین نوع بافتشناسی در میان تومورهای بدخیم اپیتلیال غده اشکی است.
بر اساس بررسی بزرگ 806 مورد، فراوانی علائم اولیه به شرح زیر است5):
| علامت | فراوانی |
|---|---|
| برجستگی چشم (اگزوفتالمی) | 27.4٪ |
| درد | 21.7% |
| تورم پلک | 10.9% |
| انحراف چشم | 10.2% |
| محدودیت حرکت چشم | 10.1% |
| کاهش بینایی | 9.3% |
| دوبینی | 6.7% |
| افتادگی پلک | 4.1% |
درد علامتی اختصاصی برای کارسینوم آدنوئید کیستیک است که به دلیل تهاجم اطراف عصبی (PNI) ایجاد میشود. این یک نکته تمایز مهم از تومورهای خوشخیم است. از آنجایی که غده اشکی در قسمت فوقانی-خارجی حدقه قرار دارد، چشم اغلب به سمت داخل-پایین منحرف میشود. ممکن است کاهش حس در ناحیه پیشانی-گیجگاهی و افتادگی پلک به شکل S نیز رخ دهد. از شروع علائم تا تشخیص به طور متوسط 11.1±18.3 ماه (محدوده 0.5 تا 120 ماه) طول میکشد5).
سرعت رشد تومور از پلئومورفیک آدنوم سریعتر است و تمایل به همراهی با درد دارد که نکته مهمی در تشخیص افتراقی است. بیرونزدگی چشم به دلیل افزایش اندازه تومور، محدودیت حرکات چشم به دلیل نفوذ به عضلات خارج چشمی و اعصاب، و کاهش بینایی به دلیل فشار بر عصب بینایی نیز نسبتاً سریع پیشرفت میکنند.
وجود یا عدم وجود درد مهمترین نکته افتراقی است. کارسینوم آدنوئید کیستیک به دلیل نفوذ اطراف عصبی با درد همراه است، در حالی که تومورهای خوشخیم (مانند پلئومورفیک آدنوم) بدون درد و با رشد آهسته هستند. اگر سیتی اسکن تخریب استخوان را نشان دهد، میتوان بدخیمی را تشخیص داد، اما مواردی از کارسینوم آدنوئید کیستیک بدون تخریب استخوان نیز وجود دارد، بنابراین در صورت وجود درد، بیوپسی باید فعالانه در نظر گرفته شود.
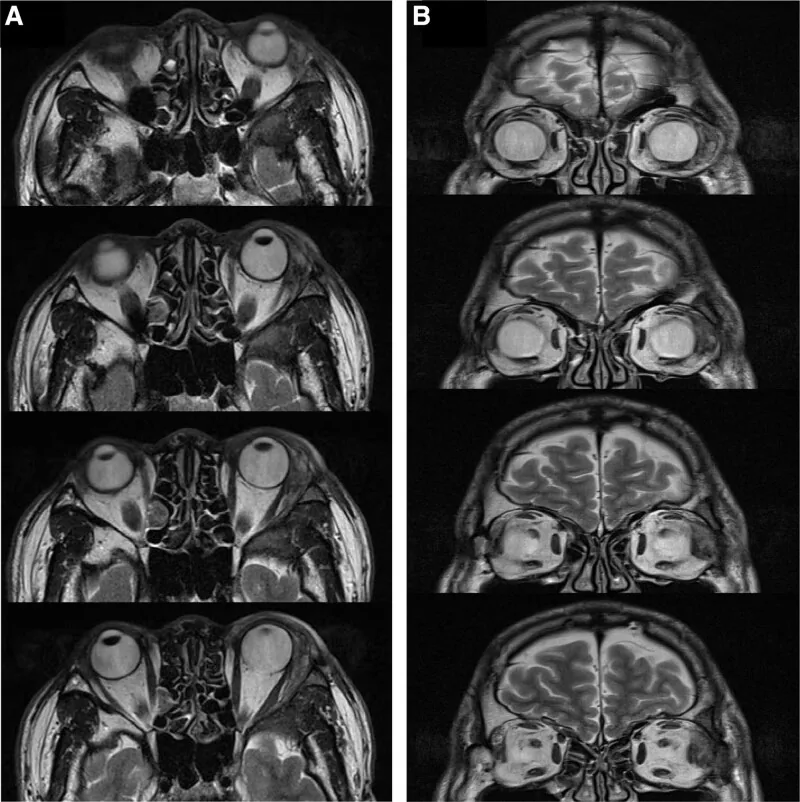
در گزارش Williams و همکاران، نفوذ به حفره اشکی در 82% بیماران از نظر بافتشناسی تأیید شده است1). اگر تومور در سیتی اسکن استخوان حدقه را تخریب کرده باشد، میتوان بدخیمی را تشخیص داد، اما باید توجه داشت که مواردی از کارسینوم آدنوئید کیستیک بدون تخریب استخوان نیز وجود دارد.
علت کارسینوم آدنوئید کیستیک ناشناخته است و عوامل خطر خاصی برای آن مشخص نشده است. تومور اغلب از لوب اربیتال غده اشکی منشأ میگیرد و بدون کپسول است.
ویژگیهای پاتولوژیک و بالینی زیر به عنوان عوامل پیشآگهی بد شناخته شدهاند:
تشخیص قطعی بر اساس ارزیابی آسیبشناسی بافتی است. در صورت مشکوک بودن به بدخیمی، بیوپسی برداشتی برای جلوگیری از کاشت سلولهای توموری در حدقه توصیه میشود. آسپیراسیون با سوزن ظریف ممکن است برای تومورهای غیرقابل برداشت مناسب باشد، اما فقط در مراکزی با آسیبشناس سلولی مجرب.
در صورت وجود علائمی مانند بیرونزدگی چشم که تومور غده اشکی را مطرح میکند، معاینات چشمی مانند بینایی، میدان بینایی و حرکات چشم انجام میشود و تصویربرداری با سیتی ساده و امآرآی با و بدون کنتراست انجام میشود. در صورت نیاز به جستجوی سیستمیک، پت-سیتی یا سیتی با کنتراست نیز انجام میشود. تشخیص قطعی با بیوپسی یا بررسی آسیبشناسی بافتی پس از برداشت کامل است.
| مرحله T | تعریف |
|---|---|
| T1 | حداکثر قطر 2 سانتیمتر یا کمتر |
| T2 | حداکثر قطر بیشتر از 2 سانتیمتر تا 4 سانتیمتر |
| T3 | بیشتر از 4 سانتیمتر در بزرگترین قطر یا گسترش به بافت نرم مدار |
| T4 | تهاجم به سینوسهای پارانازال، حفره تمپورال، حفره ناخنک، شکاف فوقانی مدار، سینوس کاورنو، یا مغز |
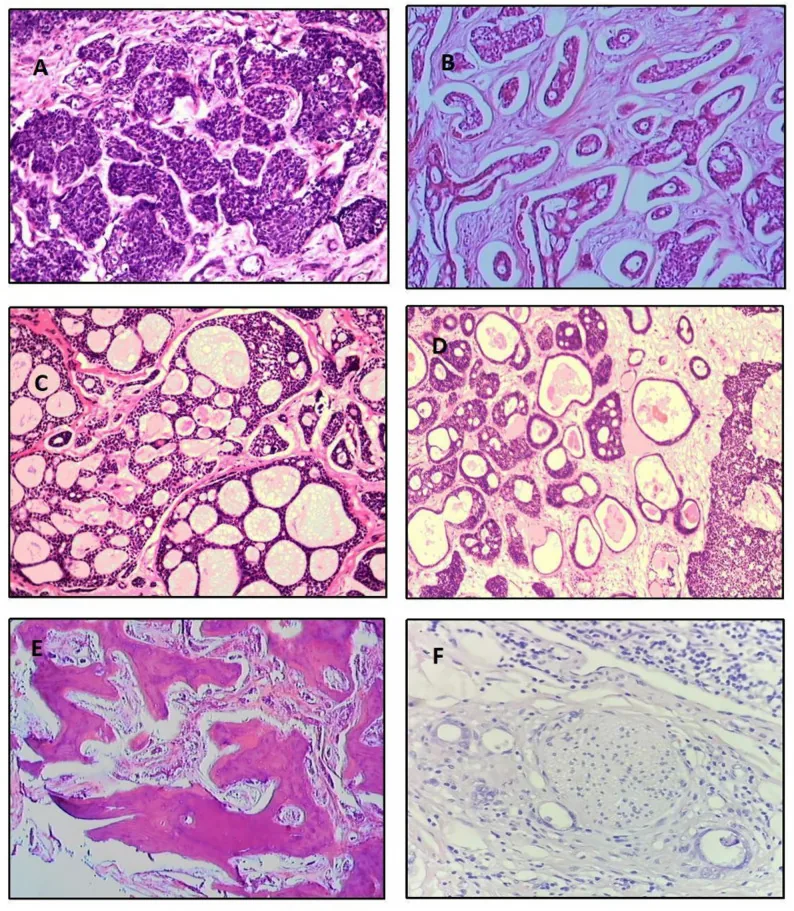
فراوانی زیرگروههای بافتی بر اساس تحلیل 515 مورد به شرح زیر است5).
نوع کریبریفرم
فراوانی: شایعترین (39.8%)
ویژگیها: ساختار لوبولار با حوضچههای دایرهای موسین. ظاهر «پنیر سوئیسی». پیشآگهی متوسط.
نوع بازالوئید
فراوانی: 31.8%
ویژگیها: تمایز ضعیف. هستههای بزرگ بازوفیل و سیتوپلاسم کم. بدترین پیشآگهی.
نوع توبولار
فراوانی: 7.4%
ویژگی: لولههای اپیتلیال پوشیده شده با ۲ تا ۳ لایه سلول. بیشترین تمایز و بهترین پیشآگهی.
سایر انواع شامل مختلط (13.9%)، تمایزنیافته (6.1%) و اسکلروزان (0.9%) هستند. اگر الگوی جامد بیش از 30% باشد، پیشآگهی ضعیف در نظر گرفته میشود1). از نظر بافتشناسی، سلولهای تومور کوچک، سیتوپلاسم کم و مایل به آبی، و هستههای غنی از کروماتین دارند. مرز بین جزایر تومور و استروما واضح است و به وضوح از آدنوم پلئومورفیک متفاوت است.
جراحی اساس درمان است و روش جراحی بر اساس مرحله تومور و یافتههای تصویربرداری تعیین میشود3)5).
تحلیل کاپلان-مایر نشان داد که جراحی حفظ چشم به همراه رادیوتراپی نسبت به اکسانتراسیون با یا بدون رادیوتراپی بقای بهتری دارد (P<0.05)5).
اگر تومور در تصویربرداری کوچک و قابل برداشت کامل باشد، هدف برداشت کامل است. اگر برداشت کامل غیرممکن تشخیص داده شود، پس از تأیید پاتولوژی با بیوپسی، برداشت وسیع یا رادیوتراپی در نظر گرفته میشود. در کارسینوم آدنوئید کیستیک غده اشکی که تومور محدود به حدقه است، اکسانتراسیون مد نظر قرار میگیرد، اما با توجه به مسائل زیبایی و سن و خواست بیمار، ممکن است درمان محافظهکارانه انتخاب شود. متاستاز لنفاوی نادر است (4-9%) و معمولاً نیاز به لنفادنکتومی نیست6).
حتی با انجام برداشت وسیع و پرتودرمانی، گاهی نمیتوان از نفوذ تومور از طریق عصب اشکی به ساقه مغز جلوگیری کرد. همچنین نمیتوان مطمئن بود که از متاستاز دوردست جلوگیری شود و پیگیری طولانیمدت ضروری است.
برای کارسینوم آدنوئید کیستیک غیرقابل جراحی، پرتودرمانی با ذرات سنگین انجام میشود و به عنوان یک روش درمانی امیدوارکننده که میتواند تومور را در عین حفظ پلک، کره چشم و حدقه کنترل کند، در نظر گرفته میشود.
NIAC اولین بار در سال ۱۹۹۸ توسط Meldrum و همکاران گزارش شد و از ترکیب تزریق شریانی سیسپلاتین (۱۰۰ میلیگرم بر متر مربع) و تزریق وریدی دوکسوروبیسین استفاده میکند3)2).
در مطالعه ۱۹ موردی Tse و همکاران (۲۰۱۳)، در ۸ موردی که شریان اشکی حفظ شده و پروتکل رعایت شده بود، نرخ بقای بدون بیماری ۱۰ ساله ۱۰۰٪ گزارش شده است2)3).
ترکیب NIAC + برداشت/تخلیه حدقه + پرتودرمانی در مقایسه با سایر روشهای درمانی نتایج بهتری با نرخ عود ۱۰.۸٪، متاستاز ۱۴.۹٪ و مرگومیر ۱۸.۹٪ نشان میدهد5). خطرات اصلی NIAC شامل فلج موقت عصب صورت، از دست دادن بینایی، ایسکمی قدامی، نوتروپنی و ترومبوسیتوپنی است3).
تحلیل کاپلان-مایر نشان داد که بقا در جراحی حفظ چشم به همراه پرتودرمانی بهتر از انوسکلئاسیون با یا بدون پرتودرمانی است (P<0.05) 5). برای تومورهای T1-T2 حفظ چشم توصیه میشود و برای تومورهای T3-T4 یا موارد با گسترش خارج حدقه، انوسکلئاسیون در نظر گرفته میشود. با این حال، به دلیل مسائل زیبایی یا خواست بیمار، ممکن است درمان محافظهکارانه انتخاب شود.
سلولهای توموری کوچک، با سیتوپلاسم کم و مایل به آبی، و هستههای غنی از کروماتین هستند. از نظر بافتشناسی، مرز بین تودههای توموری و استروما واضح است و به وضوح از آدنوم پلئومورفیک متمایز است.
در نوع کریبریفرم، لومنهای واقعی (منشأ گرفته از سلولهای مجرایی) و لومنهای کاذب (حاوی موسین که توسط سلولهای میواپیتلیال تشکیل شدهاند) با هم مخلوط میشوند و ظاهری شبیه «پنیر سوئیسی» ایجاد میکنند. نوع اسکلروتیک به صورت طنابهای سلولهای اپیتلیال همراه با استرومای هیالینیزه متراکم دیده میشود. اگر الگوی جامد بیش از 30% باشد، پیشآگهی ضعیف تلقی میشود 1).
الگوهای رشد تومور به پنج نوع (کریبریفرم، جامد، اسکلروتیک، کومدوسارکوماتوز و لولهای) طبقهبندی میشوند. در یک نمونه میتوان چندین الگوی رشد را مشاهده کرد.
| ناهنجاری مولکولی | توضیح |
|---|---|
| همجوشی MYB-NFIB | جابهجایی t(6;9)(q23;p23). در بیش از 70% کارسینوم آدنوئید کیستیک وجود دارد1) |
| بیان بیش از حد MYB | تکثیر سلولی، تمایز، رگزایی و تنظیم افزایشی فاکتورهای رشد را تقویت میکند1) |
| جهش فعالکننده NOTCH1 | محرک اصلی تکثیر و تهاجم در کارسینوم آدنوئید کیستیک متاستاتیک1)2) |
| جهشهای KRAS/NRAS/MET | به ترتیب در 46%، 8% و 13% گزارش شده است. آبشار EGFR-RAS-RAF ممکن است هدف درمانی باشد1)5) |
در کارسینوم آدنوئید کیستیک غده اشکی، بازآرایی MYB در 58% موارد تشخیص داده شده است (Mayo Clinic، 12 مورد/25 سال)، و همجوشی MYB-NFIB یک نشانگر تشخیصی بسیار اختصاصی برای کارسینوم آدنوئید کیستیک است1). همجوشی MYB-NFIB توسط سیگنالدهی IGF1R وابسته به AKT تنظیم میشود و مهار IGF1R به عنوان یک هدف درمانی امیدوارکننده در نظر گرفته میشود1)3).
تهاجم اطراف عصبی در 45.3% موارد مشاهده میشود و سلولهای توموری حتی بدون تهاجم عروقی یا لنفاوی منتشر میشوند1). تمایل شدیدی به تهاجم به اعصاب و عروق لنفاوی دارد و میتواند از مراحل اولیه از طریق عصب اشکی به ساقه مغز نفوذ کند. تهاجم اطراف عصبی با مقاومت به آپوپتوز ناشی از تنظیم افزایشی Bcl-2 مرتبط است.
در حال حاضر هیچ داروی هدفمند مولکولی برای کارسینوم آدنوئید کیستیک غده اشکی تأیید نشده است. موارد زیر به عنوان اهداف در مرحله تحقیقاتی بررسی شدهاند1)3).
نتایج کارآزماییهای بالینی فاز II نشان داده است: دوویتینیب (ORR 6%، mPFS 8.2 ماه)، لنواتینیب (ORR 16%، mPFS 17.5 ماه)، و آکسیتینیب (ORR 9%، mPFS 5.7 ماه)3).
Yu و همکاران (2022) ارزیابی ترکیبی از توالییابی ژنومی قبل و بعد از درمان و آنالیز نشانگرهای آپوپتوز (cCas3، PARP) را گزارش کردند2). فراوانی آلل جهشیافته (VAF) جهش NOTCH1 پس از NIAC از 18.07% قبل از درمان به 11.34% (کاهش 37%) پس از درمان کاهش یافت که نشاندهنده پتانسیل آن به عنوان یک نشانگر پیشبینیکننده حساسیت به سیسپلاتین است.
در حال حاضر هیچ داروی هدفمند مولکولی تأیید شدهای برای کارسینوم آدنوئید کیستیک غده اشکی وجود ندارد. همجوشی MYB-NFIB، مسیر سیگنالینگ Notch، و آبشار EGFR-RAS-RAF به عنوان اهداف درمانی در مرحله تحقیقاتی بررسی میشوند و چندین کارآزمایی بالینی فاز II در حال انجام است1)3). در صورت تمایل به درمان استاندارد، ترکیب جراحی و پرتو درمانی گزینه فعلی است.