淚腺腺樣囊狀癌(LGACC)是一種發生在淚腺的罕見惡性上皮性腫瘤,約佔所有眼眶 腫瘤的1.6%。
神經周圍浸潤 (45-85%)常見,疼痛是與良性腫瘤的重要鑑別點。從疾病早期就可能經由淚腺神經浸潤至腦幹,即使廣泛切除也可能難以阻止。
最常見的組織學亞型是篩狀型(39.8%),而基底細胞樣型(31.8%)預後最差。
標準治療是手術(保留眼球或眼眶 內容物剜除)合併術後放射治療。
據報告,5年存活率約為19-55%,10年存活率為20-30%;約50%發生肺、骨等遠處轉移。
針對MYB-NF IB融合基因和Notch訊息傳導路徑的分子標靶治療正在研究中。
腺樣囊狀癌(ACC)是一種發生在分泌腺的罕見惡性腫瘤,全球發生率為每百萬人3-4例1) 。它約佔所有頭頸部癌的1%,發生在淚腺時稱為淚腺腺樣囊狀癌1) 。
淚腺腺樣囊狀癌約佔所有眼眶 腫瘤的1.6%3) 5) ,是淚腺最常見的惡性上皮性腫瘤,佔淚腺癌的約13-40%5) 。淚腺腫瘤 約佔眼眶 佔位性病變的10%;實體淚腺腫瘤 中約20%為上皮源性,其中約45%為惡性,惡性上皮性淚腺腫瘤 中約60%為腺樣囊狀癌。
淚腺腺樣囊狀癌由Theodor Billroth首次描述,因其組織學特徵最初被命名為「圓柱瘤」5) 。
流行病學特徵 如下。
平均診斷年齡 :42.7±12.5歲(範圍9~76歲)。兒童病例佔5.9%,40歲以下佔41.9%5) 性別差異 :大規模彙整數據顯示女性略多(女性53.8%,男性46.2%)5) 。另一方面,也有報告稱男性較多,文獻間存在差異。左右差異 :幾乎無差異(右49.3%,左50.5%)。雙側極為罕見5) 預後 :5年存活率19.455.3%(806例大規模回顧)5) ,10年存活率2030%,預後不良。遠端轉移 :約50%發生肺、骨等遠端轉移。
Q
淚腺腺樣囊狀癌有多罕見?
A
約佔所有眼眶 腫瘤的1.6%,腺樣囊狀癌的全球發生率為每百萬人3~4例,極為罕見1) 5) 。在淚腺惡性上皮性腫瘤中是最常見的組織學類型。
根據806例的大規模回顧,初發症狀的頻率如下5) 。
症狀 頻率 眼球突出 27.4% 疼痛 21.7% 眼瞼腫脹 10.9% 眼球偏位 10.2% 眼球運動受限 10.1% 視力 下降9.3% 複視 6.7% 眼瞼下垂 4.1%
疼痛是腺樣囊狀癌特有的症狀,由神經周圍浸潤 (PNI)引起。這是與良性腫瘤的重要鑑別點。由於淚腺位於眼眶 外上方,眼球常向內下方偏移。也可能出現額顳部感覺減退或S形眼瞼下垂 。從症狀出現到診斷平均需要11.1±18.3個月(範圍0.5~120個月)5) 。
腫瘤的生長速度比多形性腺瘤快,且較容易伴隨疼痛,這是鑑別的重要點。隨著腫瘤增大,眼球突出 、外眼肌和神經浸潤導致的眼球運動受限、以及視神經 壓迫引起的視力 下降也相對快速進展。
Q
如何區分淚腺腺樣囊性癌和良性淚腺腫瘤?
A
有無疼痛是最重要的鑑別點。腺樣囊性癌 因神經周圍浸潤 而伴有疼痛,而良性腫瘤(如多形性腺瘤)無痛且緩慢進展。如果CT顯示骨破壞,可判斷為惡性,但也存在無骨破壞的腺樣囊性癌 ,因此如有疼痛,應積極考慮切片檢查。
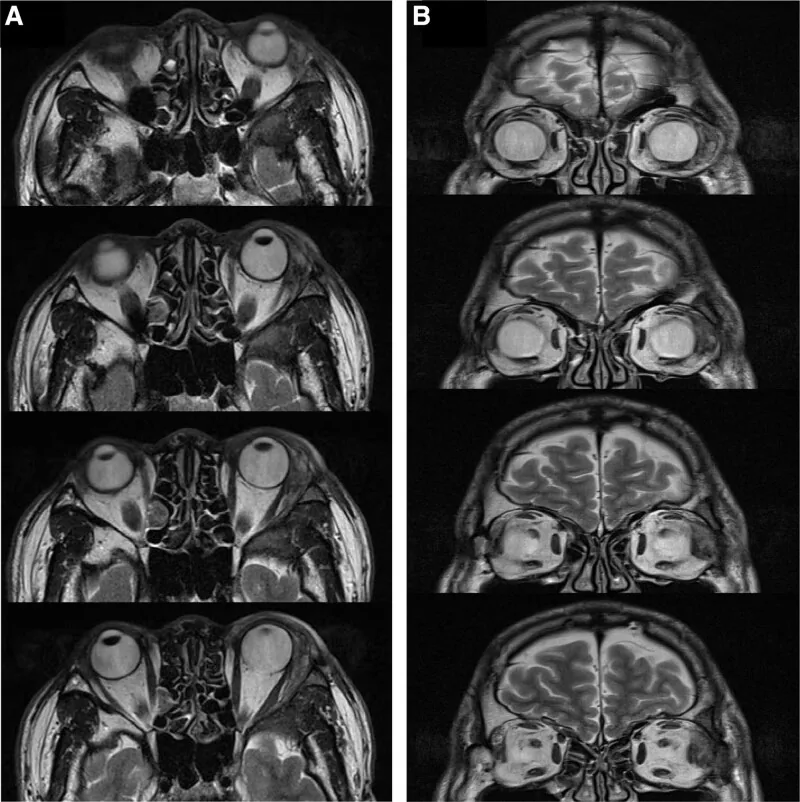
淚腺腺樣囊性癌的T2加權MRI(軸位和冠狀位):左眼眶外上方可見高信號腫塊,顯示眼眶骨壁浸潤 Liang M, Yu Z, Wang F. A case report: An unusual presentation of adenoid cystic carcinoma of the lacrimal gland. Medicine (Baltimore). 2023;102(13):e33446. Figure 1. PM
CI D: PMC10063268. License: CC BY 4.0.
T2加權軸位像(A)和冠狀位像(B)顯示左眼眶 外上方淚腺區域邊界不清的高信號腫塊,伴有眼眶 骨壁浸潤,但骨膜保留。這與本文「2. 主要症狀和臨床所見」部分討論的MRI所見(淚腺窩腫塊、骨浸潤)相對應。
CT所見 :眼眶 外上方邊界不清的卵圓形軟組織塊。骨侵蝕見於35.3%的病例,局部鈣化見於2.2% 5) 。如果CT顯示骨破壞,可判斷為惡性,但也存在無骨破壞的病例。MRI所見 :T1加權像呈等至高信號,T2加權像最常見為高信號。增強後顯示瀰漫性強化 5) 。擴散加權MRI :低ADC值(反映高細胞密度)有助於與良性病變鑑別 5) 。
根據Williams等人的報告,組織學上82%的患者確認有淚腺窩浸潤 1) 。如果CT顯示腫瘤破壞眼眶 骨,可判斷為惡性,但需注意也存在無骨破壞的腺樣囊性癌 。
腺樣囊性癌 的病因不明,尚未確定特定的風險因素。腫瘤最常發生於淚腺的眼眶 葉,是一種無包膜的腫瘤。
以下病理學和臨床特徵被認為是預後不良因素。
神經周圍浸潤 5) ,是最重要的預後不良因素之一。它可能通過淚腺神經浸潤腦幹,且可能在疾病早期發生。即使進行廣泛切除和放射治療,也可能無法阻止腦幹浸潤。基底細胞樣變異型 :預後不良的組織學類型 5) 。高T分期 :T3以上復發與轉移風險顯著較高5) 遠端轉移 :血行性,最常見於肺(40.8%)、腦(25%)、骨(22.9%)、肝(17.4%)5) 。約50%病例發生遠端轉移p53與Bcl-2異常 :p53下調與Bcl-2上調導致之細胞凋亡 障礙與預後惡化相關
確診依賴病理組織學評估。若懷疑惡性,建議進行切除性切片檢查以防止腫瘤細胞在眼眶 內播散。細針抽吸切片檢查可能適用於無法切除之腫瘤,但僅限於有經驗豐富之細胞病理學家的機構。
若因眼球突出 等症狀懷疑淚腺腫瘤 ,應進行視力 、視野、眼球運動等眼科檢查,並實施單純CT及單純/顯影MRI影像學檢查。如需全身檢查,也可進行PET-CT或顯影CT。確診依賴切片或全切除後之病理組織學檢查。
T分期 定義 T1 最大徑≤2 cm T2 最大徑>2 cm至≤4 cm T3 最大徑>4 cm或眼眶 軟組織擴展 T4 侵犯鼻竇、顳窩、翼腭窩、眶上裂、海綿竇 或腦
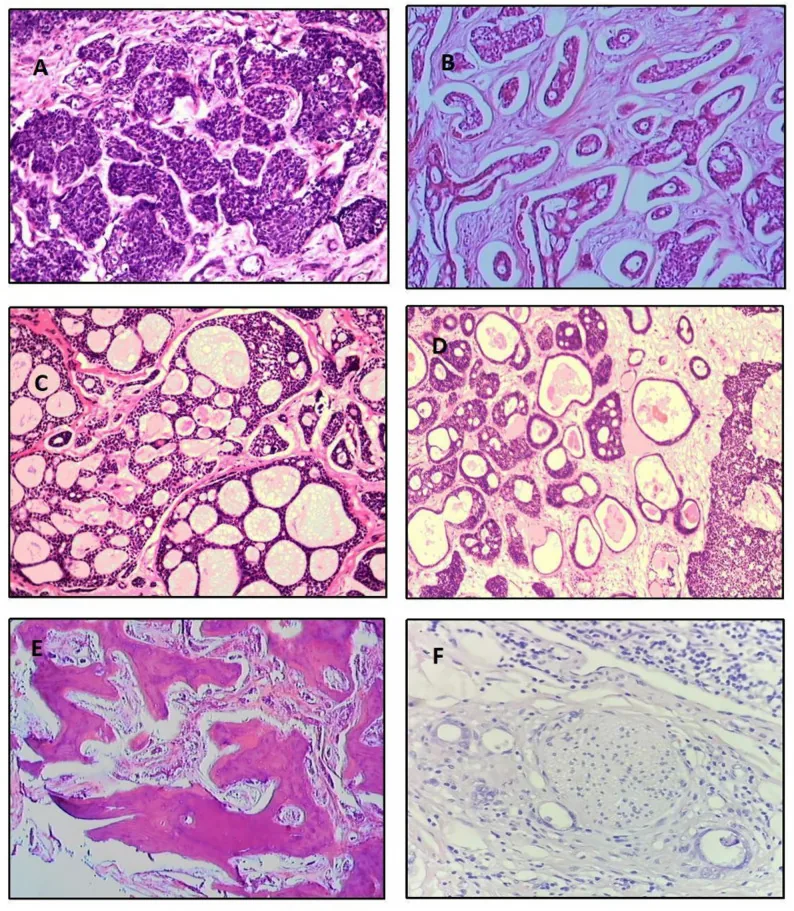
淚腺腺樣囊性癌的HE染色病理組織像:篩狀型、管狀型和實性基底細胞樣型,以及眼眶骨浸潤和神經周圍浸潤 Wu J, Cui H, Liang M, Wang F. Histological-pathological and clinical T stage of primary adenoid cystic carcinoma of the lacrimal gland in a Chinese population. BMC Cancer. 2025;26:110. Figure 1. PM
CI D: PMC12831414. License: CC BY 4.0.
HE染色的六面板病理組織像:A=實性基底細胞樣型,B=管狀型,C=篩狀型,D=管狀+篩狀混合型,E=腫瘤細胞引起的眼眶 骨浸潤,F=眼眶 神經鞘的神經周圍浸潤 (比例尺50-100 µm)。對應本文「4. 診斷與檢查方法」中討論的組織亞型分類和神經周圍浸潤 。
基於515例病例分析的組織亞型頻率如下5) 。
篩狀型
頻率 :最常見(39.8%)
特徵 :伴有圓形黏液池的小葉結構。「瑞士起司」樣外觀。中等預後。
基底細胞樣型
頻率 :31.8%
特徵 :低分化。大的嗜鹼性核和稀疏的細胞質。預後最差。
管狀型
頻率 :7.4%
特徵 :由2~3層細胞襯裡的上皮管。分化程度最高,預後最好。
其他類型包括混合型(13.9%)、未分化型(6.1%)和硬化型(0.9%)。實性成分超過30%被認為預後不良1) 。組織學上,腫瘤細胞小,細胞質少且呈嗜鹼性,核染色質豐富。腫瘤巢與間質邊界清晰,與多形性腺瘤明顯不同。
多形性腺瘤 :最常見的淚腺腫瘤 (良性)。無痛性,緩慢進展。有惡變可能。淋巴瘤/慢性淚腺炎 :需與發炎性疾病鑑別。反應性淋巴組織增生、類肉瘤病 、修格連氏症候群 :可表現為雙側淚腺腫大。其他惡性上皮性淚腺腫瘤 :多形性腺癌(20%)、原發性腺癌(10%)、黏液表皮樣癌(5%)。
手術是治療的基礎,術式根據腫瘤分期和影像學表現決定3) 5) 。
保留眼球手術(切除切片) :708例中447例(63.1%)施行。推薦用於T1~T2腫瘤5) 。眼窩內容剜除術 :708例中245例(34.6%)。適用於T3~T4腫瘤或眼窩尖/眼窩外侵犯病例5) 。
Kaplan-Meier分析顯示,保留眼球手術加放射治療的存活率優於眼窩內容剜除術±放射治療(P<0.05)5) 。
如果影像學顯示腫瘤較小且可完全切除,則爭取完全切除。若判斷無法完全切除,則行切取切片明確病理後,考慮廣泛切除或放射治療。對於侷限於眼窩內的淚腺腺樣囊狀癌,可考慮眼窩內容剜除術,但需根據美觀問題、患者年齡和意願選擇保守治療。淋巴結轉移罕見(4~9%),通常無需淋巴結廓清6) 。
即使進行廣泛切除和放射治療,仍可能無法阻止腫瘤經由淚腺神經向腦幹浸潤。並不一定能防止遠端轉移,因此需要長期追蹤。
術後輔助放射治療 :519例患者接受治療。體外照射最多(76.3%)5) 標準劑量 :常規分割照射2Gy/天,總劑量6066Gy(3033次分割)5) 6) 局部控制率 :單獨放射治療5年局部控制率可達50~80%,但改善存活率的證據有限6) R1切除後 :建議術後放射治療劑量為66Gy6) 有神經周圍浸潤 時 :通常考慮放射治療
對於無法手術的腺樣囊性癌 ,可採用重粒子治療,這是一種有希望保留眼瞼、眼球和眼眶 同時控制腫瘤的治療方法。
NIAC 於1998年由Meldrum等人首次報告,採用順鉑(100mg/m²)動脈內注射合併多柔比星靜脈注射的組合3) 2) 。
Tse等人(2013年)的19例研究中,在保留淚腺動脈並遵循方案的8例患者中,報告了10年無病存活率為100%2) 3) 。
NIAC 合併切除/眼眶 內容物剜除術及放射治療的組合,與其他治療方法相比,顯示出良好的結果:復發率10.8%,轉移率14.9%,死亡率18.9%5) 。NIAC 的主要風險包括暫時性顏面神經麻痺、視力 喪失、前部缺血、嗜中性白血球減少和血小板減少3) 。
輔助化療 :806例中135例(16.7%)接受治療。常用藥物包括順鉑(39.2%)、多柔比星(24.6%)和5-FU(10.7%)5) 新輔助化療 :806例中74例(9.2%)接受治療5) 輔助化學治療的添加,即使與放射治療合併,也未顯示統計學顯著差異(P=0.40)5)
淚腺腺樣囊狀癌復發及遠端轉移風險高,需要長期追蹤。
眼窩內容物剜除術根治性高,但美容損失大。應根據患者年齡、全身狀況及意願審慎決定術式。
NIAC 需在專業機構進行,有嚴重併發症(視力 喪失、顏面神經麻痺)的風險3) 。
Q
眼窩內容物剜除術與眼球保留手術何者較優?
A
Kaplan-Meier分析顯示,眼球保留手術加放射治療的存活率優於眼窩內容物剜除術±放射治療(P<0.05)5) 。T1~T2腫瘤建議眼球保留,T3~T4腫瘤或眼窩外擴展病例考慮眼窩內容物剜除術。但有時因美容問題或患者意願選擇保守治療。
腫瘤細胞小,細胞質少且呈藍染,核染色質豐富。組織學上腫瘤巢與間質邊界清晰,與多形性腺瘤明顯不同。
篩狀型中,真腔(來源於導管 細胞)和假腔(肌上皮細胞形成的黏液滯留腔)並存,呈「瑞士起司」樣外觀。硬化型表現為伴有緻密玻璃樣變間質的上皮細胞索。實性成分超過30%預後不良1) 。
腫瘤生長模式分為五種:篩狀、實性、硬化型、粉刺癌樣和管狀。同一標本內可觀察到多種生長模式。
分子異常 內容 MYB-NF IB融合 t(6;9)(q23;p23)轉位。存在於70%以上的腺樣囊性癌 中1) MYB過度表現 促進細胞增殖、分化、血管新生和生長因子上調1) NOTCH1活化突變 轉移性腺樣囊性癌 增殖和侵襲的主要驅動因素1) 2) KRAS/NRAS/MET突變 分別報告於46%、8%和13%的病例。EGFR-RAS-RAF級聯可能是治療靶點1) 5)
在淚腺腺樣囊性癌 中,58%的病例檢測到MYB重排(梅奧診所,12例/25年),MYB-NF IB融合是腺樣囊性癌 高度特異的診斷標誌物1) 。MYB-NF IB融合受AKT依賴性IGF1R信號調控,IGF1R抑制被認為是有前景的治療靶點1) 3) 。
45.3%的病例出現神經周圍浸潤 ,即使沒有血管或淋巴管浸潤,腫瘤細胞也能傳播1) 。有很強的侵犯神經和淋巴管的傾向,疾病早期即可通過淚腺神經浸潤至腦幹。神經周圍浸潤 與Bcl-2上調導致的凋亡抵抗有關。
目前尚無核准用於淚腺腺樣囊性癌 的分子標靶藥物。以下標靶正在研究階段中探討1) 3) 。
EGFR-TKI(erlotinib) :一例轉移性淚腺腺樣囊性癌 患者報告有效14個月3) IGF1R抑制 :Figitumumab(IGF1R單株抗體)合併dacomitinib(pan-EGFR抑制劑)治療一例,報告病情穩定1.5年3) FGFR1抑制劑AZD4547+cisplatin :NIAC 後FGFR1訊號升高,合併用藥顯示增強的殺腫瘤效果3) Survivin抑制 :腺樣囊性癌 中Survivin高度表現。三氧化二砷(As₂O₃)抑制Survivin mRNA表現並誘導細胞凋亡 3)
第二期臨床試驗結果報告了dovitinib(ORR 6%,mPFS 8.2個月)、lenvatinib(ORR 16%,mPFS 17.5個月)和axitinib(ORR 9%,mPFS 5.7個月)3) 。
TetMYB疫苗+抗PD1抗體 :第一期臨床試驗正在進行中1) Notch1抑制劑(AL101) :γ-分泌酶抑制劑的第二期ACCURACY試驗正在進行中1)
Yu等人(2022)報告了結合治療前後基因組定序和細胞凋亡 標誌物(cCas3、PARP )分析的評估2) 。NIAC 後NOTCH1突變的變異等位基因頻率(VAF)從治療前的18.07%降至治療後的11.34%(減少37%),提示其可能成為cisplatin敏感性的預測標誌物。
質子束治療 (PRT)3) 碳離子放射治療(CI RT) :一項24例的研究報告2年局部控制率93%、整體存活率96%、無病存活率87%3) VMAT(體積調控弧形治療) :在66 Gy/33次分割的案例中,急性毒性輕微(第1級皮膚炎)。已確認24個月以上無復發6)
Q
淚腺腺樣囊性癌是否可使用分子標靶治療?
A
目前尚無針對淚腺腺樣囊性癌 核准的分子標靶藥物。MYB-NF IB融合、Notch訊息傳導路徑、EGFR-RAS-RAF級聯等正作為研究階段的治療標靶進行探討,多項第二期臨床試驗正在進行中1) 3) 。希望接受標準治療的患者,目前的選擇是手術與放射治療的組合。
Powell SK, Kulakova K, Kennedy S. A Review of the Molecular Landscape of Adenoid Cystic Carcinoma of the Lacrimal Gland. Int J Mol Sci. 2023;24(18):13755.
Yu MD, Men CJ, Do H, et al. Genome Sequencing and Apoptotic Markers to Assess Treatment Response of Lacrimal Gland Adenoid Cystic Carcinoma to Intra-Arterial Cytoreductive Chemotherapy. Ophthalmic Plast Reconstr Surg. 2022;38(2):e44-e47.
Wang X, Ma H, Chen Y, et al. Treatment strategies and prognostic insights for lacrimal gland adenoid cystic carcinoma: a review. Discover Oncology. 2025;16:858.
(統合済み:PMC11567613はPMC12098222と同一論文と判断し引用3に統合)
Pal SS, Alam MS , Manikantan K, Honavar S. Adenoid cystic carcinoma of the lacrimal gland - A major review. Indian J Ophthalmol. 2025;73:1399-1411.
Benali K, Benmessaoud H, Aarab J, et al. Lacrimal gland adenoid cystic carcinoma: report of an unusual case with literature review. Radiat Oncol J. 2021;39(2):152-158.
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。