Type cribriforme
Fréquence : le plus fréquent (39,8 %)
Caractéristiques : structures lobulaires avec des espaces ronds remplis de mucine. Aspect « en fromage suisse ». Pronostic intermédiaire.

Le carcinome adénoïde kystique (ACC) est une tumeur maligne rare des glandes sécrétoires, avec une incidence mondiale de 3 à 4 cas par million d’habitants 1). Il représente environ 1 % de tous les cancers de la tête et du cou, et lorsqu’il se développe dans la glande lacrymale, on l’appelle carcinome adénoïde kystique de la glande lacrymale 1).
Le carcinome adénoïde kystique de la glande lacrymale représente environ 1,6 % de toutes les tumeurs orbitaires 3)5), et est la tumeur épithéliale maligne la plus fréquente de la glande lacrymale, constituant environ 13 à 40 % des cancers lacrymaux 5). Les tumeurs lacrymales représentent environ 10 % des lésions orbitaires occupant de l’espace, environ 20 % des tumeurs lacrymales solides sont d’origine épithéliale, dont environ 45 % sont malignes, et environ 60 % des tumeurs épithéliales malignes lacrymales sont des carcinomes adénoïdes kystiques.
Le carcinome adénoïde kystique de la glande lacrymale a été décrit pour la première fois par Theodor Billroth, et en raison de ses caractéristiques histologiques, il a été initialement nommé « cylindrome » 5).
Les caractéristiques épidémiologiques sont les suivantes.
Il représente environ 1,6 % de toutes les tumeurs orbitaires, et l’incidence mondiale du carcinome adénoïde kystique est extrêmement rare, avec 3 à 4 cas par million d’habitants1)5). C’est le type histologique le plus fréquent parmi les tumeurs épithéliales malignes de la glande lacrymale.
Selon une grande revue de 806 cas, la fréquence des symptômes initiaux est la suivante5).
| Symptôme | Fréquence |
|---|---|
| Exophtalmie | 27,4 % |
| Douleur | 21,7 % |
| Œdème palpébral | 10,9 % |
| Déviation du globe oculaire | 10,2 % |
| Limitation des mouvements oculaires | 10,1 % |
| Baisse de l’acuité visuelle | 9,3 % |
| Diplopie | 6,7 % |
| Ptosis | 4,1 % |
La douleur est un symptôme caractéristique du carcinome adénoïde kystique, provoqué par l’infiltration périneurale (PNI). C’est un point de différenciation important avec les tumeurs bénignes. Le globe oculaire est souvent dévié vers le bas et l’intérieur car la glande lacrymale est située dans la partie supéro-externe de l’orbite. Une hypoesthésie fronto-temporale ou un ptosis en forme de S peuvent également se présenter. Le délai moyen entre l’apparition des symptômes et le diagnostic est de 11,1 ± 18,3 mois (intervalle de 0,5 à 120 mois) 5).
La vitesse de croissance de la tumeur est plus rapide que celle de l’adénome pléomorphe, et elle s’accompagne souvent de douleurs, ce qui constitue un point clé pour le diagnostic différentiel. L’exophtalmie due à l’augmentation de la tumeur, la limitation des mouvements oculaires par infiltration des muscles extra-oculaires et des nerfs, ainsi que la baisse de l’acuité visuelle par compression du nerf optique progressent également relativement rapidement.
La présence ou l’absence de douleur est le point de différenciation le plus important. Le carcinome adénoïde kystique provoque des douleurs par infiltration périneurale, tandis que les tumeurs bénignes (comme l’adénome pléomorphe) sont indolores et progressent lentement. Si la tomodensitométrie montre une destruction osseuse, on peut conclure à une tumeur maligne, mais il existe des carcinomes adénoïdes kystiques sans destruction osseuse ; en cas de douleur, une biopsie doit être activement envisagée.
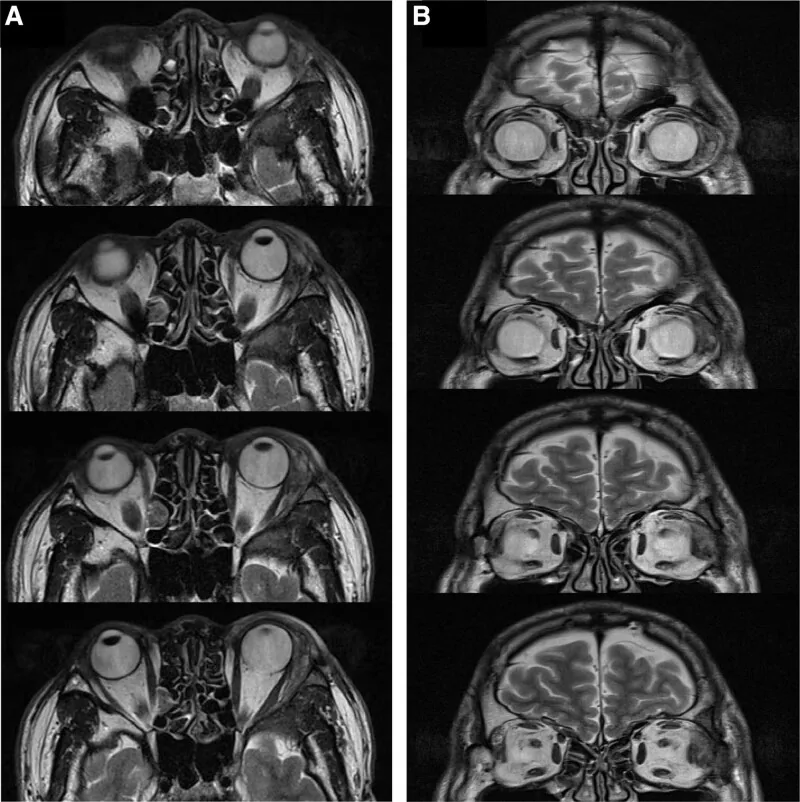
Selon le rapport de Williams et al., une infiltration de la fosse lacrymale a été confirmée histologiquement chez 82 % des patients1). Si la tomodensitométrie montre une destruction osseuse par la tumeur, on peut conclure à une tumeur maligne, mais il faut noter qu’il existe des carcinomes adénoïdes kystiques sans destruction osseuse.
La cause du carcinome adénoïde kystique est inconnue et aucun facteur de risque spécifique n’est établi. La tumeur provient le plus souvent du lobe orbitaire de la glande lacrymale et est une tumeur non encapsulée.
Les caractéristiques pathologiques et cliniques suivantes sont connues comme facteurs de mauvais pronostic :
Le diagnostic définitif repose sur l’évaluation histopathologique. En cas de suspicion de malignité, une biopsie excisionnelle est recommandée pour éviter la dissémination intrakystique des cellules tumorales. La cytoponction à l’aiguille fine peut être appropriée pour les tumeurs non résécables, mais uniquement dans des établissements disposant d’un cytopathologiste expérimenté.
En cas de symptômes tels qu’une exophtalmie suggérant une tumeur lacrymale, des examens ophtalmologiques (acuité visuelle, champ visuel, motilité oculaire) sont réalisés, ainsi qu’une imagerie par tomodensitométrie (TDM) simple et IRM avec et sans contraste. Si une recherche systémique est nécessaire, une TEP-TDM ou une TDM avec contraste peut être effectuée. Le diagnostic définitif repose sur une biopsie ou un examen histopathologique après résection complète.
| Stade T | Définition |
|---|---|
| T1 | Diamètre maximal ≤ 2 cm |
| T2 | Diamètre maximal > 2 cm à ≤ 4 cm |
| T3 | Taille maximale > 4 cm ou extension aux tissus mous orbitaires |
| T4 | Invasion des sinus paranasaux, fosse temporale, fosse ptérygopalatine, fissure orbitaire supérieure, sinus caverneux ou cerveau |
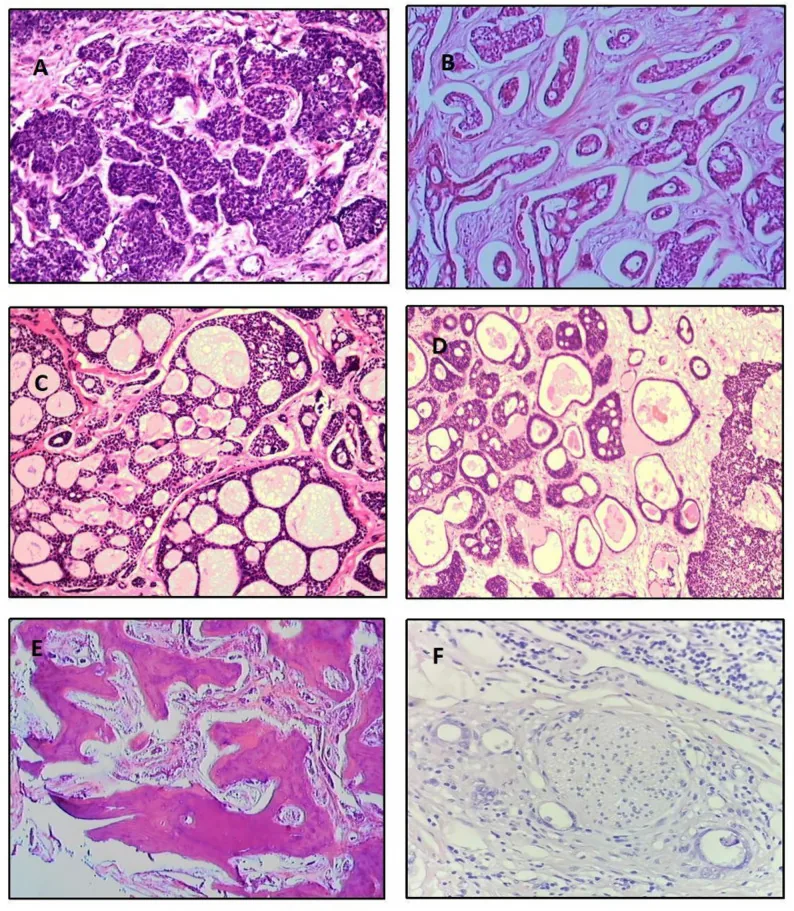
La fréquence des sous-types histologiques selon une analyse de 515 cas est la suivante 5).
Type cribriforme
Fréquence : le plus fréquent (39,8 %)
Caractéristiques : structures lobulaires avec des espaces ronds remplis de mucine. Aspect « en fromage suisse ». Pronostic intermédiaire.
Type basaloïde
Fréquence : 31,8 %
Caractéristiques : peu différencié. Noyaux basophiles volumineux et cytoplasme rare. Pronostic le plus défavorable.
Type tubulaire
Fréquence : 7,4 %
Caractéristiques : Tubes épithéliaux bordés de 2 à 3 couches de cellules. Le plus différencié, meilleur pronostic.
Il existe également des types mixtes (13,9 %), indifférenciés (6,1 %) et sclérosants (0,9 %). Un motif solide >30 % est considéré comme de mauvais pronostic1). Histologiquement, les cellules tumorales sont petites, avec un cytoplasme peu abondant et basophile, et un noyau riche en chromatine. La limite entre les îlots tumoraux et le stroma est nette, nettement différente de l’adénome pléomorphe.
La chirurgie est le traitement de base, et la technique est déterminée par le stade tumoral et les résultats d’imagerie3)5).
L’analyse de Kaplan-Meier a montré que la chirurgie conservatrice + radiothérapie avait un meilleur taux de survie que l’exentération orbitaire ± radiothérapie (P < 0,05)5).
Si l’imagerie montre une tumeur petite et complètement résécable, on vise une résection complète. Si la résection complète est jugée impossible, on réalise une biopsie pour confirmer la pathologie, puis on envisage une résection large ou une radiothérapie. Pour le carcinome adénoïde kystique lacrymal confiné à l’orbite, on peut envisager une exentération, mais on peut aussi choisir un traitement conservateur en tenant compte des problèmes esthétiques, de l’âge et des souhaits du patient. Les métastases ganglionnaires sont rares (4-9 %) et le curage ganglionnaire n’est généralement pas nécessaire6).
Même après une résection large et une radiothérapie, il peut être impossible d’empêcher l’infiltration du tronc cérébral via le nerf lacrymal. On ne peut pas non plus garantir la prévention des métastases à distance, et un suivi à long terme est nécessaire.
Pour les carcinomes adénoïdes kystiques inopérables, la radiothérapie par faisceau de particules lourdes est pratiquée et est considérée comme un traitement prometteur permettant de contrôler la tumeur tout en préservant les paupières, le globe oculaire et l’orbite.
La CIAN a été rapportée pour la première fois par Meldrum et al. en 1998, utilisant une combinaison de cisplatine intra-artériel (100 mg/m²) et de doxorubicine intraveineuse 3)2).
Dans une étude de Tse et al. (2013) portant sur 19 patients, un taux de survie sans maladie à 10 ans de 100 % a été rapporté chez 8 patients chez qui l’artère lacrymale a été préservée et le protocole respecté 2)3).
La combinaison CIAN + résection/éviscération orbitaire + radiothérapie montre de bons résultats par rapport aux autres traitements, avec un taux de récidive de 10,8 %, un taux de métastase de 14,9 % et un taux de mortalité de 18,9 % 5). Les principaux risques de la CIAN comprennent la paralysie faciale transitoire, la perte de vision, l’ischémie antérieure, la neutropénie et la thrombocytopénie 3).
L’analyse de Kaplan-Meier a montré que la survie après chirurgie conservatrice de l’œil plus radiothérapie était meilleure qu’après exentération orbitaire ± radiothérapie (P<0,05)5). La conservation de l’œil est recommandée pour les tumeurs T1-T2, tandis que l’exentération orbitaire est envisagée pour les tumeurs T3-T4 ou avec extension extra-orbitaire. Cependant, un traitement conservateur peut être choisi en raison de problèmes esthétiques ou des souhaits du patient.
Les cellules tumorales sont petites, avec un cytoplasme peu abondant et bleuté, et des noyaux riches en chromatine. Histologiquement, la limite entre les îlots tumoraux et le stroma est nette, clairement différente de l’adénome pléomorphe.
Dans le type cribriforme, les lumières vraies (dérivées des cellules canalaires) et les pseudo-lumières (cavités de mucine formées par les cellules myoépithéliales) coexistent, donnant un aspect « en fromage suisse ». Le type sclérosant se présente sous forme de cordons de cellules épithéliales avec un stroma hyalinisé dense. Un motif solide dépassant 30 % est associé à un mauvais pronostic1).
Les schémas de croissance tumorale sont classés en cinq types (cribriforme, solide, sclérosant, comédocarcinomateux, tubulaire). Plusieurs schémas de croissance peuvent être observés dans un même échantillon.
| Anomalie moléculaire | Description |
|---|---|
| Fusion MYB-NFIB | Translocation t(6;9)(q23;p23). Présente dans plus de 70% des carcinomes adénoïdes kystiques1) |
| Surexpression de MYB | Favorise la prolifération cellulaire, la différenciation, l’angiogenèse et la régulation positive des facteurs de croissance1) |
| Mutation activatrice de NOTCH1 | Principal moteur de la prolifération et de l’invasion dans le carcinome adénoïde kystique métastatique1)2) |
| Mutations KRAS/NRAS/MET | Rapportées dans 46%, 8% et 13% des cas respectivement. La cascade EGFR-RAS-RAF pourrait être une cible thérapeutique1)5) |
Dans le carcinome adénoïde kystique lacrymal, un réarrangement de MYB est détecté dans 58% des cas (Mayo Clinic, 12 cas/25 ans), et la fusion MYB-NFIB est un marqueur diagnostique hautement spécifique du carcinome adénoïde kystique1). La fusion MYB-NFIB est régulée par le signal IGF1R dépendant d’AKT, et l’inhibition d’IGF1R est considérée comme une cible thérapeutique prometteuse1)3).
L’infiltration périneurale est observée dans 45,3% des cas et permet la propagation des cellules tumorales même en l’absence d’infiltration vasculaire ou lymphatique1). Il existe une forte tendance à l’infiltration des nerfs et des vaisseaux lymphatiques, et une infiltration du tronc cérébral via le nerf lacrymal peut survenir dès le début de la maladie. L’infiltration périneurale serait associée à une résistance à l’apoptose due à la régulation positive de Bcl-2.
À l’heure actuelle, aucun médicament de thérapie ciblée moléculaire n’est approuvé pour le carcinome adénoïde kystique des glandes lacrymales. Les cibles suivantes sont à l’étude 1)3).
Les résultats d’essais cliniques de phase II rapportent : dovitinib (ORR 6%, mPFS 8,2 mois), lenvatinib (ORR 16%, mPFS 17,5 mois), axitinib (ORR 9%, mPFS 5,7 mois) 3).
Yu et al. (2022) ont rapporté une évaluation combinant le séquençage génomique avant et après traitement et l’analyse des marqueurs d’apoptose (cCas3, PARP) 2). La fréquence allélique de la mutation NOTCH1 après NIAC a diminué de 18,07 % avant traitement à 11,34 % après traitement (réduction de 37 %), suggérant un potentiel biomarqueur prédictif de la sensibilité au cisplatine.
À l’heure actuelle, aucun traitement ciblé moléculaire n’est approuvé pour le carcinome adénoïde kystique de la glande lacrymale. La fusion MYB-NFIB, la voie de signalisation Notch, la cascade EGFR-RAS-RAF, etc., sont étudiées comme cibles thérapeutiques potentielles, et plusieurs essais cliniques de phase II sont en cours1)3). Pour les patients souhaitant un traitement standard, la combinaison de la chirurgie et de la radiothérapie reste l’option actuelle.