क्रिब्रीफॉर्म प्रकार
आवृत्ति: सबसे अधिक (39.8%)
विशेषताएँ: म्यूसिन के गोल पूल के साथ लोब्यूलर संरचनाएँ। ‘स्विस चीज़’ जैसा दिखावट। मध्यम पूर्वानुमान।

एडेनॉइड सिस्टिक कार्सिनोमा (ACC) स्रावी ग्रंथियों का एक दुर्लभ घातक ट्यूमर है, जिसकी वैश्विक घटना प्रति मिलियन जनसंख्या पर 3-4 मामले हैं 1)। यह सभी सिर और गर्दन के कैंसर का लगभग 1% होता है, और लैक्रिमल ग्रंथि में होने पर इसे लैक्रिमल ग्रंथि एडेनॉइड सिस्टिक कार्सिनोमा कहा जाता है 1)।
लैक्रिमल ग्रंथि एडेनॉइड सिस्टिक कार्सिनोमा सभी ऑर्बिटल ट्यूमर का लगभग 1.6% होता है 3)5), और लैक्रिमल ग्रंथि के घातक उपकला ट्यूमर में सबसे आम है, जो लैक्रिमल कैंसर का लगभग 13-40% बनाता है 5)। लैक्रिमल ग्रंथि ट्यूमर ऑर्बिटल स्पेस-अधिग्रहण घावों का लगभग 10% होते हैं, ठोस लैक्रिमल ट्यूमर का लगभग 20% उपकला मूल के होते हैं, जिनमें से लगभग 45% घातक होते हैं, और घातक उपकला लैक्रिमल ट्यूमर का लगभग 60% एडेनॉइड सिस्टिक कार्सिनोमा होता है।
लैक्रिमल ग्रंथि एडेनॉइड सिस्टिक कार्सिनोमा का वर्णन सबसे पहले थियोडोर बिलरोथ ने किया था, और हिस्टोलॉजिकल विशेषताओं के कारण इसे शुरू में ‘सिलिंड्रोमा’ नाम दिया गया था 5)।
महामारी विज्ञान संबंधी विशेषताएँ इस प्रकार हैं।
यह सभी कक्षीय ट्यूमर का लगभग 1.6% होता है, और एडेनॉइड सिस्टिक कार्सिनोमा की वैश्विक घटना प्रति दस लाख जनसंख्या पर 3-4 मामले है, जो अत्यंत दुर्लभ है1)5)। यह लैक्रिमल ग्रंथि के घातक उपकला ट्यूमर में सबसे सामान्य हिस्टोलॉजिकल प्रकार है।
806 मामलों की बड़ी समीक्षा के अनुसार, प्रारंभिक लक्षणों की आवृत्ति इस प्रकार है5)।
| लक्षण | आवृत्ति |
|---|---|
| नेत्रगोलक का बाहर निकलना (एक्सोफ्थाल्मोस) | 27.4% |
| दर्द | 21.7% |
| पलक की सूजन | 10.9% |
| नेत्रगोलक का विचलन | 10.2% |
| नेत्र गति में प्रतिबंध | 10.1% |
| दृष्टि में कमी | 9.3% |
| द्विदृष्टि | 6.7% |
| पलक का गिरना (प्टोसिस) | 4.1% |
दर्द एडेनॉइड सिस्टिक कार्सिनोमा का एक विशिष्ट लक्षण है, जो पेरिन्यूरल आक्रमण (PNI) के कारण होता है। यह सौम्य ट्यूमर से महत्वपूर्ण अंतर है। नेत्रगोलक अक्सर अंदर और नीचे की ओर विचलित होता है क्योंकि लैक्रिमल ग्रंथि कक्षा के ऊपरी-बाहरी भाग में स्थित होती है। ललाट-टेम्पोरल क्षेत्र में संवेदना में कमी या S-आकार का प्टोसिस भी हो सकता है। लक्षणों की शुरुआत से निदान तक औसत समय 11.1 ± 18.3 महीने (सीमा 0.5 से 120 महीने) है 5).
ट्यूमर की वृद्धि दर प्लियोमॉर्फिक एडेनोमा से तेज़ होती है और इसमें दर्द होने की संभावना अधिक होती है, जो विभेदक निदान का एक महत्वपूर्ण बिंदु है। ट्यूमर के बढ़ने के कारण नेत्रगोलक का बाहर निकलना, बाह्य नेत्र पेशियों और तंत्रिकाओं में घुसपैठ के कारण नेत्र गति में प्रतिबंध, और ऑप्टिक तंत्रिका के संपीड़न के कारण दृष्टि में कमी भी अपेक्षाकृत तेज़ी से बढ़ती है।
दर्द की उपस्थिति या अनुपस्थिति सबसे महत्वपूर्ण विभेदक बिंदु है। एडेनॉइड सिस्टिक कार्सिनोमा में पेरिन्यूरल घुसपैठ के कारण दर्द होता है, जबकि सौम्य ट्यूमर (जैसे प्लियोमॉर्फिक एडेनोमा) दर्द रहित होते हैं और धीरे-धीरे बढ़ते हैं। यदि सीटी स्कैन में हड्डी का विनाश दिखाई देता है, तो इसे घातक माना जा सकता है, लेकिन बिना हड्डी विनाश वाले एडेनॉइड सिस्टिक कार्सिनोमा भी मौजूद होते हैं, इसलिए दर्द होने पर सक्रिय रूप से बायोप्सी पर विचार किया जाना चाहिए।
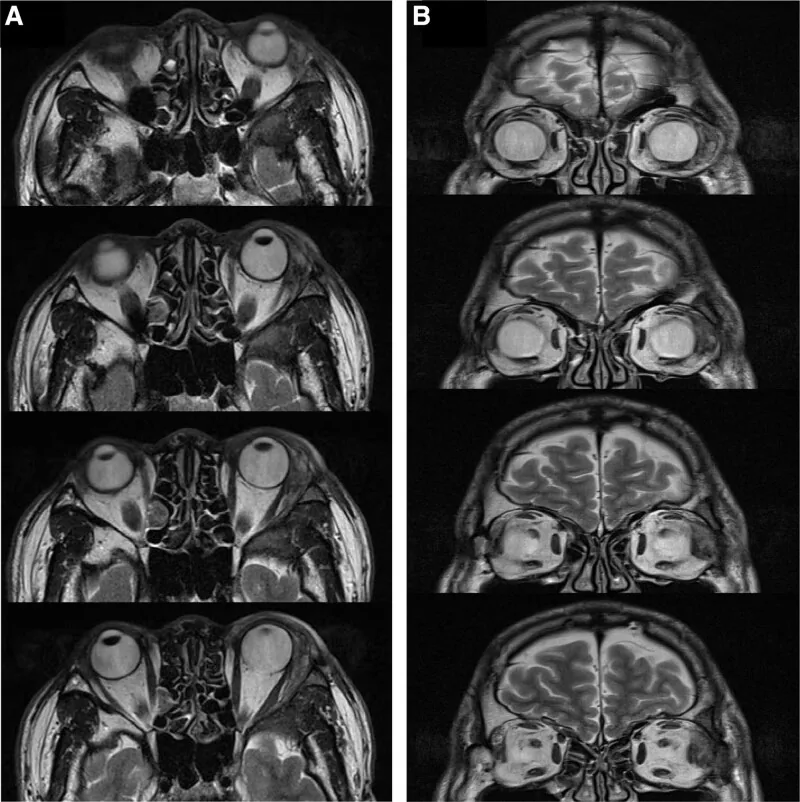
विलियम्स एट अल. की रिपोर्ट के अनुसार, 82% रोगियों में हिस्टोलॉजिक रूप से लैक्रिमल फोसा घुसपैठ की पुष्टि हुई है1)। यदि सीटी में ट्यूमर कक्षीय हड्डी को नष्ट कर रहा है, तो इसे घातक माना जा सकता है, लेकिन बिना हड्डी विनाश वाले एडेनॉइड सिस्टिक कार्सिनोमा भी मौजूद हैं, इसलिए सावधानी आवश्यक है।
एडेनॉइड सिस्टिक कार्सिनोमा का कारण अज्ञात है, और कोई विशिष्ट जोखिम कारक स्थापित नहीं है। ट्यूमर अक्सर लैक्रिमल ग्रंथि के कक्षीय लोब से उत्पन्न होता है और एक अनएनकैप्सुलेटेड ट्यूमर है।
निम्नलिखित पैथोलॉजिकल और नैदानिक विशेषताएं खराब पूर्वानुमान के कारकों के रूप में जानी जाती हैं:
निश्चित निदान पैथोहिस्टोलॉजिकल मूल्यांकन पर आधारित है। यदि घातकता का संदेह हो, तो ट्यूमर कोशिकाओं के इंट्राऑर्बिटल प्रसार को रोकने के लिए एक्सिजनल बायोप्सी की सिफारिश की जाती है। फाइन-नीडल एस्पिरेशन बायोप्सी अनरेसेक्टेबल ट्यूमर के लिए उपयुक्त हो सकती है, लेकिन केवल अनुभवी साइटोपैथोलॉजिस्ट वाले संस्थानों में।
एक्सोफ्थाल्मोस जैसे लक्षणों से लैक्रिमल ग्रंथि ट्यूमर का संदेह होने पर, दृश्य तीक्ष्णता, दृश्य क्षेत्र, और नेत्र गति जैसी नेत्र संबंधी जाँचें की जाती हैं, और सादा सीटी और सादा/कंट्रास्ट एमआरआई द्वारा इमेजिंग निदान किया जाता है। यदि प्रणालीगत खोज आवश्यक हो, तो पीईटी-सीटी या कंट्रास्ट सीटी भी की जा सकती है। निश्चित निदान बायोप्सी या पूर्ण निष्कासन के बाद पैथोहिस्टोलॉजिकल जांच पर आधारित है।
| T स्टेज | परिभाषा |
|---|---|
| T1 | अधिकतम व्यास ≤ 2 सेमी |
| T2 | अधिकतम व्यास > 2 सेमी से ≤ 4 सेमी |
| T3 | अधिकतम आकार 4 सेमी से अधिक या कक्षीय कोमल ऊतकों में विस्तार |
| T4 | परानासल साइनस, टेम्पोरल फोसा, पेटीगॉइड फोसा, सुपीरियर ऑर्बिटल फिशर, कैवर्नस साइनस या मस्तिष्क में आक्रमण |
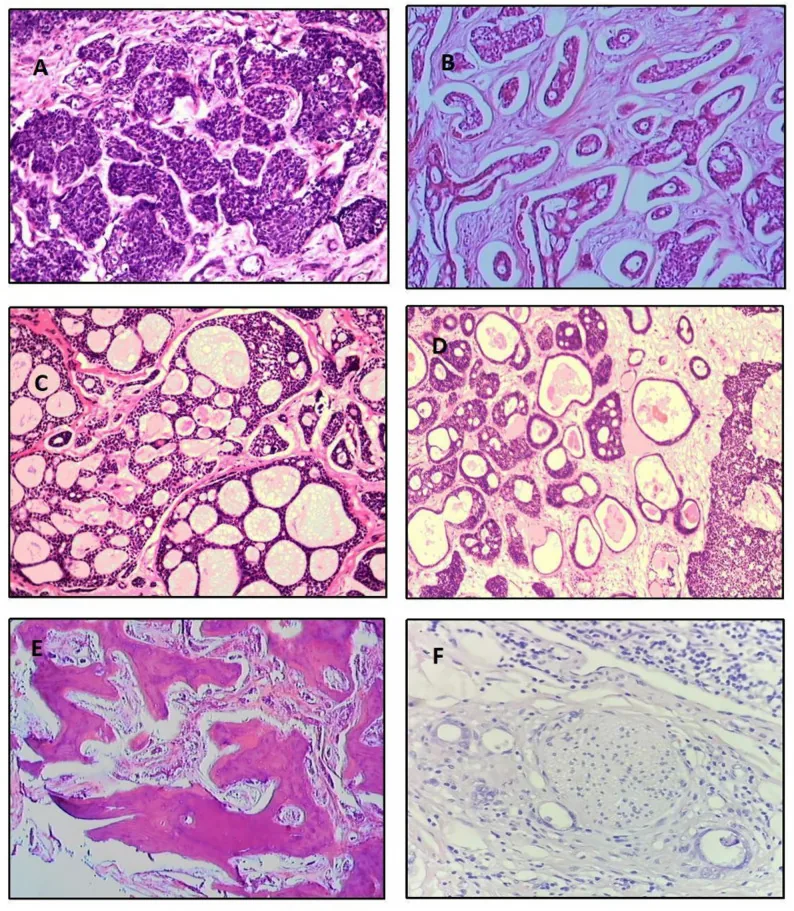
515 मामलों के विश्लेषण के अनुसार ऊतक उपप्रकारों की आवृत्ति इस प्रकार है 5)।
क्रिब्रीफॉर्म प्रकार
आवृत्ति: सबसे अधिक (39.8%)
विशेषताएँ: म्यूसिन के गोल पूल के साथ लोब्यूलर संरचनाएँ। ‘स्विस चीज़’ जैसा दिखावट। मध्यम पूर्वानुमान।
बेसलॉइड प्रकार
आवृत्ति: 31.8%
विशेषताएँ: निम्न विभेदित। बड़े बेसोफिलिक नाभिक और कम कोशिका द्रव्य। सबसे खराब पूर्वानुमान।
ट्यूबुलर प्रकार
आवृत्ति: 7.4%
विशेषताएं: 2-3 कोशिका परतों से बनी उपकला नलिकाएं। सबसे अधिक विभेदित, सर्वोत्तम पूर्वानुमान।
इसके अलावा मिश्रित प्रकार (13.9%), अविभेदित (6.1%), और स्क्लेरोज़िंग प्रकार (0.9%) भी होते हैं। 30% से अधिक ठोस पैटर्न खराब पूर्वानुमान का संकेत माना जाता है1)। ऊतकीय रूप से, ट्यूमर कोशिकाएं छोटी होती हैं, कोशिकाद्रव्य कम और नीला होता है, और केंद्रक क्रोमैटिन से भरपूर होता है। ट्यूमर समूह और स्ट्रोमा के बीच की सीमा स्पष्ट होती है, जो प्लियोमॉर्फिक एडेनोमा से स्पष्ट रूप से भिन्न होती है।
सर्जरी उपचार का आधार है, और शल्य प्रक्रिया ट्यूमर के चरण और इमेजिंग निष्कर्षों द्वारा निर्धारित की जाती है3)5)।
कापलान-मेयर विश्लेषण में, नेत्र-संरक्षण सर्जरी + विकिरण चिकित्सा ने एक्सेंटरेशन ± विकिरण चिकित्सा की तुलना में बेहतर जीवित रहने की दर दिखाई (P < 0.05)5)।
यदि इमेजिंग में ट्यूमर छोटा और पूरी तरह से हटाने योग्य है, तो पूर्ण निष्कासन का लक्ष्य रखा जाता है। यदि पूर्ण निष्कासन संभव नहीं है, तो परीक्षण चीरा द्वारा विकृति की पुष्टि की जाती है, फिर व्यापक छांटना या विकिरण चिकित्सा पर विचार किया जाता है। अश्रु ग्रंथि के एडेनोइड सिस्टिक कार्सिनोमा के लिए जो कक्षा तक सीमित है, एक्सेंटरेशन पर विचार किया जा सकता है, लेकिन कॉस्मेटिक मुद्दों और रोगी की आयु/इच्छाओं को ध्यान में रखते हुए रूढ़िवादी उपचार भी चुना जा सकता है। लिम्फ नोड मेटास्टेसिस दुर्लभ (4-9%) है, और लिम्फ नोड विच्छेदन आमतौर पर आवश्यक नहीं है6)।
व्यापक उच्छेदन और विकिरण चिकित्सा के बाद भी, लैक्रिमल तंत्रिका के माध्यम से मस्तिष्क स्टेम में घुसपैठ को रोकना संभव नहीं हो सकता है। दूर के मेटास्टेसिस को रोका जा सकेगा, इसकी भी कोई गारंटी नहीं है, और दीर्घकालिक अनुवर्ती आवश्यक है।
अपरिवर्तनीय एडेनॉइड सिस्टिक कार्सिनोमा के लिए, भारी कण विकिरण चिकित्सा की जाती है, और इसे पलक, नेत्रगोलक और कक्षा को संरक्षित करते हुए ट्यूमर को नियंत्रित करने वाला एक आशाजनक उपचार माना जाता है।
NIAC पहली बार 1998 में Meldrum और सहकर्मियों द्वारा रिपोर्ट किया गया एक उपचार है, जिसमें सिस्प्लैटिन (100 mg/m²) इंट्रा-आर्टेरियल और डॉक्सोरूबिसिन अंतःशिरा के संयोजन का उपयोग किया जाता है 3)2)।
Tse और सहकर्मियों (2013) के 19 मामलों के अध्ययन में, लैक्रिमल धमनी के संरक्षित रहने और प्रोटोकॉल का पालन करने वाले 8 मामलों में 10 वर्ष की रोग-मुक्त जीवित रहने की दर 100% बताई गई है 2)3)।
NIAC + उच्छेदन/नेत्रगर्त निकासी + विकिरण चिकित्सा का संयोजन अन्य उपचारों की तुलना में 10.8% पुनरावृत्ति दर, 14.9% मेटास्टेसिस दर और 18.9% मृत्यु दर के साथ अच्छे परिणाम दिखाता है 5)। NIAC के मुख्य जोखिमों में क्षणिक चेहरे का पक्षाघात, दृष्टि हानि, पूर्वकाल इस्कीमिया, न्यूट्रोपेनिया और थ्रोम्बोसाइटोपेनिया शामिल हैं 3)।
Kaplan-Meier विश्लेषण में नेत्र-संरक्षण सर्जरी + विकिरण चिकित्सा की जीवित रहने की दर ऑर्बिटल एक्सेंटरेशन ± विकिरण चिकित्सा से बेहतर थी (P<0.05)5)। T1-T2 ट्यूमर के लिए नेत्र-संरक्षण की सिफारिश की जाती है, और T3-T4 ट्यूमर या एक्स्ट्राऑर्बिटल विस्तार के मामलों में ऑर्बिटल एक्सेंटरेशन पर विचार किया जाता है। हालांकि, कॉस्मेटिक समस्याओं या रोगी की इच्छा के कारण कभी-कभी रूढ़िवादी उपचार चुना जाता है।
ट्यूमर कोशिकाएँ छोटी होती हैं, जिनमें कम और नीले रंग का साइटोप्लाज्म होता है, और नाभिक क्रोमैटिन से भरपूर होते हैं। हिस्टोलॉजिकल रूप से ट्यूमर आइलेट्स और स्ट्रोमा के बीच की सीमा स्पष्ट होती है, जो प्लियोमॉर्फिक एडेनोमा से स्पष्ट रूप से भिन्न होती है।
क्रिब्रीफॉर्म प्रकार में, सच्चे लुमेन (डक्टल कोशिकाओं से उत्पन्न) और छद्म लुमेन (मायोएपिथेलियल कोशिकाओं द्वारा निर्मित म्यूसिन युक्त गुहाएँ) मिश्रित होते हैं, जो ‘स्विस चीज़’ जैसा दिखता है। स्क्लेरोज़िंग प्रकार घने हाइलिनाइज़्ड स्ट्रोमा के साथ उपकला कोशिका डोरियों के रूप में देखा जाता है। 30% से अधिक ठोस (solid) पैटर्न खराब पूर्वानुमान से जुड़ा है1)।
ट्यूमर के विकास पैटर्न पाँच प्रकार के होते हैं (क्रिब्रीफॉर्म, ठोस, स्क्लेरोज़िंग, कोमेडोकार्सिनोमेटस, ट्यूबलर)। एक ही नमूने में कई विकास पैटर्न देखे जा सकते हैं।
| आणविक असामान्यता | विवरण |
|---|---|
| MYB-NFIB संलयन | t(6;9)(q23;p23) स्थानांतरण। एडेनॉइड सिस्टिक कार्सिनोमा के 70% से अधिक मामलों में मौजूद1) |
| MYB का अत्यधिक अभिव्यक्ति | कोशिका प्रसार, विभेदन, एंजियोजेनेसिस और वृद्धि कारकों के ऊपरी नियमन को बढ़ावा देता है1) |
| NOTCH1 सक्रियण उत्परिवर्तन | मेटास्टैटिक एडेनॉइड सिस्टिक कार्सिनोमा में प्रमुख प्रसार और आक्रमण चालक1)2) |
| KRAS/NRAS/MET उत्परिवर्तन | क्रमशः 46%, 8% और 13% में रिपोर्ट किए गए। EGFR-RAS-RAF कैस्केड संभावित चिकित्सीय लक्ष्य1)5) |
लैक्रिमल ग्रंथि के एडेनॉइड सिस्टिक कार्सिनोमा में 58% मामलों में MYB पुनर्व्यवस्था पाई जाती है (मेयो क्लिनिक, 12 मामले/25 वर्ष), और MYB-NFIB संलयन एडेनॉइड सिस्टिक कार्सिनोमा के लिए अत्यधिक विशिष्ट नैदानिक मार्कर है1)। MYB-NFIB संलयन AKT-निर्भर IGF1R सिग्नल द्वारा नियंत्रित होता है, और IGF1R अवरोध को चिकित्सीय लक्ष्य के रूप में आशाजनक माना जाता है1)3)।
पेरिन्यूरल आक्रमण 45.3% मामलों में देखा जाता है, और संवहनी या लसीका आक्रमण के बिना भी ट्यूमर कोशिकाएं फैल सकती हैं1)। तंत्रिकाओं और लसीका वाहिकाओं में आक्रमण करने की प्रबल प्रवृत्ति होती है, और रोग के प्रारंभिक चरण से लैक्रिमल तंत्रिका के माध्यम से ब्रेनस्टेम में आक्रमण हो सकता है। पेरिन्यूरल आक्रमण Bcl-2 के ऊपरी नियमन द्वारा एपोप्टोसिस प्रतिरोध से संबंधित माना जाता है।
वर्तमान में लैक्रिमल ग्रंथि के एडेनॉइड सिस्टिक कार्सिनोमा के लिए कोई स्वीकृत आणविक लक्षित दवा नहीं है। निम्नलिखित लक्ष्यों का अध्ययन किया जा रहा है 1)3)।
चरण II नैदानिक परीक्षणों के परिणामों में डोविटिनिब (ORR 6%, mPFS 8.2 महीने), लेनवाटिनिब (ORR 16%, mPFS 17.5 महीने), और एक्सिटिनिब (ORR 9%, mPFS 5.7 महीने) की सूचना दी गई है 3)।
Yu et al. (2022) ने उपचार से पहले और बाद के जीनोम अनुक्रमण और एपोप्टोसिस मार्करों (cCas3, PARP) विश्लेषण के संयोजन से मूल्यांकन की सूचना दी 2)। NIAC के बाद NOTCH1 उत्परिवर्तन की उत्परिवर्ती एलील आवृत्ति (VAF) उपचार से पहले 18.07% से घटकर उपचार के बाद 11.34% (37% कमी) हो गई, जो सिस्प्लैटिन संवेदनशीलता के लिए एक संभावित पूर्वानुमान मार्कर का संकेत देती है।
वर्तमान में लैक्रिमल ग्रंथि के एडेनॉइड सिस्टिक कार्सिनोमा के लिए कोई स्वीकृत आणविक लक्षित चिकित्सा नहीं है। MYB-NFIB फ्यूजन, Notch सिग्नलिंग मार्ग, EGFR-RAS-RAF कैस्केड आदि का अध्ययन संभावित चिकित्सीय लक्ष्यों के रूप में किया जा रहा है, और कई चरण II नैदानिक परीक्षण चल रहे हैं1)3)। मानक उपचार चाहने वालों के लिए सर्जरी और विकिरण चिकित्सा का संयोजन वर्तमान विकल्प है।