체상형
빈도: 가장 흔함 (39.8%)
특징: 뮤신의 원형 풀을 동반한 소엽 구조. “스위스 치즈” 모양. 중등도 예후.

선양 낭성암(ACC)은 분비샘에서 발생하는 드문 악성 종양으로, 전 세계 발생률은 인구 100만 명당 3~4예입니다1). 전체 두경부암의 약 1%를 차지하며, 눈물샘에 발생한 것을 눈물샘 선양 낭성암이라고 합니다1).
눈물샘 선양 낭성암은 전체 안와 종양의 약 1.6%를 차지하며3)5), 눈물샘 악성 상피 종양 중 가장 빈도가 높아 눈물샘암의 약 13~40%를 구성합니다5). 눈물샘 종양은 안와 내 점유 병변의 약 10%를 차지하며, 고형 눈물샘 종양의 약 20%가 상피 기원이고, 그중 약 45%가 악성이며, 악성 상피성 눈물샘 종양의 약 60%가 선양 낭성암입니다.
눈물샘 선양 낭성암은 Theodor Billroth가 처음 기술했으며, 조직학적 특징으로 인해 처음에 ‘cylindroma’로 명명되었습니다5).
역학적 특징은 다음과 같습니다.
전체 안와 종양의 약 1.6%를 차지하며, 선양 낭성 암종의 전 세계 발생률은 인구 100만 명당 3~4례로 극히 드뭅니다1)5). 눈물샘 악성 상피 종양 중에서 가장 빈도가 높은 조직형입니다.
806례의 대규모 리뷰에 따르면 초발 증상의 빈도는 다음과 같습니다5).
| 증상 | 빈도 |
|---|---|
| 안구 돌출 | 27.4% |
| 통증 | 21.7% |
| 눈꺼풀 부종 | 10.9% |
| 안구 편위 | 10.2% |
| 안구 운동 제한 | 10.1% |
| 시력 저하 | 9.3% |
| 복시 | 6.7% |
| 눈꺼풀 처짐 | 4.1% |
통증은 선양낭성암종의 특징적인 증상으로, 신경주위침윤(PNI)에 의해 발생합니다. 이는 양성 종양과의 중요한 감별점입니다. 눈물샘이 안와 외측 상방에 위치하기 때문에 안구는 종종 내하방으로 편위됩니다. 전두측두부의 감각 저하나 S자 모양의 눈꺼풀 처짐이 나타날 수도 있습니다. 증상 발현부터 진단까지 평균 11.1±18.3개월(범위 0.5~120개월)이 소요됩니다 5).
종양의 성장 속도는 다형선종보다 빠르고 통증을 동반하기 쉬운 점이 감별의 중요한 포인트입니다. 종양 증대에 따른 안구돌출, 외안근·신경 침윤에 의한 안구운동 제한, 시신경 압박에 의한 시력 저하도 비교적 급속히 진행됩니다.
통증의 유무가 가장 중요한 감별점입니다. 선양낭성암종은 신경주위 침윤으로 인해 통증을 동반하지만, 양성 종양(다형선종 등)은 무통성이며 서서히 진행됩니다. CT에서 골파괴가 확인되면 악성으로 판단할 수 있지만, 골파괴가 없는 선양낭성암종도 존재하므로 통증이 있는 경우 적극적으로 생검을 고려합니다.
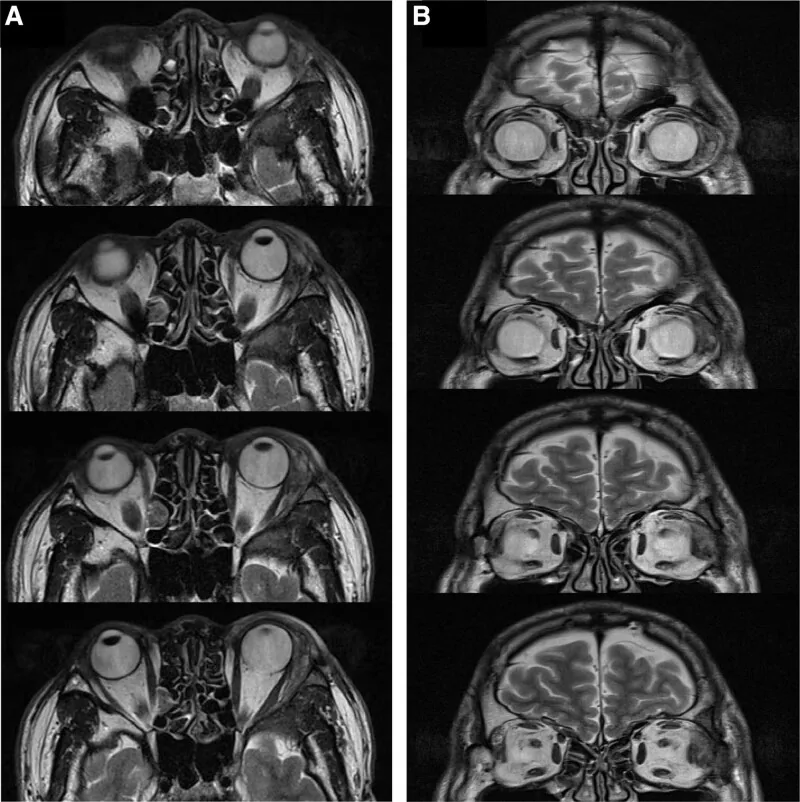
Williams 등의 보고에 따르면, 조직학적으로 82%의 환자에서 눈물샘와 침윤이 확인되었습니다 1). CT에서 종양이 안와골을 파괴하고 있으면 악성으로 판단할 수 있지만, 골파괴가 없는 선양낭성암종도 존재하므로 주의가 필요합니다.
선양낭성암종의 원인은 불명이며, 특정 위험 인자는 확립되어 있지 않습니다. 종양은 눈물샘의 안와엽(orbital lobe)에서 가장 흔히 발생하며, 피막을 가지지 않는(unencapsulated) 종양입니다.
다음의 병리학적·임상적 특징이 예후 불량 인자로 알려져 있습니다.
확진은 병리조직학적 평가에 기반합니다. 악성이 의심되는 경우, 안와 내 종양 세포 파종을 방지하기 위해 절제 생검이 권장됩니다. 세침 흡인 생검은 절제 불가능한 종양에 적합할 수 있지만, 경험이 풍부한 세포병리학자가 있는 시설로 제한됩니다.
안구 돌출 등의 증상으로 눈물샘 종양이 의심되면 시력, 시야, 안구 운동 등의 안과 검사를 시행하고, 단순 CT 및 단순/조영 MRI를 통한 영상 진단을 실시합니다. 전신 검사가 필요하면 PET-CT나 조영 CT도 시행할 수 있습니다. 확진은 생검 또는 완전 적출 후 병리조직학적 검사를 통해 이루어집니다.
| T 병기 | 정의 |
|---|---|
| T1 | 최대 직경 2cm 이하 |
| T2 | 최대 직경 2cm 초과 ~ 4cm 이하 |
| T3 | 최대 직경 >4 cm 또는 안와 연조직 침범 |
| T4 | 부비동, 측두와, 익상구개와, 상안와열, 해면정맥동, 뇌로의 침윤 |
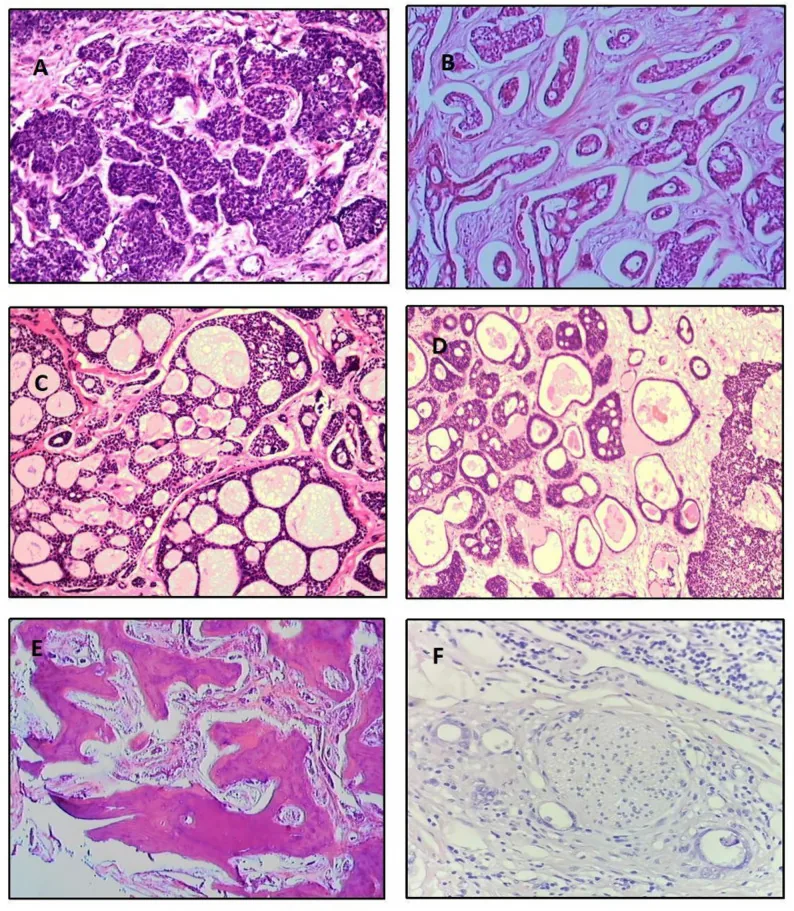
515예 분석에 따른 조직 아형의 빈도는 다음과 같습니다5).
체상형
빈도: 가장 흔함 (39.8%)
특징: 뮤신의 원형 풀을 동반한 소엽 구조. “스위스 치즈” 모양. 중등도 예후.
기저양형
빈도: 31.8%
특징: 저분화. 큰 호염기성 핵과 빈약한 세포질. 가장 나쁜 예후.
관상형
빈도: 7.4%
특징: 2~3층의 세포로 둘러싸인 상피관. 가장 분화도가 높고 예후가 가장 좋습니다.
그 외 혼합형(13.9%), 미분화형(6.1%), 경화형(0.9%)이 있습니다. 고형 패턴이 30%를 초과하면 예후가 불량한 것으로 간주됩니다1). 조직학적으로 종양 세포는 작고 세포질은 적고 청색을 띠며 핵은 염색질이 풍부합니다. 종양 세포 둥지와 간질의 경계는 명확하며 다형선종과는 확연히 다릅니다.
수술이 치료의 기본이며, 수술 방법은 종양 병기와 영상 소견에 따라 결정됩니다3)5).
Kaplan-Meier 분석에서 안구 보존 수술과 방사선 요법의 생존율이 안와 내용 제거술 ± 방사선 요법보다 우수했습니다(P<0.05)5).
영상 소견에서 종양이 작고 완전 절제가 가능하면 완전 절제를 목표로 합니다. 완전 절제가 불가능하다고 판단되면 절개 생검으로 병리를 확인한 후 광범위 절제술이나 방사선 조사를 고려합니다. 눈물샘 선양 낭성암이 안와 내에 국한된 경우 안와 내용 제거술을 고려하지만, 미용 문제나 환자의 나이, 희망을 고려하여 보존적 치료를 선택하기도 합니다. 림프절 전이는 드물며(4~9%), 림프절 곽청술은 일반적으로 필요하지 않습니다6).
광범위 절제술과 방사선 치료를 시행해도 누선 신경을 통한 뇌간 침윤을 막지 못하는 경우가 있습니다. 원격 전이를 항상 예방할 수 있는 것은 아니므로 장기적인 추적 관찰이 필요합니다.
수술이 불가능한 선양 낭성 암종에 대해서는 중입자선 치료가 시행되고 있으며, 눈꺼풀, 안구, 안와를 보존하면서 종양을 제압할 수 있는 유망한 치료법으로 자리매김하고 있습니다.
NIAC는 1998년 Meldrum 등이 처음 보고한 치료법으로, 시스플라틴(100mg/m²) 동맥 주입과 독소루비신 정맥 주입의 조합을 사용합니다3)2).
Tse 등(2013)의 19예 연구에서는 누선 동맥이 보존되고 프로토콜을 준수한 8예에서 10년 무병 생존율 100%가 보고되었습니다2)3).
NIAC + 절제/안와 내용 제거술 + 방사선 치료의 조합은 다른 치료법과 비교하여 재발률 10.8%, 전이율 14.9%, 사망률 18.9%로 양호한 성적을 보여줍니다5). NIAC의 주요 위험으로는 일과성 안면 신경 마비, 시력 상실, 전방 허혈, 호중구 감소증, 혈소판 감소증 등이 있습니다3).
Kaplan-Meier 분석에서 안구 보존 수술과 방사선 요법의 생존율이 안와 내용 제거술 ± 방사선 요법보다 우수했습니다(P<0.05)5). T1T2 종양에는 안구 보존이 권장되며, T3T4 종양 또는 안와 외 침범 사례에는 안와 내용 제거술이 고려됩니다. 그러나 미용 문제나 환자의 희망에 따라 보존적 치료를 선택하기도 합니다.
종양 세포는 작고 세포질이 적으며 청색을 띠고 핵은 염색질이 풍부합니다. 조직학적으로 종양 세포 둥지와 간질의 경계가 명확하며, 다형성 선종과는 확연히 다릅니다.
체상형에서는 진정 내강(관세포 유래)과 가성 내강(근상피 세포가 형성하는 뮤신 저류강)이 혼재하여 ‘스위스 치즈’ 모양을 나타냅니다. 경화형은 치밀한 유리질화 간질을 동반한 상피 세포 끈으로 관찰됩니다. 고형 패턴이 30%를 초과하면 예후가 불량합니다1).
종양의 증식 패턴은 5가지(체상형, 고형, 경화형, comedocarcinomatous, 관형)로 분류됩니다. 동일 표본 내에서도 여러 증식 패턴을 관찰할 수 있습니다.
| 분자 이상 | 내용 |
|---|---|
| MYB-NFIB 융합 | t(6;9)(q23;p23) 전위. 선양낭성암종의 70% 이상에서 존재1) |
| MYB 과발현 | 세포 증식, 분화, 혈관 신생 및 성장 인자 상향 조절 촉진1) |
| NOTCH1 활성화 돌연변이 | 전이성 선양낭성암종의 주요 증식 및 침윤 동인1)2) |
| KRAS/NRAS/MET 돌연변이 | 각각 46%, 8%, 13%에서 보고됨. EGFR-RAS-RAF 캐스케이드는 치료 표적이 될 수 있음1)5) |
눈물샘 선양낭성암종에서 58%에서 MYB 재배열이 검출되며(메이오 클리닉, 12예/25년), MYB-NFIB 융합은 선양낭성암종에 고도로 특이적인 진단 마커입니다1). MYB-NFIB 융합은 AKT 의존성 IGF1R 신호에 의해 조절되며, IGF1R 억제는 유망한 치료 표적으로 간주됩니다1)3).
신경주위 침윤은 45.3%에서 관찰되며, 혈관 또는 림프관 침윤이 없어도 종양 세포가 전파될 수 있습니다1). 신경 및 림프관으로 침윤하는 경향이 강하며, 질병 초기부터 눈물샘 신경을 통해 뇌간으로 침윤할 수 있습니다. 신경주위 침윤은 Bcl-2 상향 조절에 의한 세포사멸 저항성과 관련이 있습니다.
현재 눈물샘 선양 낭성암에 승인된 분자 표적 치료제는 없습니다. 다음 표적들이 연구 단계에서 검토되고 있습니다1)3).
2상 임상시험 결과, dovitinib (ORR 6%, mPFS 8.2개월), lenvatinib (ORR 16%, mPFS 17.5개월), axitinib (ORR 9%, mPFS 5.7개월)이 보고되었습니다3).
Yu 등(2022)은 치료 전후 유전체 시퀀싱과 세포자멸사 마커(cCas3, PARP) 분석을 결합한 평가를 보고했습니다2). NIAC 후 NOTCH1 돌연변이의 변이 대립유전자 빈도(VAF)가 치료 전 18.07%에서 치료 후 11.34%(37% 감소)로 감소하여, 시스플라틴 감수성의 예측 마커가 될 가능성이 제시되었습니다.
현재 눈물샘 선양낭성암에 대해 승인된 분자표적치료제는 없다. MYB-NFIB 융합, Notch 신호 경로, EGFR-RAS-RAF 캐스케이드 등이 연구 단계의 치료 표적으로 검토되고 있으며, 여러 제2상 임상시험이 진행 중이다1)3). 표준치료를 원하는 경우 수술과 방사선 치료의 병용이 현재 선택지이다.