Tipo cribiforme
Frecuencia: Más común (39.8%)
Características: Estructuras lobulillares con lagunas circulares de mucina. Aspecto de “queso suizo”. Pronóstico intermedio.

El carcinoma adenoide quístico (ACC) es un tumor maligno raro que se origina en las glándulas secretoras, con una incidencia mundial de 3–4 casos por millón de habitantes 1). Representa aproximadamente el 1% de todos los cánceres de cabeza y cuello, y cuando ocurre en la glándula lagrimal se denomina carcinoma adenoide quístico de la glándula lagrimal 1).
El carcinoma adenoide quístico de la glándula lagrimal representa aproximadamente el 1.6% de todos los tumores orbitarios 3)5) y es el tumor epitelial maligno más frecuente de la glándula lagrimal, constituyendo alrededor del 13–40% de los carcinomas de la glándula lagrimal 5). Los tumores de la glándula lagrimal representan aproximadamente el 10% de las lesiones ocupantes de espacio orbitario; alrededor del 20% de los tumores sólidos de la glándula lagrimal son de origen epitelial, de los cuales aproximadamente el 45% son malignos, y alrededor del 60% de los tumores epiteliales malignos de la glándula lagrimal son carcinomas adenoides quísticos.
El carcinoma adenoide quístico de la glándula lagrimal fue descrito por primera vez por Theodor Billroth y originalmente se denominó “cilindroma” debido a sus características histológicas 5).
Las características epidemiológicas son las siguientes.
Representa aproximadamente el 1.6% de todos los tumores orbitarios, y la incidencia mundial del carcinoma adenoide quístico es extremadamente rara, con 3–4 casos por millón de habitantes1)5). Es el tipo histológico más frecuente entre los tumores epiteliales malignos de la glándula lagrimal.
Según una gran revisión de 806 casos, la frecuencia de los síntomas iniciales es la siguiente5).
| Síntoma | Frecuencia |
|---|---|
| Proptosis | 27.4% |
| Dolor | 21.7% |
| Hinchazón del párpado | 10.9% |
| Desviación ocular | 10.2% |
| Limitación del movimiento ocular | 10.1% |
| Disminución de la visión | 9.3% |
| Visión doble | 6.7% |
| Ptosis | 4.1% |
El dolor es un síntoma característico del carcinoma adenoide quístico, causado por la invasión perineural (IPN). Es un punto importante de diferenciación con los tumores benignos. Dado que la glándula lagrimal se encuentra en la parte superolateral de la órbita, el ojo a menudo se desvía hacia abajo y adentro. También pueden presentarse hipoestesia en la región frontotemporal o ptosis en forma de S. El tiempo desde la aparición de los síntomas hasta el diagnóstico es en promedio de 11.1 ± 18.3 meses (rango 0.5–120 meses) 5).
La velocidad de crecimiento del tumor es más rápida que la del adenoma pleomorfo y es más probable que se acompañe de dolor, lo cual es un punto importante para el diagnóstico diferencial. La proptosis debida al aumento del tumor, la restricción del movimiento ocular por invasión de los músculos extraoculares y nervios, y la disminución de la agudeza visual por compresión del nervio óptico también progresan relativamente rápido.
La presencia o ausencia de dolor es el punto de diferenciación más importante. El carcinoma adenoide quístico se acompaña de dolor debido a la invasión perineural, mientras que los tumores benignos (como el adenoma pleomorfo) son indoloros y progresan lentamente. Si se confirma destrucción ósea en la TC, se puede considerar maligno, pero también existen casos de carcinoma adenoide quístico sin destrucción ósea, por lo que si hay dolor, se debe considerar activamente una biopsia.
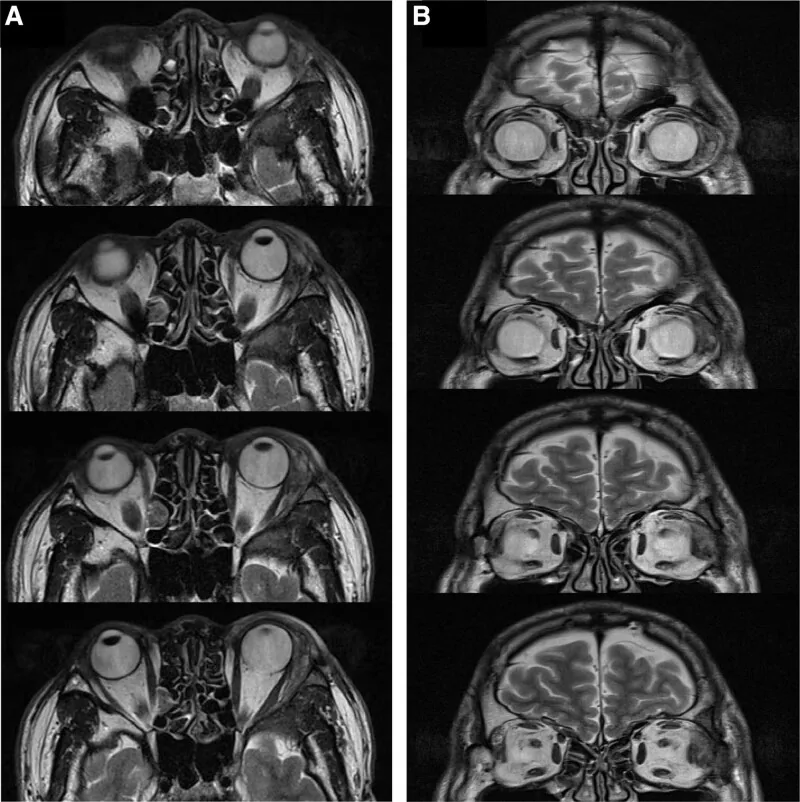
Según un informe de Williams et al., se confirmó invasión histológica de la fosa lagrimal en el 82% de los pacientes 1). Si el tumor destruye el hueso orbitario en la TC, se puede considerar maligno, pero se debe tener precaución porque también existen casos de carcinoma adenoide quístico sin destrucción ósea.
Se desconoce la causa del carcinoma adenoide quístico y no se han establecido factores de riesgo específicos. El tumor se origina con mayor frecuencia en el lóbulo orbitario de la glándula lagrimal y es un tumor sin cápsula.
Se sabe que las siguientes características patológicas y clínicas son factores de mal pronóstico.
El diagnóstico definitivo se basa en la evaluación histopatológica. Si se sospecha malignidad, se recomienda la biopsia por escisión para prevenir la diseminación intraorbitaria de células tumorales. La biopsia por aspiración con aguja fina puede ser adecuada para tumores no resecables, pero solo en centros con citopatólogos experimentados.
Si se sospecha un tumor de la glándula lagrimal debido a síntomas como proptosis, se realizan exámenes oftalmológicos como agudeza visual, campo visual y movimientos oculares, junto con estudios de imagen mediante TC simple y RM simple y con contraste. Si se necesita evaluación sistémica, también se puede realizar PET-TC o TC con contraste. El diagnóstico definitivo se realiza mediante biopsia o examen histopatológico tras la extirpación completa.
| Estadio T | Definición |
|---|---|
| T1 | Diámetro máximo ≤ 2 cm |
| T2 | Diámetro máximo > 2 cm a ≤ 4 cm |
| T3 | >4 cm de diámetro máximo o extensión a tejidos blandos orbitarios |
| T4 | Invasión de senos paranasales, fosa temporal, fosa pterigopalatina, fisura orbitaria superior, seno cavernoso o cerebro |
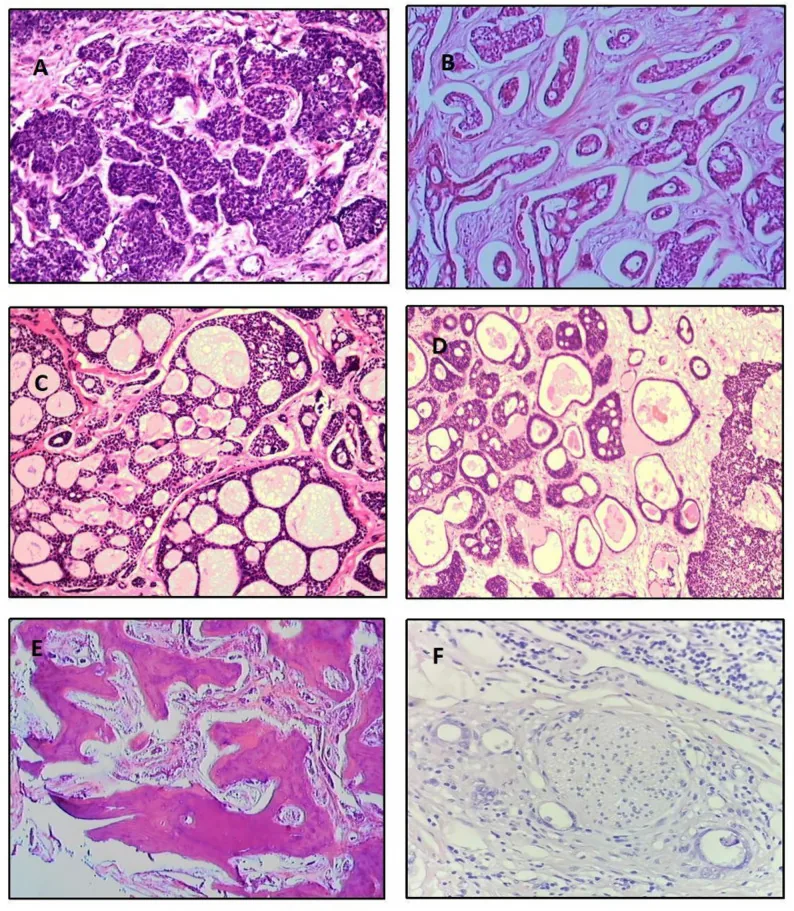
La frecuencia de los subtipos histológicos según un análisis de 515 casos es la siguiente5).
Tipo cribiforme
Frecuencia: Más común (39.8%)
Características: Estructuras lobulillares con lagunas circulares de mucina. Aspecto de “queso suizo”. Pronóstico intermedio.
Tipo basaloides
Frecuencia: 31.8%
Características: Pobremente diferenciado. Núcleos basófilos grandes y citoplasma escaso. Peor pronóstico.
Tipo tubular
Frecuencia: 7.4%
Características: Túbulos epiteliales revestidos por 2–3 capas de células. El más diferenciado, mejor pronóstico.
Otros tipos incluyen mixto (13.9%), indiferenciado (6.1%) y esclerosante (0.9%). Un patrón sólido que supere el 30% se considera de mal pronóstico1). Histológicamente, las células tumorales son pequeñas con citoplasma escaso y basófilo, y núcleos ricos en cromatina. El borde entre los nidos tumorales y el estroma es nítido, claramente diferente del adenoma pleomórfico.
La cirugía es la base del tratamiento, y el abordaje quirúrgico se determina según el estadio tumoral y los hallazgos de imagen3)5).
El análisis de Kaplan-Meier mostró que la cirugía conservadora del ojo más radioterapia tuvo una mejor supervivencia que la exenteración orbitaria con o sin radioterapia (P<0.05)5).
Si las imágenes muestran un tumor pequeño que puede resecarse completamente, se busca la resección completa. Si se considera imposible la resección completa, se realiza una biopsia incisional para confirmar la patología, luego se considera la escisión amplia o la radioterapia. Para el carcinoma adenoide quístico de la glándula lagrimal confinado a la órbita, se puede considerar la exenteración orbitaria, pero se puede optar por un tratamiento conservador según las preocupaciones estéticas, la edad del paciente y sus preferencias. La metástasis ganglionar es rara (4–9%) y la disección ganglionar generalmente no es necesaria6).
Incluso después de una escisión amplia y radioterapia, es posible que no se pueda prevenir la invasión del tronco encefálico a través del nervio lagrimal. No siempre es posible prevenir la metástasis a distancia, por lo que es necesario un seguimiento a largo plazo.
Para el carcinoma adenoide quístico irresecable, se realiza terapia con partículas pesadas, y se posiciona como un tratamiento prometedor que puede controlar el tumor mientras se preservan el párpado, el globo ocular y la órbita.
La NIAC fue reportada por primera vez por Meldrum et al. en 1998, utilizando una combinación de cisplatino intraarterial (100 mg/m²) y doxorrubicina intravenosa3)2).
En un estudio de 19 casos de Tse et al. (2013), se reportó una tasa de supervivencia libre de enfermedad a 10 años del 100% en 8 casos donde se preservó la arteria lagrimal y se siguió el protocolo2)3).
La combinación de NIAC + resección/exenteración orbitaria + radioterapia muestra resultados favorables en comparación con otros tratamientos, con una tasa de recurrencia del 10.8%, tasa de metástasis del 14.9% y tasa de mortalidad del 18.9%5). Los principales riesgos de la NIAC incluyen parálisis facial transitoria, pérdida de visión, isquemia anterior, neutropenia y trombocitopenia3).
El análisis de Kaplan-Meier mostró que las tasas de supervivencia de la cirugía de preservación ocular más radioterapia fueron mejores que las de la exenteración orbitaria con o sin radioterapia (P<0.05)5). Se recomienda la cirugía de preservación ocular para tumores T1–T2, mientras que la exenteración orbitaria se considera para tumores T3–T4 o casos con extensión extraorbitaria. Sin embargo, en ocasiones se elige un tratamiento conservador debido a problemas cosméticos o preferencias del paciente.
Las células tumorales son pequeñas, con citoplasma escaso y azulado, y núcleos ricos en cromatina. Histológicamente, el límite entre los nidos tumorales y el estroma es claro, claramente diferente del adenoma pleomórfico.
En el tipo cribiforme, coexisten luces verdaderas (derivadas de células ductales) y pseudoluces (espacios de retención de mucina formados por células mioepiteliales), dando una apariencia de “queso suizo”. El tipo escleroso se observa como cordones epiteliales con estroma hialinizado denso. Un patrón sólido que supera el 30% se asocia con mal pronóstico1).
Los patrones de crecimiento tumoral se clasifican en cinco tipos: cribiforme, sólido, escleroso, comedocarcinomatoso y tubular. Se pueden observar múltiples patrones de crecimiento dentro de la misma muestra.
| Anomalía molecular | Descripción |
|---|---|
| Fusión MYB-NFIB | Translocación t(6;9)(q23;p23). Presente en más del 70% de todos los carcinomas adenoideos quísticos1) |
| Sobreexpresión de MYB | Promueve la proliferación celular, diferenciación, angiogénesis y regulación positiva de factores de crecimiento1) |
| Mutación activadora de NOTCH1 | Principal impulsor de la proliferación e invasión en el carcinoma adenoideo quístico metastásico1)2) |
| Mutaciones KRAS/NRAS/MET | Reportadas en 46%, 8% y 13% de los casos, respectivamente. La cascada EGFR-RAS-RAF podría ser un objetivo terapéutico1)5) |
En el carcinoma adenoideo quístico de la glándula lagrimal, se detecta reordenamiento de MYB en el 58% de los casos (Mayo Clinic, 12 casos/25 años), y la fusión MYB-NFIB es un marcador diagnóstico altamente específico del carcinoma adenoideo quístico1). La fusión MYB-NFIB está regulada por la señalización de IGF1R dependiente de AKT, y la inhibición de IGF1R se considera un objetivo terapéutico prometedor1)3).
La invasión perineural se observa en el 45.3% de los casos, y las células tumorales pueden diseminarse incluso sin invasión vascular o linfática1). Existe una fuerte tendencia a invadir nervios y vasos linfáticos, y la infiltración al tronco encefálico a través del nervio lagrimal puede ocurrir temprano en la enfermedad. La invasión perineural se asocia con resistencia a la apoptosis debido a la regulación positiva de Bcl-2.
Actualmente, no hay fármacos de terapia molecular dirigida aprobados para el carcinoma adenoide quístico de la glándula lagrimal. Los siguientes blancos están siendo investigados en etapas de investigación1)3).
Los resultados de ensayos clínicos de fase II han reportado dovitinib (TRO 6%, mSLP 8.2 meses), lenvatinib (TRO 16%, mSLP 17.5 meses) y axitinib (TRO 9%, mSLP 5.7 meses)3).
Yu et al. (2022) reportaron una evaluación que combina la secuenciación genómica pre y postratamiento con el análisis de marcadores de apoptosis (cCas3, PARP)2). La frecuencia alélica variante (VAF) de la mutación NOTCH1 después de NIAC disminuyó de 18.07% antes del tratamiento a 11.34% después del tratamiento (reducción del 37%), lo que sugiere que podría ser un marcador predictivo de sensibilidad al cisplatino.
Actualmente no hay fármacos de terapia molecular dirigida aprobados para el carcinoma adenoide quístico de la glándula lagrimal. La fusión MYB-NFIB, la vía de señalización Notch, la cascada EGFR-RAS-RAF, entre otros, se están investigando como dianas terapéuticas en fase de investigación, y varios ensayos clínicos de fase II están en curso1)3). Para quienes deseen tratamiento estándar, la combinación de cirugía y radioterapia es la opción actual.