النمط الشبكي
التردد: الأكثر شيوعًا (39.8%)
الخصائص: بنية مفصصة مع تجمعات دائرية من الميوسين. مظهر “الجبن السويسري”. تشخيص متوسط.

السرطان الغدي الكيسي (ACC) هو ورم خبيث نادر يصيب الغدد الإفرازية، بمعدل حدوث عالمي يتراوح بين 3-4 حالات لكل مليون شخص سنويًا 1). يشكل حوالي 1% من جميع سرطانات الرأس والرقبة، وعند حدوثه في غدة الدمع يسمى سرطان غدة الدمع الكيسي الغدي 1).
يشكل سرطان غدة الدمع الكيسي الغدي حوالي 1.6% من جميع أورام الحجاج 3)5)، وهو الأكثر شيوعًا بين الأورام الظهارية الخبيثة في غدة الدمع، ويمثل حوالي 13-40% من سرطانات غدة الدمع 5). تشكل أورام غدة الدمع حوالي 10% من الآفات الحجمية داخل الحجاج، وحوالي 20% من أورام غدة الدمع الصلبة هي من أصل ظهاري، وحوالي 45% منها خبيثة، وحوالي 60% من أورام غدة الدمع الظهارية الخبيثة هي سرطان غدي كيسي.
تم وصف سرطان غدة الدمع الكيسي الغدي لأول مرة بواسطة تيودور بيلروث، وتم تسميته في البداية “سيليندروم” بسبب خصائصه النسيجية 5).
الخصائص الوبائية هي كما يلي:
يمثل حوالي 1.6% من جميع أورام الحجاج، ومعدل الإصابة العالمي لسرطان الغدة الدمعية الكيسي الغدي هو 3-4 حالات لكل مليون شخص، وهو نادر جدًا1)5). وهو النوع النسيجي الأكثر شيوعًا بين الأورام الظهارية الخبيثة في الغدة الدمعية.
وفقًا لمراجعة كبيرة لـ 806 حالة، فإن تكرار الأعراض الأولية هو كما يلي5):
| الأعراض | التكرار |
|---|---|
| جحوظ العين | 27.4% |
| ألم | 21.7% |
| تورم الجفن | 10.9% |
| انحراف مقلة العين | 10.2% |
| تقييد حركة العين | 10.1% |
| انخفاض الرؤية | 9.3% |
| ازدواج الرؤية | 6.7% |
| تدلي الجفن | 4.1% |
الألم هو عرض مميز للسرطان الغدي الكيسي، وينتج عن الارتشاح حول العصب (PNI). وهو نقطة تفريق مهمة عن الأورام الحميدة. نظرًا لأن الغدة الدمعية تقع في الجزء العلوي الجانبي من الحجاج، غالبًا ما تنحرف مقلة العين إلى الداخل والأسفل. قد يحدث أيضًا نقص الإحساس في المنطقة الجبهية الصدغية وتدلي الجفن على شكل حرف S. يستغرق الأمر متوسط 11.1 ± 18.3 شهرًا (المدى 0.5-120 شهرًا) من ظهور الأعراض حتى التشخيص 5).
معدل نمو الورم أسرع من الورم الغدي متعدد الأشكال، وغالبًا ما يكون مصحوبًا بألم، وهذه نقطة مهمة في التشخيص التفريقي. جحوظ العين الناتج عن زيادة حجم الورم، وتقييد حركة العين بسبب تسلل العضلات خارج العين والأعصاب، وانخفاض الرؤية الناتج عن ضغط العصب البصري، كلها تتقدم بسرعة نسبيًا.
وجود الألم هو أهم نقطة تفريق. سرطان الغدة الدمعية الكيسي الحُوَيصِلي يسبب ألمًا بسبب تسلل حول العصب، بينما الأورام الحميدة (مثل الورم الغدي متعدد الأشكال) غير مؤلمة وتتقدم ببطء. إذا أظهر التصوير المقطعي المحوسب تدميرًا عظميًا، يمكن اعتبار الورم خبيثًا، ولكن هناك حالات من سرطان الغدة الدمعية الكيسي الحُوَيصِلي دون تدمير عظمي، لذلك إذا كان هناك ألم، يجب النظر في الخزعة بنشاط.
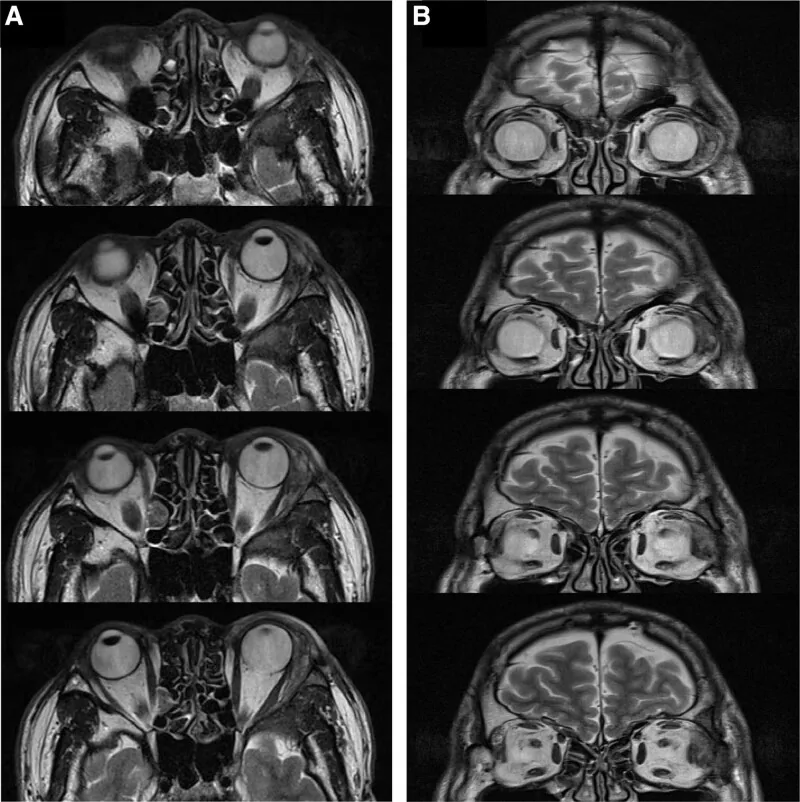
في تقرير Williams وآخرين، تم تأكيد تسلل حفرة الغدة الدمعية نسيجيًا في 82% من المرضى 1). إذا دمر الورم عظم الحجاج في التصوير المقطعي المحوسب، يمكن اعتباره خبيثًا، ولكن يجب الحذر لأن هناك حالات من سرطان الغدة الدمعية الكيسي الحُوَيصِلي بدون تدمير عظمي.
سبب سرطان الغدة الدمعية الكيسي الحُوَيصِلي غير معروف، ولم يتم تحديد عوامل خطر محددة. ينشأ الورم غالبًا من الفص الحجاجي للغدة الدمعية، وهو ورم غير مغلف.
تُعرف الخصائص المرضية والسريرية التالية كعوامل إنذار سيئة:
التشخيص النهائي يعتمد على التقييم النسيجي المرضي. في حالة الاشتباه في الورم الخبيث، يُوصى بالخزعة الاستئصالية لمنع انتشار الخلايا السرطانية داخل الحجاج. قد تكون الخزعة بالإبرة الدقيقة مناسبة للأورام غير القابلة للاستئصال، ولكن فقط في المرافق التي يوجد بها أخصائي علم أمراض خلوية ذو خبرة.
في حالة الاشتباه في وجود ورم في الغدة الدمعية بسبب أعراض مثل جحوظ العين، يتم إجراء فحوصات عينية مثل حدة البصر والمجال الحركي وحركة العين، بالإضافة إلى التصوير التشخيصي باستخدام التصوير المقطعي المحوسب غير المعزز والتصوير بالرنين المغناطيسي المعزز وغير المعزز. إذا كان الفحص الجهازي ضروريًا، يتم إجراء التصوير المقطعي بالإصدار البوزيتروني أو التصوير المقطعي المحوسب المعزز. التشخيص النهائي يعتمد على الفحص النسيجي المرضي بعد الخزعة أو الاستئصال الكامل.
| مرحلة T | التعريف |
|---|---|
| T1 | قطر أقصى 2 سم أو أقل |
| T2 | قطر أقصى أكبر من 2 سم إلى 4 سم أو أقل |
| T3 | قطر أكبر من 4 سم أو امتداد إلى الأنسجة الرخوة في الحجاج |
| T4 | غزو الجيوب الأنفية، الحفرة الصدغية، الحفرة الجناحية، الشق الحجاجي العلوي، الجيب الكهفي، الدماغ |
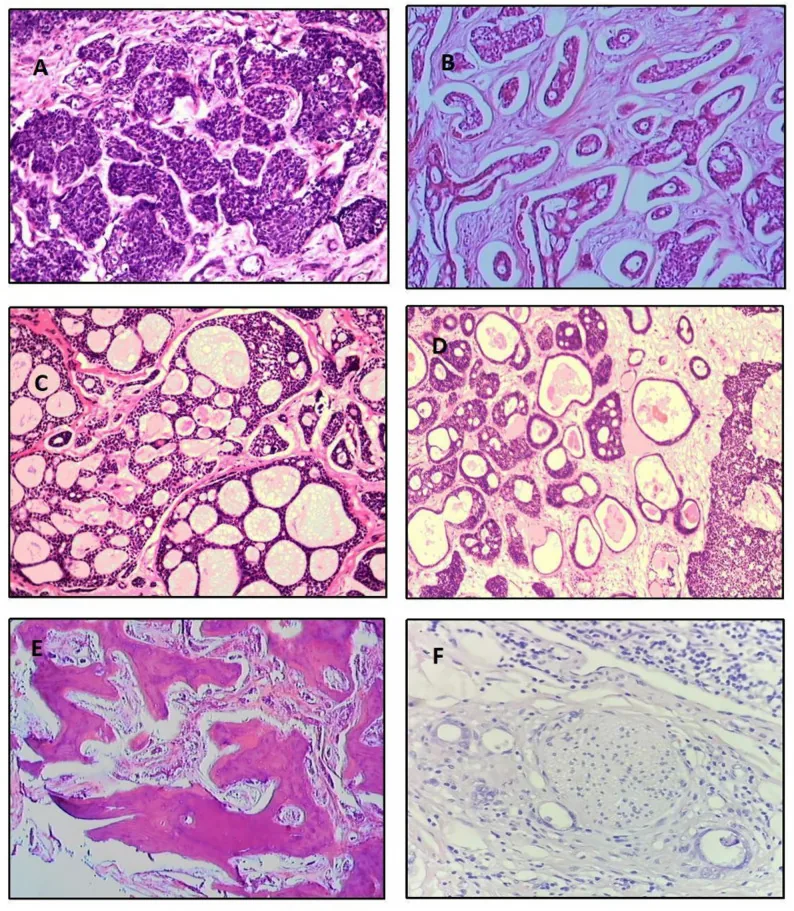
تردد الأنواع الفرعية النسيجية بناءً على تحليل 515 حالة هو كما يلي5).
النمط الشبكي
التردد: الأكثر شيوعًا (39.8%)
الخصائص: بنية مفصصة مع تجمعات دائرية من الميوسين. مظهر “الجبن السويسري”. تشخيص متوسط.
النمط القاعدي الخلوي
التردد: 31.8%
الخصائص: ضعيف التمايز. أنوية كبيرة قاعدية اللون وسيتوبلازم ضئيل. أسوأ تشخيص.
النمط الأنبوبي
التردد: 7.4%
السمات: أنابيب ظهارية مبطنة بطبقتين إلى ثلاث طبقات من الخلايا. الأكثر تمايزًا وأفضل تشخيص.
بالإضافة إلى ذلك، توجد الأنواع المختلطة (13.9%)، وغير المتمايزة (6.1%)، والمصلبة (0.9%). إذا تجاوز النمط الصلب 30%، يُعتبر التشخيص سيئًا 1). نسيجيًا، الخلايا الورمية صغيرة، السيتوبلازم قليل ومزرق، والنواة غنية بالكروماتين. الحدود بين البؤر الورمية والسدى واضحة، وتختلف بوضوح عن الورم الغدي متعدد الأشكال.
الجراحة هي أساس العلاج، ويتم تحديد الإجراء الجراحي بناءً على مرحلة الورم والنتائج التصويرية 3)5).
أظهر تحليل كابلان-ماير أن الجراحة الحافظة للعين مع العلاج الإشعاعي كانت أفضل في البقاء على قيد الحياة مقارنة باستئصال المحجر مع أو بدون العلاج الإشعاعي (P<0.05) 5).
إذا كان الورم صغيرًا وقابلاً للاستئصال الكامل وفقًا للتصوير، يُهدف إلى الاستئصال الكامل. إذا اعتُبر الاستئصال الكامل غير ممكن، يتم تأكيد علم الأمراض عن طريق الخزعة الاستئصالية، ثم يُنظر في الاستئصال الواسع أو العلاج الإشعاعي. بالنسبة لسرطان الغدة الدمعية الكيسي الغدي، إذا كان الورم محصورًا داخل المحجر، يُفكر في استئصال المحجر، ولكن قد يتم اختيار العلاج التحفظي مع مراعاة المشاكل التجميلية وعمر المريض ورغباته. النقائل اللمفاوية نادرة (4-9%)، وعادة لا تكون هناك حاجة لتشريح العقد اللمفاوية 6).
حتى مع الاستئصال الواسع والعلاج الإشعاعي، قد لا يمكن منع الارتشاح إلى جذع الدماغ عبر العصب الدمعي. كما أنه ليس من المضمون منع النقائل البعيدة، وتكون المتابعة طويلة الأمد ضرورية.
بالنسبة للسرطان الغدي الكيسي غير القابل للجراحة، يُستخدم العلاج بأيونات الكربون الثقيلة، ويُعتبر علاجًا واعدًا يمكنه السيطرة على الورم مع الحفاظ على الجفن ومقلة العين والمحجر.
تم الإبلاغ عن NIAC لأول مرة بواسطة Meldrum وآخرين في عام 1998، باستخدام مزيج من السيسبلاتين (100 ملغ/م²) عن طريق الشريان والدوكسوروبيسين عن طريق الوريد 3)2).
في دراسة أجراها Tse وآخرون (2013) على 19 حالة، تم الإبلاغ عن معدل بقاء خالٍ من المرض لمدة 10 سنوات بنسبة 100% في 8 حالات تم فيها الحفاظ على الشريان الدمعي واتباع البروتوكول 2)3).
يُظهر مزيج NIAC + الاستئصال/إزالة محتويات المحجر + العلاج الإشعاعي نتائج جيدة مقارنة بالعلاجات الأخرى، مع معدل تكرار 10.8%، ومعدل نقائل 14.9%، ومعدل وفيات 18.9% 5). تشمل المخاطر الرئيسية لـ NIAC شلل الوجه المؤقت، وفقدان البصر، ونقص التروية الأمامي، وقلة العدلات، وقلة الصفيحات 3).
أظهر تحليل كابلان-ماير أن معدل البقاء على قيد الحياة للجراحة الحافظة للعين مع العلاج الإشعاعي أفضل من استئصال محجر العين مع أو بدون العلاج الإشعاعي (P<0.05) 5). يُوصى بالحفاظ على العين للأورام T1-T2، بينما يُنظر في استئصال محجر العين للأورام T3-T4 أو في حالات الامتداد خارج المحجر. ومع ذلك، قد يتم اختيار العلاج التحفظي بسبب مشاكل تجميلية أو رغبة المريض.
الخلايا الورمية صغيرة الحجم، ذات سيتوبلازم قليل ومزرق، ونواتها غنية بالكروماتين. حدود الأقبية الورمية مع السدى واضحة نسيجيًا، وتختلف بوضوح عن الورم الغدي متعدد الأشكال.
في النمط الغربالي، تختلط التجاويف الحقيقية (من أصل قنوي) والتجاويف الكاذبة (تجاويف تحتوي على موسين تتكون من الخلايا الظهارية العضلية) مما يعطي مظهرًا يشبه الجبن السويسري. النمط المتصلب يُرى على شكل حبال ظهارية مع سدى زجاجي كثيف. إذا تجاوز النمط الصلب 30%، يُعتبر مؤشرًا سيئًا للإنذار 1).
تُصنف أنماط نمو الورم إلى 5 أنواع (غربالي، صلب، متصلب، شبيه بالسرطان الكوميدو، أنبوبي). يمكن ملاحظة أنماط نمو متعددة في نفس العينة.
| الخلل الجزيئي | المحتوى |
|---|---|
| اندماج MYB-NFIB | انتقال t(6;9)(q23;p23). يوجد في أكثر من 70% من حالات السرطان الغدي الكيسي 1) |
| فرط التعبير عن MYB | يعزز تكاثر الخلايا، والتمايز، وتكوين الأوعية الدموية، وتنظيم النمو التصاعدي 1) |
| طفرات تنشيط NOTCH1 | المحرك الرئيسي للتكاثر والغزو في السرطان الغدي الكيسي النقيلي 1)2) |
| طفرات KRAS/NRAS/MET | تم الإبلاغ عنها بنسبة 46% و8% و13% على التوالي. قد يكون مسار EGFR-RAS-RAF هدفًا علاجيًا 1)5) |
في سرطان الغدة الدمعية الكيسي، تم اكتشاف إعادة ترتيب MYB في 58% من الحالات (Mayo Clinic 12 حالة/25 سنة)، ويعتبر اندماج MYB-NFIB علامة تشخيصية عالية الخصوصية للسرطان الغدي الكيسي 1). يتم تنظيم اندماج MYB-NFIB بواسطة إشارات IGF1R المعتمدة على AKT، ويعتبر تثبيط IGF1R هدفًا علاجيًا واعدًا 1)3).
يحدث الارتشاح حول العصب في 45.3% من الحالات، ويمكن للخلايا السرطانية أن تنتشر حتى في غياب الارتشاح الوعائي أو اللمفاوي 1). هناك ميل قوي للارتشاح في الأعصاب والأوعية اللمفاوية، ويمكن أن يحدث غزو لجذع الدماغ عبر العصب الدمعي في مرحلة مبكرة من المرض. يرتبط الارتشاح حول العصب بمقاومة الاستماتة الناتجة عن زيادة تنظيم Bcl-2.
لا توجد حاليًا أدوية علاج موجه جزيئيًا معتمدة لسرطان الغدة الدمعية الكيسي الغدي. فيما يلي الأهداف قيد الدراسة 1)3).
أظهرت نتائج التجارب السريرية من المرحلة الثانية: دوفيتينيب (معدل الاستجابة الموضوعي 6%، متوسط البقاء دون تقدم 8.2 شهرًا)، لينفاتينيب (معدل الاستجابة الموضوعي 16%، متوسط البقاء دون تقدم 17.5 شهرًا)، وأكسيتينيب (معدل الاستجابة الموضوعي 9%، متوسط البقاء دون تقدم 5.7 شهرًا) 3).
أبلغ Yu et al. (2022) عن تقييم يجمع بين التسلسل الجينومي قبل وبعد العلاج وتحليل علامات الاستماتة (cCas3، PARP) 2). انخفض تواتر الأليل الطافر (VAF) لطفرة NOTCH1 بعد NIAC من 18.07% قبل العلاج إلى 11.34% بعد العلاج (انخفاض بنسبة 37%)، مما يشير إلى إمكانية استخدامه كعلامة تنبؤية للحساسية للسيسبلاتين.
لا توجد حاليًا أدوية علاج موجه جزيئي معتمدة لسرطان الغدة الدمعية الكيسي الغدي. يتم دراسة اندماج MYB-NFIB، مسار إشارات Notch، وسلسلة EGFR-RAS-RAF كأهداف علاجية في مرحلة البحث، وهناك العديد من التجارب السريرية من المرحلة الثانية جارية1)3). إذا كنت ترغب في العلاج القياسي، فإن الجمع بين الجراحة والعلاج الإشعاعي هو الخيار الحالي.