Tipo cribriforme
Frequenza: più comune (39,8%)
Caratteristiche: strutture lobulari con accumuli rotondi di mucina. Aspetto «a formaggio svizzero». Prognosi intermedia.

Il carcinoma adenoido cistico (ACC) è un raro tumore maligno delle ghiandole secretorie, con un’incidenza mondiale di 3-4 casi per milione di abitanti 1). Rappresenta circa l’1% di tutti i tumori della testa e del collo e, quando si sviluppa nella ghiandola lacrimale, viene chiamato carcinoma adenoido cistico della ghiandola lacrimale 1).
Il carcinoma adenoido cistico della ghiandola lacrimale rappresenta circa l’1,6% di tutti i tumori orbitari 3)5) ed è il tumore epiteliale maligno più frequente della ghiandola lacrimale, costituendo circa il 13-40% dei carcinomi lacrimali 5). I tumori della ghiandola lacrimale rappresentano circa il 10% delle lesioni occupanti spazio orbitarie, circa il 20% dei tumori solidi lacrimali sono di origine epiteliale, di cui circa il 45% sono maligni, e circa il 60% dei tumori epiteliali maligni lacrimali sono carcinomi adenoido cistici.
Il carcinoma adenoido cistico della ghiandola lacrimale fu descritto per la prima volta da Theodor Billroth e, per le sue caratteristiche istologiche, fu inizialmente chiamato «cilindroma» 5).
Le caratteristiche epidemiologiche sono le seguenti.
Costituisce circa l’1,6% di tutti i tumori orbitali e l’incidenza mondiale del carcinoma adenoido cistico è di 3-4 casi per milione di abitanti, estremamente rara1)5). È il tipo istologico più frequente tra i tumori epiteliali maligni della ghiandola lacrimale.
Secondo un’ampia revisione di 806 casi, la frequenza dei sintomi iniziali è la seguente5).
| Sintomo | Frequenza |
|---|---|
| Es oftalmo | 27,4% |
| Dolore | 21,7% |
| Gonfiore palpebrale | 10,9% |
| Deviazione del bulbo oculare | 10,2% |
| Limitazione dei movimenti oculari | 10,1% |
| Riduzione dell’acuità visiva | 9,3% |
| Diplopia | 6,7% |
| Ptosi | 4,1% |
Il dolore è un sintomo caratteristico del carcinoma adenoido cistico, causato dall’infiltrazione perineurale (PNI). È un importante punto di differenziazione dai tumori benigni. Il bulbo oculare è spesso deviato verso il basso e l’interno poiché la ghiandola lacrimale si trova nella parte supero-esterna dell’orbita. Possono anche presentarsi ipoestesia fronto-temporale o ptosi a forma di S. Il tempo medio dalla comparsa dei sintomi alla diagnosi è di 11,1 ± 18,3 mesi (intervallo da 0,5 a 120 mesi) 5).
La velocità di crescita del tumore è più rapida di quella dell’adenoma pleomorfo e tende a essere dolorosa, il che è un punto chiave per la diagnosi differenziale. L’esoftalmo dovuto all’aumento del tumore, la limitazione dei movimenti oculari per infiltrazione dei muscoli extraoculari e dei nervi, e la riduzione dell’acuità visiva per compressione del nervo ottico progrediscono anch’essi relativamente rapidamente.
La presenza o assenza di dolore è il punto di differenziazione più importante. Il carcinoma adenoido cistico causa dolore per infiltrazione perineurale, mentre i tumori benigni (come l’adenoma pleomorfo) sono indolori e progrediscono lentamente. Se la TC mostra distruzione ossea, si può concludere per una neoplasia maligna, ma esistono carcinomi adenoido cistici senza distruzione ossea; in caso di dolore, si deve considerare attivamente una biopsia.
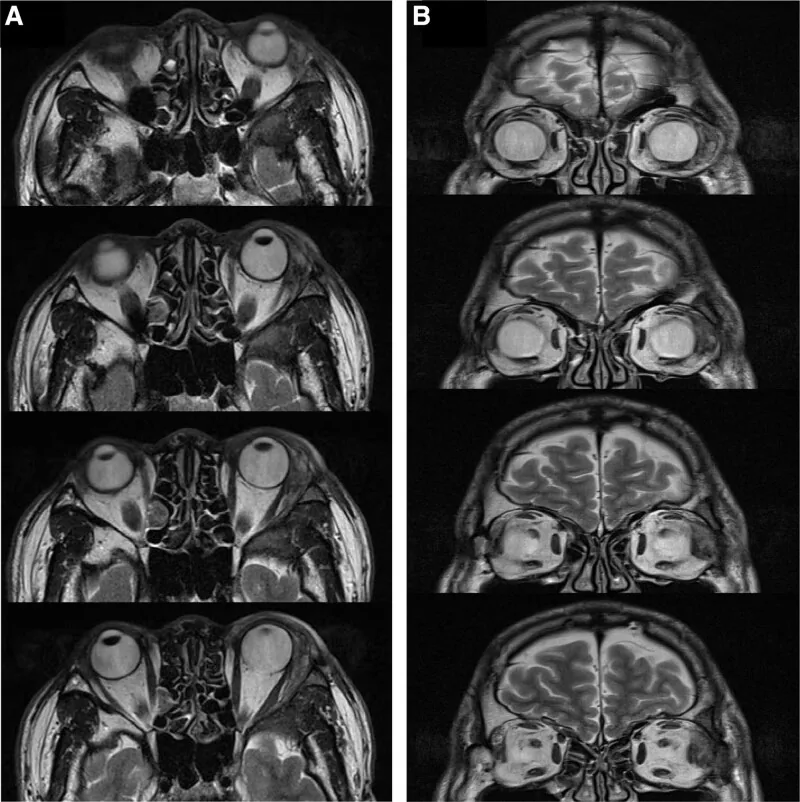
Secondo il rapporto di Williams et al., l’infiltrazione della fossa lacrimale è stata confermata istologicamente nell’82% dei pazienti1). Se la TC mostra che il tumore distrugge l’osso orbitario, si può concludere per una neoplasia maligna, ma occorre notare che esistono carcinomi adenoido cistici senza distruzione ossea.
La causa del carcinoma adenoido cistico è sconosciuta e non sono stabiliti fattori di rischio specifici. Il tumore origina più frequentemente dal lobo orbitario della ghiandola lacrimale ed è un tumore non incapsulato.
Le seguenti caratteristiche patologiche e cliniche sono note come fattori di prognosi sfavorevole:
La diagnosi definitiva si basa sulla valutazione istopatologica. In caso di sospetta malignità, si raccomanda una biopsia escissionale per prevenire la disseminazione intraorbitaria delle cellule tumorali. L’agoaspirato può essere appropriato per tumori non resecabili, ma solo in strutture con un citopatologo esperto.
In presenza di sintomi come esoftalmo che suggeriscono un tumore della ghiandola lacrimale, si eseguono esami oftalmologici (acuità visiva, campo visivo, motilità oculare) e imaging con TC nativa e RM nativa e con contrasto. Se necessaria una ricerca sistemica, si può eseguire PET-TC o TC con contrasto. La diagnosi definitiva si basa su biopsia o esame istopatologico dopo resezione completa.
| Stadio T | Definizione |
|---|---|
| T1 | Diametro massimo ≤ 2 cm |
| T2 | Diametro massimo > 2 cm fino a ≤ 4 cm |
| T3 | Dimensione massima > 4 cm o estensione ai tessuti molli orbitari |
| T4 | Invasione dei seni paranasali, fossa temporale, fossa pterigoidea, fessura orbitaria superiore, seno cavernoso o cervello |
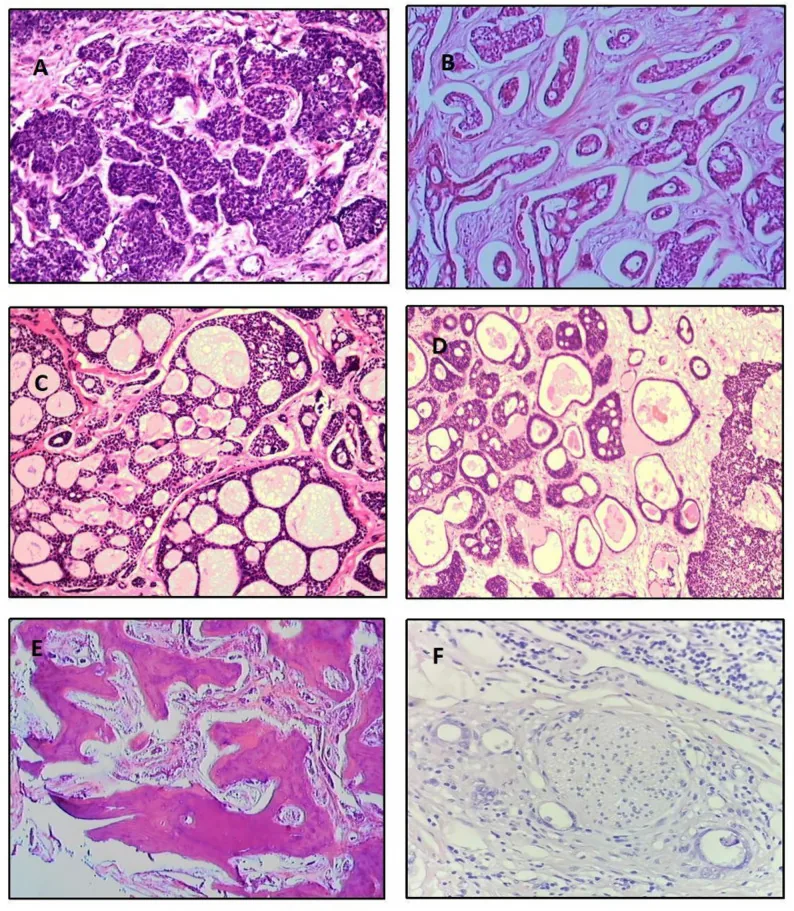
La frequenza dei sottotipi istologici secondo un’analisi di 515 casi è la seguente 5).
Tipo cribriforme
Frequenza: più comune (39,8%)
Caratteristiche: strutture lobulari con accumuli rotondi di mucina. Aspetto «a formaggio svizzero». Prognosi intermedia.
Tipo basaloide
Frequenza: 31,8%
Caratteristiche: scarsamente differenziato. Nuclei basofili grandi e citoplasma scarso. Prognosi peggiore.
Tipo tubulare
Frequenza: 7,4%
Caratteristiche: Tubuli epiteliali rivestiti da 2-3 strati di cellule. Il più differenziato, migliore prognosi.
Esistono anche tipi misti (13,9%), indifferenziati (6,1%) e sclerosanti (0,9%). Un pattern solido >30% è considerato di prognosi sfavorevole1). Istologicamente, le cellule tumorali sono piccole, con citoplasma scarso e basofilo, e nucleo ricco di cromatina. Il confine tra nidi tumorali e stroma è netto, chiaramente diverso dall’adenoma pleomorfo.
La chirurgia è il trattamento di base e la procedura è determinata dallo stadio del tumore e dai reperti di imaging3)5).
L’analisi di Kaplan-Meier ha mostrato che la chirurgia conservativa + radioterapia aveva una migliore sopravvivenza rispetto all’exenterazione ± radioterapia (P < 0,05)5).
Se l’imaging mostra un tumore piccolo e completamente resecabile, si mira alla resezione completa. Se la resezione completa non è possibile, si esegue una biopsia incisionale per confermare la patologia, quindi si considera un’escissione ampia o la radioterapia. Per il carcinoma adenoido cistico lacrimale confinato all’orbita, si può considerare l’exenterazione, ma tenendo conto dei problemi estetici e dell’età/desideri del paziente, si può optare per un trattamento conservativo. Le metastasi linfonodali sono rare (4-9%) e la dissezione linfonodale di solito non è necessaria6).
Anche dopo un’ampia resezione e radioterapia, a volte non è possibile impedire l’infiltrazione del tronco encefalico attraverso il nervo lacrimale. Non si può nemmeno garantire la prevenzione delle metastasi a distanza, ed è necessario un follow-up a lungo termine.
Per i carcinomi adenoidi cistici inoperabili, viene eseguita la radioterapia con particelle pesanti, considerata un trattamento promettente in grado di controllare il tumore preservando palpebra, bulbo oculare e orbita.
La NIAC è stata riportata per la prima volta da Meldrum et al. nel 1998, utilizzando una combinazione di cisplatino intra-arterioso (100 mg/m²) e doxorubicina endovenosa 3)2).
In uno studio di Tse et al. (2013) su 19 casi, in 8 casi con preservazione dell’arteria lacrimale e aderenza al protocollo è stata riportata una sopravvivenza libera da malattia a 10 anni del 100% 2)3).
La combinazione NIAC + resezione/exenteratio orbitae + radioterapia mostra buoni risultati rispetto ad altri trattamenti, con un tasso di recidiva del 10,8%, di metastasi del 14,9% e di mortalità del 18,9% 5). I principali rischi della NIAC includono paralisi facciale transitoria, perdita della vista, ischemia anteriore, neutropenia e trombocitopenia 3).
L’analisi di Kaplan-Meier ha mostrato che la sopravvivenza dopo chirurgia conservativa dell’occhio più radioterapia era migliore rispetto all’exenteratio orbitae ± radioterapia (P<0,05)5). Per i tumori T1-T2 si raccomanda la conservazione dell’occhio, mentre per i tumori T3-T4 o con estensione extraorbitaria si considera l’exenteratio. Tuttavia, a causa di problemi estetici o delle preferenze del paziente, a volte si sceglie un trattamento conservativo.
Le cellule tumorali sono piccole, con citoplasma scarso e bluastro, e nuclei ricchi di cromatina. Istologicamente, il confine tra i nidi tumorali e lo stroma è netto, chiaramente diverso dall’adenoma pleomorfo.
Nel tipo cribriforme, i lumi veri (derivati dalle cellule duttali) e i pseudolumi (cavità di mucina formate dalle cellule mioepiteliali) sono mescolati, dando un aspetto a «formaggio svizzero». Il tipo sclerosante si presenta come cordoni di cellule epiteliali con stroma ialinizzato denso. Un pattern solido superiore al 30% è considerato prognostico sfavorevole1).
I pattern di crescita tumorale sono classificati in cinque tipi (cribriforme, solido, sclerosante, comedocarcinoma, tubulare). Nello stesso campione si possono osservare più pattern di crescita.
| Anomalia molecolare | Contenuto |
|---|---|
| Fusione MYB-NFIB | Traslocazione t(6;9)(q23;p23). Presente in oltre il 70% dei carcinomi adenoidi cistici1) |
| Iperespressione di MYB | Promuove la proliferazione cellulare, la differenziazione, l’angiogenesi e la regolazione positiva dei fattori di crescita1) |
| Mutazione attivante di NOTCH1 | Principale motore di proliferazione e invasione nel carcinoma adenoideo cistico metastatico1)2) |
| Mutazioni KRAS/NRAS/MET | Riportate rispettivamente nel 46%, 8% e 13% dei casi. La cascata EGFR-RAS-RAF come possibile bersaglio terapeutico1)5) |
Nel carcinoma adenoideo cistico della ghiandola lacrimale, il riarrangiamento di MYB è rilevato nel 58% dei casi (Mayo Clinic, 12 casi/25 anni), e la fusione MYB-NFIB è un marcatore diagnostico altamente specifico per il carcinoma adenoideo cistico1). La fusione MYB-NFIB è regolata dal segnale IGF1R dipendente da AKT, e l’inibizione di IGF1R è considerata un bersaglio terapeutico promettente1)3).
L’infiltrazione perineurale è osservata nel 45,3% dei casi e le cellule tumorali possono diffondersi anche in assenza di infiltrazione vascolare o linfatica1). C’è una forte tendenza a infiltrare nervi e vasi linfatici, e l’infiltrazione del tronco encefalico attraverso il nervo lacrimale può verificarsi nelle fasi iniziali della malattia. L’infiltrazione perineurale è associata alla resistenza all’apoptosi dovuta alla regolazione positiva di Bcl-2.
Attualmente non esiste alcun farmaco di terapia a bersaglio molecolare approvato per il carcinoma adenoido cistico delle ghiandole lacrimali. I seguenti bersagli sono in fase di studio 1)3).
I risultati di studi clinici di fase II riportano: dovitinib (ORR 6%, mPFS 8,2 mesi), lenvatinib (ORR 16%, mPFS 17,5 mesi), axitinib (ORR 9%, mPFS 5,7 mesi) 3).
Yu et al. (2022) hanno riportato una valutazione che combina il sequenziamento genomico pre e post trattamento e l’analisi dei marcatori di apoptosi (cCas3, PARP) 2). La frequenza allelica mutante (VAF) della mutazione NOTCH1 dopo NIAC è diminuita dal 18,07% pre-trattamento all’11,34% post-trattamento (riduzione del 37%), suggerendo un potenziale marcatore predittivo di sensibilità al cisplatino.
Attualmente non esiste alcun farmaco mirato approvato per il carcinoma adenoido cistico della ghiandola lacrimale. La fusione MYB-NFIB, la via di segnalazione Notch, la cascata EGFR-RAS-RAF, ecc., sono in fase di studio come potenziali bersagli terapeutici e sono in corso diversi studi clinici di fase II1)3). Per i pazienti che desiderano un trattamento standard, la combinazione di chirurgia e radioterapia è l’opzione attuale.