Dạng Cribriform
Tần suất: Phổ biến nhất (39,8%)
Đặc điểm: Cấu trúc tiểu thùy với các hồ mucin tròn. Hình dạng “giống phô mai Thụy Sĩ”. Tiên lượng trung bình.

Ung thư biểu mô tuyến nang (ACC) là một khối u ác tính hiếm gặp phát sinh từ các tuyến tiết, với tỷ lệ mắc toàn cầu khoảng 3-4 ca trên một triệu dân mỗi năm 1). Chiếm khoảng 1% tổng số ung thư đầu và cổ, và khi xảy ra ở tuyến lệ được gọi là ung thư biểu mô tuyến nang tuyến lệ 1).
Ung thư biểu mô tuyến nang tuyến lệ chiếm khoảng 1,6% tổng số u hốc mắt 3)5), và là loại thường gặp nhất trong các khối u biểu mô ác tính của tuyến lệ, chiếm khoảng 13-40% ung thư tuyến lệ 5). U tuyến lệ chiếm khoảng 10% các tổn thương chiếm chỗ trong hốc mắt, khoảng 20% u đặc tuyến lệ có nguồn gốc biểu mô, trong đó khoảng 45% là ác tính, và khoảng 60% u biểu mô ác tính tuyến lệ là ung thư biểu mô tuyến nang.
Ung thư biểu mô tuyến nang tuyến lệ được Theodor Billroth mô tả lần đầu tiên và ban đầu được đặt tên là “cylindroma” do đặc điểm mô học của nó 5).
Đặc điểm dịch tễ học như sau:
Chiếm khoảng 1,6% tổng số u hốc mắt, tỷ lệ mắc ung thư biểu mô tuyến nang trên toàn cầu là 3–4 ca trên một triệu dân, cực kỳ hiếm1)5). Đây là loại mô học thường gặp nhất trong các u biểu mô ác tính tuyến lệ.
Theo đánh giá lớn 806 ca, tần suất các triệu chứng khởi phát như sau5):
| Triệu chứng | Tần suất |
|---|---|
| Lồi mắt | 27,4% |
| Đau | 21,7% |
| Sưng mí mắt | 10,9% |
| Lệch nhãn cầu | 10,2% |
| Hạn chế vận động mắt | 10,1% |
| Giảm thị lực | 9,3% |
| Song thị (nhìn đôi) | 6,7% |
| Sụp mí mắt | 4,1% |
Đau là triệu chứng đặc trưng của ung thư biểu mô tuyến nang, do sự xâm lấn quanh dây thần kinh (PNI) gây ra. Đây là điểm phân biệt quan trọng với các khối u lành tính. Vì tuyến lệ nằm ở phía trên ngoài của hốc mắt, nhãn cầu thường bị lệch vào trong và xuống dưới. Cũng có thể xuất hiện giảm cảm giác vùng trán thái dương và sụp mí mắt hình chữ S. Thời gian trung bình từ khi xuất hiện triệu chứng đến khi chẩn đoán là 11,1 ± 18,3 tháng (khoảng 0,5–120 tháng) 5).
Tốc độ phát triển của khối u nhanh hơn u tuyến đa hình, và thường kèm theo đau, đây là điểm quan trọng trong chẩn đoán phân biệt. Lồi mắt do khối u lớn, hạn chế vận nhãn do xâm lấn cơ ngoài nhãn cầu và dây thần kinh, và giảm thị lực do chèn ép thần kinh thị giác cũng tiến triển tương đối nhanh.
Sự hiện diện hay không của đau là điểm phân biệt quan trọng nhất. Ung thư biểu mô tuyến nang gây đau do xâm lấn quanh dây thần kinh, trong khi các khối u lành tính (như u tuyến đa hình) không đau và tiến triển chậm. Nếu CT cho thấy phá hủy xương, có thể đánh giá là ác tính, nhưng cũng có ung thư biểu mô tuyến nang không phá hủy xương, do đó nếu có đau, cần tích cực xem xét sinh thiết.
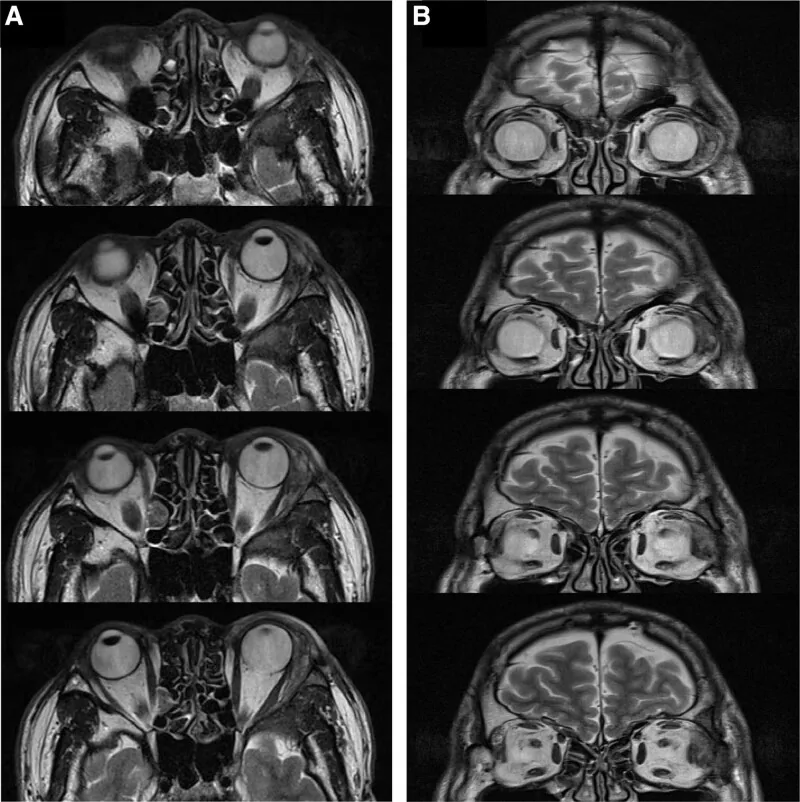
Trong báo cáo của Williams và cộng sự, xâm lấn hố tuyến lệ được xác nhận về mô học ở 82% bệnh nhân 1). Nếu CT cho thấy khối u đã phá hủy xương hốc mắt, có thể đánh giá là ác tính, nhưng cần lưu ý vì có ung thư biểu mô tuyến nang không phá hủy xương.
Nguyên nhân của ung thư biểu mô tuyến nang chưa rõ, và chưa xác định được yếu tố nguy cơ cụ thể. Khối u thường phát sinh từ thùy hốc mắt của tuyến lệ, và là khối u không có vỏ bọc.
Các đặc điểm bệnh lý và lâm sàng sau đây được biết đến là yếu tố tiên lượng xấu:
Chẩn đoán xác định dựa trên đánh giá mô bệnh học. Nếu nghi ngờ ác tính, sinh thiết cắt bỏ được khuyến cáo để ngăn ngừa sự lan rộng của tế bào khối u trong hốc mắt. Sinh thiết hút kim nhỏ có thể phù hợp với các khối u không thể cắt bỏ, nhưng chỉ ở các cơ sở có bác sĩ giải phẫu tế bào giàu kinh nghiệm.
Nếu nghi ngờ khối u tuyến lệ do các triệu chứng như lồi mắt, tiến hành các xét nghiệm nhãn khoa như thị lực, thị trường và vận động mắt, cùng với chẩn đoán hình ảnh bằng CT không cản quang và MRI có và không cản quang. Nếu cần tìm kiếm toàn thân, thực hiện PET-CT hoặc CT có cản quang. Chẩn đoán xác định dựa trên xét nghiệm mô bệnh học sau sinh thiết hoặc cắt bỏ toàn bộ.
| Giai đoạn T | Định nghĩa |
|---|---|
| T1 | Đường kính tối đa 2 cm hoặc nhỏ hơn |
| T2 | Đường kính tối đa lớn hơn 2 cm đến 4 cm hoặc nhỏ hơn |
| T3 | Đường kính lớn nhất >4 cm hoặc lan rộng đến mô mềm ổ mắt |
| T4 | Xâm lấn xoang cạnh mũi, hố thái dương, hố chân bướm, khe ổ mắt trên, xoang hang, não |
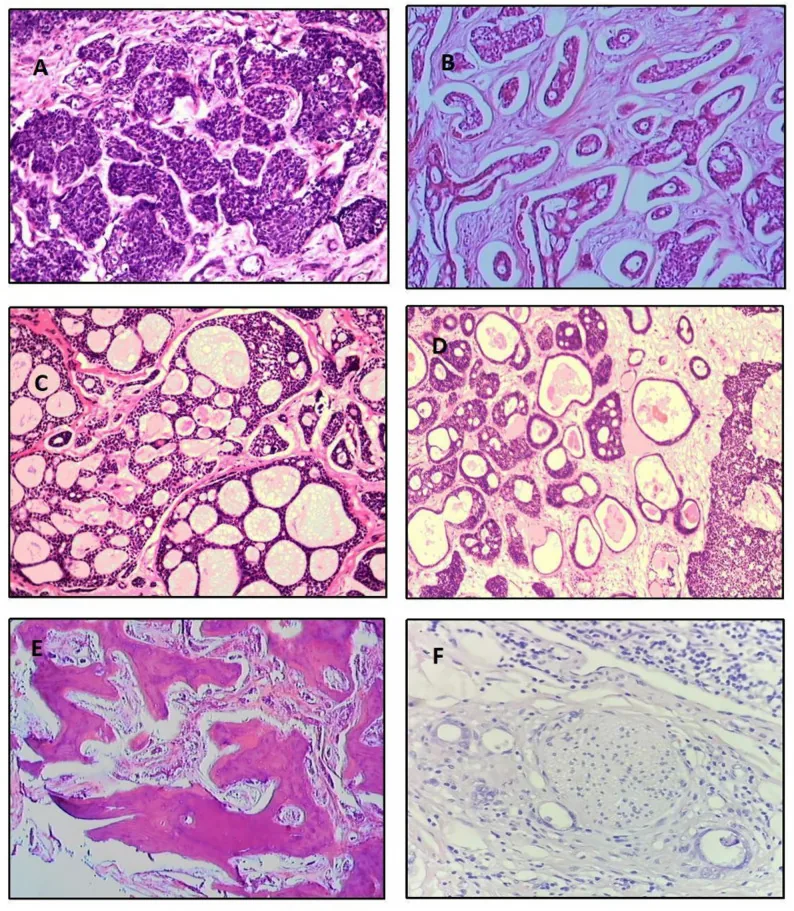
Tần suất các phân nhóm mô học dựa trên phân tích 515 trường hợp như sau5).
Dạng Cribriform
Tần suất: Phổ biến nhất (39,8%)
Đặc điểm: Cấu trúc tiểu thùy với các hồ mucin tròn. Hình dạng “giống phô mai Thụy Sĩ”. Tiên lượng trung bình.
Dạng Tế bào đáy
Tần suất: 31,8%
Đặc điểm: Biệt hóa kém. Nhân ưa kiềm lớn và tế bào chất ít. Tiên lượng xấu nhất.
Dạng Ống
Tần suất: 7,4%
Đặc điểm: Ống biểu mô lót bởi 2-3 lớp tế bào. Biệt hóa cao nhất, tiên lượng tốt nhất.
Ngoài ra, còn có các loại hỗn hợp (13,9%), không biệt hóa (6,1%) và xơ cứng (0,9%). Nếu dạng đặc vượt quá 30%, tiên lượng xấu 1). Về mô học, tế bào u nhỏ, bào tương ít và hơi xanh, nhân giàu chất nhiễm sắc. Ranh giới giữa đám u và mô đệm rõ ràng, khác biệt rõ với u tuyến đa dạng.
Phẫu thuật là phương pháp điều trị cơ bản, và phương pháp phẫu thuật được xác định dựa trên giai đoạn u và kết quả hình ảnh 3)5).
Phân tích Kaplan-Meier cho thấy phẫu thuật bảo tồn mắt kết hợp xạ trị có tỷ lệ sống sót tốt hơn so với nội soi hốc mắt có hoặc không có xạ trị (P<0,05) 5).
Nếu u nhỏ và có thể cắt bỏ hoàn toàn theo hình ảnh, hãy nhắm đến cắt bỏ hoàn toàn. Nếu không thể cắt bỏ hoàn toàn, hãy thực hiện sinh thiết cắt bỏ để xác nhận giải phẫu bệnh, sau đó xem xét cắt bỏ rộng hoặc xạ trị. Đối với ung thư biểu mô tuyến nang tuyến lệ, nếu u chỉ giới hạn trong hốc mắt, hãy xem xét nội soi hốc mắt, nhưng có thể chọn điều trị bảo tồn dựa trên vấn đề thẩm mỹ, tuổi tác và mong muốn của bệnh nhân. Di căn hạch bạch huyết hiếm gặp (4-9%), và thường không cần nạo vét hạch 6).
Ngay cả khi phẫu thuật cắt bỏ rộng và xạ trị, đôi khi không thể ngăn chặn sự xâm lấn vào thân não qua dây thần kinh lệ. Không phải lúc nào cũng ngăn ngừa được di căn xa, do đó cần theo dõi lâu dài.
Đối với ung thư biểu mô tuyến nang không thể phẫu thuật, liệu pháp ion carbon nặng đã được thực hiện và được coi là liệu pháp đầy hứa hẹn có thể kiểm soát khối u trong khi bảo tồn mí mắt, nhãn cầu và hốc mắt.
NIAC lần đầu tiên được báo cáo bởi Meldrum và cộng sự vào năm 1998, sử dụng phối hợp cisplatin (100 mg/m²) qua động mạch và doxorubicin tĩnh mạch 3)2).
Trong nghiên cứu 19 ca của Tse và cộng sự (2013), tỷ lệ sống không bệnh 10 năm là 100% được báo cáo ở 8 ca bảo tồn được động mạch lệ và tuân thủ phác đồ 2)3).
Sự kết hợp NIAC + cắt bỏ/nạo hốc mắt + xạ trị cho thấy kết quả tốt so với các liệu pháp khác, với tỷ lệ tái phát 10,8%, di căn 14,9% và tử vong 18,9% 5). Các nguy cơ chính của NIAC bao gồm liệt mặt tạm thời, mất thị lực, thiếu máu cục bộ vùng trước, giảm bạch cầu trung tính và giảm tiểu cầu 3).
Phân tích Kaplan-Meier cho thấy tỷ lệ sống sót của phẫu thuật bảo tồn nhãn cầu kết hợp xạ trị tốt hơn so với phẫu thuật nội soi hốc mắt có hoặc không có xạ trị (P<0,05) 5). Đối với khối u T1-T2, khuyến cáo bảo tồn nhãn cầu; đối với khối u T3-T4 hoặc lan rộng ngoài hốc mắt, cân nhắc phẫu thuật nội soi hốc mắt. Tuy nhiên, đôi khi điều trị bảo tồn được lựa chọn do vấn đề thẩm mỹ hoặc mong muốn của bệnh nhân.
Tế bào u nhỏ, bào tương ít và hơi xanh, nhân giàu chất nhiễm sắc. Về mặt mô học, ranh giới giữa các đám u và mô đệm rõ ràng, khác biệt rõ với u tuyến đa dạng.
Ở thể cribriform, có sự pha trộn giữa lòng thật (có nguồn gốc từ tế bào ống) và lòng giả (khoang chứa nhầy do tế bào biểu mô cơ tạo thành), tạo ra hình ảnh giống phô mai Thụy Sĩ. Thể xơ cứng được quan sát dưới dạng dây biểu mô với mô đệm hyalin hóa dày đặc. Nếu mô hình đặc vượt quá 30%, tiên lượng được coi là xấu 1).
Các mô hình tăng trưởng của khối u được phân loại thành 5 loại (cribriform, đặc, xơ cứng, ung thư biểu mô dạng comedocarcinoma, hình ống). Có thể quan sát thấy nhiều mô hình tăng trưởng trong cùng một mẫu bệnh phẩm.
| Bất thường phân tử | Nội dung |
|---|---|
| Dung hợp MYB-NFIB | Chuyển đoạn t(6;9)(q23;p23). Có mặt trong hơn 70% ung thư biểu mô tuyến dạng nang 1) |
| Biểu hiện quá mức MYB | Thúc đẩy tăng sinh tế bào, biệt hóa, tạo mạch và điều hòa tăng yếu tố tăng trưởng 1) |
| Đột biến hoạt hóa NOTCH1 | Động lực chính của sự tăng sinh và xâm lấn trong ung thư biểu mô tuyến dạng nang di căn 1)2) |
| Đột biến KRAS/NRAS/MET | Được báo cáo lần lượt là 46%, 8% và 13%. Thác EGFR-RAS-RAF có thể là mục tiêu điều trị 1)5) |
Trong ung thư biểu mô tuyến dạng nang tuyến lệ, tái sắp xếp MYB được phát hiện trong 58% trường hợp (Mayo Clinic 12 ca/25 năm), và dung hợp MYB-NFIB là dấu ấn chẩn đoán đặc hiệu cao cho ung thư biểu mô tuyến dạng nang 1). Dung hợp MYB-NFIB được điều hòa bởi tín hiệu IGF1R phụ thuộc AKT, và ức chế IGF1R được coi là mục tiêu điều trị đầy hứa hẹn 1)3).
Xâm lấn quanh dây thần kinh được tìm thấy trong 45,3% trường hợp, và các tế bào khối u có thể lan rộng ngay cả khi không có xâm lấn mạch máu hoặc bạch huyết 1). Có xu hướng mạnh mẽ xâm lấn dây thần kinh và mạch bạch huyết, và xâm lấn thân não qua dây thần kinh lệ có thể xảy ra từ giai đoạn đầu của bệnh. Xâm lấn quanh dây thần kinh có liên quan đến kháng apoptosis do tăng điều hòa Bcl-2.
Hiện tại chưa có thuốc điều trị nhắm mục tiêu phân tử nào được phê duyệt cho ung thư biểu mô tuyến nang tuyến lệ. Các mục tiêu sau đây đang được nghiên cứu 1)3).
Kết quả thử nghiệm lâm sàng giai đoạn II báo cáo: dovitinib (ORR 6%, mPFS 8,2 tháng), lenvatinib (ORR 16%, mPFS 17,5 tháng) và axitinib (ORR 9%, mPFS 5,7 tháng) 3).
Yu et al. (2022) báo cáo đánh giá kết hợp giải trình tự gen trước và sau điều trị với phân tích dấu ấn apoptosis (cCas3, PARP) 2). Tần số alen biến thể (VAF) của đột biến NOTCH1 sau NIAC giảm từ 18,07% trước điều trị xuống 11,34% sau điều trị (giảm 37%), cho thấy tiềm năng là dấu ấn dự đoán nhạy cảm với cisplatin.
Hiện tại không có thuốc điều trị nhắm mục tiêu phân tử nào được phê duyệt cho ung thư biểu mô tuyến nang của tuyến lệ. Sự dung hợp MYB-NFIB, con đường tín hiệu Notch và dòng thác EGFR-RAS-RAF đang được nghiên cứu như các mục tiêu điều trị, và một số thử nghiệm lâm sàng giai đoạn II đang tiến hành1)3). Nếu muốn điều trị tiêu chuẩn, kết hợp phẫu thuật và xạ trị là lựa chọn hiện tại.