معاینه فوندوس
ناحیه آتروفی: ناحیه هیپوپیگمانته با مرزهای واضح. دارای لبههای اسکالوپ (دندانهدار).
یافتههای اطراف: دروسن و تغییرات رنگدانهای در اطراف ضایعه مشاهده میشود.
فنوتیپ ضایعه: ناحیه آتروفی RPE و/یا کوریوکاپیلاریس با مرزهای مشخص2).

آواسینکاپتاد پگول (Avacincaptad pegol; ACP) یک آپتامر RNA پگیله است که به مکمل C5 متصل میشود. نام تجاری آن IZERVAY (آیزرِوی) است. توسط شرکت آستلاس فارما ساخته شده و به عنوان محلول تزریق داخل زجاجیهای عرضه میشود. در آگوست 2023، FDA ایالات متحده آن را به عنوان درمانی برای آتروفی جغرافیایی (GA) ناشی از دژنراسیون ماکولا وابسته به سن تأیید کرد1). این دومین داروی تأیید شده برای GA پس از پگستاکوپلان (Syfovre)، یک مهارکننده مکمل C3/C3b است2).
GA (آتروفی جغرافیایی) یک فرم پیشرفته از دژنراسیون ماکولا وابسته به سن است که باعث از دست دادن غیرقابل برگشت بینایی به دلیل آتروفی اپیتلیوم رنگدانه شبکیه (RPE)، سلولهای گیرنده نور و لایه مویرگی مشیمیه میشود1). شیوع جهانی GA حدود 8.7٪ است و حدود 5 میلیون نفر در جهان (1 تا 1.6 میلیون نفر در ایالات متحده) را مبتلا میکند1). این بیماری علت اصلی از دست دادن بینایی مرکزی در افراد بالای 55 سال است، با شیوع 3.5٪ در سن 75 سالگی و حدود 22٪ در افراد بالای 90 سال1). حدود 20٪ از موارد نابینایی قانونی در ایالات متحده و حدود 26٪ در بریتانیا ناشی از GA است3). در ژاپن، این بیماری در مردان و زنان بالای 50 سال (نسبت مرد به زن حدود 3:1) رخ میدهد و با دگرگونی بینایی و اسکوتوم مرکزی شروع میشود و با پیشرفت، دید اصلاح شده به کمتر از 0.1 میرسد.
این یک آپتامر RNA پگیله است که مکمل C5 را مهار میکند. این دارو در سال 2023 توسط FDA برای درمان آتروفی جغرافیایی تأیید شد و گسترش ضایعه GA را کند میکند، اما در حال حاضر نشان داده نشده است که بافت آتروفی شده را ترمیم یا بینایی را بهبود بخشد. برای جزئیات بیشتر به بخش «روشهای درمانی استاندارد» مراجعه کنید.
علائم ذهنی اصلی GA به شرح زیر است1).
GA نسبت به دژنراسیون ماکولای وابسته به سن از نوع اگزوداتیو کاهش بینایی آهستهتری دارد، اما تأثیر طولانیمدت آن بر عملکرد بینایی قابل توجه است2). در طی دو سال، حدود 75٪ از چشمهای مبتلا 5 حرف، حدود 50٪ 10 حرف (3 خط) و حدود 25٪ 15 حرف (6 خط) از دست میدهند3). پیشرفت GA بر کیفیت زندگی (هم مرتبط با بینایی و هم سلامت عمومی) تأثیر منفی میگذارد و با مشکلاتی در زندگی مستقل و سلامت روان همراه است3). افزایش افسردگی و اضطراب نیز گزارش شده است4).
در طی دو سال، حدود 75٪ از چشمها 5 حرف (1 خط)، حدود 50٪ 10 حرف (3 خط) و حدود 25٪ 15 حرف (6 خط) از بینایی خود را از دست میدهند3). در ضایعات منفرد که فووه آ را درگیر میکنند، خطر کاهش بینایی بالاست، در حالی که در ضایعات متعدد، سرعت گسترش سریعتر است اما تأثیر بر بینایی نسبتاً آهستهتر است4).
معاینه فوندوس
ناحیه آتروفی: ناحیه هیپوپیگمانته با مرزهای واضح. دارای لبههای اسکالوپ (دندانهدار).
یافتههای اطراف: دروسن و تغییرات رنگدانهای در اطراف ضایعه مشاهده میشود.
فنوتیپ ضایعه: ناحیه آتروفی RPE و/یا کوریوکاپیلاریس با مرزهای مشخص2).
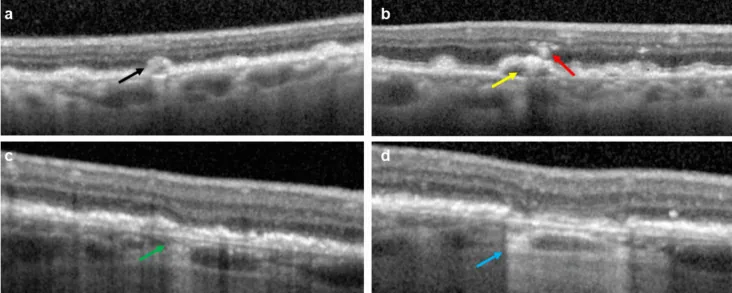
FAF و OCT
فلورسانس خودبخودی فوندوس (FAF): هیپوفلورسانس شدید به دلیل کمبود لیپوفوسین. الگوی هیپرفلورسانس اطراف، سرعت گسترش GA را پیشبینی میکند.
OCT (شبکیه خارجی): از دست دادن لایه هستهای خارجی، ناحیه بیضیشکل (EZ) و ناحیه بیندیجیتاسیون، از دست دادن RPE، افزایش شفافیت به مشیمیه (choroidal hypertransmission). یکپارچگی EZ برای پیشبینی پیشآگهی بینایی مفید است4).
GA یک فرم پیشرفته از دژنراسیون ماکولا وابسته به سن است و عوامل خطر آن با عوامل خطر کلی دژنراسیون ماکولا وابسته به سن همپوشانی دارد.
عوامل خطر غیرقابل اصلاح:
عوامل خطر قابل اصلاح:
زمینه پاتولوژیک: تجمع دروزن باعث تخریب گیرندههای نوری و سلولهای اپیتلیوم رنگدانه شبکیه (RPE) شده و به سمت آتروفی پیشرفت میکند 1). فعالسازی غیرطبیعی سیستم کمپلمان نقش مهمی در شروع و پیشرفت GA ایفا میکند 1)3). ضایعات پیشدرآمد GA شامل ناهنجاریهای اپیتلیوم رنگدانه شبکیه (تغییر رنگدانه، هیپرپیگمانتاسیون، هیپوپیگمانتاسیون) و دروزن نرم هستند.
برای تشخیص GA، ترکیبی از تصویربرداری چندوجهی توصیه میشود 2).
ویژگیهای هر آزمایش در زیر آورده شده است.
| روش آزمایش | هدف اصلی | نکات ویژه |
|---|---|---|
| فلورسانس خودبخودی فوندوس (FAF) | اندازهگیری محدوده GA | روش اندازهگیری استاندارد. قابلیت پیشبینی سرعت پیشرفت نیز وجود دارد |
| OCT (SD/SS) | ارزیابی لایههای خارجی شبکیه و RPE | پیشبینی پیشآگهی بینایی با یکپارچگی EZ 4) |
| میکروپریمتری | اندازهگیری کمی حساسیت شبکیه | امکان ارزیابی عملکرد باقیمانده 4) |
روش تجویز ACP: 2 میلیگرم (0.1 میلیلیتر از محلول 20 میلیگرم/میلیلیتر) به صورت تزریق داخل زجاجیهای یک بار در ماه 1).
اثربخشی ACP در دو کارآزمایی تصادفیسازی شده دوسوکور GATHER1 (فاز 2/3) و GATHER2 (فاز 3) ارزیابی شد.
| آزمایش | نرخ مهار گسترش GA | آمار |
|---|---|---|
| GATHER1 (12 ماه، تبدیل ریشه مربع) | کاهش 27.4% | p=0.00727) |
| GATHER1 (18 ماه، مقادیر مشاهدهشده) | کاهش 32.2% | 95%CI 0.480–1.8338) |
| GATHER2 (12 ماه، مقادیر مشاهدهشده) | کاهش 17.7% | p=0.0041) |
نتایج 12 ماهه GATHER2 توسط Khanani و همکاران (2023) نشان داد که در گروه ACP (n=271) در مقایسه با گروه sham (n=269)، نرخ رشد GA 0.336 در مقابل 0.392 میلیمتر در سال (تفاوت 0.056 میلیمتر در سال؛ 95%CI 0.016–0.096؛ p=0.006) مهار معنیداری مشاهده شد6).
دادههای 24 ماهه GATHER2 نشان داد که در گروه تزریق ماهانه 14% کاهش و در گروهی که پس از 12 ماه از تزریق ماهانه به دو ماه یکبار تغییر یافت، 19% کاهش مشاهده شد2).
بهبود معنیدار در بهترین دید اصلاحشده در هیچیک از GATHER1 و GATHER2 نشان داده نشد1)2). با این حال، در تحلیلهای پسروی، از دست دادن 15 حرف یا بیشتر از بهترین دید اصلاحشده در 4.0% از گروه ACP در مقابل 7.6% از گروه sham مشاهده شد و خطر از دست دادن پایدار 15 حرف 56% کاهش یافت (HR 0.44؛ 95%CI 0.21–0.92)1)5).
پگستاکوپلان (Syfovre)، یک مهارکننده کمپلمان C3/C3b، در کارآزماییهای فاز 3 OAKS/DERBY با تزریق ماهانه، پس از 12 ماه کاهش گسترش GA را به میزان 21% (در کارآزمایی OAKS) نشان داد2).
عوارض جانبی اصلی (ادغام GATHER1 و GATHER2) در زیر آورده شده است1).
| عوارض جانبی | گروه ACP | گروه sham |
|---|---|---|
| خونریزی زیر ملتحمه | 13% | 9% |
| افزایش فشار داخل چشم | 9% | 1% |
| تاری دید | 8% | 5% |
| تبدیل عروق جدید ماکولار | 7% | 4% |
| درد چشم | 4% | 3% |
اندوفتالمیت و نوروپاتی ایسکمیک بینایی در طی ۱۲ ماه گزارش نشده است1). افزایش فشار چشم عمدتاً گذرا و مرتبط با تزریق است1).
خطر تبدیل عروق جدید ماکولار در GATHER1، گروه ACP 2mg 9.0% در مقابل گروه sham 2.7% و در GATHER2، گروه ACP 2mg 6.7% در مقابل گروه sham 4.1% بود1). در صورت بروز عروق جدید ماکولار (عروق جدید مشیمیه)، درمان با anti-VEGF ضروری است2).
موارد منع مصرف: عفونت چشمی یا اطراف چشم، التهاب فعال داخل چشمی.
در آزمایش GATHER بهبود قابل توجهی در بهترین حدت بینایی اصلاح شده نشان داده نشد1)2). با این حال، تحلیلهای پسرویدادی نشان میدهد که خطر کاهش مداوم بینایی ۱۵ حرف یا بیشتر ۵۶٪ کاهش مییابد (HR 0.44)، که انتظار میرود به حفظ طولانیمدت بینایی کمک کند5).
در دادههای تلفیقی مطالعه GATHER، تبدیل به رگهای جدید ماکولا در ۷٪ از گروه درمان و ۴٪ از گروه شم مشاهده شد2). در صورت بروز رگهای جدید ماکولا، با درمان ضد VEGF مدیریت میشود. پایش منظم با OCT ضروری است.
فعالسازی غیرطبیعی سیستم کمپلمان نقش اصلی را در بروز و پیشرفت GA ایفا میکند.
سیستم کمپلمان از سه مسیر کلاسیک، لکتین و جایگزین تشکیل شده است1). هر سه مسیر در برش C3 توسط آنزیم C3 کانورتاز (C3 → C3a + C3b) همگرا میشوند1). سپس آنزیم C5 کانورتاز، C5 را به C5a (آنافیلاتوکسین) و C5b برش میدهد1).
با افزایش سن، تنظیم افزایشی بیان ژنهای مرتبط با سیستم کمپلمان افزایش مییابد1). پلیمورفیسمهای ژنتیکی در CFH، CFB، C3 و ARMS2 با حساسیت به GA مرتبط هستند1)2).
ACP یک الیگونوکلئوتید تکرشتهای سنتز شیمیایی است که با پگیلاسیون، پایداری زیستی و کاهش کلیرانس آن افزایش یافته است1).
با میل ترکیبی بالا به C5 متصل شده و از برش آن به C5a و C5b جلوگیری میکند1).
مزیت نظری مهار C5: با حفظ C3a (که دارای عملکردهای ضدالتهابی و دفاع میزبان است) در بالادست C5، از تجمع اینفلامازوم و تشکیل MAC جلوگیری میکند1). در حالی که مهارکنندههای C3 ممکن است عملکرد دفاعی در برابر عفونت را در بالادست مختل کنند، مهار C5 به عنوان یک نقطه اثر انتخابیتر در نظر گرفته میشود1).
تصور میشود که محصولات برش C5 یعنی C5a و MAC از طریق آسیب التهابی به RPE باعث پیشرفت GA میشوند1). با مهار C5، از تشکیل MAC و تولید C5a جلوگیری شده و در عین حال عملکرد ضدالتهابی و دفاع میزبان C3a در بالادست حفظ میشود. از آنجایی که مهار C3 نگرانی افزایش خطر عفونت را به همراه دارد، C5 به عنوان هدف ایمنتری در نظر گرفته میشود1).
دادههای ۲۴ ماهه GATHER2 نشان داد که در گروه دریافتکننده ماهانه ۱۴٪ و در گروهی که پس از ۱۲ ماه به دوز دو ماه یکبار تغییر یافت ۱۹٪ کاهش در گسترش GA مشاهده شد2). این احتمال وجود دارد که تغییر به دوز دو ماه یکبار نرخ مهار GA را کاهش ندهد و بهینهسازی فاصله دوز یک چالش آینده است.
تحلیلهای پسرویدادی کاهش ۵۶٪ در خطر از دست دادن پایدار ۱۵ حرف یا بیشتر از حدت بینایی (HR 0.44) را نشان داد، اما این یک تحلیل پسرویدادی و اکتشافی است و نتیجه قطعی نیست1)5). تأیید با یک مطالعه آیندهنگر که نقطه پایانی بینایی را به عنوان معیار اصلی در نظر میگیرد، ضروری است.
کاربرد یکپارچگی ناحیه بیضیشکل (EZ) به عنوان یک بیومارکر در حال بررسی است1). تحقیقات در مورد پیشبینی عملکرد بینایی از طریق بیومارکرهای OCT با استفاده از یادگیری ماشین نیز در حال پیشرفت است4). اهمیت تشخیص زودهنگام GA و مداخله زودهنگام درمانی تأکید شده است1) و انتظار میرود این بیومارکرها به عنوان ابزارهای پیشبینی پیشآگهی تثبیت شوند.
الوسیدن مکانیسم افزایش خطر نئوواسکولاریزاسیون ماکولا (نئوواسکولاریزاسیون مشیمیهای) ناشی از مهار کمپلمان یک چالش مهم باقیمانده است1). فرضیهای وجود دارد که سیستم کمپلمان در مهار رگزایی نیز نقش دارد و درک تعادل آن میتواند بر طراحی داروهای آینده تأثیر بگذارد.