眼底檢查
萎縮區域:邊界清晰的低色素區域,邊緣呈扇形。
周圍所見:病變周圍可見玻璃膜疣和色素改變。
病變表現型:RPE和/或脈絡膜毛細血管板的邊界清晰的萎縮區2)。

阿伐西卡普他德聚乙二醇(Avacincaptad pegol; ACP)是一種結合補體C5的聚乙二醇化RNA適體。商品名為IZERVAY。由安斯泰來製藥開發,作為玻璃體內注射液提供。2023年8月,美國FDA核准其用於治療年齡相關性黃斑部退化繼發的地圖狀萎縮(GA)1)。它是繼補體C3/C3b抑制劑pegcetacoplan(Syfovre)之後第二個獲准用於GA的藥物2)。
GA(地圖狀萎縮)是年齡相關性黃斑部退化的進展形式,由於視網膜色素上皮(RPE)、感光細胞和脈絡膜微血管層的萎縮,導致不可逆的視力喪失1)。GA的全球盛行率約為8.7%,全球約500萬人(美國100-160萬人)受影響1)。它是55歲以上人群中心視力喪失的主要原因,75歲時盛行率為3.5%,90歲以上約為22%1)。美國約20%的法律失明病例、英國約26%由GA引起3)。在日本,50歲以上男女(男:女≈3:1)發病,始於視物變形和中心暗點,進展至矯正視力低於0.1。
它是一種抑制補體C5的聚乙二醇化RNA適體。2023年FDA核准用於治療地圖狀萎縮,可延緩GA病灶擴大,但目前尚未顯示能恢復萎縮組織或改善視力。詳情請參見「標準治療方法」一節。
GA的主要自覺症狀如下1)。
GA比滲出型年齡相關性黃斑部病變視力下降更緩慢,但對長期視功能影響較大2)。2年內約75%的患眼喪失5個字母,約50%喪失10個字母(3行),約25%喪失15個字母(6行)3)。GA進展對生活品質(視覺相關和健康相關)產生負面影響,並伴隨獨立生活和精神健康的困難3)。憂鬱和焦慮的增加也有報告4)。
2年內約75%的眼睛喪失5個字母(1行),約50%喪失10個字母(3行),約25%喪失15個字母(6行)的視力3)。累及中心凹的單一病變視力下降風險高,多發病變擴大速度快但對視力影響相對緩慢4)。
眼底檢查
萎縮區域:邊界清晰的低色素區域,邊緣呈扇形。
周圍所見:病變周圍可見玻璃膜疣和色素改變。
病變表現型:RPE和/或脈絡膜毛細血管板的邊界清晰的萎縮區2)。
FAF和OCT
眼底自體螢光(FAF):因脂褐素缺乏而呈現的濃密低自體螢光。周圍的高自體螢光模式可預測GA的擴大速度。
OCT(外層視網膜):外核層、橢圓體帶(EZ)和指間帶喪失,RPE喪失,脈絡膜透光增強。EZ完整性有助於預測視力預後4)。
GA是年齡相關性黃斑部病變的進展形式,其風險因素與整體年齡相關性黃斑部病變的風險因素重疊。
不可改變的風險因素:
可改變的風險因素:
病理背景:玻璃膜疣積聚誘導光感受器和RPE變性,進而進展為萎縮1)。補體系統的異常活化在GA的發生和進展中扮演重要角色1)3)。GA的前驅病變包括視網膜色素上皮異常(色素不均、色素沉著、低色素)和軟性玻璃膜疣。
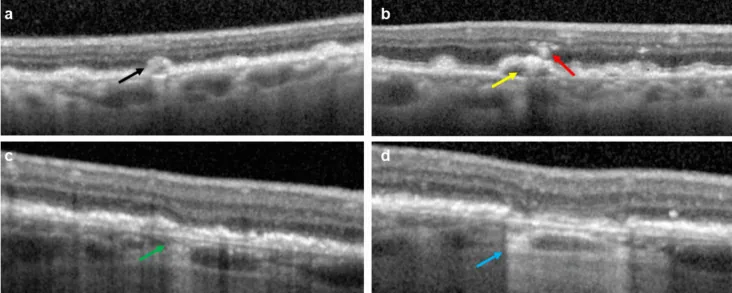
GA的診斷建議採用多模式影像組合2)。
各項檢查的特性如下所示。
| 檢查方法 | 主要目的 | 備註 |
|---|---|---|
| 眼底自體螢光(FAF) | 測量GA範圍 | 標準測量方法。也可預測進展速度。 |
| OCT(SD/SS) | 外層視網膜/RPE評估 | EZ完整性預測視力預後4) |
| 微視野檢查 | 視網膜敏感度定量 | 可評估殘餘功能4) |
ACP給藥方法:2mg(20mg/mL溶液0.1mL)每月一次玻璃體內注射1)。
GATHER1(2/3期)和GATHER2(3期)兩項隨機雙盲試驗評估了ACP的有效性。
| 試驗 | GA擴大抑制率 | 統計 |
|---|---|---|
| GATHER1(12個月,平方根轉換) | 減少27.4% | p=0.00727) |
| GATHER1(18個月,觀測值) | 減少32.2% | 95%CI 0.480–1.8338) |
| GATHER2(12個月,觀測值) | 減少17.7% | p=0.0041) |
Khanani等人(2023)的GATHER2 12個月結果顯示,ACP組(n=271)與假手術組(n=269)相比,GA生長率顯著抑制:0.336 vs 0.392 mm/年(差異0.056 mm/年;95%CI 0.016–0.096;p=0.006)6)。
GATHER2的24個月數據顯示,每月給藥組減少14%,12個月後從每月給藥轉為隔月給藥組減少19%2)。
GATHER1和GATHER2均未顯示最佳矯正視力有顯著改善1)2)。但事後分析提示,最佳矯正視力喪失15個字母或以上的比例在ACP組為4.0%,假手術組為7.6%,持續性15個字母喪失風險降低56%(HR 0.44;95%CI 0.21–0.92)1)5)。
補體C3/C3b抑制劑佩格塞塔科普蘭(Syfovre)在OAKS/DERBY的第三期試驗中,每月一次給藥,12個月時GA擴大抑制率為21%(OAKS試驗)2)。
主要不良反應(GATHER1/GATHER2合併)如下所示1)。
| 不良反應 | ACP組 | 假注射組 |
|---|---|---|
| 結膜下出血 | 13% | 9% |
| 眼壓升高 | 9% | 1% |
| 視力模糊 | 8% | 5% |
| 黃斑新生血管轉化 | 7% | 4% |
| 眼痛 | 4% | 3% |
12個月內未報告眼內炎或缺血性視神經病變1)。眼壓升高主要與注射操作相關,且為一過性1)。
黃斑新生血管轉化風險:在GATHER1中,ACP 2mg組為9.0%,假注射組為2.7%;在GATHER2中,ACP 2mg組為6.7%,假注射組為4.1%1)。如果發生黃斑新生血管(脈絡膜新生血管),需要抗VEGF治療2)。
禁忌:患有眼或眼周感染、活動性眼內炎症的患者。
GATHER試驗未顯示最佳矯正視力有顯著改善1)2)。但事後分析提示,持續15個字母或以上的視力喪失風險降低56%(HR 0.44),有望有助於長期維持視力5)。
GATHER試驗的整合數據顯示,治療組7%、假手術組4%出現黃斑新生血管轉化2)。發生黃斑新生血管時,以抗VEGF治療處理。定期OCT監測不可或缺。
補體系統的異常活化在GA的發生與進展中扮演核心角色。
補體系統由古典途徑、凝集素途徑與替代途徑三條途徑構成1)。三條途徑均經由C3轉化酶切割C3(C3→C3a+C3b)匯合1)。隨後,C5轉化酶將C5切割為C5a(過敏毒素)與C5b1)。
隨著年齡增長,補體系統相關基因的表現上調1)。CFH、CFB、C3與ARMS2的基因多型性與GA易感性相關1)2)。
ACP是一種化學合成的單股寡核苷酸,經由聚乙二醇化提高生物穩定性並延緩清除1)。
它與C5高親和力結合,抑制其切割為C5a與C5b1)。
C5抑制的理論優勢:在保留C5上游C3a(具有抗發炎與宿主防禦功能)的同時,阻斷發炎小體募集與MAC形成1)。與可能損害上游宿主防禦功能的C3抑制劑相比,C5抑制被認為是更具選擇性的標靶1)。
C5切割產物C5a與MAC被認為透過對RPE的發炎損傷促進GA進展1)。抑制C5可阻止MAC形成與C5a生成,同時保留上游C3a的抗發炎與宿主防禦功能。由於C3抑制存在感染風險升高的疑慮,C5被認為是更安全的標靶1)。
GATHER2的24個月數據顯示,每月給藥組的GA擴大抑制率為14%,12個月後轉為隔月給藥組的抑制率為19% 2)。這表明轉為隔月給藥可能不會降低GA抑制率,給藥間隔的最佳化是未來的課題。
事後分析提示持續15個字母或以上的視力喪失風險降低56%(HR 0.44),但這是事後探索性分析,並非確定性結論 1)5)。需要以視力終點為主要評估指標的前瞻性試驗進行驗證。
EZ(橢圓體帶)完整性作為生物標誌物的實用性正在探索中 1)。利用機器學習從OCT生物標誌物預測視功能的研究也在進行中 4)。GA早期發現和早期治療介入的重要性被強調 1),這些生物標誌物有望被確立為預後預測工具。
闡明補體抑制導致黃斑新生血管(脈絡膜新生血管)發生風險增加的機制是一個重要的未解決問題 1)。有假說認為補體系統也參與抑制血管新生,理解這一平衡被認為會影響未來的藥物設計。