眼底检查
萎缩区域:边界清晰的低色素区域,边缘呈扇形。
周围所见:病变周围可见玻璃膜疣和色素改变。
病变表型:RPE和/或脉络膜毛细血管板的边界清晰的萎缩区2)。

阿伐西卡普他德聚乙二醇(Avacincaptad pegol; ACP)是一种结合补体C5的聚乙二醇化RNA适配体。商品名为IZERVAY。由安斯泰来制药开发,作为玻璃体内注射液提供。2023年8月,美国FDA批准其用于治疗年龄相关性黄斑变性继发的地图状萎缩(GA)1)。它是继补体C3/C3b抑制剂pegcetacoplan(Syfovre)之后第二个获批用于GA的药物2)。
GA(地图状萎缩)是年龄相关性黄斑变性的进展形式,由于视网膜色素上皮(RPE)、感光细胞和脉络膜毛细血管层的萎缩,导致不可逆的视力丧失1)。GA的全球患病率约为8.7%,全球约500万人(美国100-160万人)受累1)。它是55岁以上人群中心视力丧失的主要原因,75岁时患病率为3.5%,90岁以上约为22%1)。美国约20%的法律失明病例、英国约26%由GA引起3)。在日本,50岁以上男女(男:女≈3:1)发病,始于视物变形和中心暗点,进展至矫正视力低于0.1。
它是一种抑制补体C5的聚乙二醇化RNA适配体。2023年FDA批准用于治疗地图状萎缩,可延缓GA病变扩大,但目前尚未显示能恢复萎缩组织或改善视力。详情请参见“标准治疗方法”一节。
GA的主要自觉症状如下1)。
GA比渗出型年龄相关性黄斑变性视力下降更缓慢,但对长期视功能影响较大2)。2年内约75%的患眼丧失5个字母,约50%丧失10个字母(3行),约25%丧失15个字母(6行)3)。GA进展对生活质量(视觉相关和健康相关)产生负面影响,并伴有独立生活和精神健康的困难3)。抑郁和焦虑的增加也有报道4)。
2年内约75%的眼睛丧失5个字母(1行),约50%丧失10个字母(3行),约25%丧失15个字母(6行)的视力3)。累及中心凹的单发病变视力下降风险高,多发病变扩大速度快但对视力影响相对缓慢4)。
眼底检查
萎缩区域:边界清晰的低色素区域,边缘呈扇形。
周围所见:病变周围可见玻璃膜疣和色素改变。
病变表型:RPE和/或脉络膜毛细血管板的边界清晰的萎缩区2)。
FAF和OCT
眼底自发荧光(FAF):由于脂褐素缺乏而呈现的浓密低自发荧光。周围的高自发荧光模式可预测GA的扩大速度。
OCT(外层视网膜):外核层、椭圆体带(EZ)和指间带缺失,RPE缺失,脉络膜透光增强。EZ完整性有助于预测视力预后4)。
GA是年龄相关性黄斑变性的进展形式,其风险因素与整体年龄相关性黄斑变性的风险因素重叠。
不可改变的风险因素:
可改变的风险因素:
病理背景:玻璃膜疣积聚诱导光感受器和RPE变性,进而进展为萎缩1)。补体系统的异常激活在GA的发生和进展中起重要作用1)3)。GA的前驱病变包括视网膜色素上皮异常(色素不均、色素沉着、色素减退)和软性玻璃膜疣。
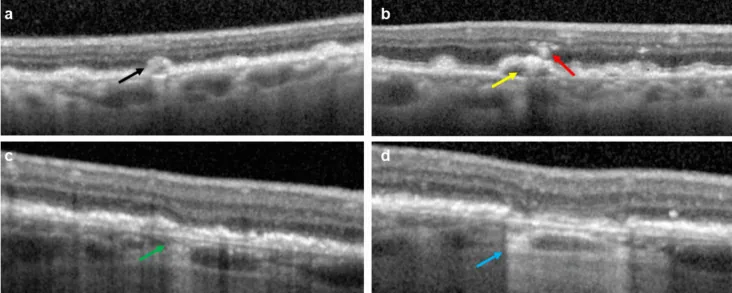
GA的诊断推荐采用多模态成像组合2)。
各项检查的特点如下所示。
| 检查方法 | 主要目的 | 备注 |
|---|---|---|
| 眼底自发荧光(FAF) | 测量GA范围 | 标准测量方法。也可预测进展速度。 |
| OCT(SD/SS) | 外层视网膜/RPE评估 | EZ完整性预测视力预后4) |
| 微视野检查 | 视网膜敏感度定量 | 可评估残留功能4) |
ACP给药方法:2mg(20mg/mL溶液0.1mL)每月一次玻璃体内注射1)。
GATHER1(2/3期)和GATHER2(3期)两项随机双盲试验评估了ACP的有效性。
| 试验 | GA扩大抑制率 | 统计 |
|---|---|---|
| GATHER1(12个月,平方根转换) | 减少27.4% | p=0.00727) |
| GATHER1(18个月,观测值) | 减少32.2% | 95%CI 0.480–1.8338) |
| GATHER2(12个月,观测值) | 减少17.7% | p=0.0041) |
Khanani等人(2023)的GATHER2 12个月结果显示,ACP组(n=271)与假手术组(n=269)相比,GA生长率显著抑制:0.336 vs 0.392 mm/年(差值为0.056 mm/年;95%CI 0.016–0.096;p=0.006)6)。
GATHER2的24个月数据显示,每月给药组减少14%,12个月后从每月给药转为隔月给药组减少19%2)。
GATHER1和GATHER2均未显示最佳矫正视力有显著改善1)2)。但事后分析提示,最佳矫正视力丧失15个字母或以上的比例在ACP组为4.0%,假手术组为7.6%,持续性15个字母丧失风险降低56%(HR 0.44;95%CI 0.21–0.92)1)5)。
补体C3/C3b抑制剂佩格塞塔科普兰(Syfovre)在OAKS/DERBY的3期试验中,每月一次给药,12个月时GA扩大抑制率为21%(OAKS试验)2)。
主要不良反应(GATHER1/GATHER2合并)如下所示1)。
| 不良反应 | ACP组 | 假注射组 |
|---|---|---|
| 结膜下出血 | 13% | 9% |
| 眼压升高 | 9% | 1% |
| 视物模糊 | 8% | 5% |
| 黄斑新生血管转化 | 7% | 4% |
| 眼痛 | 4% | 3% |
12个月内未报告眼内炎或缺血性视神经病变1)。眼压升高主要与注射操作相关,且为一过性1)。
黄斑新生血管转化风险:在GATHER1中,ACP 2mg组为9.0%,假注射组为2.7%;在GATHER2中,ACP 2mg组为6.7%,假注射组为4.1%1)。如果发生黄斑新生血管(脉络膜新生血管),需要抗VEGF治疗2)。
禁忌:患有眼或眼周感染、活动性眼内炎症的患者。
GATHER试验未显示最佳矫正视力有显著改善1)2)。但事后分析提示,持续15个字母或以上的视力丧失风险降低56%(HR 0.44),有望有助于长期维持视力5)。
GATHER试验的综合数据显示,治疗组7%、假手术组4%出现黄斑新生血管转化2)。发生黄斑新生血管时,采用抗VEGF治疗。定期OCT监测必不可少。
补体系统的异常激活在GA的发生和进展中起核心作用。
补体系统由经典途径、凝集素途径和旁路途径三条途径组成1)。三条途径均通过C3转化酶切割C3(C3→C3a+C3b)汇合1)。随后,C5转化酶将C5切割为C5a(过敏毒素)和C5b1)。
随着年龄增长,补体系统相关基因的表达上调1)。CFH、CFB、C3和ARMS2的基因多态性与GA易感性相关1)2)。
ACP是一种化学合成的单链寡核苷酸,通过聚乙二醇化提高生物稳定性并延缓清除1)。
它与C5高亲和力结合,抑制其切割为C5a和C5b1)。
C5抑制的理论优势:在保留C5上游C3a(具有抗炎和宿主防御功能)的同时,阻断炎症小体募集和MAC形成1)。与可能损害上游宿主防御功能的C3抑制剂相比,C5抑制被认为是更具选择性的靶点1)。
C5切割产物C5a和MAC被认为通过对RPE的炎症损伤促进GA进展1)。抑制C5可阻止MAC形成和C5a生成,同时保留上游C3a的抗炎和宿主防御功能。由于C3抑制存在感染风险升高的担忧,C5被认为是更安全的靶点1)。
GATHER2的24个月数据显示,每月给药组的GA扩大抑制率为14%,12个月后转为隔月给药组的抑制率为19% 2)。这表明转为隔月给药可能不会降低GA抑制率,给药间隔的优化是未来的课题。
事后分析提示持续15个字母或以上的视力丧失风险降低56%(HR 0.44),但这是事后探索性分析,并非确定性结论 1)5)。需要以视力终点为主要评估指标的前瞻性试验进行验证。
EZ(椭圆体带)完整性作为生物标志物的实用性正在探索中 1)。利用机器学习从OCT生物标志物预测视功能的研究也在进行中 4)。GA早期发现和早期治疗干预的重要性被强调 1),这些生物标志物有望被确立为预后预测工具。
阐明补体抑制导致黄斑新生血管(脉络膜新生血管)发生风险增加的机制是一个重要的未解决问题 1)。有假说认为补体系统也参与抑制血管生成,理解这一平衡被认为会影响未来的药物设计。