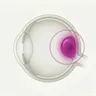
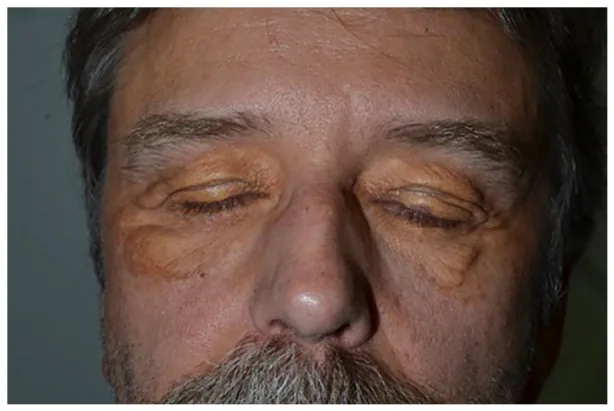
壊死性黄色肉芽腫(necrobiotic xanthogranuloma, NXG)は眼窩 周囲に好発する非ランゲルハンス細胞組織球症 の一種で、1980年に初めて報告された稀な疾患である。
患者の77〜84%が生涯いずれかの時点で血液疾患(意義不明の単クローン性免疫グロブリン血症・多発性骨髄腫など)を発症する。
系統的レビューでは175例中65%(114例)にパラプロテイン血症または悪性疾患の合併が認められた。1)
診断はNelsonら(2020年)の基準に基づき、主要基準2項目と副基準1項目以上の充足が必要である。
免疫グロブリン静注療法 (IVI G)は系統的レビューで奏効率81%を示し、副腎皮質ステロイド とともに第一選択治療として推奨される。1) 外科的切除後の再発率は最大40%と高く、視機能を脅かす場合にのみ推奨される。
多発性骨髄腫への進行は壊死性黄色肉芽腫発症から最大6年後まで報告されており、長期の血液疾患フォローアップが不可欠である。
壊死性黄色肉芽腫は、非ランゲルハンス細胞組織球症 の一種である。皮膚および眼窩 周囲組織を主に侵す慢性肉芽腫性多臓器疾患である。1980年、KossardとWinkelmannが初めて報告した。1)
発症年齢は60代が多く、性差はない。1) 皮膚外病変として心臓、肺、気管支、肝臓、脾臓、口咽頭、消化管にも及ぶことがある。
壊死性黄色肉芽腫の最大の特徴は血液疾患との強い関連である。
パラプロテイン血症の合併 : 175例中95例(55%)。IgG-κ型が最多サブタイプ1) 悪性疾患の合併 : 175例中19例(11%)。多発性骨髄腫が12例(7%)で最多。ホジキンリンパ腫、慢性リンパ性白血病も報告1) パラプロテイン血症および/または悪性疾患の総合併率 : 175例中114例(65%)1) 生涯における血液疾患発症率 : 壊死性黄色肉芽腫患者の77〜84%がいずれかの時点で血液疾患を発症多発性骨髄腫への進行 : 壊死性黄色肉芽腫発症から最大6年後まで報告されており、長期フォローアップが必要
なお、多発性骨髄腫(形質細胞の腫瘍性増殖)ではまれに皮膚の黄色腫が生じることが一般的に知られている。また、肉芽腫はマクロファージ由来の類上皮細胞と多核巨細胞からなる小結節状病巣を特徴とする増殖性慢性炎症であり、壊死性黄色肉芽腫はその一形態である。
Q
壊死性黄色肉芽腫と診断されたら必ず血液疾患になるのですか?
A
壊死性黄色肉芽腫患者の77〜84%が生涯いずれかの時点で血液疾患を発症するとされており、必ずしも全例ではないが高頻度である。多発性骨髄腫への進行は壊死性黄色肉芽腫発症から最大6年後まで報告されているため、定期的な血液疾患のスクリーニングが重要である。
Anne-Sophie Smilga et al. Long-standing necrobiotic xanthogranuloma limited to the skin: A case report. SAGE Open Medical Case Reports. 2021 Nov 9; 9:2050313X211057929. Figure 1. PM
CI D: PMC8581771. License: CC BY.
???????????????????????????????????????????????????????????????????????
掻痒・疼痛 : 皮膚病変に伴う掻痒や痛みが生じることがある。無症状の場合もある。眼症状 : 壊死性黄色肉芽腫患者の約50%に認める。視覚障害、複視 、眼球突出 感など血液疾患先行 : 患者の約54%は壊死性黄色肉芽腫発症前に血液疾患を発症している
皮膚・眼窩周囲所見
特徴的皮膚病変 :硬結を伴う黄色〜オレンジ色の丘疹・結節・斑。通常多発性で眼窩 周囲に最多。
進行所見 :萎縮、毛細血管拡張、潰瘍化、瘢痕化が生じる。瘢痕部位に新病変が頻発する。
眼窩 周囲合併症兎眼 を引き起こす。
分布 :顔面以外に体幹・四肢近位部にも生じうる。
眼症状
眼窩 病変眼窩 腫瘤、眼球突出 、拘束性斜視 、眼瞼下垂 。
結膜 ・強膜 病変結膜 病変、上強膜炎 、強膜炎 、びまん性結膜 充血 。
角膜 病変角膜 炎、点状表層角膜炎 、角膜潰瘍 。
眼表面合併症 :角膜 ・結膜 の下皮線維化。
Q
壊死性黄色肉芽腫の眼症状にはどのようなものがありますか?
A
壊死性黄色肉芽腫患者の約50%に眼症状が認められる。眼窩 腫瘤・眼球突出 ・拘束性斜視 ・眼瞼下垂 などの眼窩 病変に加え、結膜 病変・強膜炎 ・角膜 炎・兎眼 ・瘢痕性外反など多彩な所見を呈する。詳細は「臨床所見」の項 を参照。
壊死性黄色肉芽腫の直接的な病因は不明である。パラプロテイン血症との強い関連が知られているが、具体的な因果関係は解明されていない。
発症年齢 : 平均60代、性差なし1) 最大のリスク要因 : 意義不明の単クローン性免疫グロブリン血症(MGUS)・多発性骨髄腫パラプロテイン仮説 : 単クローン性ガンマグロブリン血症が巨細胞肉芽腫反応の刺激または補因子として作用する可能性1) リポタンパク結合仮説 : 単クローン性免疫グロブリンがリポタンパク質に結合し、マクロファージによる取り込みを促進する可能性低HDL仮説 : 壊死性黄色肉芽腫患者はHDL値(特にHDL-3C)が低い傾向があり、標的臓器からのコレステロール逆転送が減少すると考えられている
多発性骨髄腫は形質細胞の腫瘍性増殖による疾患で、50歳以上の男性に多く、骨と骨髄を主に侵す。
Nelsonら(2020年)が提唱した診断基準は以下の通りである。異物・感染症・その他の特定可能な原因がない場合にのみ適用する。
主要基準(両方必須)
皮膚病変 :丘疹・斑・結節(黄色〜オレンジ色が多い)の存在。
病理所見 :リンパ血漿細胞浸潤と壊死変性領域を伴う柵状肉芽腫。コレステロール裂隙・巨細胞は症例による。
副基準(1つ以上)
血液疾患 :パラプロテイン血症(多くはIgG-κ型)、形質細胞疾患、および/またはリンパ増殖性疾患の合併。
病変分布 :皮膚病変が眼窩 周囲に分布している。
真皮・皮下組織の変化 : 真皮中層〜皮下組織に及ぶ肉芽腫と壊死変性コラーゲン領域1) 炎症浸潤 : リンパ血漿細胞浸潤を伴う柵状肉芽腫コレステロール裂隙 : 本疾患の特徴的所見(“cholesterol clefts are a hallmark”)1) 巨細胞 : トゥートン型巨細胞および大型異型異物型巨細胞1) 表皮 : 潰瘍化していない場合は正常な表皮・真皮浅層を呈する
各検査の意義を以下に示す。
検査項目 所見・目的 血清タンパク電気泳動 血液疾患スクリーニング(強く推奨) 補体 値(C4)64%でC4低値 脂質パネル(HDL-3C) 低HDLコレステロール血症の確認 クリオグロブリン値 23%でクリオグロブリン血症 ビタミンDパネル 25-OHビタミンD低値、1,25-(OH)₂D正常〜高値
多発性骨髄腫の診断においては、Bence Jones蛋白の尿中検出および骨髄生検が重要である。
以下の疾患との鑑別が必要である。
類脂質性壊死変性(necrobiosis lipoidica)
正常脂質性平面黄色腫
眼瞼黄色腫 (xanthelasma )播種性黄色腫
多中心性網状組織球症
若年性黄色肉芽腫 エルドハイム・チェスター病
異物肉芽腫
サルコイドーシス 関節リウマチの結節
皮下環状肉芽腫
アミロイドーシス
Q
壊死性黄色肉芽腫の確定診断にはどのような検査が必要ですか?
A
Nelsonら(2020年)の診断基準に基づき、主要基準2項目(特徴的皮膚病変+病理所見)を両方満たし、副基準(パラプロテイン血症や眼窩 周囲分布)を1つ以上充足することが必要である。血清タンパク電気泳動は血液疾患の既往がない場合には強く推奨される。
壊死性黄色肉芽腫に対する特定治療のコンセンサスガイドラインは存在しない。無作為化比較試験は稀少疾患のため実施されておらず1) 、治療方針は関連する悪性腫瘍の有無を考慮して決定する。
系統的レビュー(175例)に基づく各薬剤の奏効率を以下に示す(完全奏効:CR、部分奏効:PR)。1)
治療法 例数 完全奏効+部分奏効 奏効持続期間中央値 免疫グロブリン静注療法 26例 81%(完全27%・部分54%) 12か月(範囲6-48か月) 副腎皮質ステロイド 45例 31%(完全11%・部分20%) 12か月(範囲2-24か月) レナリドミド±ステロイド 22例 50%(完全18%・部分32%) —
全体では175例中128例(73%)で改善(完全奏効+部分奏効)、25例で安定、22例(13%)で進行であった。1) 免疫グロブリン静注療法 と副腎皮質ステロイド を壊死性黄色肉芽腫の第一選択治療とすることが推奨される。1)
多発性骨髄腫に対する治療として、眼窩 内浸潤には放射線療法(20〜40グレイ)が用いられる。全身療法としてはメルファラン投与、ステロイド +メルファラン併用、造血幹細胞移植がある。分子標的薬としてボルテゾミブ、サリドマイド、サリドマイド誘導体のレナリドミド(副作用軽減)が使用される。
ステロイド の局所塗布または病変内注射テノン嚢 下トリアムシノロン 注入(NXG関連強膜炎 に対して)インターフェロンα
シクロスポリン 、代謝拮抗剤、インフリキシマブ 、血漿交換、アルキル化剤(クロラムブシル、シクロホスファミド、メルファラン)、クラドリビンなど複数の薬剤が報告されている。
レーザー治療 放射線療法 PUVA(プソラレン+紫外線A波)療法
外科的切除後の再発率は最大40%と高い。重度の瘢痕性外反や兎眼 など視力 に影響する場合にのみ推奨される。
壊死性黄色肉芽腫に特化したコンセンサスガイドラインが存在しないため、治療は個別化が必要である。
外科的切除は再発率が最大40%と高く、適応を慎重に判断する。
関連する血液悪性腫瘍が存在する場合は、その治療が壊死性黄色肉芽腫の皮膚病変にも影響を与える可能性がある。
Q
壊死性黄色肉芽腫の治療で最も効果が高いのはどの薬剤ですか?
A
系統的レビューで免疫グロブリン静注療法 が奏効率(完全奏効+部分奏効)81%と最も高く、副腎皮質ステロイド とともに第一選択治療として推奨されている。1) ステロイド 単独の奏効率は31%にとどまるが、免疫グロブリン静注療法 との併用が標準的である。
壊死性黄色肉芽腫の病態生理は完全には解明されていない。パラプロテイン血症との関連から、以下の仮説が提唱されている。
パラプロテイン仮説 : 単クローン性ガンマグロブリン血症が巨細胞肉芽腫反応の引き金または補因子として作用する1) リポタンパク結合仮説 : 単クローン性免疫グロブリンがリポタンパク質に結合し、マクロファージによる取り込みを促進する低HDL仮説 : 壊死性黄色肉芽腫患者でHDL値(特にHDL-3C)が低い傾向があり、皮膚等標的臓器からのコレステロール逆転送が減少する
肉芽腫はマクロファージ由来の類上皮細胞と多核巨細胞からなる小結節状病巣を特徴とする増殖性慢性炎症である。壊死性黄色肉芽腫における特徴的所見は以下の通りである。
肉芽腫の範囲 : 真皮から皮下脂肪組織に及ぶ1) 特徴的巨細胞 : トゥートン型巨細胞および大型異型異物型巨細胞が頻出1) コレステロール裂隙 : 本疾患の病理学的な特徴的所見であり、診断に重要1)
これらの組織学的特徴は、脂質代謝の異常とパラプロテイン血症が組み合わさった特有の病態を反映していると考えられている。
Steinhelferら(2022)の系統的レビュー(175例)は、壊死性黄色肉芽腫に関する最大規模の解析であるが、ほとんどが症例報告・症例シリーズに基づく。壊死性黄色肉芽腫の重症度スケールが存在せず、治療反応の標準化評価が困難であるという根本的な問題がある。1) 前向きランダム化比較試験が必要だが、症例数の少なさから実現は困難とされている。
ボルテゾミブ、リツキシマブ 、アダリムマブ 、ミコフェノール酸モフェチル 、クロファジミンなどの個別症例報告が蓄積しつつある。1) いずれも症例数が少なく、標準治療としての位置づけには至っていない。
また、毎月の免疫グロブリン静注療法 +毎日のサリドマイド+シクロホスファミド+低用量経口プレドニゾンの多剤併用療法で長期寛解が得られた症例が報告されている。
Steinhelfer L, Kühnel T, Jägle H, Mayer S, Karrer S, Haubner F, Schreml S. Systemic therapy of necrobiotic xanthogranuloma: a systematic review. Orphanet J Rare Dis. 2022;17(1):132. doi:10.1186/s13023-022-02291-z. PMID:35331271; PMCI D:PMC8944121.
Chen PY, Jing J, Hong YY, Li JX, Zhang H, Chen JQ, et al. Sitosterolemia-related necrobiotic xanthogranuloma. J Am Acad Dermatol. 2026;94(1):258-261. PMID: 40902653.
Navarro-Triviño F, Ródenas-Herranz T, Linares-Gonzalez L, Ruiz-Villaverde R. Disseminated Necrobiotic Xanthogranuloma. Med Clin (Barc). 2021;157(10):505. PMID: 33775398.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください