กลุ่มอาการครันช์เป็นภาวะแทรกซ้อนที่เกิดจากการรักษา ซึ่งจอประสาทตาลอก แบบดึงรั้ง (TRD) เกิดขึ้นหรือแย่ลงหลังการฉีดสารต้าน VEGF เข้าน้ำวุ้นตา
อุบัติการณ์อยู่ระหว่าง 1.5% ถึง 18.4% ตามรายงานต่างๆ โดยทั่วไปประมาณ 5% 1)
เกิดส่วนใหญ่ในเบาหวานขึ้นจอประสาทตา ระยะ proliferative (PDR) แต่ยังมีรายงานในจอประสาทตา ผิดปกติชนิด proliferative อื่นๆ เช่น หลอดเลือดดำจอประสาทตาส่วนกลางอุดตัน (CRVO ) 3)
การมองเห็น ลดลงอย่างรวดเร็วเกิดขึ้นภายใน 1–6 สัปดาห์หลังฉีด และมากกว่า 80% ของกรณีเกิดขึ้นภายใน 5 วันหลังฉีดครั้งแรก 1) การรักษามาตรฐานคือการผ่าตัดน้ำวุ้นตา ฉุกเฉิน (PPV ) ร่วมกับการนำเยื่อพังผืดออก และการแทรกแซงตั้งแต่เนิ่นๆ มีผลต่อการพยากรณ์โรค
ผู้ป่วยที่มีการเจริญของเส้นเลือดและพังผืดเป็นบริเวณกว้าง หรือมีจอประสาทตาลอก แบบดึงรั้ง (TRD) อยู่ก่อนแล้วมีความเสี่ยงสูง และจำเป็นต้องประเมินอย่างรอบคอบก่อนให้ยา anti-VEGF 2)
Crunch syndrome เป็นภาวะที่เกิดจอประสาทตาลอก แบบดึงรั้ง (TRD) ขึ้นใหม่หรือรุนแรงขึ้นอย่างรวดเร็วในตาที่มีจอประสาทตา ผิดปกติแบบมี proliferative retinopathy หลังการฉีดยา anti-VEGF (vascular endothelial growth factor) เข้าในน้ำวุ้นตา 1, 2, 3)
ชื่อ “crunch” มาจากลักษณะของจอประสาทตาลอก ที่ปิดเข้าหาจุดรับภาพเหมือนขากรรไกรกำลังเคี้ยว 3)
ส่วนใหญ่รายงานใน proliferative diabetic retinopathy แต่ก็สามารถเกิดใน proliferative retinopathy อื่นๆ เช่น central retinal vein occlusion, retinopathy of prematurity (ROP ), Eales disease, familial exudative vitreoretinopathy (FEVR ) และ Coats disease 3)
อุบัติการณ์อยู่ระหว่าง 1.5–18.4% ตามรายงานต่างๆ โดยทั่วไปประมาณ 5% 1) ระยะเวลาที่เกิดคือ 1–6 สัปดาห์หลังฉีด anti-VEGF โดยเฉลี่ย 13 วัน (ช่วง 3–31 วัน) 1, 2) มากกว่า 80% ของกรณีเกิดขึ้นภายใน 5 วันหลังฉีดครั้งแรก 1)
ผู้ป่วยที่มี proliferative diabetic retinopathy รุนแรง, TRD อยู่ก่อนแล้ว หรือพังผืดเป็นบริเวณกว้างมีอุบัติการณ์สูงกว่า หมายเหตุ: การเกิด TRD ร่วมกับ rhegmatogenous retinal detachment โดยปกติมีเพียง 0.05–0.5% แต่สามารถสูงถึง 43% หากมี circumferential fibrovascular membrane
Q
Crunch syndrome เกิดขึ้นบ่อยแค่ไหน?
A
อุบัติการณ์อยู่ระหว่าง 1.5–18.4% ตามรายงานต่างๆ โดยทั่วไปประมาณ 5% 1) ความเสี่ยงเพิ่มขึ้นในกรณี proliferative diabetic retinopathy รุนแรง, TRD อยู่ก่อนแล้ว หรือพังผืดเป็นบริเวณกว้าง ระยะเวลาที่เกิดมักอยู่ภายใน 1–6 สัปดาห์หลังฉีด (เฉลี่ย 13 วัน) และมากกว่า 80% ของกรณีเกิดขึ้นภายใน 5 วันหลังฉีดครั้งแรก
การมองเห็น ลดลงอย่างรวดเร็วการมองเห็น ลดลงจาก 20/25 เหลือ hand motion ใน 3 วัน 2) ในกรณีของ Bromeo บันทึกการลดลงจาก 20/30-2 เหลือ hand motion 3) อาการเห็นจุดลอย (Floaters): การรับรู้สิ่งลอยในน้ำวุ้นตา จากเลือดออกในน้ำวุ้นตา ข้อบกพร่องของลานสายตา (Visual field defect): การสูญเสียลานสายตาตามขอบเขตของจอประสาทตาลอก แบบดึงรั้ง (TRD)
เลือดออกในน้ำวุ้นตา (Vitreous hemorrhage): พบร่วมในผู้ป่วยส่วนใหญ่ 1, 2, 3) จอประสาทตาลอก แบบดึงรั้ง1, 2, 3) การเจริญของเส้นใยหลอดเลือดและเนื้อเยื่อแผลเป็น (Fibrovascular proliferation and scar tissue): การเกิดพังผืดที่ดำเนินไปเมื่อเนื้อเยื่อเส้นเลือดใหม่หดตัว 2, 3) TRD รูปแบบขากรรไกรหมาป่า (Wolf-jaw configuration TRD): ลักษณะเฉพาะ 1) การหดตัวของเยื่อเส้นเลือดใหม่ (Contraction of neovascular membrane): อาจเร่งขึ้นหลังให้ยา anti-VEGF
ผลการตรวจภาพหลักแสดงไว้ด้านล่าง
การตรวจ สิ่งที่ประเมินได้ OCT ขอบเขต TRD, การลุกลามเข้าไปในจุดรับภาพ, จอประสาทตา บวมน้ำ OCTA เส้นเลือดใหม่, บริเวณขาดเลือด อัลตราซาวนด์ การประเมิน TRD ในภาวะเลือดออกในน้ำวุ้นตา
OCT มีประโยชน์ในการประเมินขอบเขตของ TRD การลุกลามเข้าจุดภาพชัด และอาการบวมน้ำของจอประสาทตา 1, 3) OCTA ใช้สำหรับการประเมินเชิงปริมาณของเส้นเลือดใหม่และบริเวณขาดเลือด 2) เมื่อไม่สามารถสังเกตอวัยวะภายในตาได้เนื่องจากเลือดออกในน้ำวุ้นตา การประเมิน TRD จะทำโดยอัลตราซาวนด์ 4, 5)
การฉีดยา anti-VEGF เข้าในน้ำวุ้นตา เป็นตัวกระตุ้นให้เกิดกลุ่มอาการครันช์ 1, 2, 3) ยาที่พบบ่อยที่สุดคือ bevacizumab 1, 2) และยังมีรายงานใน pegaptanib และ ranibizumab 2) รายงานแรกกับ conbercept โดย Li & Zhang (2025) 2) ปัจจุบันยังไม่มีรายงานความเกี่ยวข้องกับ aflibercept 2)
นอกจากยา anti-VEGF แล้ว การจี้จอประสาทตา ทั่วทั้งจอ (PRP ) เพียงอย่างเดียวหรือร่วมกับ anti-VEGF ก็สามารถกระตุ้นให้เกิดครันช์ได้เช่นกัน เชื่อว่าการอักเสบและความร้อนทำให้คอลลาเจนหดตัว และการใช้ anti-VEGF ร่วมกับ PRP /การจี้เย็น อาจทำให้แรงดึงแย่ลงแบบเสริมฤทธิ์กัน 3)
ด้านล่างนี้คือสถานะรายงานครันช์แยกตามยา anti-VEGF:
ชื่อยา รายงานครันช์ Bevacizumab รายงานมากที่สุด Ranibizumab มีรายงาน Conbercept รายงานแรก (2025) 2) อะฟลิเบอร์เซปต์ ไม่มีรายงาน
ปัจจัยเฉพาะที่ของตา
เบาหวานขึ้นจอประสาทตา ระยะ proliferative ชนิดรุนแรงเบาหวานขึ้นจอประสาทตา สูง ความเสี่ยงยิ่งเพิ่มขึ้น1)
การเจริญของเนื้อเยื่อเส้นใยและหลอดเลือดอย่างกว้างขวาง : หลอดเลือดใหม่ที่ทำงานอยู่และการยึดเกาะระหว่างวุ้นตา และจอประสาทตา อย่างกว้างขวาง2)
TRD ที่มีอยู่ก่อน : หากมี TRD อยู่ก่อนเริ่มเกิด
เยื่อเส้นใยและหลอดเลือดแบบวงแหวน : มีความเสี่ยงสูงเป็นพิเศษ2)
บริเวณขาดเลือดกว้าง : ยิ่งบริเวณขาดเลือดรอบนอกกว้างเท่าไร ยิ่งอันตราย
ปัจจัยทางระบบและการรักษา
การควบคุมระดับน้ำตาลในเลือดไม่ดี : ความเสี่ยงเพิ่มขึ้นหากมีระยะเวลาเป็นเบาหวานนาน2)
จำนวนการฉีดยา anti-VEGF เพิ่มขึ้น : การให้ยาซ้ำๆ ส่งเสริมการเกิดพังผืด
การขาดการติดตามผลหรือการยืดระยะเวลา : ความเสี่ยงเพิ่มขึ้นเมื่อความต่อเนื่องของการรักษาหายไป3)
การใช้ร่วมกับการจี้แสงทั่วจอประสาทตา /การจี้เย็น : ผลเสริมกันทำให้แรงดึงรั้งแย่ลง3)
Q
Crunch syndrome เกิดขึ้นเมื่อใดหลังฉีดยาต้าน VEGF?
A
โดยปกติจะเกิดขึ้นภายใน 1-6 สัปดาห์หลังการฉีด โดยเฉลี่ย 13 วัน (ช่วง 3-31 วัน) 1, 2) ผู้ป่วยมากกว่า 80% เกิดขึ้นภายใน 5 วันหลังการฉีดครั้งแรก และมีรายงานเกิดขึ้นเร็วที่สุด 3 วันหลังการฉีด ในผู้ป่วยที่มีความเสี่ยงสูง จำเป็นต้องติดตามอย่างใกล้ชิดตั้งแต่ระยะแรกหลังการฉีด
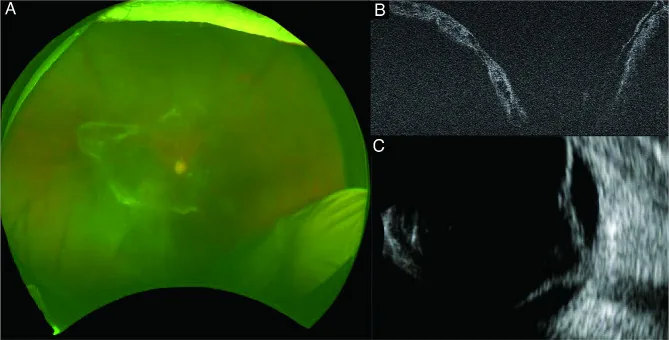
ภาพ Crunch Syndrome Akihiko Shiraki; Nobuhiko Shiraki; Susumu Sakimoto; Kazuichi Maruyama; Takatoshi Maeno; Kohji Nishida. Intraoperative challenges and management of fibrovascular membrane with tractional retinoschisis in proliferative diabetic retinopathy. BMC Ophthalmol. 2024 Jul 20; 24:299. Figure 1. PM
CI D: PMC11264879. License: CC BY.
ภาพก่อนผ่าตัด (A) พบ
จอประสาทตา หลุดลอกและเยื่อ fibrovascular บางส่วน แต่ยากที่จะตรวจสอบรายละเอียดของอวัยวะภายในตาเนื่องจาก
ต้อกระจก หนาแน่น (B) Optical coherence tomography แสดง
จอประสาทตา หลุดลอกบริเวณ macular และเยื่อ fibrovascular (C) การตรวจอัลตราซาวนด์ B-scan ตรวจพบ
จอประสาทตา หลุดลอกที่อาจเกี่ยวข้องกับเยื่อ fibrovascular
การวินิจฉัยขึ้นอยู่กับประวัติทางการแพทย์ ผลการตรวจอวัยวะภายในตา และการตรวจภาพเป็นหลัก
ประวัติทางการแพทย์ : การมองเห็น ลดลงอย่างเฉียบพลันภายใน 1-6 สัปดาห์หลังฉีดยาต้าน VEGF เป็นกุญแจสำคัญ 1, 2) การตรวจอวัยวะภายในตา : ยืนยันเลือดออกในน้ำวุ้นตา จอประสาทตา หลุดลอกแบบ traction, fibrovascular proliferation และการหดตัวของเส้นเลือดใหม่ 1, 2, 3) OCT จอประสาทตา หลุดลอกแบบ traction, การเกี่ยวข้องกับ macular และจอประสาทตา บวมน้ำ 1, 3) OCTA 2) การตรวจอัลตราซาวนด์ : ประเมิน TRD เมื่อไม่สามารถตรวจดูจอประสาทตา ได้เนื่องจากเลือดออกในน้ำวุ้นตา 4, 5) การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : ประเมินบริเวณที่มีการอุดตันของเส้นเลือดฝอยกว้างและเส้นเลือดใหม่ 3)
การดำเนินของ TRD ตามธรรมชาติของจอประสาทตาเสื่อมจากเบาหวาน ชนิด proliferative : อาจเป็นเหตุการณ์ที่ไม่ขึ้นกับการให้ยา anti-VEGF 2) การแย่ลงของ traction จากการจี้จอประสาทตา ทั้งหมด (panretinal photocoagulation) : การจี้จอประสาทตา ทั้งหมดอาจเป็นสาเหตุโดยตรง 3) Crunch ในจอประสาทตา ผิดปกติชนิด proliferative อื่นๆ : อาจเกิดได้ในจอประสาทตาผิดปกติในทารกคลอดก่อนกำหนด , โรค Eales, FEVR , โรค Coats เป็นต้น 3)
เมื่อเกิด Crunch syndrome การผ่าตัดน้ำวุ้นตา ฉุกเฉิน (PPV ) คือการรักษามาตรฐาน 1, 2, 3)
การนำเยื่อ proliferative ออก (membranectomy) : การลอกเยื่อ fibrovascular อย่างระมัดระวังเพื่อปลด traction จอประสาทตา 2) การจี้เลเซอร์ภายในตา (endolaser PRP ) : เพื่อยับยั้งการทำงานของเส้นเลือดใหม่หลังผ่าตัด 2, 3) การอุดตันภายในตา (tamponade) : รักษาตำแหน่งจอประสาทตา ด้วยซิลิโคนออยล์ หรือแก๊ส 2, 3)
ในกรณีของ Li ได้ทำการอุดตันด้วยซิลิโคนออยล์ 2) ในกรณีของ Bromeo ได้นำซิลิโคนออยล์ ออกหลัง 6 เดือนพร้อมกับการผ่าตัดต้อกระจก 3)
การผ่าตัดฉุกเฉิน (การรักษามาตรฐาน)
การผ่าตัดน้ำวุ้นตา + การนำเยื่อ proliferative ออก
การจี้จอตาด้วยเลเซอร์ ทั่วจอตา (Endolaser panretinal photocoagulation)
การอุดด้วยซิลิโคนออยล์ /แก๊ส : เพื่อรักษาการประคับจอตาให้อยู่ตำแหน่ง
ทางเลือกสำหรับกรณีที่ไม่สามารถผ่าตัดได้
การฉีดยา anti-VEGF เป็นประจำ : ทำให้คงที่โดยการให้ยาอย่างสม่ำเสมอทุก 8-12 สัปดาห์
ข้อจำกัดของข้อบ่งชี้ : ทางเลือกพิเศษเฉพาะในกรณีที่มีความเสี่ยงสูงในการผ่าตัด เช่น โรคหัวใจ1)
ข้อควรระวัง : การยืดระยะห่างระหว่างการฉีดเป็นความเสี่ยงต่อการกลับเป็นซ้ำของเลือดออกในน้ำวุ้นตา
มีหลักฐานว่าการให้ยา anti-VEGF ก่อนผ่าตัดช่วยลดระยะเวลาการผ่าตัด ลดจำนวนจอตาฉีกขาด และลดปริมาณเลือดออกระหว่างผ่าตัด4, 5) การทบทวนอย่างเป็นระบบของ Cochrane แสดงให้เห็นว่าการให้ยา bevacizumab ก่อนหรือระหว่างผ่าตัดช่วยลดเลือดออกในน้ำวุ้นตา หลังผ่าตัด4, 5)
ในกรณีที่มีความเสี่ยงในการผ่าตัดสูงมาก เช่น โรคหัวใจ การรักษาด้วย anti-VEGF เพียงอย่างเดียวถูกเลือกเป็นกรณีพิเศษ ในกรณีของ Yuan มีรายงานว่าผู้ป่วยที่ไม่สามารถผ่าตัดได้เนื่องจากโรคหัวใจได้รับการฉีด bevacizumab เป็นประจำทุก 8-12 สัปดาห์นานกว่า 1.5 ปี และสามารถคงสภาพ PDR ให้คงที่และรักษาการยึดติดของรอยบุ๋มจอตา ได้1)
หากมีพังผืดเป็นบริเวณกว้าง การใช้ anti-VEGF เพียงอย่างเดียวจะเพิ่มความเสี่ยงของกลุ่มอาการ crunch ดังนั้นควรพิจารณาทำ PPV ก่อน2)
หลังจากใช้ anti-VEGF เพื่อช่วยก่อนผ่าตัด แนะนำให้ทำการผ่าตัดภายใน 1-2 สัปดาห์3)
การรักษาด้วย anti-VEGF เพียงอย่างเดียวในกรณีที่ไม่สามารถผ่าตัดได้เป็นเพียงทางเลือกพิเศษ และการยืดระยะห่างระหว่างการฉีดเป็นความเสี่ยงต่อการกลับเป็นซ้ำของเลือดออกในน้ำวุ้นตา 1)
Q
หากเกิดกลุ่มอาการ crunch ขึ้น จะสามารถคาดหวังการฟื้นฟูการมองเห็นได้หรือไม่?
A
การตรวจพบตั้งแต่เนิ่นๆ และการผ่าตัดตั้งแต่เนิ่นๆ มีความสำคัญ แต่การพยากรณ์โรคทางสายตาไม่จำเป็นต้องดีเสมอไป ในกรณีของ Li ค่าสายตาหลังการตัดน้ำวุ้นตา อยู่ที่ระดับนับนิ้ว 2) ส่วนกรณีของ Bromeo รายงานว่าอยู่ที่ 20/400 หลังจาก 6 เดือน 3) แม้ในกรณีที่ไม่สามารถผ่าตัดได้ ก็มีรายงานการคงตัวของ TRD และการคงอยู่ของรอยบุ๋มจอประสาทตา ด้วยการรักษาด้วย anti-VEGF เพียงอย่างเดียว 1) แต่การแทรกแซงตั้งแต่เนิ่นๆ เป็นกุญแจสำคัญในการปรับปรุงการพยากรณ์โรค
ในจอประสาทตา เบาหวานชนิด增殖 การเพิ่มขึ้นของ VEGF ทำให้เกิดการสร้างเส้นเลือดใหม่ ซึ่งนำไปสู่การเจริญของหลอดเลือดเข้าสู่ชั้นวุ้นตา ด้านหลัง หลังจากนั้น เนื้อเยื่อเส้นใยจะก่อตัวและหดตัว ดำเนินไปสู่ TRD 1) จอประสาทตา เบาหวานชนิด增殖จะเปลี่ยนจากระยะที่มีการสร้างเส้นเลือดใหม่เด่นไปเป็นระยะที่มีการเกิดพังผืดเด่นตามเวลา แต่การให้ anti-VEGF อาจเร่งการดำเนินไปนี้ 2)
Li & Zhang (2025) กล่าวถึงกลไกการกระตุ้น crunch หลังการให้ anti-VEGF ว่าประกอบด้วยการเปลี่ยนแปลงอย่างฉับพลันของแรงดึงเนื่องจากการถดถอยอย่างรวดเร็วของเส้นเลือดใหม่ รวมถึงการส่งเสริมการเกิดพังผืดและจอประสาทตา แข็งที่เกี่ยวข้องกับการลดลงของ VEGF และการเพิ่มขึ้นของ TGF-β สารยับยั้ง VEGF ที่มีฤทธิ์แรงอาจกระตุ้นการตอบสนองแบบพังผืดที่เด่นชัดกว่า 2)
Bromeo และคณะ (2021) รายงานในการทดลองในหลอดทดลองว่า bevacizumab เพิ่มการควบคุม TGF-β2, CTGF และ CNTF ในเซลล์ RPE และเซลล์เกลีย ทำให้เกิดพังผืดเร็วขึ้น 3)
รูปแบบการยึดเกาะระหว่างวุ้นตา กับจอประสาทตา ที่มีอยู่ก่อน และความเครียดทางชีวกลศาสตร์จากการเจริญของเส้นใยและหลอดเลือดเป็นเวลานาน เชื่อว่ามีส่วนทำให้เกิดการเสียสมดุลเฉียบพลันหลังการให้ anti-VEGF 2)
การจี้แสงทั่วจอประสาทตา ทำลายเซลล์ RPE ส่วนปลายและเซลล์รับแสง ลดการใช้ออกซิเจนในชั้นนอก ทำให้ออกซิเจนแพร่ไปยังชั้นในเพิ่มขึ้น ลดการกระตุ้นการผลิต VEGF และยับยั้งการสร้างเส้นเลือดใหม่เพิ่มเติม 6) ในทางกลับกัน การอักเสบและความร้อนจากการจี้แสงทั่วจอประสาทตา อาจกระตุ้นการหดตัวของคอลลาเจน ทำให้แรงดึงแย่ลง 3)
ในจอประสาทตา เบาหวานชนิด增殖 เส้นเลือดใหม่ที่เปราะบางทำให้เกิดการรั่วของของเหลวและโปรตีน ส่งผลให้เกิดจอประสาทตา บวมน้ำและเลือดออก เมื่อเส้นเลือดผิดปกติเกิดพังผืดและดึงรั้งจอประสาทตา จะเกิด TRD 6)
ในบางกรณี หลังการฉีด anti-VEGF เส้นเลือดใหม่จะถดถอยและแรงดึงระหว่างวุ้นตา กับจอประสาทตา ลดลง ทำให้ TRD ดีขึ้น ปรากฏการณ์นี้เรียกว่า “crunch ที่ดี”
ในรายงานของ Lee และคณะ TRD แบนลงหรือหายไปใน 3 ใน 4 ตา 1)
Q
"Favorable crunch" (การหดรัดตัวที่ดี) คืออะไร?
A
หมายถึงปรากฏการณ์ที่เส้นเลือดใหม่ฝ่อลงหลังการฉีดยา anti-VEGF ทำให้แรงดึงของวุ้นตา -จอประสาทตา หลุดออกและภาวะจอประสาทตาลอก แบบมีแรงดึง (TRD) ดีขึ้น ซึ่งเป็นผลลัพธ์ที่ตรงกันข้ามกับ crunch ทั่วไป (ชนิดที่ทำให้แรงดึงแย่ลง) ในรายงานของ Lee และคณะ TRD แบนลงหรือหายไปใน 3 ใน 4 ตา 1) แสดงให้เห็นว่าไม่ใช่ทุกกรณีที่แย่ลงจาก crunch
DRCR.net Protocol S เปรียบเทียบ ranibizumab กับการจี้จอประสาทตา ทั่วทั้งจอ (panretinal photocoagulation) และไม่พบความแตกต่างที่มีนัยสำคัญทางสถิติในอัตราการเกิด TRD ในจอประสาทตาเสื่อมจากเบาหวาน ชนิด proliferative อย่างไรก็ตาม หากผู้ป่วยจอประสาทตาเสื่อมจากเบาหวาน ชนิด proliferative ขาดการติดตามผลระหว่างการฉีด anti-VEGF ผลลัพธ์ทางสายตาและกายวิภาคจะแย่กว่าเมื่อเทียบกับผู้ป่วยที่ได้รับการจี้จอประสาทตา ทั่วทั้งจอ 4, 5)
ผลลัพธ์นี้ชี้ให้เห็นว่าการรักษาด้วย anti-VEGF เพียงอย่างเดียวสามารถพิจารณาได้เฉพาะในผู้ป่วยที่สามารถติดตามผลได้อย่างสม่ำเสมอ 4, 5)
รายงานแรกของ crunch syndrome ที่เกิดจาก conbercept ได้รับการตีพิมพ์ในปี 2025 2) ว่ายับยั้ง VEGF ที่มีฤทธิ์แรง เช่น aflibercept และ conbercept จะกระตุ้นการตอบสนองแบบพังผืดที่เด่นชัดกว่าหรือไม่นั้นยังคงเป็นคำถามสำหรับการวิจัยในอนาคต 2)
การเปลี่ยนแปลงของโปรไฟล์ไซโตไคน์รวมถึง TGF-β อาจเกี่ยวข้องกับการเกิด crunch syndrome 2) และคาดว่าการอธิบายกลไกในระดับโมเลกุลจะนำไปสู่กลยุทธ์การรักษาในอนาคต
เกี่ยวกับความเสี่ยงของเหตุการณ์ลิ่มเลือดอุดตันในหลอดเลือดแดงทั่วร่างกายที่เกี่ยวข้องกับการฉีดยา anti-VEGF เข้าในน้ำวุ้นตา ยังไม่มีข้อสรุปที่แน่ชัดจากการทดลองทางคลินิกในปัจจุบัน 7)
Yuan M, Hoyek S, Kim LA, Chaaya C, Patel N. Antivascular endothelial growth factor injections for the chronic treatment of macula-off, fovea-on diabetic tractional retinal detachment with vitreous hemorrhage. J VitreoRetin Dis. 2025;9(2):236-240.
Li Z, Zhang Y. Anti-vascular endothelial growth factor crunch syndrome in proliferative diabetic retinopathy. JCEM Case Rep. 2025;3:luaf083.
Bromeo AJ, Veloso A, Lerit SJ, Gomez MC. Tractional retinal detachment (‘crunch’ phenomenon) from intravitreal anti-vascular endothelial growth factor injection in central retinal vein occlusion. BMJ Case Rep. 2021;14:e240506.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. 2nd ed. AAO ; 2019.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. AAO ; 2024.
O’Leary F, Campbell M. The blood-retina barrier in health and disease. FEB S J. 2023;290(4):878-891.
American Academy of Ophthalmology. Retinal Vein Occlusions Preferred Practice Pattern. AAO ; 2024.