ภาวะเกล็ดเลือดต่ำจากลิ่มเลือดอุดตัน (TTP) เป็นโรคเลือดที่พบได้ยาก โดยมีลักษณะเฉพาะคือ โลหิตจางจากการแตกของเม็ดเลือดแดงในหลอดเลือดขนาดเล็ก เกล็ดเลือดต่ำ และความผิดปกติทางระบบประสาท
อาการทางตาพบได้ใน 14-20% ของผู้ป่วย ได้แก่ เลือดออกในจอตา การอุดตันของหลอดเลือด จอตาลอกชนิดมีน้ำใต้จอตา และบวมของหัวประสาทตา
สาเหตุพื้นฐานคือการเกิดลิ่มเลือดขนาดเล็กที่อุดมด้วยเกล็ดเลือดจากการลดลงของกิจกรรม ADAMTS13
อัตราการเสียชีวิตหากไม่รักษาอยู่ที่ประมาณ 90% แต่สามารถลดลงเหลือ 10-20% ด้วยการแลกเปลี่ยนพลาสมา
การแลกเปลี่ยนพลาสมา เป็นการรักษาหลักอันดับแรก และการให้เกล็ดเลือดมีข้อห้ามเนื่องจากทำให้ลิ่มเลือดขนาดเล็กแย่ลงการแบ่งระดับความเสี่ยงโดยใช้คะแนน PLASMIC มีประโยชน์ในการวินิจฉัยและการตัดสินใจเริ่มการรักษา
การจี้ด้วยแสง ถือเป็นทางเลือกสำหรับเส้นเลือดใหม่ที่เกิดจากภาวะขาดเลือดของจอประสาทตา โรคจ้ำเลือดเกล็ดเลือดต่ำจากลิ่มเลือด (TTP) เป็นโรคเลือดที่พบได้ยาก เรียกอีกชื่อว่าโรคมอสช์โควิทซ์ มีลักษณะเฉพาะคือกลุ่มอาการห้าอย่าง: โลหิตจางจากการแตกของเม็ดเลือดแดงแบบไมโครแองจิโอพาธี (MAHA), จ้ำเลือดจากเกล็ดเลือดต่ำ, ไตวายเฉียบพลัน, ความผิดปกติทางระบบประสาท (การเปลี่ยนแปลงของสภาวะจิต), และไข้
อาการทางตาพบได้ใน 14-20% ของผู้ป่วย โดยมีลักษณะต่างๆ จากการเกิดลิ่มเลือดขนาดเล็กในหลอดเลือดจอประสาทตา และคอรอยด์
อุบัติการณ์ประมาณ 3.7–11 รายต่อล้านคนต่อปี ในประชากรผู้ใหญ่ชาวฝรั่งเศส รายงาน 1.5 รายต่อล้านคนต่อปี 5) ความชุกต่อปีประมาณ 10 รายต่อล้านคน 7) และเป็นที่ทราบกันว่าพบในผู้หญิงบ่อยกว่า
ความแตกต่างทางเพศ : ผู้หญิงป่วยบ่อยกว่าผู้ชาย 2–3 เท่า 6) ภูมิหลังที่พบบ่อย : พบมากในผู้ที่มีเชื้อสายแอฟโฟร-แคริบเบียนและผู้ป่วยโรคอ้วนอัตราการเสียชีวิตหากไม่รักษา : ประมาณ 90% เมื่อใช้การแลกเปลี่ยนพลาสมา ลดลงเหลือ 10–20% 3)
TTP แบ่งเป็นชนิด先天性 (แต่กำเนิด) และชนิดที่ได้มา
TTP แต่กำเนิด (Upshaw-Schulman syndrome) : เกิดจากการกลายพันธุ์ของยีน ADAMTS13 คิดเป็นประมาณ 5% ของผู้ป่วยทั้งหมด มีการระบุตำแหน่งกลายพันธุ์มากกว่า 260 ตำแหน่งในฐานข้อมูล NCBI ClinVar โดยประมาณ 60% เป็นการกลายพันธุ์แบบ missense และประมาณ 20% เป็นการขาดหายหรือแทรกชิ้นส่วนขนาดเล็ก6) .TTP ที่ได้มา : เกิดจากแอนติบอดีต่อตนเองที่ต่อต้าน ADAMTS13 คิดเป็นประมาณ 95% ของผู้ป่วยทั้งหมด3) .
Q
อาการทางจักษุของ TTP เกิดขึ้นบ่อยแค่ไหน?
A
มีรายงานอาการทางจักษุใน 14-20% ของผู้ป่วย รวมถึงเลือดออกในจอประสาทตา การอุดตันของหลอดเลือด จอประสาทตาลอกชนิดมีน้ำใต้จอประสาทตา และ papilledema อาการทางตาอาจเกิดขึ้นก่อนอาการทางระบบ ดังนั้นจักษุแพทย์อาจเป็นคนแรกที่สงสัย TTP
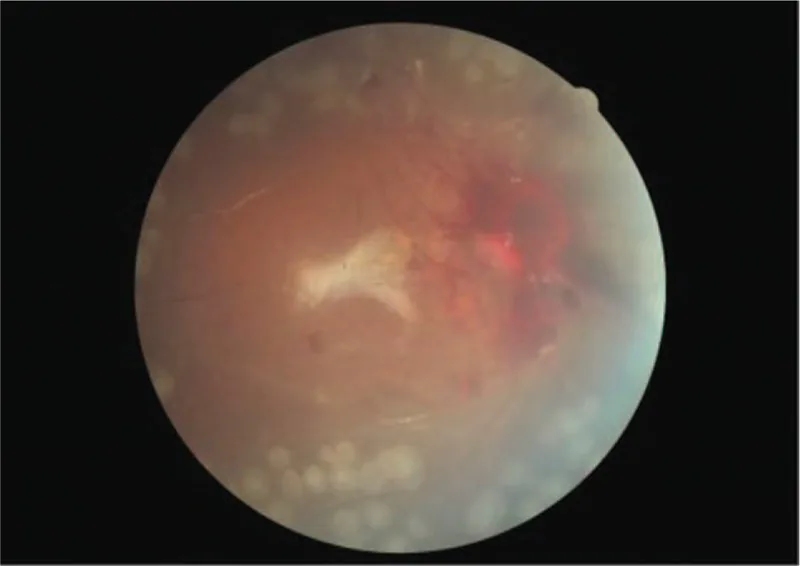
ภาพจอประสาทตาแสดงเลือดออกที่ขั้วประสาทตาหลังผ่าตัด TTP Bilateral proliferative retinopathy and ischemic optic neuropathy in a patient with atypical hemolytic-uremic syndrome: A case report. Medicine (Baltimore). 2019 Sep 27; 98(39):e17232. Figure 4. PM
CI D: PMC6775429. License: CC BY.
ภาพถ่ายสีของจอประสาทตา ข้างขวาหลังการผ่าตัด แม้จะมีเลือดออกที่มองเห็นได้รอบขั้วประสาทตา แต่จอประสาทตา ยังคงติดดีอยู่
มีรายงานอาการที่ผู้ป่วยรู้สึกได้ทางจักษุวิทยาดังต่อไปนี้
การมองเห็น ลดลงอย่างเฉียบพลันจอประสาทตา ตามัว : เกิดขึ้นเป็นลำดับรองจากอาการบวมของขั้วประสาทตาภาพซ้อน (diplopia)ความผิดปกติของการเคลื่อนไหวลูกตา จากอัมพาตของเส้นประสาทสมองตามัวชั่วคราว และมองเห็นเป็นสีเหลือง3) .
อาการทั่วร่างกายของ TTP ได้แก่ ปวดศีรษะ การเปลี่ยนแปลงของสติสัมปชัญญะ ความผิดปกติทางจิต ชัก การขาดดุลทางระบบประสาทเฉพาะที่ ไข้ อ่อนเพลีย ปวดข้อ ดีซ่าน คลื่นไส้และอาเจียน 1) การตกเลือดที่ผิวหนังและเยื่อเมือก (จ้ำเลือด จุดเลือดออก เลือดออกตามไรฟัน) ยังเกิดขึ้นเป็นผลรองจากภาวะเกล็ดเลือดต่ำ 3) .
อาการแสดงทางคลินิกทางจักษุวิทยาแบ่งออกเป็นอาการแสดงที่จอประสาทตา และอาการแสดงทางประสาทจักษุวิทยา
อาการแสดงที่จอประสาทตาและคอรอยด์
เลือดออกในจอประสาทตา : เกิดขึ้นสัมพันธ์กับโรคหลอดเลือดขนาดเล็กผิดปกติ
การอุดตันของหลอดเลือดแดงหรือหลอดเลือดดำจอตา : ภาวะขาดเลือดของจอตาจากการอุดตันของหลอดเลือดจอตาเนื่องจากลิ่มเลือด
จอตาลอกชนิดมีน้ำใต้จอตา : เกิดจากความผิดปกติของการไหลเวียนเลือดในคอรอยด์
เส้นเลือดใหม่ : เกิดขึ้นจากภาวะขาดเลือดของจอตา
จอตาเสื่อม : มักเกิดร่วมกับโรคไต โดยพบประมาณ 10% ของผู้ป่วย
อาการแสดงทางประสาทจักษุวิทยา
ปุ่มประสาทตาบวม (papilledema)
รูม่านตาไม่เท่ากัน (anisocoria)
ตาเหล่ (ocular misalignment)
จอประสาทตา และเส้นประสาทตา อักเสบจากความดันโลหิตสูง
สาเหตุพื้นฐานของ TTP คือการลดลงของกิจกรรม ADAMTS13 ADAMTS13 เป็นโปรตีเอสที่ตัดโมเลกุลขนาดใหญ่ของ von Willebrand factor (vWF) เมื่อกิจกรรมลดลง โมเลกุลขนาดใหญ่ของ vWF จะไม่ถูกตัดและสะสมในกระแสเลือด ทำให้เกิดลิ่มเลือดขนาดเล็กที่อุดมด้วยเกล็ดเลือด
สาเหตุของ TTP ชนิด先天性 (กรรมพันธุ์) คือการกลายพันธุ์ของยีน ADAMTS13 และมักแสดงอาการเมื่อถูกกระตุ้นโดยการตั้งครรภ์ ใน TTP ชนิด先天性 ความเสี่ยงของการกลับเป็นซ้ำระหว่างตั้งครรภ์สูงถึง 100% ในขณะที่ชนิด后天性อยู่ที่ 0-50% 3) .
การติดเชื้อ : ภาวะติดเชื้อในกระแสเลือด การติดเชื้อซัลโมเนลลา เป็นต้น 8) .การตั้งครรภ์ : ในช่วงท้ายของการตั้งครรภ์ ระดับ vWF เพิ่มขึ้น 1.5-3.0 เท่า และ ADAMTS13 ลดลงเหลือ 25-30% 3) .โรคภูมิต้านตนเอง : SLE , กลุ่มอาการแอนไทฟอสโฟไลปิด (APS), กลุ่มอาการโจเกรน เป็นต้น 1) 7) .ยา : ยายับยั้งไทโรซีนไคเนส เป็นต้นวัคซีน : มีรายงานผู้ป่วยหลังฉีดวัคซีนโควิด-19 โดยพบมากที่สุดหลังฉีด BNT162b2 (7 ใน 10 รายในเอกสาร) 5) .การผ่าตัด : มีผู้ป่วยหลังการผ่าตัดหัวใจ (เปลี่ยนลิ้นหัวใจ, TAVR) 4) .การติดเชื้อเอชไอวี 7) .
Q
TTP ถ่ายทอดทางพันธุกรรมหรือไม่?
A
TTP ชนิด先天性 (Upshaw-Schulman syndrome) เกิดจากการกลายพันธุ์ของยีน ADAMTS13 และเป็นโรคทางพันธุกรรม ฐานข้อมูล NCBI ClinVar มีตำแหน่งกลายพันธุ์มากกว่า 260 ตำแหน่ง มักอยู่ในรูปแบบการกลายพันธุ์แบบ compound heterozygous อย่างไรก็ตาม ประมาณ 95% ของ TTP ทั้งหมดเป็นชนิดที่ได้มาและเกิดจากแอนติบอดีต่อ ADAMTS13
การวินิจฉัย TTP ขึ้นอยู่กับการยืนยันเกณฑ์หลักสองประการ ได้แก่ ภาวะโลหิตจางจากการแตกของเม็ดเลือดแดงแบบไมโครแองจิโอพาธี (MAHA) และภาวะจ้ำเลือดจากเกล็ดเลือดต่ำ ต้องเริ่มการรักษาโดยไม่ต้องรอผลการตรวจกิจกรรมของ ADAMTS13
จำนวนเกล็ดเลือด : ปกติ <20×10⁹/ลิตร1) ฮีโมโกลบิน : ปกติ <8 กรัม/เดซิลิตร (80 กรัม/ลิตร)1) LDH และบิลิรูบิน : เพิ่มขึ้นเนื่องจากภาวะเม็ดเลือดแดงแตกในหลอดเลือด 1) .การย้อมเลือดส่วนปลาย : ยืนยันพบเม็ดเลือดแดงแตกเป็นชิ้น (schistocytes) 2) .เรติคิวโลไซต์ : เพิ่มขึ้น 2) .แฮปโตโกลบิน : ลดลง 5) .กิจกรรม ADAMTS13 : น้อยกว่า 10% มีนัยสำคัญในการวินิจฉัยที่แน่ชัด มีรายงานกรณีที่น้อยกว่า 5% เช่นกัน 5) .แอนติบอดีต่อ ADAMTS13 : ใช้เพื่อยืนยัน TTP ที่ได้มา 2) .โทรโปนิน : ตัวบ่งชี้ความเสียหายของหัวใจ ระดับ ≥0.25 ไมโครกรัม/ลิตร เป็นปัจจัยทำนายการเสียชีวิตอย่างอิสระ (OR 2.87)3) .
คะแนน PLASMIC เป็นระบบการให้คะแนนที่ใช้ในการแบ่งระดับความเสี่ยงของ TTP
รายการ เนื้อหา เกล็ดเลือด <30×10⁹/ลิตร 1 คะแนน สัญญาณของการแตกของเม็ดเลือดแดง 1 คะแนน ไม่มีมะเร็งที่กำลังดำเนิน 1 คะแนน ไม่มีประวัติการปลูกถ่ายอวัยวะ 1 คะแนน MCV <90 fL 1 คะแนน INR <1.5 1 คะแนน Cr <2 mg/dL 1 คะแนน
0–4 คะแนน: ความเสี่ยงต่ำ, 5 คะแนน: ความเสี่ยงปานกลาง, 6–7 คะแนน: ความเสี่ยงสูง4) .
อาจไม่สามารถแยก TTP ออกได้แม้ระดับกิจกรรม ADAMTS13 อยู่ที่ 10–30% (ผู้ป่วยความเสี่ยงปานกลาง/สูง)4) .
ในกรณีที่เกี่ยวข้องกับการตั้งครรภ์ สิ่งสำคัญคือต้องแยกโรคจากภาวะต่อไปนี้:
กลุ่มอาการ HELLP กลุ่มอาการเม็ดเลือดแดงแตก-ยูรีเมีย (HUS) ตับไขมันเฉียบพลัน APS ทางสูติศาสตร์ 3) .
นอกจากนี้ โรคอื่นที่ทำให้ ADAMTS13 ต่ำ เช่น ภาวะติดเชื้อในกระแสเลือด กลุ่มอาการ DIC โรคตับ และไข้มาลาเรียชนิดฟัลซิปารัม ก็จำเป็นต้องแยกโรคด้วย
หากพบความผิดปกติทางจักษุวิทยา ให้ซักประวัติโดยละเอียดเกี่ยวกับอาการทางระบบอื่นๆ และตรวจสอบว่ามีอาการคลาสสิก 5 ประการของ TTP หรือไม่
การแลกเปลี่ยนพลาสมา เป็นการรักษาทางเลือกแรก คาดว่าจะได้ผล 4 ประการดังนี้
การเสริม ADAMTS13
การกำจัดสารยับยั้ง (แอนติบอดีตนเอง)
การกำจัด vWF มัลติเมอร์ที่มีมวลโมเลกุลสูงมาก (UL-vWFM)
การเสริม vWF ปกติ
ใน TTP ระหว่างตั้งครรภ์ ให้ทำ 2000 มล./ครั้ง (40-60 มล./กก.) วันละ 1-2 ครั้ง 3) อัตราการเสียชีวิตหากไม่รักษาคือ 90% สามารถลดลงเหลือ 10-20% ด้วยการนำพลาสมาเอ็กซ์เชนจ์มาใช้ 3) .
หากไม่มีภาวะขาด ADAMTS13 ชนิดรุนแรงที่ได้มา การให้พลาสมาแช่แข็งสดก็เป็นทางเลือกหนึ่ง
กลูโคคอร์ติคอยด์ : เริ่มทันทีหากมีข้อสงสัยทางคลินิกระดับปานกลางขึ้นไป 4) .การรักษาด้วยสเตียรอยด์ แบบชีพจร : การให้เมทิลเพรดนิโซโลนขนาดสูงทางหลอดเลือดดำ
ใช้เป็นยาเสริมสำหรับผู้ป่วยที่ดื้อต่อการรักษาหรือกลับเป็นซ้ำ
ขนาดมาตรฐาน: 375 มก./ตร.ม. สัปดาห์ละครั้ง นาน 4 สัปดาห์5)
ขนาดต่ำ (100 มก./สัปดาห์ × 4 ครั้ง) ก็มีรายงานว่าทำให้โรคสงบสมบูรณ์ได้2) อัตราการสงบสมบูรณ์อยู่ที่ 83–100%2)
กรณีดื้อและกลับเป็นซ้ำ : อาจพิจารณาใช้ยากดภูมิคุ้มกัน เช่น วินคริสทีนซัลเฟตและไซโคลฟอสฟาไมด์ รวมถึงการตัดม้ามการรักษาทางจักษุวิทยาสำหรับภาวะขาดเลือดของจอประสาทตา : ทำการจี้ด้วยแสง (photocoagulation) เพื่อจัดการกับเส้นเลือดใหม่ที่ผิดปกติ
การให้เกล็ดเลือดเป็นข้อห้าม ไม่ควรให้เพราะจะทำให้ลิ่มเลือดขนาดเล็กแย่ลงคอร์ติโคสเตียรอยด์ ขนาดสูงมีความเสี่ยงต่อภาวะความดันโลหิตสูงและภาวะน้ำเกิน และไม่แนะนำในผู้ป่วยที่มีภาวะสมองส่วนท้ายทอยบวมจากการทำงานผิดปกติแบบผันกลับได้ (PRES)1) .
Q
เหตุใดการให้เกล็ดเลือดจึงมีข้อห้ามใน TTP?
A
ใน TTP ลิ่มเลือดขนาดเล็กที่อุดมด้วยเกล็ดเลือดจะก่อตัวในหลอดเลือดขนาดเล็กทั่วร่างกาย การให้เกล็ดเลือดในภาวะนี้อาจส่งเสริมการเกิดลิ่มเลือดขนาดเล็กเพิ่มเติมและเสี่ยงต่อการทำให้โรคแย่ลง การรักษาทางเลือกแรกคือการแลกเปลี่ยนพลาสมา และไม่ควรให้เกล็ดเลือดเว้นแต่มีเลือดออกที่คุกคามชีวิต
Q
การรักษาภาวะแทรกซ้อนทางจักษุวิทยาทำอย่างไร?
A
หากเกิดภาวะขาดเลือดของจอประสาทตา จะทำการจี้ด้วยแสง (photocoagulation) เพื่อจัดการกับเส้นเลือดใหม่ที่เกิดตามหลังภาวะขาดเลือดของจอประสาทตา อาการบวมของจานประสาทตา อาจเกิดจากความดันในกะโหลกศีรษะสูงหรือความดันโลหิตสูงชนิดร้ายแรง และต้องจัดการควบคู่ไปกับการรักษาโรคต้นเหตุ (TTP)
กลไกของอาการทางจักษุวิทยาใน TTP เกิดจากสายโซ่ของการเกิดลิ่มเลือดขนาดเล็กซึ่งเริ่มต้นจากการขาด ADAMTS13
vWF เป็นโปรตีนที่หลั่งจากเยื่อบุหลอดเลือดและเมกะคาริโอไซต์ โดยปกติจะถูกตัดและย่อยสลายโดย ADAMTS13 ใน TTP ที่ได้มา จะเกิดแอนติบอดีต่อตนเองต่อ ADAMTS13 ส่วนใน TTP แต่กำเนิด สาเหตุคือการกลายพันธุ์ที่ตำแหน่งยีน ADAMTS13
การขาดหรือการทำงานของ ADAMTS13 ที่ลดลงทำให้เกิดการสะสมของ vWF น้ำหนักโมเลกุลสูง (multimer vWF ขนาดใหญ่มาก) ที่ทนต่อเอนไซม์ย่อยสลายในพลาสมา สารนี้จับกับเกล็ดเลือดเกิดเป็นไมโครทรอมบัสที่อุดมด้วยเกล็ดเลือด อุดตันหลอดเลือดขนาดเล็กทั่วร่างกาย เกิดภาวะโลหิตจางจากการแตกของเม็ดเลือดแดงเชิงกล (microangiopathic hemolytic anemia) ร่วมด้วย
ไมโครทรอมบัสในหลอดเลือดจอตาและคอรอยด์ → การไหลเวียนเลือดไปจอตาลดลง → จอตาตกเลือด หลอดเลือดอุดตัน และจอตาลอกแบบมีน้ำใต้จอตาการเปลี่ยนแปลงทุติยภูมิจากจอตาขาดเลือด → การสร้างเส้นเลือดใหม่ความผิดปกติของเส้นประสาทสมองทุติยภูมิจากภาวะขาดเลือดเนื่องจากลิ่มเลือด → รูม่านตาไม่เท่ากัน และตำแหน่งลูกตาผิดปกติภาวะไตวายร่วม → ภาวะฉุกเฉินความดันโลหิตสูง (ความดันโลหิตสูงชนิดร้ายแรง) → จานประสาทตา บวม จอตาจากความดันโลหิตสูง และประสาทตาอักเสบ
ความชุกของโรคหลอดเลือดสมองใน TTP รายงานอยู่ที่ 13.9% ซึ่งสูงกว่าเมื่อเทียบกับ 6.3–7.8% ในผู้สูงอายุทั่วไป 1) กลุ่มอาการสมองส่วนหลังกลับคืนได้ (PRES) เป็นภาวะที่อาจเกิดร่วมกับ TTP และการถ่ายภาพด้วยคลื่นแม่เหล็กไฟฟ้าแบบแพร่ (DWI) มีประโยชน์ในการแยกความแตกต่างระหว่างสมองบวมจากหลอดเลือดและสมองบวมจากพิษต่อเซลล์ 1)
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
Caplacizumab เป็นนาโนบอดี (แอนติบอดีโดเมนเดี่ยว) ที่ถูกทำให้เป็นมนุษย์ ซึ่งกำหนดเป้าหมายที่โดเมน A1 ของ vWF ในการทดลอง HERCULES พบว่ายาช่วยให้จำนวนเกล็ดเลือดกลับสู่ปกติเร็วขึ้น ลดจำนวนครั้งของการแลกเปลี่ยนพลาสมา และลดอัตราการกลับเป็นซ้ำ 2) 3) นอกจากนี้ยังมีรายงานถึงประสิทธิภาพใน TTP ที่ดื้อต่อการรักษา 5) .
ในการทบทวนผู้ป่วย TTP ระหว่างตั้งครรภ์โดย Xu et al (2024) พบว่า ADAMTS13 recombinant มีศักยภาพในการเอาชนะแอนติบอดีที่ยับยั้งและทำให้กิจกรรมการตัด vWF กลับมาเป็นปกติ จึงคาดหวังให้เป็นทางเลือกในการรักษาในอนาคต3) .
N-อะเซทิลซิสเทอีน : ลดขนาดและกิจกรรมของ vWF 3) .บอร์ทีโซมิบ : กำลังศึกษาวิจัยเพื่อลดปริมาณแอนติบอดี ADAMTS13 3) .การบำบัดทดแทนเอนไซม์ด้วยโปรตีนที่แสดงออกจากยีน : กำลังมีการวิจัยในฐานะทางเลือกการรักษาในอนาคตอันใกล้
Galindo-Calvillo และคณะ (2021) รายงานผู้ป่วย TTP ที่กลับเป็นซ้ำซึ่งบรรลุการทุเลาทางโลหิตวิทยาอย่างสมบูรณ์ด้วย rituximab ขนาดต่ำ (100 มก./สัปดาห์ × 4 ครั้ง) และ prednisone (1 มก./กก.) เพียงอย่างเดียวโดยไม่ต้องเปลี่ยนพลาสมาในช่วงการระบาดของ COVID-192) สิ่งนี้ชี้ให้เห็นถึงความเป็นไปได้ของกลยุทธ์การรักษาที่ไม่ต้องเปลี่ยนพลาสมาในกลุ่มย่อยของผู้ป่วย TTP ที่กลับเป็นซ้ำซึ่งมีอาการคงที่และไม่มีความเสียหายของอวัยวะ
รายงานการเกิด TTP หลังการฉีดวัคซีน BNT162b2 มีมากที่สุดในเอกสารทางการแพทย์ (7 ใน 10 ราย) ส่วนใหญ่เกิดขึ้นหลังเข็มที่สอง5) สันนิษฐานว่ามีกลไกการเลียนแบบเอพิโทป แต่จำเป็นต้องมีการวิจัยเพิ่มเติมเพื่อสร้างความสัมพันธ์เชิงสาเหตุ
Zhu H, Liu J-Y. Thrombotic thrombocytopenic purpura with neurological impairment: A Review. Medicine. 2022;101(49):e31851.
Galindo-Calvillo CD, Torres-Villalobos G, Higuera-Calleja J, et al. Treating thrombotic thrombocytopenic purpura without plasma exchange during the COVID-19 pandemic. Transfus Apher Sci. 2021;60:103107.
Xu J, Cai H, Xu J, et al. Case report of thrombotic thrombocytopenic purpura during pregnancy with a review of the relevant research. Medicine. 2024;103(20):e38112.
Shao X, Hao P, Dong X, et al. Thrombotic Thrombocytopenia Purpura (TTP) following emergent aortic valve replacement after a complicated TAVR procedure. J Cardiothorac Surg. 2024;19:545.
Hammami E, Mdhaffar M, Jamoussi K, et al. Acquired Thrombotic Thrombocytopenic Purpura After BNT162b2 COVID-19 Vaccine: Case Report and Literature Review. Lab Med. 2022.
Li P, Lv T, Chen S, et al. An ADAMTS13 mutation that causes hereditary thrombotic thrombocytopenic purpura: a case report and literature review. BMC Med Genomics. 2021;14:252.
Lin HC, Chen PC, Chen YF, et al. Concurrence of immune thrombocytopenic purpura and thrombotic thrombocytopenic purpura: a case report and review of the literature. J Med Case Rep. 2023;17:38.
Wang Z, Xu H, Peng B, et al. Flavorubredoxin, a Candidate Trigger Related to Thrombotic Thrombocytopenic Purpura. Front Cell Infect Microbiol. 2022;12:864087.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต