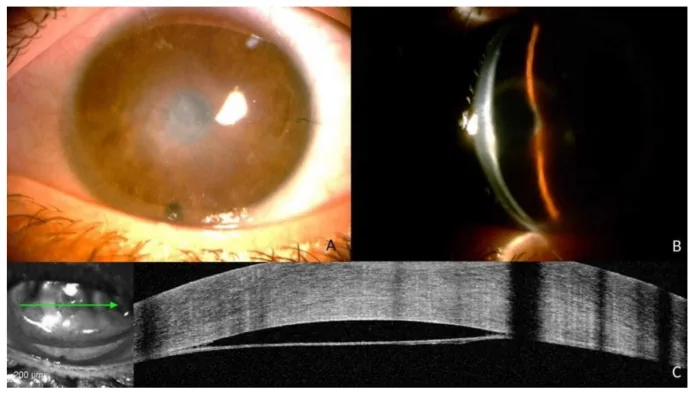
การหลุดลอกของเยื่อเดสเซเมต (DMD) เป็นภาวะที่เยื่อเดสเซเมตหลุดออกจากผิวด้านหลังของสโตรมาของกระจกตา
การผ่าตัดต้อกระจก เป็นสาเหตุที่พบบ่อยที่สุด โดยอัตราการเกิดที่มีนัยสำคัญทางคลินิกหลังการสลายต้อกระจก ด้วยคลื่นเสียงความถี่สูง (PEA ) อยู่ระหว่าง 0.044% ถึง 0.5%
การหลุดลอกของเยื่อเดสเซเม็ท (DMD) แบบกว้างทำให้เกิดอาการบวมน้ำที่กระจกตา และการมองเห็น ลดลง จำเป็นต้องทำการตรึงเยื่อเดสเซเม็ท (descemetopexy) ตั้งแต่เนิ่นๆ
การตรวจเอกซเรย์เชื่อมโยงแสงช่วงหน้าตา (AS-OCT ) เป็นมาตรฐานทองคำในการวินิจฉัย DMD การประเมินขอบเขต และการกำหนดแนวทางการรักษา
DMD ขนาดเล็กบริเวณรอบนอกมักจะกลับมาแนบเองได้เมื่อสังเกตอาการ
การหลุดลอกของเยื่อเดสเซเม็ท (Descemet membrane detachment: DMD) เป็นภาวะที่เยื่อเดสเซเม็ทหลุดออกจากผิวด้านหลังของสโตรมาของกระจกตา เกิดขึ้นส่วนใหญ่เป็นภาวะแทรกซ้อนของการผ่าตัดภายในลูกตา อาจเกิดจากการบาดเจ็บที่ตาหรือพบได้น้อยคือเกิดขึ้นเอง รหัส ICD-10 คือ H18.33
การผ่าตัดต้อกระจก เป็นสถานการณ์ที่พบบ่อยที่สุด โดยมีรายงานอัตราการเกิดหลังการผ่าตัดต้อกระจก แบบถุงนอก (ECCE ) 2.5% และหลัง PEA 0.5% ด้วยความก้าวหน้าล่าสุดของเทคนิค PEA ความถี่ของ DMD แบบกว้างที่มีนัยสำคัญทางคลินิกลดลงเหลือ 0.044% ในทางกลับกัน การตรวจอย่างละเอียดด้วย OCT ตรวจพบ DMD ขนาดเล็กใน 37.1% ของกรณีในวันแรกหลังผ่าตัด แต่ลดลงเหลือ 4.5% หลังจาก 1-3 เดือน และหายไปหลังจาก 3 เดือน
ภาพการหลุดลอกของเยื่อเดสเซเม็ท Antonio Moramarco, Danilo Iannetta, Luca Cimino, Vito Romano, et al. Case Report: “Spontaneous Descemet Membrane Detachment” 2022 Dec 31 J Clin Med. 2022 Dec 31; 12(1):330 Figure 1. PM
CI D: PMC9820967. License: CC BY.
A คือภาพถ่ายช่วงหน้าตาที่มีความขุ่นตรงกลาง B คือภาพจากกล้องจุลทรรศน์ชีวภาพจากด้านข้าง C คือ
AS-OCT แสดง DMD แบบกว้างที่แยกออกจากผิวด้านหลังของ
กระจกตา เป็นแนวโค้ง สามารถเปรียบเทียบขอบเขตการหลุดลอกระหว่างภาพทางคลินิกและภาพตัดขวางได้
ข้อร้องเรียนหลักคือ การมองเห็น ดีขึ้นไม่ดีการมองเห็น ลดลงอย่างกะทันหันต้อกระจก ผู้ป่วยอาจบ่นว่า ตามัว เนื่องจากอาการบวมน้ำที่กระจกตา หรือ รู้สึกมีสิ่งแปลกปลอม เนื่องจากความไม่สม่ำเสมอของเยื่อบุกระจกตา
ผลการตรวจด้วยกล้องจุลทรรศน์ชีวภาพ
เส้น DM : เส้นการหลุดลอกของเยื่อเดสเซเม็ทจะสังเกตเห็นได้ในช่องหน้าลูกตา ตรงกับบริเวณที่กระจกตา ขุ่น
อาการบวมน้ำที่กระจกตา : มีอาการบวมน้ำเฉพาะที่หรือกระจายในชั้นสโตรมาและเยื่อบุกระจกตา
ช่องหน้าม่านตา สองชั้น : ใน DMD ที่กว้างและอยู่ตรงกลาง จะมีลักษณะเด่นคือ “ช่องหน้าม่านตา สองชั้น”
รอยย่นของ DM : อาจพบรอยย่นของเยื่อเดสเซเม็ต
การจำแนกและลักษณะ
DMD เฉพาะที่ : การลอกเฉพาะที่รอบแผลผ่าตัด ≤1 มม. ไม่มีผลต่อการมองเห็น สามารถสังเกตอาการได้
DMD กว้าง : ทำให้เกิดอาการบวมน้ำในชั้นสโตรมากระจกตา อย่างกว้างขวาง ลดการมองเห็น ภายในช่องหน้าม่านตา
DMD ชนิดมีเลือดออก : เลือดไหลเข้าไปในช่องว่างที่ลอกหลังการผ่าตัดคลองชเลมม์ เกิดขึ้นใน 1.6–9.1% หลังการผ่าตัด canaloplasty2)
DMD ชนิดไม่มีเลือดออก : การลอกที่ใส ประกอบด้วยสารหนืดยืดหยุ่น หรืออารมณ์ขัน aqueous
DMD มักเกิดขึ้นเมื่อ aqueous humor เข้าสู่ช่องว่างหน้าเยื่อเดสเซเม็ตผ่านรอยฉีกขาดในเยื่อเดสเซเม็ต
การผ่าตัด ลักษณะ การผ่าตัดต้อกระจก พบบ่อยที่สุด ผลกระทบทางกลต่อแผลผ่าตัด การผ่าตัด canaloplasty การสะสมของสารหนืดหยุ่นในส่วนล่าง2) การตัดม่านตาด้วยเลเซอร์ Nd:YAG (LPI )การฉีกขาดของเยื่อหุ้มเดสเซเมทจากคลื่นกระแทก8)
กลไกการเกิดในการผ่าตัดต้อกระจก : การสร้างแผลด้วยมีดทื่อ การนำเครื่องมือผ่าตัดเข้า-ออกอย่างไม่ระมัดระวังผ่านแผลขนาดเล็ก การฉีดน้ำหล่อเลี้ยงเข้าไปในเนื้อกระจกตา โดยผิดพลาดระหว่างการให้ความชุ่มชื้นหรือ OVD ความเสี่ยงของ DMD สูงเมื่อทำการให้ความชุ่มชื้นใกล้ลิ้นภายในอุโมงค์ (ใกล้เยื่อหุ้มเดสเซเมท)
การผ่าตัดต้อกระจก หลัง DALK : หลัง DALK จะมีระนาบแยกระหว่างเนื้อกระจกตา ของผู้บริจาคและชั้นก่อนเยื่อหุ้มเดสเซเมทของผู้รับ ในระหว่างการให้ความชุ่มชื้นแผล น้ำเกลือสมดุล (BSS) อาจไปถึงระนาบนี้และทำให้เกิด DMD จากแรงดันน้ำ7) .
การผ่าตัด canaloplasty : สารหนืดหยุ่นที่ฉีดระหว่างการดึงสายสวนขนาดเล็กจะสะสมในจตุภาคล่างของคลองชเลมม์ ทำให้เกิดแรงดันเกินจุดสิ้นสุดของเยื่อหุ้มเดสเซเมทที่เส้นชวาลเบอ ส่งผลให้เกิด DMD อุบัติการณ์สูงขึ้นในการผ่าตัดร่วม (phaco-canaloplasty)2) .
หลังการตัดม่านตาด้วยเลเซอร์ Nd:YAG : คลื่นกระแทกจากการสลายด้วยแสงอาจทำให้เกิดการฉีกขาดเป็นเส้นตรงที่ระดับเยื่อหุ้มเดสเซเมทและนำไปสู่ DMD ช่องหน้าม่านตาตื้น และภาวะเทียมลอกเป็นปัจจัยเสี่ยง8) .
ปัจจัยผู้ป่วย : อายุมากกว่า 65 ปี โรคเยื่อบุกระจกตา เสื่อมชนิด Fuchs กระจกตา guttata กลุ่มอาการเทียมลอก โรคกระจกตา เสื่อม เบาหวานปัจจัยระหว่างผ่าตัด : มีดทื่อ แผลขนาดเล็ก การฉีด OVD /น้ำหล่อเลี้ยงที่ไม่เหมาะสม การเข้าช่องหน้าม่านตา ในช่องตื้น การยืดเวลาผ่าตัดปัจจัยหลังผ่าตัด : ปัจจัยทางพันธุกรรมที่เกี่ยวข้องกับการยึดเกาะที่ไม่ดีระหว่างเยื่อหุ้มเดสเซเมทและเนื้อกระจกตา ชั้นหลัง
Q
ทำไม DMD จึงเกิดได้ง่ายกว่าในการผ่าตัดต้อกระจกหลัง DALK?
A
ในการผ่าตัด DALK เนื้อเยื่อสโตรมาของกระจกตา ผู้บริจาคจะถูกแทนที่จนถึงชั้นก่อนเดสเซเม็ทของผู้รับ การผ่าตัดนี้ทำให้เกิดระนาบการแยก (cleavage plane) ระหว่างสโตรมาผู้บริจาคและชั้นก่อนเดสเซเม็ทของผู้รับ เมื่อน้ำหล่อเลี้ยงระหว่างการผ่าตัดต้อกระจก ไปถึงระนาบนี้ จะเกิด DMD ได้ง่ายเนื่องจากแรงดันน้ำ 7) DMD นี้จำกัดอยู่เฉพาะใน graft DALK และไม่ลามไปยังส่วนปลายของกระจกตา ผู้รับ 7)
การวินิจฉัยขึ้นอยู่กับ ประวัติโรค และ การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp)กระจกตา อย่างรุนแรง การถ่ายภาพเป็นสิ่งจำเป็น
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด กระจกตา ใส จะสามารถเห็นเส้น DMD ได้โดยตรง ใน DMD ที่กว้าง อาการบวมน้ำที่กระจกตา ทำให้ตรวจพบ DMD ได้ยากOCT ส่วนหน้า (AS-OCT )4) 5) OCT แบบ swept-source ความละเอียดสูงมีประโยชน์ในการกำหนดแผนการรักษาและประเมินประสิทธิภาพการรักษา 4) การตรวจ Gonioscopy : มีประโยชน์ในการประเมิน DMD ส่วนปลายเฉพาะที่กล้องจุลทรรศน์อัลตราซาวนด์ (UBM ) : ใช้เมื่อการถ่ายภาพด้วยแสงทำได้ยากเนื่องจากกระจกตา ขุ่น
อัลกอริทึม HELP ถูกเสนอเป็นแนวทางที่มีโครงสร้างสำหรับการจัดการ DMD โดยใช้ AS-OCT 5) โดยประเมินความสูง (Height) ขอบเขต (Extent) ความยาว (Length) และความสัมพันธ์กับรูม่านตา (Pupil) เพื่อกำหนดแผนการรักษา
ข้อบ่งชี้ในการรักษาแบบประคับประคอง : ความสูง <100 ไมครอน และความยาว <1 มม. / ความสูง 100-300 ไมครอน และความยาว 1-2 มม. และไม่เกี่ยวข้องกับรูม่านตา ข้อบ่งชี้ในการรักษาโดยการผ่าตัด : ถ้าเกี่ยวข้องกับส่วนกลางของกระจกตา (ภายใน 5 มม.) หรือถ้ากว้าง
สิ่งสำคัญคือต้องแยกจากอาการบวมน้ำที่สโตรมาของกระจกตา อาการบวมน้ำที่สโตรมามีขอบเขต ไม่ชัดเจนและไม่สม่ำเสมอ เมื่อเทียบกับกระจกตา ปกติ ในขณะที่ DMD มีขอบเขต ชัดเจนและเป็นรูปโค้ง
Q
ทำไม AS-OCT จึงมีความสำคัญในการวินิจฉัย DMD?
A
ใน DMD ที่กว้าง อาการบวมน้ำที่กระจกตา ทำให้การประเมินด้วยกล้องจุลทรรศน์ชนิดกรีดทำได้ยาก AS-OCT ให้ภาพตัดขวางของกระจกตา ได้อย่างรวดเร็วและไม่สัมผัส ทำให้สามารถประเมินตำแหน่ง ความสูง และขอบเขตของ DMD ได้อย่างแม่นยำ 4) นอกจากนี้ยังจำเป็นสำหรับการกำหนดแผนการรักษาตามอัลกอริทึม HELP 5) และมีประโยชน์ในการยืนยันการกลับมาแนบกันอีกครั้งหลังการรักษา
DMD เฉพาะที่ขนาด <1 มม. สามารถ สังเกตอาการ ได้ การรักษาแบบประคับประคองใช้ ยาหยอดสเตียรอยด์ เฉพาะที่ (ลดการอักเสบ ป้องกันพังผืด) และ ยาหยอดไฮเปอร์โทนิก (ทำให้สตรอมขาดน้ำ) อัตราการติดเองตามธรรมชาติรายงานประมาณ 60%
เป็นมาตรฐานทองคำสำหรับ DMD ที่คงอยู่ ฉีดแก๊สเข้าช่องหน้าม่านตา เพื่อให้เยื่อเดสเซเมท ที่หลุดลอกกลับไปติดที่ผิวด้านหลังของสตรอมกระจกตา อัตราความสำเร็จในการติดกลับคือ 90-100% แต่ 4-7% ของกรณีจำเป็นต้องฉีดซ้ำ
แก๊สที่ใช้ :
อากาศ : ใช้เป็นตัวเลือกแรก การผ่าตัดสิ้นสุดโดยการแทนที่อารมอร์น้ำทั้งหมดด้วยอากาศ และรักษาศีรษะให้อยู่ในตำแหน่งที่แก๊สกระทบกับบริเวณ DMD หลังผ่าตัดSF₆ (ซัลเฟอร์เฮกซะฟลูออไรด์) : ความเข้มข้นไอโซเอกซ์แพนซีฟ 20% ระยะเวลาคงอยู่ประมาณ 2 สัปดาห์ ใช้ในกรณีที่กลับเป็นซ้ำหรือการฉีดอากาศครั้งแรกไม่สำเร็จC₃F₈ (ออกตะฟลูออโรโพรเพน) : ความเข้มข้นไอโซเอกซ์แพนซีฟ 14% ระยะเวลาคงอยู่ประมาณ 6 สัปดาห์ เนื่องจาก SF₆ และ C₃F₈ ขยายตัว จึงจำเป็นต้องทำม่านตา ตัดหรือขยายรูม่านตา เพื่อป้องกันการอุดตันของรูม่านตา
เทคนิค : ฉีดแก๊สด้วยเข็ม 27-30G หลังจากเติมช่องหน้าม่านตา ด้วยแก๊สเป็นเวลา 15-20 นาที ให้เอาฟองแก๊สออกหนึ่งในสามเพื่อป้องกันการอุดตันของรูม่านตา หลังผ่าตัด ให้รักษาท่านอนหงาย
เป็นเทคนิคใหม่สำหรับ DMD ที่ม้วน 1) ขั้นแรก ใช้ฟองเล็กเพื่อคลายการม้วนของ DM จากนั้นใช้ฟองใหญ่เพื่อให้ DM ติดกลับ ในหญิงอายุ 62 ปีที่มี DMD กว้างหลังผ่าตัดต้อกระจก (ที่มีการม้วน) ค่าการมองเห็น ที่ดีที่สุดที่แก้ไขแล้ว 6/9 บรรลุผลหลังจาก 6 สัปดาห์ด้วยวิธีนี้ 1)
นี่คือเทคนิคที่ทำการกรีดกระจกตา บางส่วนด้วยเข็ม 23G ในส่วนที่ลึกที่สุดของ DMD เพื่อระบายของเหลวที่เหลืออยู่ในช่องเหนือเยื่อเดสเซเม็ตหลังการทำเดสเซเมโทเพกซี 5) การศึกษาใน 5 รายพบว่าการฟื้นตัวของการมองเห็น เร็วขึ้น (ภายใน 1 สัปดาห์) เมื่อเทียบกับวิธีดั้งเดิม 5) หนึ่งรายจำเป็นต้องปลูกถ่ายกระจกตา เนื่องจาก DMD กลับเป็นซ้ำ 5)
ในกรณี DMD ที่เกิดขึ้นช้า 45 ปีหลังการปลูกถ่ายกระจกตา ทั้งชั้นซึ่งไม่ตอบสนองต่อการทำเดสเซเมโทเพกซีด้วยอากาศ/SF₆ ได้ทำการตัดเยื่อเดสเซเม็ตบางส่วนทางด้านศูนย์กลางของรอยต่อกราฟต์-โฮสต์ เพื่อปลดแรงดึงและทำให้เยื่อเดสเซเม็ตติดใหม่ทั้งหมด 6) นี่เป็นทางเลือกการรักษาใหม่สำหรับ DMD ชนิดดึงรั้งโดยไม่มีการฉีกขาดของเยื่อเดสเซเม็ต 6)
การปลูกถ่ายกระจกตา จะพิจารณาในกรณีที่กลับเป็นซ้ำหลายครั้งแม้จะฉีดแก๊สหลายครั้ง หรือเมื่อเกิดภาวะกระจกตา พุพอง (bullous keratopathy) ประมาณ 7-8% ของทุกกรณีจำเป็นต้องปลูกถ่ายกระจกตา โดยเลือก DMEK หรือ DSAEK
ภาวะแทรกซ้อนของการทำเดสเซเมโทเพกซี
DMD แบบต่อเนื่อง : ภาวะแทรกซ้อนที่พบบ่อยที่สุด
ความดันลูกตา สูง
ต้อหิน แบบปิดม่านตา ม่านตา ส่วนล่าง
ยูเวียอักเสบ : พบได้น้อย
การจัดการเมื่อกลับเป็นซ้ำ
การขุ่นมัวอีกครั้งหลังจากกระจกตา ใส : สงสัยสูงว่า DMD กลับเป็นซ้ำ ให้ฉีดแก๊สซ้ำทันที
กลับเป็นซ้ำหลายครั้ง : พิจารณาเปลี่ยนจากอากาศเป็น SF₆ หรือ C₃F₈
กรณีดื้อต่อการรักษา : พิจารณาการเย็บเยื่อเดสเซเม็ตหรือการตัดเยื่อเดสเซเม็ตบางส่วน 6)
Q
ควรเลือกใช้อากาศหรือ SF₆/C₃F₈ สำหรับฉีดเข้าช่องหน้าม่านตา?
A
หลักการพื้นฐานคือเลือกใช้อากาศในครั้งแรก อากาศปลอดภัยและทำให้เกิดความเสียหายต่อเอ็นโดทีเลียมกระจกตา น้อยกว่า หากเกิดซ้ำ ให้พิจารณาใช้ SF₆ หรือ C₃F₈ ก๊าซเหล่านี้มีประสิทธิภาพและคงอยู่ได้นาน แต่มีความเสี่ยงต่อการอุดตันรูม่านตา และต้อหินทุติยภูมิ เนื่องจากคุณสมบัติการขยายตัว แม้ในกรณีที่เกิดซ้ำ ก็มีความเห็นว่าการใช้อากาศซ้ำปลอดภัยกว่า โดยคำนึงถึงความเสียหายของเอ็นโดทีเลียมจากการคงอยู่ของก๊าซเป็นเวลานาน
กลไกการเกิด DMD คือการที่ aqueous humor เข้าสู่ช่องว่างก่อนเยื่อเดสเซเมท (pre-descemetic space) ผ่านบริเวณที่เยื่อเดสเซเมท ฉีกขาด ระหว่างการกรีดกระจกตา จะเกิดช่องว่างระหว่างสโตรมาและเยื่อเดสเซเมท และผ่านช่องว่างนี้ น้ำล้างหรือ OVD จะเข้าไป
เยื่อเดสเซเมท คือเยื่อฐานของเอ็นโดทีเลียมกระจกตา ประกอบด้วยชั้นแถบด้านหน้า (ABL, หนาประมาณ 3 ไมโครเมตร, สร้างก่อนเกิด) และชั้นไม่มีแถบด้านหลัง (PNBL, หลั่งโดยเซลล์เอ็นโดทีเลียมตลอดชีวิต, ประมาณ 3 ไมโครเมตรเมื่ออายุ 20 ปี, ประมาณ 10 ไมโครเมตรเมื่ออายุ 80 ปี)
ในกระจกตา หลัง DALK จะมีระนาบแยก (cleavage plane) ระหว่างสโตรมาของผู้บริจาคและชั้นก่อนเยื่อเดสเซเมท ของผู้รับ 7) ระหว่างการผ่าตัดต้อกระจก เมื่อ BSS มาถึงระนาบนี้ผ่านการให้ความชุ่มชื้น จะเกิด DMD จากแรงดันน้ำ ลักษณะเฉพาะคือ DMD จำกัดอยู่ภายใน graft และไม่ขยายไปยังบริเวณรอบนอกของกระจกตา ผู้รับ 7)
ใน DMD ที่เกิดช้าหลัง PK การปรับโครงสร้างของเนื้อเยื่อแผลเป็นระยะยาวที่รอยต่อ graft-ผู้รับ และการดำเนินของโรคกระจกตา รูปกรวยในฝั่งผู้รับ ทำให้เกิดแรงดึงที่ไม่สมดุลทั้งสองข้างของรอยต่อ ซึ่งอาจทำให้เกิด DMD 6) กลไกการดึงนี้ไม่เกี่ยวข้องกับการฉีกขาดของเยื่อเดสเซเมท และการทำ descemetopexy ด้วยอากาศ/แก๊สจะเกิดซ้ำอีก 6)
คลื่นกระแทกจากการสลายด้วยแสงและคลื่นความดันเสียงทำให้เกิดรอยแตกเชิงเส้นที่ระดับเยื่อเดสเซเมท 8) ในกรณีช่องหน้าม่านตาตื้น ระยะห่างระหว่างกระจกตา และพลาสมาสั้น ส่งผลให้พลังงานส่วนเกินถูกส่งไปยังเอ็นโดทีเลียมกระจกตา ในภาวะ pseudoexfoliation การหนาตัวแบบกระจายและไม่สม่ำเสมอของเยื่อเดสเซเมท และการสะสมของสาร pseudoexfoliation จะเพิ่มความเปราะบางต่อ DMD 8)
ระหว่างการผ่าตัด DSAEK เมื่อใส่เลนส์ด้วย Sheets glide ขอบเลื่อนที่ไม่เรียบอาจเกี่ยวเยื่อเดสเซเมท และทำให้เกิด DMD 3) นี่เป็นภาวะแทรกซ้อนที่พบได้น้อยมาก แต่การตรวจพบตั้งแต่เนิ่นๆ และการทำ descemetopexy อย่างรวดเร็วมีความสำคัญในการป้องกัน graft failure ปฐมภูมิ 3)
Köppe MK และคณะ (2024) ใช้เครื่อง OCT แหล่งกำเนิดแสงแบบกวาดความละเอียดสูง (Anterion) เพื่อวินิจฉัยและติดตามการรักษา DMD และยืนยันความสำเร็จทันทีของการอัดแก๊สใน DMD หลังผ่าตัดต้อกระจก ในชายอายุ 71 ปี พวกเขาแสดงให้เห็นว่า SS-OCT ความละเอียดสูงเป็นเครื่องมือที่มีประโยชน์ในการนำทางการตัดสินใจทางคลินิก 4)
Kundan S และคณะ (2025) รายงานการใช้ descemetopexy (C₃F₈ หรือ SF₆) ร่วมกับการกรีดระบายอากาศที่กระจกตา ในผู้ป่วย DMD หลังผ่าตัดต้อกระจก 5 ราย การฟื้นฟูการมองเห็น ที่ดีเกิดขึ้นภายในหนึ่งสัปดาห์ใน 4 ราย พวกเขาสรุปว่าการกำจัดของเหลวที่เหลืออยู่ในช่องเหนือเยื่อหุ้มเดสเซเม็ทมีส่วนช่วยให้ DM ติดใหม่เร็วขึ้น 5)
Sharma A และคณะ (2023) รายงานเทคนิค pneumodescemetopexy แบบฟองคู่สำหรับ DMD ที่ม้วนตัว เทคนิคที่ควบคุมได้สูงนี้ใช้ฟองเล็กเพื่อคลายการม้วนของ DM และฟองใหญ่เพื่อให้ติดใหม่ หลีกเลี่ยงการปลูกถ่ายเยื่อบุผิวดวงตา 1)
Hasan SM และคณะ (2021) รายงาน DMD ที่เกิดขึ้นช้า 45 ปีหลังการปลูกถ่ายกระจกตา แบบทะลุทะลวง ซึ่ง descemetopexy ด้วยอากาศและ SF₆ ล้มเหลว จากนั้นจึงติดใหม่ทั้งหมดด้วยการตัดเยื่อหุ้มเดสเซเม็ทบางส่วน พวกเขาเสนอกลไกการดึงรั้งและแสดงให้เห็นว่าการปลดการดึงรั้งเป็นกุญแจสำคัญในการรักษา 6)
เนื้อหาในบทความนี้มีวัตถุประสงค์เพื่อให้ข้อมูลทางการศึกษาแก่บุคลากรทางการแพทย์ และไม่สามารถใช้แทนการวินิจฉัยหรือการรักษาเฉพาะบุคคล การตัดสินใจทางคลินิกที่แท้จริงควรกระทำภายใต้ความรับผิดชอบของแพทย์ผู้รักษา
Sharma A, Sharma R, Kulshreshta A, Nirankari VS. Double bubble pneumodescemetopexy for the management of Descemet membrane detachment: An innovative technique. Indian J Ophthalmol. 2023;71(5):2234-2236.
Orejudo de Rivas M, Martínez Morales J, Pardina Claver E, et al. Descemet’s Membrane Detachment during Phacocanaloplasty: Case Series and In-Depth Literature Review. J Clin Med. 2023;12(17):5461.
Bevara A, Murthy SI. Iatrogenic Descemet membrane detachment in the donor lenticule during Descemet stripping automated endothelial keratoplasty. BMJ Case Rep. 2023;16(12):e256380.
Köppe MK, Khoramnia R, Auffarth GU, Augustin VA. Pseudophakic corneal edema caused by Descemet membrane detachment using high-resolution swept-source OCT imaging. GMS Ophthalmol Cases. 2024;14:Doc12.
Kundan S, Sahu PK, Sharma A, Das GK, Aamir PA. Descemet Membrane Detachment Assessed by Anterior Segment-Optical Coherence Tomography and Managed With Descemetopexy and Corneal Venting Incision: A Case Series. Cureus. 2025;17(6):e86631.
Hasan SM, Jakob-Girbig J, Pateronis K, Meller D. Partial descemetorhexis for delayed Descemet membrane detachment following penetrating keratoplasty, suggestion of a pathomechanism. Am J Ophthalmol Case Rep. 2021;22:101077.
Das AK, Panigrahi A, Gupta N. Central and bullous Descemet membrane detachment during cataract wound hydration: an insightful complication in a post-DALK eye. BMJ Case Rep. 2022;15(3):e249260.
Turaga K, Kalary J, Velamala IP. Descemet’s membrane detachment after Nd:YAG laser iridotomy in a patient with pseudoexfoliation. BMJ Case Rep. 2022;15(2):e246071.