수술 관련 요인

수술 후 괴사성 공막염
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 수술 후 괴사성 공막염이란
섹션 제목: “1. 수술 후 괴사성 공막염이란”수술 후 괴사성 공막염(surgically induced necrotizing scleritis: SINS)은 안과 수술 후 수술 창에 인접한 공막 조직에 염증과 괴사가 발생하는 드문 합병증입니다. 여러 차례의 안과 수술 후에 가장 흔히 발생합니다. 이 질환을 지칭하는 다른 명칭으로 수술 유발 공막 괴사(surgically-induced scleral necrosis), 수술 후 공막 용해(postoperative scleral melting) 등이 있습니다.
발생률은 1만 예 중 1예 미만으로 추정되며, 10만 예 중 1예 미만이라는 보고도 있습니다 2). 여성이 약 70%를 차지하고, 평균 연령은 68.2세입니다 3). 수술부터 SINS 발병까지의 평균 기간은 9개월이지만, 수술 후 수일에서 최장 51년까지 보고되었습니다.
SINS와 관련이 보고된 안과 수술 중 익상편 수술이 가장 많아 전체의 63.4%를 차지합니다. 다음으로 백내장 수술이 17.5%, 공막 돌륭술이 11.3%입니다 3). 그 외 사시 수술, 섬유주 절제술, 유리체 절제술 후에도 보고가 있습니다. 마이토마이신 C를 사용하는 수술에서도 위험이 높아집니다.
발생률은 1만 예 중 1예 미만이며, 10만 예 중 1예 미만으로 추정하기도 합니다 2). 그러나 SINS는 초기 증상이 경미하여 간과될 가능성이 있어 실제 발생률은 더 높을 수 있습니다. 익상편 수술 후 공막 괴사가 SINS로 올바르게 진단되지 않는 경우도 있다고 지적됩니다 4).
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”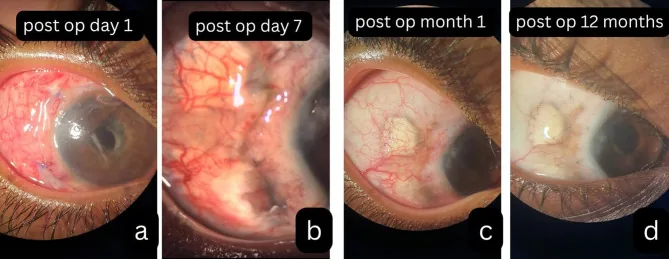
자각 증상
섹션 제목: “자각 증상”- 충혈: 수술 창상에 인접한 국소적인 심한 충혈로 나타납니다.
- 안통: 심한 통증을 동반하는 경우가 많으며, 안구 운동 시 악화됩니다.
- 눈물 및 압통: 안구 촉진 시 압통이 있습니다.
임상 소견 (의사가 진찰 시 확인하는 소견)
섹션 제목: “임상 소견 (의사가 진찰 시 확인하는 소견)”- 수술 창상 인접부의 공막 괴사: 수술 부위에 인접한 공막 조직의 염증과 괴사가 특징적입니다. 공막이 얇아지고 ‘도자기 모양(porcelainized)’ 외관을 나타냅니다 3).
- 포도막 투시 및 탈출: 심한 괴사에서는 얇아진 공막을 통해 포도막이 투시됩니다. 천공에 이를 수도 있습니다.
- 괴사성 각막염의 합병: 염증이 각막으로 파급될 수 있습니다. 주변부 각막 침윤을 동반하기도 합니다 3).
- 후부 공막염으로의 파급: 드물게 염증이 후방으로 파급되어 후부 공막염을 일으킵니다. 익상편 수술 후 미만성 전부 공막염에 후부 공막염이 합병된 증례가 보고되었습니다 4).
- 안내 염증: 전방 내 염증 세포나 각막 후면 침착물이 나타날 수 있습니다 1).
Nakagawa 등은 공막 돌륭술 후 Stenotrophomonas maltophilia 감염이 합병된 SINS 1예를 보고했습니다. 돌륭 제거 후 공막 얇아짐과 안내 염증이 진행되어 교정 시력이 20/25에서 20/1000으로 감소했으나, 경구 스테로이드 시작 후 20/32까지 회복되었습니다 1).
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”SINS의 정확한 병태생리는 알려져 있지 않습니다. 수술로 인해 변성되거나 노출된 공막 조직 항원에 대한 지연형 과민반응(IV형 알레르기 반응)이 주요 기전으로 생각됩니다. 병리학 연구에서는 결막 생검에서 IgM 및 IgG 침착, HLA-DR 발현 증가, 보조 T 세포의 관여가 나타났습니다.
SINS와 전신 자가면역 질환 사이에는 강한 연관성이 있습니다. SINS 발병 후 검사에서 잠재적인 전신 질환이 발견되는 경우가 많습니다. 백내장 수술 후 SINS의 약 절반에서 전신 질환의 병력이 있으며, 그중 류마티스 관절염이 가장 흔했습니다3).
위험 요인
섹션 제목: “위험 요인”전신 요인
결합 조직 질환: 류마티스 관절염, 전신 홍반성 루푸스 등이 심부 공막상 정맥총의 콜라게나제 관련 혈관염을 유발합니다.
자가면역 질환: 다발혈관염 육아종증(GPA), ANCA 관련 혈관염 등.
당뇨병: 허혈성 및 염증성 환경을 조장합니다2). 당뇨병 합병 예에서는 결핵 등의 기회 감염과의 합병에도 주의가 필요합니다3).
여성: 약 70%가 여성입니다3).
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”임상 진단
병력 및 진찰: SINS는 안과 수술 병력과 수술 창에 인접한 괴사성 공막염의 존재에 기반한 임상 진단입니다.
감염 배제: 세균 배양, PCR 검사, 공막 생검을 통해 감염성 원인을 배제합니다2). 결막 긁기와 전방수의 PCR 분석이 권장됩니다.
전신 검사
자가면역 선별검사: RF, ANA, ANCA(PR3-ANCA, MPO-ANCA), CRP, HLA-B27을 평가합니다2).
감염병 선별검사: 투베르쿨린 반응 검사, IGRA(인터페론 감마 방출 검사), 흉부 X선을 시행합니다3). 특히 결핵 유행 지역에서는 결핵 배제가 중요합니다.
감별 진단
섹션 제목: “감별 진단”| 감별 질환 | SINS와의 차이점 |
|---|---|
| 감염성 공막염 | 녹농균이 가장 많음. 배양 양성. |
| 자가면역성 괴사성 공막염 | 양안성인 경우가 많음. 수술력 불필요 |
감염성 공막염에서는 녹농균이 가장 흔하며, 감염성 공막염 증례의 최대 85%를 차지합니다. 그 외에 황색포도상구균, 폐렴구균이 분리됩니다. 진균성 공막염은 가장 중증이며, 항진균제의 침투가 좋지 않아 조절이 어렵습니다.
자가면역성 괴사성 공막염은 SINS와 임상 양상이 유사하지만, 양안성인 경우가 많고 반드시 안과 수술 병력을 동반하지는 않습니다. 여러 차례의 안과 수술 병력이 있고 수술 부위에 공막염이 발생한 경우 SINS 진단이 우선됩니다.
SINS는 감염과 합병될 수도 있습니다. 공막 돌륭술 후 SINS의 97.2%에서 감염이 관여했다는 보고가 있습니다3). 익상편 수술 후 SINS에서도 71.4%에서 감염이 관련되었습니다3).
5. 표준적 치료법
섹션 제목: “5. 표준적 치료법”내과적 치료
섹션 제목: “내과적 치료”SINS 치료를 시작하기 전에 감염성 원인을 배제하는 것이 매우 중요합니다.
- 1차 선택: 고용량 경구 프레드니솔론이 급성 SINS의 표준 치료입니다. 국소 프레드니솔론 점안을 병용하기도 합니다. SINS에 대해 NSAIDs는 1차 선택으로 권장되지 않습니다.
- 중증 예: 메틸프레드니솔론 정맥 펄스 요법(1,000 mg/일×3일)을 시행합니다.
- 난치성: 아자티오프린이나 시클로포스파미드 등의 면역억제제로 전환합니다. 생물학적 제제(인플릭시맙, 리툭시맙)의 유효 예도 보고되었습니다.
- 감염 합병 예: 항균제 치료와 병행하여 스테로이드를 투여합니다. 감염이 조절되어도 SINS의 염증이 지속되는 경우, 스테로이드 전신 투여가 필수적입니다1).
- 결핵 합병 예: 항결핵 요법(이소니아지드, 리팜피신, 피라진아미드, 에탐부톨)을 시작합니다. Ruiz-Lozano 등은 익상편 수술 12년 후 발생한 결핵 합병 SINS에 대해 항결핵 요법 시작 1개월 만에 공막 괴사가 소실되었다고 보고했습니다3).
Nakagawa 등의 보고에 따르면, 공막돌륜술 후 SINS에 대해 메틸프레드니솔론 30 mg/일 경구 투여로 안내 염증이 소실되고 얇아진 공막이 결막 조직으로 덮였습니다. 교정 시력은 20/1000에서 20/32로 개선되었고, 저용량(1 mg/일)으로 2년간 안정적으로 유지되었습니다1).
외과적 치료
섹션 제목: “외과적 치료”내과적 치료에도 불구하고 공막융해가 진행되는 경우 외과적 개입이 필요합니다.
- 공막 패치 이식술: 괴사된 공막을 절제하고 공여자 공막으로 보강합니다2).
- 구조적 층판 각막 이식술: 천공된 경우 괴사 조직을 절제하고 각막 또는 각공막 패치 이식편으로 재건합니다.
- 결막판/테논낭판: 양막 이식이나 결막판 이식도 선택지입니다.
치료 시작 시점은 시력 예후에 큰 영향을 미칩니다. 발병 1개월 이내에 고용량 스테로이드를 시작한 환자는 Snellen 시력표에서 평균 1~3줄 감소에 그친 반면, 3개월 이후에 치료를 시작한 환자는 5줄 이상의 영구적인 시력 저하를 보인다고 보고되었습니다. 공막포도종이나 공막융해로 인한 구조적 파괴를 피하기 위해 감염을 배제한 후 신속하게 전신 스테로이드 요법을 시작하는 것이 중요합니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”지연형 과민반응과 면역 복합체
섹션 제목: “지연형 과민반응과 면역 복합체”SINS의 근본적인 기전은 수술로 노출된 공막 콜라겐 등의 조직 항원에 대한 IV형 과민반응(지연형 과민반응)으로 생각됩니다. 수술에 의한 외상이 촉발 요인이 되어 공막 혈관벽에 면역 복합체가 침착됩니다. 병리학적으로는 IgM 및 IgG 침착, HLA-DR 발현 증가, T 보조 세포의 침윤이 확인되었습니다.
잠재적 자가면역의 발현
섹션 제목: “잠재적 자가면역의 발현”SINS는 기존의 아임상적 자가면역 질환을 발현시키는 것으로 생각됩니다. 수술 후 SINS 발병까지 수년 이상의 잠복기가 있는 경우, 전신에서 유발된 면역 반응이 나중에 눈으로 파급되었을 가능성이 높습니다. 백내장 수술 후 SINS의 약 절반에서 전신 자가면역 질환(특히 류마티스 관절염)이 발견됩니다3).
허혈과 효소 분해
섹션 제목: “허혈과 효소 분해”마이토마이신 C와 베타선 조사는 국소 혈관 손상과 허혈을 유발합니다. 그러나 정상 공막은 원래 혈관이 부족하기 때문에 허혈만으로는 괴사의 전체 과정을 설명할 수 없습니다. 수술 조작과 상피 파괴에 따른 공막 콜라겐의 효소 분해가 주요 기전으로 제시되고 있습니다. 결합 조직 질환 환자에서는 심부 상공막 정맥총의 혈관에 작용하는 콜라게나제 관련 혈관염이 추가됩니다.
감염과의 관계
섹션 제목: “감염과의 관계”감염은 SINS의 직접적인 원인 또는 이차적 합병증으로 해석될 수 있습니다. 수술 후 혈관 손상, 조직 파괴, 상처 치유 지연이 감염의 토대를 형성합니다3). 공막 돌륭술 후에는 감염 합병률이 97.2%로 특히 높습니다3). 한편, 감염이 SINS의 면역 반응을 증폭시킬 가능성도 시사되고 있습니다.
Matsuura 등은 익상편 절제술(결막 자가 이식 + 마이토마이신 C 병용) 후 18개월에 발생한 SINS 1예를 보고했습니다. 이 증례에서는 미만성 전방 공막염에 더해 후방 공막염이 합병되었으며, 이는 익상편 수술 후 후방 공막염의 첫 보고입니다. 홍채 표면에 다수의 육아종성 침착물이 관찰되었으나 감염 및 악성 종양은 배제되었고, 면역학적 기전에 의한 안내 염증으로 결론지어졌습니다4).
7. 참고 문헌
섹션 제목: “7. 참고 문헌”- Nakagawa Y, Suzuki T, Suzuki Y. Surgically-Induced Necrotizing Scleritis After Scleral Buckling With Stenotrophomonas maltophilia Infection. Cureus. 2024;16(2):e53876.
- Vatkar V, Bhavsar D, Agrawal T, et al. Necrotizing Scleritis Post Cataract Surgery: A Diagnostic Dilemma. Cureus. 2024;16(10):e70861.
- Ruiz-Lozano RE, Rodriguez-Garcia A, Colorado-Zavala MF, Alvarez-Guzman C. Surgically induced scleral necrosis associated with concomitant tuberculosis infection: a diagnostic challenge. GMS Ophthalmol Cases. 2023;13:Doc04.
- Matsuura K, Terasaka Y. Diffuse anterior and posterior scleritis with multiple iris granular deposits following pterygium excision. Rom J Ophthalmol. 2021;65(4):399-402.
- Ruiz-Lozano RE, Rodriguez-Garcia A, et al. The clinical and pathogenic spectrum of surgically-induced scleral necrosis: A review. Surv Ophthalmol. 2021;66(4):594-611.
- Akbari MR, et al. Multifocal Surgically Induced Necrotizing Scleritis Following Strabismus Surgery: A Case Report. Strabismus. 2016;24(3):101-5.
- Amesur A, et al. Surgically induced necrotizing scleritis: clinical features and outcomes. Ocul Immunol Inflamm. 2021;29(1):137-143.
