色素上皮囊肿
部位:典型位置为瞳孔缘至虹膜后面。
外观:半透明至棕褐色光滑囊壁。由两层色素上皮分离形成。
特征:通常较小且稳定。

虹膜囊肿(iris cyst)是虹膜内或虹膜表面形成的含液囊状结构的总称。
流行病学与分类概述
虹膜囊肿主要分为原发性和继发性。原发性包括虹膜色素上皮(IPE)囊肿和基质囊肿,继发性包括外伤或手术后上皮植入性囊肿(implantation cyst)、药物诱导性囊肿等。原发性中,基质囊肿占所有虹膜囊肿的11%。3)
成人继发性囊肿多由外伤或眼内手术引起。儿童和青少年中快速增大的囊肿多为基质囊肿。后部色素上皮囊肿更常见,通常体积小、无症状,无需治疗。
家族性色素上皮囊肿
已有家族性病例报道。在一个家系中,三代8名成员出现双侧瞳孔缘IPE囊肿,证实为常染色体显性遗传模式。4) 该病与ACTA2和MYH11突变(家族性胸主动脉瘤/夹层;FTAAD)相关,建议进行心血管评估。4)
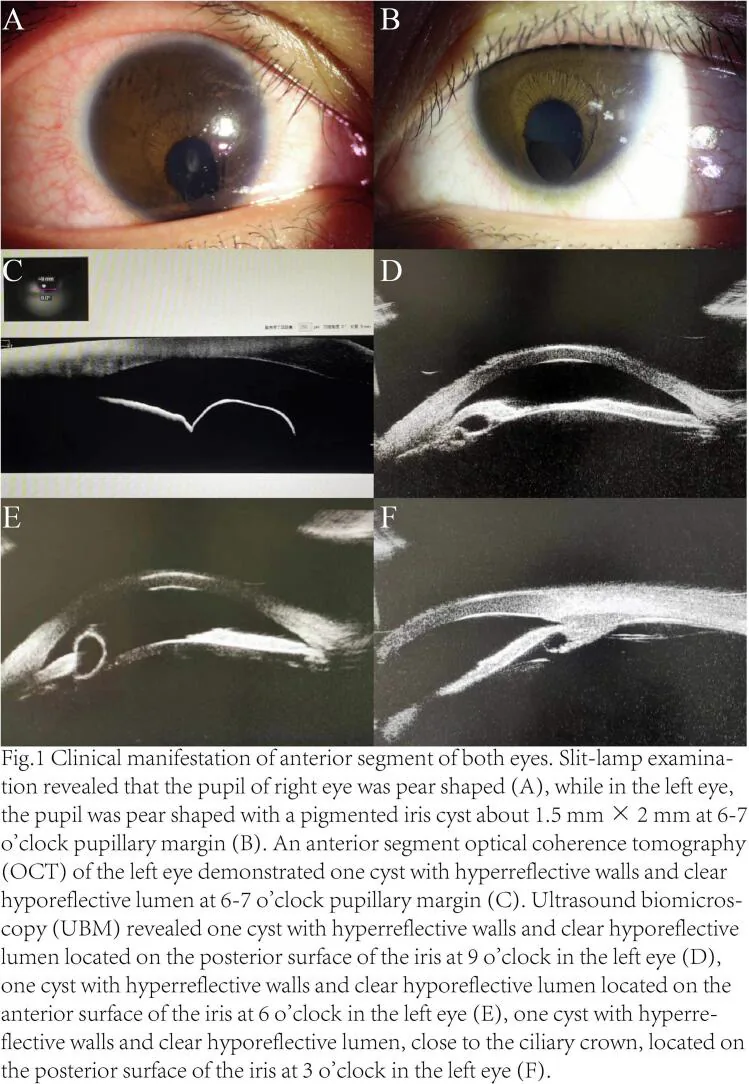
色素上皮囊肿
部位:典型位置为瞳孔缘至虹膜后面。
外观:半透明至棕褐色光滑囊壁。由两层色素上皮分离形成。
特征:通常较小且稳定。
间质囊肿
部位:虹膜实质内。
外观:内部充满透明至浑浊液体。含有来自外胚层迷入的黏液分泌细胞。
并发症:黏液性青光眼(黏液性物质导致房水流出受阻)。
继发性(上皮植入性)囊肿:外伤或手术后发生。快速增大,可能导致角膜内皮损伤和青光眼。UBM显示薄的高回声壁。2)
角膜内皮损伤:大囊肿接触并压迫角膜内皮,导致角膜水肿和内皮细胞损伤。在一例58岁男性报告中,囊肿占据前房容积的1/3,直接接触内皮,矫正视力降至0.3。1)
前房内游离:色素上皮囊肿可能游离至前房,作为前房内自由漂浮的囊肿被观察到。9)
通常原因不明。间质囊肿来源于外胚层残留。
家族性色素上皮囊肿:据报道与ACTA2、MYH11基因突变相关。询问家族史很重要。4)
标准诊断方法,最有助于与实体肿瘤鉴别。使用50MHz超声探头确认虹膜实质内薄壁、充满液体的囊腔。3)
Joshi等人(2022)报告一例先天性双侧间质囊肿(出生后1个月),UBM(50MHz)显示薄壁、无回声囊腔,有助于排除实体肿瘤。3)
还评估房角变窄、最大虹膜厚度、睫状体厚度、IPE后弯和前移。
作为UBM的辅助检查使用。显示囊壁高反射、内腔低反射的模式。9)
Ho等人报道,在游离IPE囊肿中,AS-OCT显示高反射壁和低反射腔,通过ImageJ测量的囊液光学密度与眼内液相当(21.5)。9)
评估囊肿内部血流,有助于与血管性病变(血管瘤、AVM)鉴别。2)
用于监测随时间的变化。检查有无房角关闭、色素播散和血管桥接。
通常不需要。如果检查时观察到无染料渗漏的强荧光,则与囊肿相符。
| 检查 | 主要用途 | 特点 |
|---|---|---|
| UBM | 标准诊断 | 与实体肿瘤鉴别 |
| 前节OCT | 辅助/随访 | 无创 |
| 彩色多普勒 | 血流评估 | 排除血管性病变 |
抽吸液的细胞学检查旨在排除恶性病变。在纤维蛋白组织标本中,可见无角化的复层鳞状上皮(外伤性囊肿)或立方上皮(含色素巨噬细胞)。8)
UBM可显示后极部(睫状体、房角),因此推荐作为标准检查。眼前节OCT无创、易于重复,适合随访。理想情况下应互补使用两者。
根据囊肿的类型、大小及有无并发症,逐步决定治疗方案。
| 囊肿状态 | 推荐治疗 |
|---|---|
| 小型、无症状 | 观察 |
| 中型、无视轴遮挡 | 激光/抽吸 |
| 大型、有并发症 | 手术切除 |
小型、无症状的原发性色素上皮囊肿以观察为主。即使观察10年,也常见自然消退或稳定。
Nd:YAG激光:通过穿孔囊壁使其塌陷。对小型囊肿有效,但大型囊肿复发率高。家族性IPE囊肿(3代病例)中,单次照射0.3–1.0 mJ后9个月无复发。4) 两兄妹病例中,Nd:YAG激光(1.0 mJ)维持稳定2年。10)
氩激光:有时用于基质囊肿和术后囊肿。
二极管内激光光凝术:有报告在前房内镜引导下照射196点、215 mW、50毫秒,然后用玻璃体切割器切除囊肿前壁。1)
用30G针抽吸并塌陷囊肿内容物。需要辅助治疗以防止复发。
无水乙醇灌注:注入囊腔破坏上皮的成熟方法。商业获取困难和毒性是挑战。
丝裂霉素C(MMC)注射:有报道采用三联疗法,包括抽吸、丝裂霉素C(0.0002 mg/mL,5分钟)注射、玻璃体切割器前壁切除和后壁烧灼。两个1mm切口无需虹膜切除,6个月无复发。5)
纤维蛋白胶注射(TISSEEL VH):抽吸后向囊腔内注入纤维蛋白原和稀释凝血酶(1:10)以粘合囊壁。一名61岁男性(囊肿4.20×7.56×8.22mm)视力从20/200改善至20/30,3个月无复发。6)
粘弹性物质剥离(visco-dissection)+ 囊肿切除 + 扇形虹膜切除术:用于大型囊肿和婴儿病例(出生1个月的双侧囊肿)。3)
台盼蓝染色辅助切除:27G针抽吸 → 0.06%台盼蓝注入40秒(染色可视化)→ 用镊子 + 23G玻璃体切割器切除。术后7天无复发。7)
纤维蛋白胶辅助小儿切除(miOCT引导):31G针抽吸2/3量 → 注入并硬化纤维蛋白胶(0.04 mL)→ 整块切除。两名婴幼儿(出生6个月和3个月)分别在2.5年和3个月后无复发。病理:复层非角化鳞状上皮(病例1),立方上皮伴含色素巨噬细胞(病例2)。8)
同时进行DMEK:当囊肿导致角膜内皮严重损伤时,一期进行二极管眼内激光光凝 + 玻璃体切割器切除 + DMEK移植,6个月无复发,最佳矫正视力改善至20/25。1)
单纯抽吸会残留囊肿壁的上皮细胞,导致高复发率。为预防复发,建议联合使用无水乙醇灌注、丝裂霉素C注射、纤维蛋白胶或激光烧灼等方法。
由于虹膜后部两层色素上皮(前层和后层)分离所致。分离的层间积聚液体,形成囊肿。
来源于外胚层组织迷离。内壁含有黏液分泌细胞,分泌的黏液(黏多糖)可阻塞房水流出通道,引起黏液性青光眼。
外伤或手术创口使结膜或角膜上皮细胞进入前房,增殖并增大。进展时广泛覆盖角膜内皮、虹膜和前房角,导致难治性青光眼和角膜内皮功能不全。由于植入细胞保留功能性上皮分泌能力,囊肿持续增大。
ACTA2(α-平滑肌肌动蛋白)和MYH11(平滑肌肌球蛋白重链)突变导致平滑肌功能障碍。这些在虹膜括约肌和开大肌的平滑肌组织中表达的蛋白质功能下降被认为促进囊肿形成。4)
关于瞳孔缘色素上皮囊肿(所谓的flocculi),ACTA2突变携带者到85岁时主动脉事件风险估计达到75%,强烈建议进行心血管筛查。4)
从传统手术切除向更具组织保留性的技术转变正在推进。
Duphare等人(2022)对一例大型术后间质囊肿(4.20×7.56×8.22mm)实施了纤维蛋白胶辅助抽吸术,3个月后无复发,视力20/30。纤维蛋白胶被认为是无水乙醇或硬化剂的有前景替代品。6)
Arnold等人(2022)对一例合并角膜内皮功能障碍的复发性虹膜囊肿实施了二极管激光光凝+25G玻璃体切割器切除+DMEK移植的一期手术。术后6个月无囊肿复发,矫正视力为20/25。1)
Rashid等人(2025)报告了在婴幼儿病例(出生后6个月和3个月)中应用miOCT引导的纤维蛋白胶辅助整块切除术。该新技术通过术中OCT确认囊肿内纤维蛋白胶填充的同时实现整块切除,最长随访2.5年无复发。8)
家族性色素上皮囊肿与ACTA2/MYH11基因突变之间的关联逐渐明确。4) 有专家建议对所有病例进行基因检测、心血管评估和家族筛查。未来有望建立针对基因突变携带者的系统性筛查项目。
通过前节OCT的ImageJ分析对囊肿液光学密度进行定量,可能用于评估内容液的性质(区分眼内液和黏液)。9)