Pigmentepithelzyste
Lokalisation: Typischerweise vom Pupillenrand bis zur Irisrückfläche.
Aussehen: Glatte, halbtransparente bis bräunliche Zystenwand. Entsteht durch Ablösung der beiden Pigmentepithelschichten.
Merkmale: Klein und meist stabil.

Eine Iriszyste (iris cyst) ist ein Sammelbegriff für flüssigkeitsgefüllte, zystische Strukturen innerhalb der Iris oder auf ihrer Oberfläche.
Epidemiologie und Klassifikation im Überblick
Iriszysten werden in primäre und sekundäre unterteilt. Zu den primären gehören Irispigmentepithel (IPE)-Zysten und Stromazysten, zu den sekundären gehören epitheliale Implantationszysten nach Trauma oder Operation sowie medikamenteninduzierte Zysten. Unter den primären machen Stromazysten 11 % aller Iriszysten aus. 3)
Sekundäre Zysten bei Erwachsenen sind oft auf Traumata oder intraokulare Chirurgie zurückzuführen. Bei Kindern und jungen Erwachsenen sind schnell wachsende Zysten meist Stromazysten. Zysten des hinteren Pigmentepithels sind häufiger, normalerweise klein, asymptomatisch und bedürfen keiner Behandlung.
Familiäre Pigmentepithelzyste
Es wurden familiäre Fälle berichtet. In einer Familie zeigten 8 Mitglieder über drei Generationen bilaterale IPE-Zysten am Pupillenrand, mit einem bestätigten autosomal-dominanten Vererbungsmuster. 4) Diese Erkrankung wird mit ACTA2- und MYH11-Mutationen (familiäres thorakales Aortenaneurysma und -dissektion; FTAAD) in Verbindung gebracht, und eine kardiovaskuläre Beurteilung wird empfohlen. 4)
Iriszysten sind fast immer gutartige Läsionen. Allerdings kann eine Abgrenzung zum Iris-Melanom oder soliden Tumoren erforderlich sein, wobei UBM oder Vorderabschnitts-OCT die innere Struktur bestätigen. Fehlen tumorverdächtige Merkmale (solide Anteile, Pigmentierung, abnorme Gefäße), werden die meisten lediglich beobachtet.
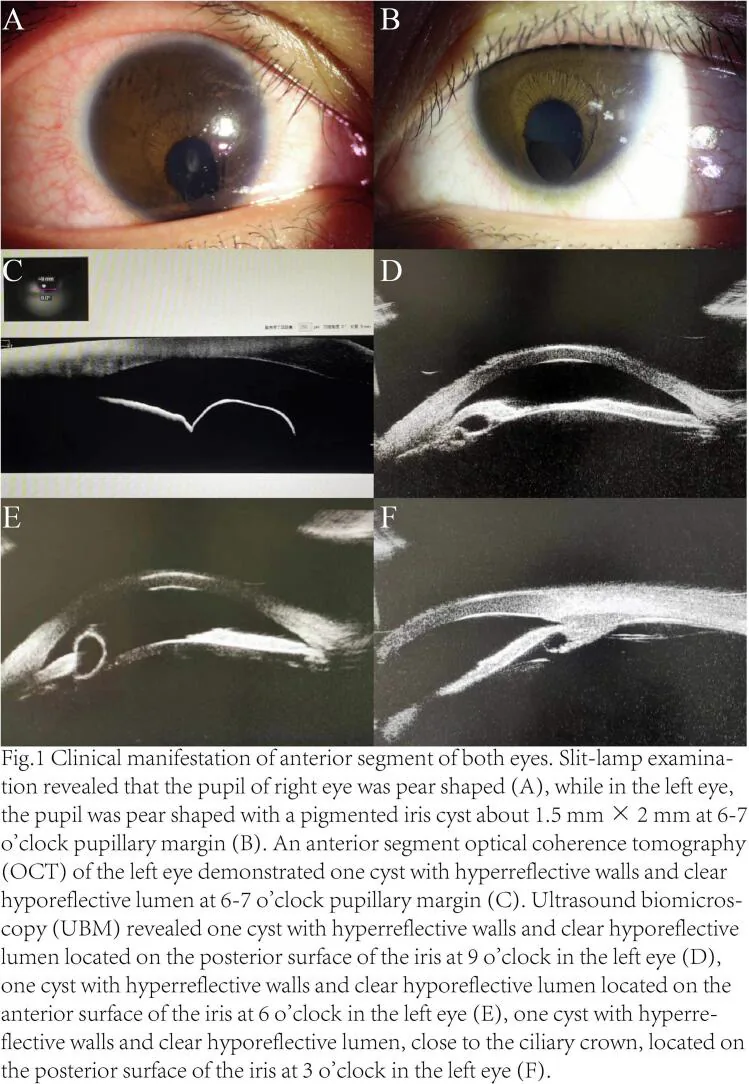
Pigmentepithelzyste
Lokalisation: Typischerweise vom Pupillenrand bis zur Irisrückfläche.
Aussehen: Glatte, halbtransparente bis bräunliche Zystenwand. Entsteht durch Ablösung der beiden Pigmentepithelschichten.
Merkmale: Klein und meist stabil.
Stromazyste
Lokalisation: Im Irisstroma.
Aussehen: Gefüllt mit klarer bis trüber Flüssigkeit. Entsteht aus ektodermaler Fehlbildung, enthält muzinproduzierende Zellen.
Komplikationen: Muzogenes Glaukom (Abflussbehinderung des Kammerwassers durch muzinöses Material).
Sekundäre (Epithelimplantations-) Zysten: Treten nach Trauma oder Operation auf. Rasche Größenzunahme, können Hornhautendothelschädigung und Glaukom verursachen. Im UBM dünne, echoreiche Wand. 2)
Hornhautendothelschädigung : Große Zysten, die das Hornhautendothel berühren und komprimieren, verursachen ein Hornhautödem und Endothelzellschäden. In einem Bericht über einen 58-jährigen Mann nahm die Zyste ein Drittel des Vorderkammervolumens ein und stand in direktem Kontakt mit dem Endothel, wodurch der korrigierte Visus auf 0,3 abfiel. 1)
Freisetzung in die Vorderkammer: Eine Pigmentepithelzyste kann in die Vorderkammer freigesetzt werden und als frei flottierende Zyste beobachtet werden. 9)
Die Spaltlampenuntersuchung bestätigt die Transparenz und glatte Oberfläche der Zyste, während UBM und Vorderabschnitts-OCT die innere Flüssigkeitskomponente bestätigen. Pigmentierung, feste Bestandteile, abnormale Gefäßneubildung und schnelles Wachstum sind verdächtige Anzeichen für Malignität. Die Beurteilung des inneren Blutflusses mittels hochfrequentem Farbdoppler hilft bei der Differenzialdiagnose.
Oft unbekannter Ursache. Stromazysten entstehen aus ektodermalen Resten.
Familiäre pigmentierte Epithelzyste: Es wurden Assoziationen mit ACTA2- und MYH11-Genmutationen berichtet. Die Erhebung der Familienanamnese ist wichtig. 4)
Standarddiagnoseverfahren, am nützlichsten zur Abgrenzung von soliden Tumoren. Eine 50-MHz-Ultraschallsonde bestätigt die dünne Wand und die Flüssigkeitsfüllung des Hohlraums im Irisstroma. 3)
Joshi et al. (2022) berichteten, dass die UBM (50 MHz) bei einer angeborenen bilateralen Stromazyste (1 Monat alt) eine dünnwandige, hell erscheinende Zyste darstellte und zum Ausschluss eines soliden Tumors nützlich war. 3)
Beurteilen Sie auch die Kammerwinkelabflachung, die maximale Irisdicke, die Ziliarkörperdicke, die hintere Krümmung des Irispigmentepithels und die anteriore Verlagerung.
Wird als ergänzende Untersuchung zur UBM eingesetzt. Es zeigt ein Muster mit hoher Reflexion der Zystenwand und niedriger Reflexion des Lumens. 9)
Ho et al. berichteten, dass die AS-OCT bei freien IPE-Zysten eine hyperreflektive Wand und ein hyporeflektives Lumen zeigte und die mit ImageJ gemessene optische Dichte der Zystenflüssigkeit der intraokularen Flüssigkeit (21,5) entsprach. 9)
Bewertet den Blutfluss im Inneren der Zyste und ist nützlich zur Unterscheidung von vaskulären Läsionen (Hämangiom, AVM). 2)
Wird zur Überwachung von Veränderungen im Laufe der Zeit verwendet. Überprüft auf Vorhandensein von Winkelblock, Pigmentdispersion und vaskulären Brücken.
In der Regel nicht erforderlich. Wenn während der Untersuchung eine Hyperfluoreszenz ohne Farbstoffleckage festgestellt wird, entspricht dies einer Zyste.
| Untersuchung | Hauptanwendung | Merkmale |
|---|---|---|
| UBM | Standarddiagnostik | Abgrenzung zu soliden Tumoren |
| Vorderabschnitts-OCT | Hilfs- und Verlaufskontrolle | Nicht-invasiv |
| Farbdoppler | Blutflussbeurteilung | Ausschluss vaskulärer Läsionen |
Die Zytologie der Aspirationsflüssigkeit dient dem Ausschluss maligner Befunde. In Fibrinproben werden nicht verhornendes mehrschichtiges Plattenepithel (traumatische Zyste) oder kubisches Epithel (pigmenthaltige Makrophagen) nachgewiesen. 8)
UBM kann den hinteren Pol (Ziliarkörper, Kammerwinkel) darstellen und wird daher als Standarduntersuchung empfohlen. Die Vorderabschnitts-OCT ist nicht-invasiv, leicht wiederholbar und für die Verlaufskontrolle geeignet. Idealerweise werden beide ergänzend eingesetzt.
Die Behandlungsauswahl erfolgt stufenweise basierend auf Art, Größe und Vorhandensein von Komplikationen der Zyste.
| Zustand der Zyste | Empfohlene Behandlung |
|---|---|
| Klein, asymptomatisch | Beobachtung |
| Mittelgroß, ohne Visusachsenblockade | Laser/Aspiration |
| Groß, mit Komplikationen | Chirurgische Exzision |
Kleine, asymptomatische primäre Pigmentepithelzysten werden in der Regel beobachtet. Selbst nach 10 Jahren Beobachtung kommt es häufig zu spontaner Rückbildung oder Stabilität.
Nd:YAG-Laser : Ziel ist die Perforation der Zystenwand zur Entleerung. Wirksam bei kleinen Zysten, aber hohe Rezidivrate bei großen. Bei familiären IPE-Zysten (3 Generationen) führte eine Einzelpulsbestrahlung mit 0,3–1,0 mJ zu einer 9-monatigen Rezidivfreiheit. 4) Bei zwei Geschwistern wurde nach Nd:YAG-Laser (1,0 mJ) eine 2-jährige Stabilität festgestellt. 10)
Argon-Laser : Wird gelegentlich bei Stroma- und postoperativen Zysten eingesetzt.
Dioden-Endolaser-Photokoagulation : Unter vorderer Segmentendoskopie wurden 196 Spots, 215 mW, 50 ms appliziert, gefolgt von einer Exzision der Zystenvorderwand mit einem Vitrektom. 1)
Den Zysteninhalt mit einer 30G-Nadel aspirieren und kollabieren lassen. Zur Rezidivprophylaxe ist eine adjuvante Therapie erforderlich.
Absolute-Ethanol-Perfusion : etablierte Methode zur Zerstörung des Epithels durch Injektion in die Zystenhöhle. Herausforderungen sind die schwierige kommerzielle Verfügbarkeit und Toxizität.
Mitomycin-C (MMC)-Injektion: Es gibt einen Bericht über eine Dreifachtherapie: Aspiration → Mitomycin-C-Injektion (0,0002 mg/mL, 5 Minuten) → Resektion der Vorderwand mit dem Vitrektom → Koagulation der Hinterwand. Zwei 1 mm breite Inzisionen ohne Iridektomie, nach 6 Monaten kein Rezidiv. 5)
Fibrinkleber-Injektion (TISSEEL VH) : Nach Aspiration werden Fibrinogen und verdünntes Thrombin (1:10) in die Zystenhöhle injiziert, um die Zystenwand zu verkleben. Bei einem 61-jährigen Mann (4,20×7,56×8,22 mm Zyste) verbesserte sich die Sehkraft von 20/200 auf 20/30, nach 3 Monaten kein Rezidiv. 6)
Viskoelastische Dissektion (Visko-Dissektion) + Zystektomie + fächerförmige Iridektomie: Angewendet bei großen Zysten und Säuglingsfällen (bilaterale Zysten im Alter von 1 Monat). 3)
Trypanblau-gefärbte Resektion: 27G-Nadelaspiration → 0,06% Trypanblau-Injektion für 40 Sekunden (Färbungsvisualisierung) → Resektion mit Pinzette und 23G-Vitrektom. Kein Rezidiv nach 7 Tagen postoperativ. 7)
Fibrinkleber-unterstützte pädiatrische Resektion (miOCT-gesteuert) : Aspiration von 2/3 des Volumens mit 31G-Nadel → Injektion von Fibrinkleber (0,04 mL) und Aushärtung → En-bloc-Resektion. Zwei Säuglinge (6 Monate und 3 Monate alt) nach 2,5 Jahren bzw. 3 Monaten rezidivfrei. Pathologie: mehrschichtiges nicht verhornendes Plattenepithel (Fall 1), kubisches Epithel + pigmenthaltige Makrophagen (Fall 2). 8)
Gleichzeitige DMEK : Bei fortschreitender Hornhautendothelschädigung durch eine Zyste wurde eine einzeitige Dioden-Endolaser-Photokoagulation + Vitrektomiekopf-Resektion + DMEK-Transplantation durchgeführt, mit einem berichteten rezidivfreien Verlauf nach 6 Monaten und Verbesserung des BCVA auf 20/25. 1)
Die alleinige Aspiration hinterlässt Epithelzellen der Zystenwand, was zu einer hohen Rezidivrate führt. Zur Rezidivprophylaxe wird die Kombination von wasserfreier Ethanolspülung, Mitomycin-C-Injektion, Fibrinkleber oder Laserkoagulation empfohlen.
Sie entsteht durch die Dissoziation der beiden Schichten des Pigmentepithels (vordere und hintere Schicht) im hinteren Teil der Iris. Zwischen den dissoziierten Schichten sammelt sich Flüssigkeit an und bildet eine Zyste.
Sie geht von einem ektodermalen Rest (ektodermaler Rest) aus. Die Innenwand enthält schleimproduzierende Zellen, und der abgesonderte Schleim (Mukopolysaccharid) kann den Abflussweg des Kammerwassers verstopfen und ein mukogenes Glaukom verursachen.
Durch ein Trauma oder eine chirurgische Wunde gelangen Bindehaut- oder Hornhautepithelzellen in die Vorderkammer, proliferieren und vergrößern sich. Im fortgeschrittenen Stadium bedecken sie ausgedehnt das Hornhautendothel, die Iris und den Kammerwinkel, was zu einem refraktären Glaukom und Hornhautendothelversagen führt. Da die implantierten Zellen funktionell eine epitheliale Sekretionsfähigkeit behalten, wächst die Zyste kontinuierlich weiter.
ACTA2 (α-glattmuskelaktin)- und MYH11 (Glattmuskelmyosin-Schwerkette)-Mutationen verursachen eine Funktionsstörung der glatten Muskulatur. Eine verminderte Funktion dieser Proteine, die im glatten Muskelgewebe des Irissphinkters und des Pupillendilatators exprimiert werden, wird als förderlich für die Zystenbildung angesehen. 4)
Im Zusammenhang mit den Pigmentepithelzysten des Pupillenrandes (sogenannte Flocculi) wird das Risiko eines Aortenereignisses bei ACTA2-Mutationsträgern bis zum Alter von 85 Jahren auf schätzungsweise 75 % geschätzt, weshalb ein kardiovaskuläres Screening dringend empfohlen wird. 4)
Es findet ein Wandel von der traditionellen chirurgischen Resektion hin zu gewebeschonenderen Techniken statt.
Duphare et al. (2022) führten eine Fibrinkleber-unterstützte Aspiration bei einer großen postoperativen Stromazyste (4,20 × 7,56 × 8,22 mm) durch und berichteten nach 3 Monaten über kein Rezidiv und einen Visus von 20/30. Fibrinkleber gilt als vielversprechende Alternative zu absolutem Ethanol oder Sklerosierungsmitteln. 6)
Arnold et al. (2022) führten eine einzeitige Operation mit Dioden-Endolaser-Photokoagulation, 25G-Vitrektom-Resektion und DMEK-Transplantation bei einem rezidivierenden Iriszyste mit Hornhautendothelschädigung durch. 6 Monate postoperativ zeigte sich kein Zystenrezidiv und der korrigierte Visus betrug 20/25. 1)
Rashid et al. (2025) berichteten über eine miOCT-gesteuerte Fibrinkleber-unterstützte En-bloc-Resektion bei Säuglingen (6 und 3 Monate alt). Diese neue Technik ermöglicht eine En-bloc-Resektion unter Bestätigung der Fibrinkleberfüllung in der Zyste mittels intraoperativem OCT, mit rezidivfreiem Verlauf bis zu 2,5 Jahren. 8)
Der Zusammenhang zwischen familiären Pigmentepithelzysten und ACTA2/MYH11-Genmutationen wird zunehmend deutlicher. 4) Einige Experten empfehlen Gentests, kardiovaskuläre Beurteilung und Familien-Screening für alle Fälle. Zukünftig wird die Etablierung systematischer Screening-Programme für Genträger erwartet.
Die Quantifizierung der optischen Dichte von Zystenflüssigkeit mittels ImageJ-Analyse des Vorderabschnitts-OCT könnte zur Beurteilung der Flüssigkeitseigenschaften (Unterscheidung von Intraokularflüssigkeit und Schleim) eingesetzt werden. 9)