كيسة الظهارة الصبغية
الموقع: نموذجيًا من حافة الحدقة إلى السطح الخلفي للقزحية.
المظهر: جدار كيسي أملس شفاف إلى بني اللون. يحدث نتيجة انفصال طبقتين من الظهارة الصبغية.
السمة: صغيرة وغالبًا ما تكون مستقرة.

كيس القزحية (iris cyst) هو مصطلح عام لتكوين كيسي يحتوي على سائل ينشأ داخل القزحية أو على سطحها.
ملخص علم الأوبئة والتصنيف
تنقسم أكياس القزحية إلى أولية وثانوية. تشمل الأولية أكياس الظهارة الصباغية للقزحية (IPE) وأكياس السدى، بينما تشمل الثانوية أكياس الانغراس الظهاري بعد الصدمة أو الجراحة (implantation cyst) والأكياس الناتجة عن الأدوية. من بين الأولية، تشكل أكياس السدى 11% من جميع أكياس القزحية. 3)
غالبًا ما تنتج الأكياس الثانوية لدى البالغين عن الصدمات أو الجراحة داخل العين. الأكياس التي تنمو بسرعة لدى الأطفال والشباب تكون في الغالب أكياس خلالية. الأكياس الظهارية الصبغية الخلفية أكثر شيوعًا، وعادة ما تكون صغيرة الحجم ولا تسبب أعراضًا ولا تحتاج إلى علاج.
كيسة ظهارية صبغية عائلية
تم الإبلاغ عن حالات عائلية. في إحدى العائلات، ظهرت أكياس IPE حدقية ثنائية لدى 8 أفراد عبر 3 أجيال، وتم تأكيد نمط الوراثة الجسدية السائدة. 4) وقد تم ربط هذا المرض بطفرات ACTA2 وMYH11 (تمدد الأوعية الدموية الصدري العائلي والتسلخ؛ FTAAD)، ويوصى بتقييم القلب والأوعية الدموية الكبيرة. 4)
أكياس القزحية هي آفات حميدة في جميع الحالات تقريبًا. ومع ذلك، قد يكون من الضروري التمييز بينها وبين الورم الميلانيني في القزحية أو الكتل الصلبة، ويتم تأكيد البنية الداخلية باستخدام الموجات فوق الصوتية الحيوية (UBM) أو التصوير المقطعي للجزء الأمامي (OCT). إذا لم تكن هناك سمات مشبوهة للورم (مكون صلب، تصبغ، أوعية دموية غير طبيعية)، فغالبًا ما تتم متابعتها بالمراقبة.
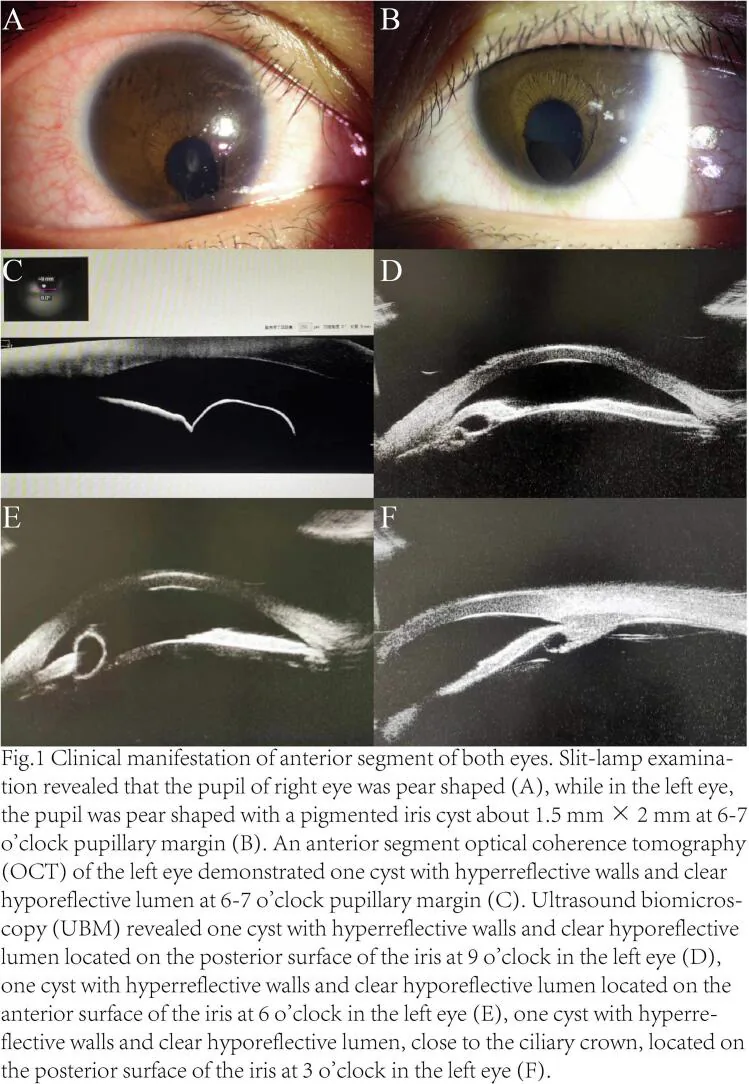
كيسة الظهارة الصبغية
الموقع: نموذجيًا من حافة الحدقة إلى السطح الخلفي للقزحية.
المظهر: جدار كيسي أملس شفاف إلى بني اللون. يحدث نتيجة انفصال طبقتين من الظهارة الصبغية.
السمة: صغيرة وغالبًا ما تكون مستقرة.
كيسة خلالية
الموقع: داخل سدى القزحية.
المظهر: مليئة بسائل شفاف إلى عكر. تحتوي على خلايا منتجة للمخاط ناشئة من انتباذ الأديم الظاهر.
المضاعفات: الزرق المخاطي (انسداد تدفق الخلط المائي بسبب المادة المخاطية).
الكيسة الثانوية (زرع الظهارة): تحدث بعد الصدمة أو الجراحة. تنمو بسرعة، وقد تسبب تلفًا في بطانة القرنية والزرق. يُكشف جدار رقيق عالي الصدى باستخدام التصوير بالموجات فوق الصوتية (UBM). 2)
اضطراب بطانة القرنية: يؤدي ملامسة الكيس الكبير وضغطه على سطح بطانة القرنية إلى وذمة القرنية وتلف الخلايا البطانية. في تقرير عن رجل يبلغ من العمر 58 عامًا، كان الكيس يشغل ثلث حجم الغرفة الأمامية ويلامس البطانة مباشرة، مما أدى إلى انخفاض حدة البصر المصححة إلى 0.3. 1)
الانفصال داخل الغرفة الأمامية: قد ينفصل كيس الظهارة الصبغية داخل الغرفة الأمامية ويُلاحظ ككيس عائم حر داخل الغرفة الأمامية. 9)
يكشف فحص المصباح الشقي عن شفافية الكيس وسطحه الأملس، ويؤكد التصوير بالموجات فوق الصوتية (UBM) أو التصوير المقطعي للقطعة الأمامية (OCT) وجود مكون سائل داخلي. التصبغ، المكونات الصلبة، الأوعية الدموية غير الطبيعية، والنمو السريع هي علامات تشير إلى الورم الخبيث. يساعد تقييم تدفق الدم الداخلي باستخدام الدوبلر الملون عالي التردد في التشخيص التفريقي.
غالبًا ما يكون السبب غير معروف. تنشأ الأكياس الخلالية من بقايا الأديم الظاهر (ectodermal rest).
الكيس الظهاري الصبغي العائلي: تم الإبلاغ عن ارتباطه بطفرات جينات ACTA2 وMYH11. من المهم أخذ التاريخ العائلي. 4)
طريقة التشخيص القياسية، وهي الأكثر فائدة في التمييز بين الكتل الصلبة. باستخدام مسبار الموجات فوق الصوتية بتردد 50 ميجاهرتز، يتم التأكد من وجود جدران رقيقة وتجويف مملوء بالسوائل داخل سدى القزحية. 3)
أفاد جوشي وآخرون (2022) أن الموجات فوق الصوتية عالية التردد (UBM بتردد 50 ميجاهرتز) في حالة كيس خلقي ثنائي بين الخلالي (عمر شهر واحد) أظهرت كيسًا رقيق الجدار ومشرق التجويف، وكانت مفيدة في استبعاد الورم الصلب. 3)
يتم أيضًا تقييم انسداد الزاوية، وأقصى سمك للقزحية، وسمك الجسم الهدبي، وانحناء الظهارة الصباغية للقزحية، والإزاحة الأمامية.
يُستخدم كفحص مساعد لـ UBM. يُظهر نمط انعكاس عالي لجدار الكيس وانعكاس منخفض للتجويف الداخلي. 9)
ذكر Ho وزملاؤه أن AS-OCT أظهر جدارًا عالي الانعكاس وتجويفًا منخفض الانعكاس في كيسات IPE الحرة، وأن الكثافة البصرية لسائل الكيس المقاسة بواسطة ImageJ كانت مماثلة للسائل داخل العين (21.5). 9)
تقييم تدفق الدم داخل الكيس، مفيد للتمييز بين الآفات الوعائية (ورم وعائي، تشوه شرياني وريدي). 2)
تُستخدم لمراقبة التغيرات بمرور الوقت. يتم التحقق من وجود انسداد الزاوية، انتشار الصبغة، أو جسور الأوعية الدموية.
عادةً لا يكون ضروريًا. إذا تم الكشف عن فرط التألق دون تسرب الصبغة أثناء الإجراء، فإنه يتوافق مع الكيس.
| الفحص | الاستخدام الرئيسي | الخصائص |
|---|---|---|
| UBM | التشخيص القياسي | التفريق بين الورم الصلب |
| التصوير المقطعي للجزء الأمامي | المساعدة والمتابعة | غير جراحي |
| دوبلر ملون | تقييم تدفق الدم | استبعاد الآفات الوعائية |
يهدف الفحص الخلوي للسائل المستنشق إلى استبعاد الأورام الخبيثة. في عينات النسيج الليفي، يتم ملاحظة ظهارة حرشفية طبقية غير متقرنة (كيسة رضحية) أو ظهارة مكعبة (بلاعم محتوية على صبغة). 8)
يوصى باستخدام التصوير بالموجات فوق الصوتية (UBM) كفحص قياسي لأنه يمكنه تصوير الجزء الخلفي (الجسم الهدبي والزاوية). التصوير المقطعي للجزء الأمامي من العين (OCT) غير جراحي وسهل التكرار ومناسب للمتابعة. من المثالي استخدامهما بشكل تكميلي.
يتم تحديد خيارات العلاج بشكل تدريجي بناءً على نوع الكيس وحجمه ووجود مضاعفات.
| حالة الكيس | العلاج الموصى به |
|---|---|
| صغير الحجم، بدون أعراض | مراقبة |
| متوسط الحجم، لا يعيق المحور البصري | ليزر/شفط |
| كبير الحجم، مع مضاعفات | استئصال جراحي |
المراقبة هي الأساس للكيسات الظهارية الصبغية الأولية الصغيرة وغير المصحوبة بأعراض. حتى في حالات المراقبة لمدة 10 سنوات، يكون التراجع التلقائي والاستقرار شائعين.
ليزر Nd:YAG: يهدف إلى إحداث انهيار الكيس عن طريق ثقب جداره. فعال في الأكياس الصغيرة، لكن معدل التكرار مرتفع في الأكياس الكبيرة. في أكياس IPE العائلية (3 أجيال)، لم يحدث تكرار لمدة 9 أشهر بعد جرعة واحدة من 0.3-1.0 مللي جول. 4) في حالتين لأخوين، تم تأكيد الاستقرار لمدة عامين باستخدام ليزر Nd:YAG (1.0 مللي جول). 10)
ليزر الأرجون: يُستخدم أحيانًا للأكياس الخلالية والأكياس بعد الجراحة.
التخثير الضوئي بالليزر الثنائي الطرفي: تم الإبلاغ عن حالة تم فيها استخدام 196 بقعة، 215 ملي واط، 50 مللي ثانية تحت تنظير الجزء الأمامي، ثم استئصال الجدار الأمامي للكيس باستخدام قاطع الزجاجي. 1)
يتم شفط محتويات الكيس وتفريغه بإبرة 30G. لمنع التكرار، هناك حاجة إلى علاج مساعد.
تروية الإيثانول اللامائي: طريقة مثبتة لحقنه في تجويف الكيس لتدمير الظهارة. التحديات تشمل صعوبة الحصول عليه تجاريًا والسمية.
حقن الميتوميسين C (MMC): تم الإبلاغ عن علاج ثلاثي يجمع بين الشفط، حقن الميتوميسين C (0.0002 ملغم/مل، 5 دقائق)، استئصال الجدار الأمامي باستخدام قاطع الزجاجي، وكي الجدار الخلفي. شقان بعرض 1 مم بدون الحاجة لاستئصال القزحية، ولا تكرار بعد 6 أشهر. 5)
حقن غراء الفيبرين (TISSEEL VH): بعد الشفط، يتم حقن الفيبرينوجين والثرومبين المخفف (1:10) في تجويف الكيس لإلصاق جدار الكيس. رجل يبلغ من العمر 61 عامًا (كيس 4.20×7.56×8.22 مم) تحسنت الرؤية من 20/200 إلى 20/30، ولا تكرار بعد 3 أشهر. 6)
تسليح المادة اللزجة (visco-dissection) + استئصال الكيس + استئصال القزحية المروحي: استُخدم في الأكياس الكبيرة وحالات الرضع (كيس ثنائي الجانب بعمر شهر واحد). 3)
الاستئصال بمساعدة صبغة التريبان الأزرق: شفط بإبرة 27G → حقن 0.06% تريبان أزرق لمدة 40 ثانية (تصوير الصبغة) → استئصال بالملقط وقاطع الزجاجي 23G. لا تكرار بعد 7 أيام من الجراحة. 7)
استئصال الأطفال بمساعدة الفيبرين غراء (تحت توجيه miOCT): شفط 2/3 الحجم بإبرة 31G → حقن غراء الفيبرين (0.04 مل) وتصلبه → استئصال الكتلة الواحدة (en bloc). حالتان لرضيعين (عمر 6 أشهر و3 أشهر) دون انتكاس بعد 2.5 سنة و3 أشهر. علم الأمراض: ظهارة حرشفية غير متقرنة (حالة 1)، ظهارة مكعبة مع بلاعم تحتوي على صبغة (حالة 2). 8)
إجراء DMEK المتزامن: في حالة تقدم تلف القرنية الناتج عن الكيس، تم إجراء تخثير ضوئي بالليزر ديود + استئصال بالقطع الزجاجي + زرع DMEK في مرحلة واحدة، مع تقارير تشير إلى عدم وجود انتكاس لمدة 6 أشهر وتحسن حدة البصر المصححة إلى 20/25. 1)
بما أن الشفط وحده يترك خلايا ظهارية في جدار الكيس، فإنه يؤدي إلى تكرار حدوث الكيس بنسبة عالية. للوقاية من التكرار، يُوصى بدمج تقنيات مثل الري بالإيثانول اللامائي، وحقن الميتوميسين C، والفيبرين غراء، والكي بالليزر.
تحدث بسبب انفصال الطبقتين الظهاريتين الصبغيتين (الأمامية والخلفية) في الجزء الخلفي من القزحية. يتراكم السائل بين الطبقتين المنفصلتين مكونًا كيسًا.
ينشأ من بقايا نسيج الأديم الظاهر (ectodermal rest). يحتوي الجدار الداخلي على خلايا منتجة للمخاط، وقد يؤدي المخاط المفرز (mucopolysaccharide) إلى انسداد مسار تدفق الخلط المائي مسببًا الجلوكوما المخاطية (mucogenic glaucoma).
تتسلل خلايا ظهارة الملتحمة والقرنية إلى الحجرة الأمامية من خلال جرح خارجي أو جراحي، ثم تتكاثر وتنمو. مع تقدم الحالة، تغطي هذه الخلايا بطانة القرنية والقزحية والزاوية على نطاق واسع، مما يؤدي إلى الجلوكوما المقاومة للعلاج وفشل بطانة القرنية. نظرًا لأن الخلايا المتسللة تحتفظ بقدرة إفرازية ظهارية وظيفية، يستمر الكيس في النمو.
تؤدي طفرات ACTA2 (أكتين العضلات الملساء ألفا) و MYH11 (سلسلة الميوزين الثقيلة للعضلات الملساء) إلى خلل في وظيفة العضلات الملساء. يُعتقد أن انخفاض وظيفة هذه البروتينات المعبر عنها في الأنسجة العضلية الملساء للعضلة العاصرة للقزحية والعضلة الموسعة يعزز تكوين الكيس. 4)
فيما يتعلق بالكيسات الظهارية الصبغية لحافة الحدقة (ما يسمى flocculi)، يُقدر أن خطر الأحداث الأبهري يصل إلى 75% بحلول سن 85 لدى حاملي طفرة ACTA2، ويوصى بشدة بإجراء فحص القلب والأوعية الدموية. 4)
هناك تحول من الاستئصال الجراحي التقليدي نحو تقنيات أكثر حفظًا للأنسجة.
أجرى Duphare وآخرون (2022) شفطًا بمساعدة غراء الفيبرين لكيس خلالي كبير بعد الجراحة (4.20×7.56×8.22 مم)، وأبلغوا عن عدم وجود تكرار بعد 3 أشهر ورؤية 20/30. يُعتبر غراء الفيبرين بديلاً واعدًا للإيثانول اللامائي أو عوامل التصلب. 6)
أجرى Arnold وآخرون (2022) جراحة في مرحلة واحدة لكيس القزحية المتكرر المصحوب باضطراب بطانة القرنية، باستخدام التخثير الضوئي بالليزر الثنائي الطرفي + استئصال باستخدام قاطع زجاجي 25G + زرع DMEK. بعد 6 أشهر من الجراحة، لم يحدث تكرار للكيس، وكانت حدة البصر المصححة 20/25. 1)
أبلغ Rashid وآخرون (2025) عن استئصال كتلي بمساعدة غراء الفيبرين الموجه بـ miOCT في حالات الرضع (عمر 6 أشهر و3 أشهر). تسمح هذه التقنية الجديدة بالاستئصال الكتلي مع التأكد من ملء غراء الفيبرين داخل الكيس باستخدام OCT أثناء الجراحة، ولم يلاحظ أي تكرار لمدة تصل إلى 2.5 سنة. 8)
تتضح العلاقة بين كيسات الظهارة الصباغية العائلية وطفرات جينات ACTA2/MYH11. 4) هناك آراء خبراء توصي بإجراء الفحص الجيني وتقييم القلب والأوعية الدموية الكبرى وفحص الأسرة لجميع الحالات. في المستقبل، من المتوقع إنشاء برامج فحص منهجية لحاملي الطفرات الجينية.
تشير الدراسات إلى إمكانية تطبيق القياس الكمي للكثافة البصرية لسائل الكيس باستخدام تحليل ImageJ للتصوير المقطعي التوافقي البصري للجزء الأمامي في تقييم خصائص السائل (التمييز بين السائل داخل العين والمخاط). 9)