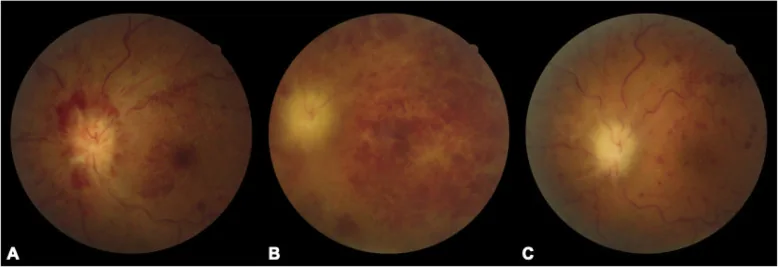
โรคซาร์คอยโดซิส ทางระบบประสาท (NS) เป็นโรคอักเสบชนิดแกรนูโลมาของระบบประสาทส่วนกลางและส่วนปลาย ซึ่งเกิดขึ้นในผู้ป่วยซาร์คอยโดซิส 5-15%
ในประมาณ 70% ของกรณี อาการทางระบบประสาทเป็นอาการแรกของโรค และมักไม่มีการวินิจฉัยซาร์คอยโดซิส ทั้งระบบมาก่อน
อาการมีความหลากหลาย รวมถึงอัมพาตของเส้นประสาทสมอง (ที่พบบ่อยที่สุดคือเส้นประสาทเฟเชียล), ม่านตาอักเสบ , เยื่อหุ้มสมองอักเสบ, ความผิดปกติของไขสันหลัง, และภาวะต่อมใต้สมองทำงานน้อย
การวินิจฉัยที่แน่นอนต้องอาศัยการยืนยันเนื้อเยื่อของแกรนูโลมาแบบไม่เป็นก้อนเนื้อตาย แต่เนื่องจากหลายกรณีวินิจฉัยได้ยาก จึงใช้การวินิจฉัยแบบเป็นขั้นตอนตามเกณฑ์ Zajicek
การรักษาทางเลือกแรกคือคอร์ติโคสเตียรอยด์ ทั้งระบบ และในกรณีที่ดื้อต่อการรักษาให้เพิ่ม methotrexate หรือ TNF inhibitor
ในญี่ปุ่น ซาร์คอยโดซิส เป็นสาเหตุอันดับหนึ่งของม่านตาอักเสบ และการตรวจตาได้รับการประเมินตามเกณฑ์ IWOS
การวินิจฉัยตั้งแต่เนิ่นๆ และการรักษาที่เหมาะสมสามารถควบคุมโรคได้ ในขณะที่การวินิจฉัยที่ล่าช้าหรือการดื้อต่อการรักษาอาจทำให้เกิดความบกพร่องทางระบบประสาทอย่างรุนแรง
ซาร์คอยโดซิส เป็นโรคอักเสบเรื้อรังที่ไม่ทราบสาเหตุ มีลักษณะเฉพาะคือแกรนูโลมาแบบไม่เป็นก้อนเนื้อตาย ปอด ผิวหนัง และตาเป็นอวัยวะที่พบบ่อย แต่เมื่อเกิดกับระบบประสาทส่วนกลาง (CNS) และ/หรือระบบประสาทส่วนปลาย (PNS) จะเรียกว่า ซาร์คอยโดซิส ทางระบบประสาท (Neurosarcoidosis ; NS)ซาร์คอยโดซิส ของอวัยวะอื่นหรือเกิดเฉพาะระบบประสาทเท่านั้น
อัตราการเกิดโรค : ในสหรัฐอเมริกา 11 ต่อ 100,000 คนในคนผิวขาว และ 35.5-36 ต่อ 100,000 คนในชาวแอฟริกันอเมริกันความชุก : ประมาณ 152-215 ต่อ 100,000 คนอายุที่พบบ่อย : 30-50 ปี พบมากในผู้หญิงแอฟริกันอเมริกันความถี่ของการมีพยาธิสภาพทางระบบประสาท : พบในผู้ป่วยซาร์คอยโดซิส 5-15%4) 7) ในการชันสูตรพลิกศพพบหลักฐานสูงถึง 25% แสดงว่าอาจมีกรณีแฝงอยู่การเริ่มต้นด้วยอาการทางระบบประสาท : ประมาณ 70% ของกรณี อาการทางระบบประสาทเป็นอาการเริ่มแรก และมักไม่มีการวินิจฉัยทางระบบมาก่อน3)
ในประเทศญี่ปุ่น ซาร์คอยโดซิส พบได้ค่อนข้างบ่อย และเป็นสาเหตุอันดับหนึ่งของโรคม่านตาอักเสบ ในเพศชายมักพบในช่วงอายุ 20 ปี ส่วนในเพศหญิงพบสองช่วงอายุสูงสุดคือช่วงอายุ 20 ปี และ 50-60 ปี
Q
ซาร์คอยโดซิสทางระบบประสาทเกิดขึ้นบ่อยแค่ไหน?
A
พบรอยโรคทางระบบประสาทในผู้ป่วยซาร์คอยโดซิส 5-15%4) 7) ในการชันสูตรพลิกศพพบสัญญาณของซาร์คอยโดซิส ทางระบบประสาทสูงถึง 25% แสดงว่ามีหลายกรณีที่แฝงอยู่ ประมาณ 70% ของกรณี อาการทางระบบประสาทเป็นสัญญาณแรกของโรค3)
???????????????????????? Chaoyi Feng, Qian Chen, Wei Liu et al. Neuro
sarcoidosis presenting as
CRVO combined
CRAO : a biopsy-proven case report of a Chinese patient. BMC Ophthalmology. 2020 Aug 27; 20:348. Figure 1. PM
CI D: PMC7457306. License: CC BY.
????????????????????????????????????????????????????????????????
อาการของ NS หลากหลายตามตำแหน่งของรอยโรค ตั้งแต่อาการเดียวไปจนถึงอาการที่ซับซ้อนซึ่งเกี่ยวข้องกับหลายอวัยวะ
อาการทั่วไป/ไม่จำเพาะ
อ่อนเพลีย มีไข้ น้ำหนักลด
ปวดศีรษะ, ความบกพร่องทางการรู้คิด, ความผิดปกติทางอารมณ์
ความผิดปกติของเส้นประสาทสมอง
อัมพาตเส้นประสาทใบหน้า : ความผิดปกติของเส้นประสาทสมองที่พบบ่อยที่สุด อาจมีต่อมหูบวมร่วมด้วยความผิดปกติของเส้นประสาทตา : การมองเห็น ลดลง, จุดบอดในลานสายตา (ส่วนกลางหรือรอบนอก)ความผิดปกติของการเคลื่อนไหวลูกตา เห็นภาพซ้อน , หนังตาตก มีรายงานอัมพาตเส้นประสาทสมองคู่ที่สี่ด้วย 9)
อาการทางประสาทจักษุวิทยา
ม่านตาอักเสบ ส่วนหน้าหรือส่วนหลัง, ปวดตา , ตาโปน, ตาแห้ง
อาการเยื่อหุ้มสมองอักเสบ
คอแข็ง, ปวดศีรษะ, คลื่นไส้และอาเจียน
อาการของไขสันหลังและเส้นประสาทส่วนปลาย
ความรู้สึกผิดปกติ, กล้ามเนื้ออ่อนแรง, อัมพาตครึ่งล่างแบบกึ่งเฉียบพลัน
ความผิดปกติของกระเพาะปัสสาวะและทวารหนัก, ภาวะหย่อนสมรรถภาพทางเพศ 6)
อาการทางต่อมไร้ท่อ
เบาจืด, ภาวะโปรแลคตินในเลือดสูง, ภาวะไทรอยด์ต่ำ พบการเกี่ยวข้องของต่อมใต้สมองใน 10-15%
ในรายรุนแรง, ภาวะต่อมใต้สมองทำงานต่ำทั้งหมด: ระดับคอร์ติซอล (1.9 mcg/dL), FT4 (0.4 ng/dL), โปรแลคติน (86.8 ng/mL) ลดลงอย่างชัดเจน 4)
อาการที่เกี่ยวข้องกับหลอดเลือดอักเสบ
ปวดศีรษะ 69% อาการทางการเคลื่อนไหว 48% โรคเส้นประสาทสมอง 41% การเปลี่ยนแปลงด้านความรู้ความเข้าใจและพฤติกรรม 28%7)
อาการชักจากโรคลมชัก
ในเด็ก อาการชักเกิดขึ้นใน 24.5% ของผู้ป่วย5)
อาการแสดงหลักของรอยโรคระบบประสาทส่วนกลาง
การเพิ่มสัญญาณของเยื่อหุ้มสมองชั้นในแบบกระจาย : ผลตรวจที่พบบ่อยที่สุดในการตรวจ MRI ด้วยสารทึบรังสีแกโดลิเนียม
การเพิ่มสัญญาณของเส้นประสาทสมอง : การเพิ่มสัญญาณของเส้นประสาทสมองรวมถึงเส้นประสาทเฟเชียลและออปติก
รอยโรคคล้ายก้อนเนื้องอกในสมอง : พบเดี่ยวหรือหลายจุด มักถูกเข้าใจผิดว่าเป็นเนื้องอกหรือมะเร็งแพร่กระจาย
ภาวะน้ำคั่งในโพรงสมอง : ทั้งชนิดติดต่อและไม่ติดต่อ พบใน 57% ของผู้ป่วย2)
อาการแสดงทางตา (เกณฑ์ IWOS 6 ข้อ)
ม่านตาอักเสบ ส่วนหน้าชนิดแกรนูโลมากระจกตา , ปุ่มที่ม่านตา
ปุ่มที่มุมตา หรือการยึดติดของม่านตา ส่วนปลายรูปเต็นท์ : อาการแสดงเฉพาะของส่วนหน้าของตา
ความขุ่นของวุ้นตา เป็นก้อน
เยื่อบุหลอดเลือดจอตาอักเสบ : การอักเสบรอบหลอดเลือดและปุ่มที่เกิดขึ้นส่วนใหญ่ในหลอดเลือดดำ
รอยโรคขี้ผึ้งที่คอรอยด์ และจอประสาทตา หลายแห่ง : หรือรอยโรคฝ่อคล้ายรอยจอประสาทตา ถูกจี้ด้วยแสง
แกรนูโลมาของหัวประสาทตาหรือคอรอยด์ : หัวประสาทตาแดง และบวม
รูปแบบ MRI ไขสันหลัง 4 แบบ (PMC11213433) 6)
ไขสันหลังอักเสบตามขวางแบบยาว (LETM) : 45%. รอยโรคตามขวางกว้างตามยาวจาก C2 ถึงโคนไขสันหลังเยื่อหุ้มสมองและรากประสาทไขสันหลังอักเสบ : 23%.ไขสันหลังอักเสบแบบก้อน : 23%.ไขสันหลังอักเสบส่วนหน้า : 10%. เกิดขึ้นบริเวณใกล้เคียงกับหมอนรองกระดูกเสื่อม
ผลตรวจร่วมที่อ้างอิงสำหรับซาร์คอยโดซิส ที่ตา : กระจกตา แห้ง, เยื่อบุตา ชั้นนอกอักเสบ/ตาขาว อักเสบ, ต่อมน้ำตาบวม, เส้นประสาทใบหน้าเป็นอัมพาต
ภาวะแทรกซ้อนของซาร์คอยโดซิส ที่ตา : จุดรับภาพบวมน้ำแบบถุงน้ำ, เยื่อเหนือจอประสาทตา , ต้อหินทุติยภูมิ , ต้อกระจก ร่วม
ลักษณะของโรคเส้นประสาทตา : 28% เกิดทั้งสองข้างต่อเนื่องกัน, 37% มีหัวประสาทตาบวม, 4% มีเยื่อหุ้มเส้นประสาทตาอักเสบ 10) .
Q
ดวงตามีอาการอย่างไร?
A
ม่านตาอักเสบ (ยูเวียอักเสบ) พบบ่อยที่สุด โดยมีลักษณะเป็นม่านตาอักเสบ ส่วนหน้าแบบแกรนูโลมาที่มีตะกอนที่กระจกตา แบบไขมันและปุ่มที่ม่านตา สงสัยซาร์คอยโดซิส ที่ตาเมื่อมีเกณฑ์ IWOS 6 ข้อ (ม่านตาอักเสบ ส่วนหน้าแบบแกรนูโลมา, ปุ่มที่มุมตา, ขุ่นในวุ้นตา แบบก้อน, เยื่อบุหลอดเลือดจอประสาทตาอักเสบ , รอยโรคขี้ผึ้งที่คอรอยด์ และจอประสาทตา , แกรนูโลมาที่หัวประสาทตา/คอรอยด์ ) ตั้งแต่ 2 ข้อขึ้นไป ในโรคเส้นประสาทตา 28% เกิดทั้งสองข้าง10) .
ยังไม่ทราบสาเหตุของ NS พยาธิสภาพพื้นฐานคือการสร้างแกรนูโลมาแบบไม่เป็นก้อนเนื้อตายจากปฏิกิริยาภูมิคุ้มกันแบบเซลล์ Th1 (ภูมิแพ้ชนิดที่ 4) สันนิษฐานว่ามีการกระตุ้นแมคโครฟาจและทีเซลล์มากเกินไปจากการสัมผัสกับสิ่งกระตุ้นแอนติเจนเป็นเวลานาน ในญี่ปุ่น มีรายงานที่บ่งชี้ถึงการเกี่ยวข้องของ Propionibacterium acnes
การสัมผัสจากการทำงาน : ทำงานเกษตรกรรม สัมผัสยาฆ่าแมลงและเชื้อราปัจจัยทางพันธุกรรม : พบมากในชาวอเมริกันเชื้อสายแอฟริกัน การกลายพันธุ์ของยีน BTNL2 อาจเพิ่มความไวต่อโรคปัจจัยทางเศรษฐกิจสังคม : สถานะทางเศรษฐกิจสังคมต่ำอาจเพิ่มความเสี่ยงผ่านความเครียดและความผิดปกติของภูมิคุ้มกัน3)
ไม่มีวิธีการป้องกันที่พิสูจน์แล้วสำหรับโรคซาร์คอยด์ของระบบประสาท หากคุณมีอาการ (การมองเห็น ลดลง ชาหรืออัมพาตที่ใบหน้า ปวดหัว เดินลำบาก ฯลฯ) ให้ไปพบแพทย์แต่เนิ่นๆ หากได้รับการวินิจฉัยว่าเป็นซาร์คอยด์ สิ่งสำคัญคือต้องไปพบจักษุแพทย์และแพทย์ระบบประสาทอย่างสม่ำเสมอ
การวินิจฉัย NS ทำได้โดยการรวมภาพทางคลินิกที่หลากหลายและผลการตรวจ การวินิจฉัยที่แน่นอนต้องยืนยันเนื้อเยื่อแกรนูโลมาแบบไม่เป็นก้อนเนื้อตาย แต่เนื่องจากการตัดชิ้นเนื้อระบบประสาทส่วนกลาง (CNS) มีความเสี่ยง จึงใช้เกณฑ์การวินิจฉัยหลายอย่าง
ระดับความแน่นอน ข้อกำหนดหลัก แน่นอน (Definite) การตัดชิ้นเนื้อ CNS พบแกรนูโลมาแบบไม่เป็นก้อนเนื้อตาย + อาการทางคลินิก + การแยกโรคอื่นออก น่าจะเป็น (Probable) หลักฐานเนื้อเยื่อของซาร์คอยด์ทั่วร่างกาย + ผลการตรวจการอักเสบของ CNS เป็นไปได้ (Possible) อาการทางคลินิกชี้แนะแต่ไม่เข้าเกณฑ์ข้างต้น
กลุ่มวินิจฉัยทางเนื้อเยื่อ (แน่นอน) : รอยโรคใน ≥2 อวัยวะ + ผลตรวจ ≥2 รายการ + ผลชิ้นเนื้อทางพยาธิวิทยาเป็นบวกกลุ่มวินิจฉัยทางคลินิก (เกือบแน่นอน) : รอยโรคใน ≥2 อวัยวะ + ผลตรวจ ≥2 รายการภาวะที่ควรแยกออก : มะเร็งต่อมน้ำเหลืองชนิดร้าย วัณโรค แกรนูโลมาโทซิสกับโพลีแองจิไอติส (GP A) โรคที่เกี่ยวข้องกับ IgG4 กลุ่มอาการโจเกรน ฯลฯ
แน่นอน : ยืนยันด้วยชิ้นเนื้อ + ม่านตาอักเสบ สันนิษฐาน : ต่อมน้ำเหลืองฮิลัสทั้งสองข้างโต (BHL) + ม่านตาอักเสบ (ไม่มีการตรวจชิ้นเนื้อ)มีความเป็นไปได้สูง : สัญญาณภายในตา 3 อย่าง + ผลตรวจ 2 รายการเป็นไปได้ : สัญญาณภายในตา 4 อย่าง + ผลตรวจ 2 รายการ
ACE ในซีรัม : การเพิ่มขึ้นมีประโยชน์ช่วยในการวินิจฉัย (เช่น 73 U/L9) ). มีประโยชน์สำหรับซาร์คอยโดซิส ทั่วร่างกาย แต่ความจำเพาะไม่เพียงพอสำหรับชนิดทางระบบประสาทไลโซไซม์ในซีรัม : พบว่ามีการเพิ่มขึ้นsIL-2R ในซีรัม : เพิ่มขึ้น ร่วมกับภาวะลิมโฟไซต์ต่ำ เป็นเครื่องหมายที่มีประสิทธิภาพสำหรับซาร์คอยโดซิส ทางตาการตรวจด้วย 67Ga-citrate scintigram หรือ FDG-PET : การสะสมของสารรังสีที่เป็นบวกช่วยในการวินิจฉัย
โปรตีนในน้ำไขสันหลัง : สูงขึ้น (74%) 7) เซลล์เพิ่มขึ้น : 78% (ส่วนใหญ่เป็นลิมโฟไซต์) 7) ดัชนี IgG : สูงขึ้น (56%) 7) Oligoclonal band : พบผลบวก 25-30% 7) ACE ในน้ำไขสันหลัง : การเพิ่มขึ้นช่วยในการวินิจฉัย (เช่น 56.9 U/L 5) )ความผิดปกติของน้ำไขสันหลังพบได้ 70% ของผู้ป่วยแม้ภาพถ่ายรังสีปกติ
MRI ด้วยการฉีดแกโดลิเนียม : มีความไวสูงที่สุด การเพิ่มความเข้มของเยื่อหุ้มสมองชั้นเลปโตเมนินจีสแบบกระจาย/หนาตัวเป็นสิ่งที่พบบ่อยที่สุด การกระจายรอบโพรงสมองร่วมกับการเพิ่มความเข้มของเยื่อเลปโตเมนินจีสเป็นการรวมกันของสองสิ่งที่พบได้ทั่วไป 1) CT ทรวงอก : เพื่อยืนยัน BHL ในคนผิวขาว ไม่สามารถตัดซาร์คอยโดซิส ออกได้แม้ CT ทรวงอกปกติFDG-PET : มีประโยชน์ในการประเมินรอยโรคในตำแหน่งอื่นและเลือกตำแหน่งตัดชิ้นเนื้อ 3) MRI ผนังหลอดเลือด (VWI) : มีประโยชน์ในการประเมินหลอดเลือดอักเสบที่เกี่ยวข้องกับ neurosarcoidosis
การยืนยัน granuloma ชนิดไม่เป็น caseous เป็นมาตรฐานทองคำ การตัดชิ้นเนื้อระบบประสาทส่วนกลางเป็นวิธีที่ดีที่สุดแต่มีความรุกรานสูง ดังนั้นจึงพิจารณาการตัดชิ้นเนื้อจากตำแหน่งอื่น เช่น ต่อมน้ำเหลือง ผิวหนัง เยื่อบุตา หรือการตัดชิ้นเนื้อปอดผ่านหลอดลมเป็นทางเลือก
เยื่อหุ้มสมองอักเสบจากวัณโรค, โรคปลอกประสาทเสื่อมแข็ง, มะเร็งต่อมน้ำเหลืองในระบบประสาทส่วนกลาง, โรคแกรนูโลมาโตซิสชนิดลิมโฟมาทอยด์ที่สัมพันธ์กับ EB V
โรคแกรนูโลมาโตซิสกับโพลีแองจิอักเสบ (GP A), เยื่อหุ้มสมอง瘤, เนื้องอกเกลียของเส้นประสาทตา , โรคเบห์เซ็ต, โรคที่เกี่ยวข้องกับ IgG4
Q
จำเป็นต้องตรวจอะไรบ้างเพื่อการวินิจฉัยที่แน่นอนของโรคซาร์คอยด์ของระบบประสาท?
A
การวินิจฉัยที่แน่นอนต้องยืนยันเนื้อเยื่อแกรนูโลมาแบบไม่เป็นก้อนเนื้อตายผ่านการตัดชิ้นเนื้อระบบประสาทส่วนกลาง อย่างไรก็ตาม เนื่องจากมีความรุกรานสูง จึงมักใช้การวินิจฉัยแบบเป็นขั้นตอนโดยรวมการตรวจน้ำไขสันหลัง (โปรตีนสูง, เม็ดเลือดขาวลิมโฟไซต์เพิ่ม), MRI ด้วยแกโดลิเนียม, ACE และ sIL-2R ในซีรั่ม, และ CT ทรวงอก (ยืนยัน BHL) หากยืนยันแกรนูโลมาแบบไม่เป็นก้อนเนื้อตายในตำแหน่งอื่น (ต่อมน้ำเหลือง, ผิวหนัง, การตัดชิ้นเนื้อผ่านหลอดลม ฯลฯ) ก็สามารถวินิจฉัยว่าเป็นไปได้
เนื่องจากโรคนี้มีกิจกรรมที่ผันผวน ในกรณีที่ไม่รุนแรงอาจคาดหวังการฟื้นตัวได้เองและสังเกตอาการด้วยยาหยอดตาสเตียรอยด์ เท่านั้น ในกรณีรุนแรง ให้สเตียรอยด์ ทั่วร่างกาย
การอักเสบของส่วนหน้าของตา
ยาหยอดตาสเตียรอยด์ : Rinderon 0.1% วันละ 4 ครั้ง ใช้ต่อเนื่องแม้ไม่มีอาการอักเสบในช่องหน้าม่านตา เพื่อป้องกันก้อนที่มุมตายาขยายม่านตา : Midrin P วันละ 3 ครั้ง (เพื่อป้องกันการยึดติดของม่านตา ด้านหลัง)
การอักเสบของส่วนหลังของตา (กรณีรุนแรง)
สเตียรอยด์ ชนิดรับประทาน
ด้านล่างนี้เป็นตัวอย่างใบสั่งยาสำหรับการลดขนาดเพรดนิโซโลน
ระยะเวลา ขนาดยา 2 สัปดาห์ 30 มก./วัน 1 เดือน 20 มก./วัน 1 เดือน 15 มก./วัน 1 เดือน 10 มก./วัน 1 เดือน 7.5 มก./วัน 1 เดือน 5 มก./วัน 1 เดือน 5 มก. วันเว้นวัน
การฉีดใต้ถุงเทนอน ส่วนหลัง : สเตียรอยด์ ชนิดออกฤทธิ์นาน (Kenacort A 40 มก.) มีประสิทธิภาพสำหรับจอประสาทตา บวมน้ำชนิดซีสตอยด์และขุ่นมัวในวุ้นตา จุดสูงสุดของฤทธิ์ประมาณ 1 เดือน ระยะเวลาออกฤทธิ์ประมาณ 3 เดือน
การรักษาภาวะแทรกซ้อนทางตา
ต้อกระจก ร่วมสเตียรอยด์ ต้อหินทุติยภูมิ ต้อหินจากสเตียรอยด์ บริเวณไร้หลอดเลือดจากหลอดเลือดอักเสบอุดตัน : การจี้จอประสาทตาด้วยแสง
ทางเลือกแรก
คอร์ติโคสเตียรอยด์ ชนิดกิน
คอร์ติโคสเตียรอยด์ ชนิดฉีดเข้าเส้น (pulse)สเตียรอยด์ Methylprednisolone 1 กรัม × 5 วัน → prednisolone ชนิดกิน 1 มก./กก.6)
ทางเลือกที่สอง
Methotrexate (MTX) : ยากดภูมิคุ้มกันที่ใช้บ่อยที่สุด ต้องใช้เวลาในการออกฤทธิ์จึงใช้ร่วมกับสเตียรอยด์
Azathioprine, mycophenolate mofetil : ใช้เป็นทางเลือกหรือเพิ่มเติมจาก MTX
ทางเลือกที่สาม
Infliximab : ยายับยั้ง TNF -α ใช้แม้ในกรณีที่มีหลอดเลือดสมองอักเสบร่วม
Adalimumab : เป็นยายับยั้ง TNF -α เช่นกัน มีการใช้เพิ่มขึ้นในกรณีดื้อต่อการรักษา
กรณีที่มีหลอดเลือดสมองอักเสบร่วม : การใช้ glucocorticoid ร่วมกับ MTX/cyclophosphamide/infliximab เป็นกลยุทธ์การรักษาหลัก7) อัตราส่วนอันตรายของเหตุการณ์หลอดเลือดสมองภายใน 5 ปีหลังการวินิจฉัย sarcoidosis คือ 10.06 ซึ่งสูงอย่างมีนัยสำคัญ7)
โรคลมชักร่วม : ใช้ยาต้านโรคลมชัก เช่น levetiracetam ร่วมด้วย 5)
ภาวะน้ำคั่งในโพรงสมอง : การผ่าตัดใส่ท่อระบายน้ำ (VP shunt) (วาล์ว 5 ซม.น้ำ + อุปกรณ์ป้องกันไซฟอน) ร่วมกับสเตียรอยด์ ได้ผลดี 2) หากเกิดการยุบตัวของโพรงสมองอย่างรวดเร็ว (slit ventricles) ชั่วคราวหลังผ่าตัด ให้เปลี่ยนวาล์วเป็น 15 ซม.น้ำ 2) การกดทับไขสันหลัง (รอยโรคเหนือเยื่อดูรา) : อาจต้องผ่าตัดลดการกดทับ (laminectomy) 8) เว้นแต่จะมีภาวะแทรกซ้อนที่คุกคามชีวิต โดยหลักการแล้วข้อบ่งชี้ในการผ่าตัดมีจำกัด
ในภาวะต่อมใต้สมองทำงานน้อยทั่วจากรอยโรคต่อมใต้สมอง จำเป็นต้องทดแทนฮอร์โมนด้วยไฮโดรคอร์ติโซน เลโวไทรอกซิน และเดสโมเพรสซิน (สำหรับเบาจืด) ความเสียหายทางระบบประสาทมักไม่สามารถฟื้นคืนได้ และอาจต้องทดแทนตลอดชีวิต 4)
เนื่องจากสเตียรอยด์ ชนิดทั่วร่างกายทำให้ผลชิ้นเนื้อเป็นลบ โดยหลักการแล้วควรงดให้สเตียรอยด์ ชนิดทั่วร่างกายจนกว่าจะทำการตรวจชิ้นเนื้อเพื่อวินิจฉัย เช่น การตรวจชิ้นเนื้อปอดผ่านหลอดลมเสร็จสิ้น
ในการใช้สเตียรอยด์ ระยะยาว ต้องระวังความเสี่ยงต่อโรคกระดูกพรุน เบาหวาน และการติดเชื้อ ผู้ป่วยบางรายอาจต้องใช้ขนาดรักษา (5-10 มก./วัน) เป็นเวลานาน
ยากดภูมิคุ้มกัน (เช่น MTX, azathioprine) ต้องใช้เวลาหลายสัปดาห์ถึงหลายเดือนจึงจะออกฤทธิ์ ดังนั้นการให้ร่วมกับสเตียรอยด์ ตั้งแต่เนิ่นๆ จึงสำคัญ
Q
การรักษาด้วยสเตียรอยด์ใช้เวลานานเท่าใด?
A
แตกต่างกันมากตามกิจกรรมของโรค ในซาร์คอยด์ที่ตา โดยทั่วไปเริ่มด้วย prednisolone 30 มก. และค่อยๆ ลดลงเหลือ 5 มก. วันเว้นวันภายในประมาณ 7 เดือน ในกรณีรุนแรงหรือกลับเป็นซ้ำ อาจต้องใช้ขนาดรักษา (5-10 มก./วัน) เป็นเวลานาน ซาร์คอยด์ของระบบประสาทมักกลับเป็นซ้ำและทุเลา ดังนั้นการติดตามระยะยาวจึงจำเป็น
เซลล์ Th1 ปล่อย IL-2 และ IFN-γ ซึ่งกระตุ้นให้มาโครฟาจเคลื่อนที่และถูกกระตุ้น มาโครฟาจที่ถูกกระตุ้นจะหลั่งไซโตไคน์และคงการสร้างแกรนูโลมาอย่างต่อเนื่อง ทางจุลกายวิภาคศาสตร์ เซลล์เอพิธีลิออยด์และเซลล์ยักษ์หลายนิวเคลียสก่อตัวเป็นศูนย์กลาง โดยมีลิมโฟไซต์ พลาสมาเซลล์ และมาสต์เซลล์สะสมอยู่รอบๆ อาจพบแอสเทอรอยด์บอดีภายในเซลล์ยักษ์หลายนิวเคลียส
แกรนูโลมาเกิดขึ้นภายในหรือรอบๆ ผนังหลอดเลือด โดยเฉพาะอย่างยิ่งในหลอดเลือดแดงเจาะขนาดเล็ก อัตราส่วนความเสี่ยงของเหตุการณ์หลอดเลือดสมองภายใน 5 ปีหลังการวินิจฉัยซาร์คอยโดซิส คือ 10.06 ซึ่งบ่งชี้ถึงความเสี่ยงที่สูงขึ้นอย่างชัดเจนของภาวะแทรกซ้อนทางหลอดเลือดสมอง 7)
การทำลายไมอีลินจากการอักเสบเป็นองค์ประกอบหลัก การตรวจชิ้นเนื้อเส้นประสาทและกล้ามเนื้อยืนยันการมีแกรนูโลมาที่เยื่อหุ้มเส้นประสาทชั้นนอกและการแทรกซึมที่เยื่อหุ้มเส้นประสาทชั้นใน 6)
เกิดการอุดตันของทางเดินน้ำไขสันหลังจากแผลเป็นแกรนูโลมาที่เยื่อหุ้มสมอง และการดูดซึมน้ำไขสันหลังบกพร่องเนื่องจากการอักเสบของวิลไลอะแร็กนอยด์ สามารถเกิดได้ทั้งชนิดติดต่อและไม่ติดต่อ 2)
การแทรกซึมของแกรนูโลมาเข้าไปในไฮโปทาลามัส ก้านต่อมใต้สมอง และต่อมใต้สมอง ทำให้แกนต่อมไร้ท่อเสียหาย ในกรณีที่รุนแรง อาจเกิดเบาจืดจากส่วนกลางร่วมกับ Na 168 (ภาวะโซเดียมในเลือดสูง) 4)
เทคนิคการถ่ายภาพผนังหลอดเลือดด้วย MRI คาดว่าจะช่วยเพิ่มความแม่นยำในการวินิจฉัยหลอดเลือดอักเสบที่เกี่ยวข้องกับ neurosarcoidosis
ในการทบทวนอย่างเป็นระบบโดย Focke และคณะ (2025) การตรวจหารอยโรคที่ผนังหลอดเลือดด้วย MRI VWI ประสบความสำเร็จในผู้ป่วย NS 9 จาก 13 ราย (69%) 7) อาจสามารถมองเห็นการอักเสบของผนังหลอดเลือดที่ยากต่อการจับภาพด้วย MRI ที่ใช้สารทึบแสงแกโดลิเนียมแบบดั้งเดิม
ในฐานะตัวบ่งชี้ทางชีวภาพ ของ NS ที่เกี่ยวข้องกับหลอดเลือดอักเสบ นีออปเทอรินและไลโซไซม์ในน้ำไขสันหลังกำลังได้รับความสนใจ
Focke และคณะ (2025) รายงานว่านีออปเทอรินในน้ำไขสันหลังสูงขึ้นใน 100% ของกรณี (เฉลี่ย 5.2 ng/ml) และไลโซไซม์สูงขึ้นใน 75% (เฉลี่ย 4.25 mg/l) ในกรณี NS ที่เกี่ยวข้องกับหลอดเลือดอักเสบ 7) ตัวบ่งชี้เหล่านี้อาจกลายเป็นเครื่องมือวินิจฉัย
ในฐานะการถ่ายภาพที่ไม่พึ่งพา FDG-PET การถ่ายภาพตัวรับโซมาโตสแตตินและการถ่ายภาพ PET ที่กำหนดเป้าหมาย CXCR4 (ซึ่งแสดงออกบนแมคโครฟาจที่ถูกกระตุ้น) กำลังถูกสำรวจ
สารยับยั้ง JAK เช่น โทฟาซิทินิบและบาริซิทินิบอยู่ในขั้นตอนการสำรวจเพื่อประยุกต์ใช้ในซาร์คอยโดซิส ที่ดื้อต่อการรักษา
แม้จะมีรายงานการปรับปรุงอาการในบางกรณีของ NS ที่ดื้อต่อการรักษา แต่บทบาทของริตูซิแมบใน NS ยังไม่ชัดเจนในปัจจุบัน 6)
Ach T, Ben Yahia W, Halloul I, et al. Neurosarcoidosis -Induced Hypophysitis Mimicking Pituitary Macroadenoma. Cureus. 2023;15(6):e39865.
Kafai Golahmadi A, Craven CL, Watkins LD. Neurosarcoidosis Mimicking Normal Pressure Hydrocephalus. Cureus. 2023;15(6):e40281.
Hanif Z, Gonzalez Ramos KN, Razminia P, et al. A Perplexing Case of Bladder Mass Biopsy-Proven Neurosarcoidosis . Cureus. 2023;15(6):e40865.
Alfares K, Han HJ. Neurosarcoidosis -Induced Panhypopituitarism. Cureus. 2023;15(8):e43169.
Khawaja MA, Awesat BE, Yasini MN, et al. Neurosarcoidosis Presented as an Isolated Brain Lesion. Cureus. 2023;15(9):e45837.
Chaubey M, Meena K, Singh T, et al. Neurosarcoidosis : An under-diagnosed cause of myelopathy. J Family Med Prim Care. 2024;13:2157-60.
Focke JK, Brokbals M, Becker J, et al. Cerebral vasculitis related to neurosarcoidosis : a case series and systematic literature review. J Neurol. 2025;272:135.
Shields R, Sagan O, Roebke L, et al. Rare case of multifocal extradural and intramedullary neurosarcoidosis without pulmonary involvement. Spinal Cord Ser Cases. 2021;7:89.
Sarac E, Erzurum SA, Arif A. An Unusual Presentation of Neurosarcoidosis . Am J Case Rep. 2022;23:e937125.
Desmond PK, Ben JB, Elizabeth MG, Gordon TP. Optic neuropathy associated with systemic sarcoidosis . Neurol Neuroimmunol Neuroinflammation. 2016;3:e270.
Kidd D, Beynon HL. The neurological complications of systemic sarcoidosis . Sarcoidosis Vasc Diffus Lung Dis. 2003;20:85-94.