
Terapia con luce rossa (controllo della progressione della miopia)
1. Cos’è la terapia con luce rossa (controllo della progressione miopica)
Sezione intitolata “1. Cos’è la terapia con luce rossa (controllo della progressione miopica)”La terapia con luce rossa ripetuta a bassa intensità (Repeated Low-Level Red Light Therapy: RLRL) è un trattamento non invasivo che inibisce la progressione della miopia nei bambini mediante l’esposizione dell’occhio a luce visibile rossa di una specifica lunghezza d’onda (principalmente 650-670 nm) a bassa intensità. Il protocollo standard prevede l’uso di un dispositivo portatile dedicato, con sessioni di 3 minuti due volte al giorno per 5 giorni a settimana.
Posizionamento della terapia RLRL
Sezione intitolata “Posizionamento della terapia RLRL”La terapia RLRL è un trattamento relativamente nuovo per il controllo della progressione miopica, con evidenze accumulate rapidamente a partire dagli anni 2020. È considerata una “quarta opzione” dopo le tre principali terapie convenzionali (collirio a base di atropina a bassa concentrazione, ortocheratologia e lenti a contatto multifocali), e la maggior parte degli studi è stata condotta in Asia orientale, principalmente in Cina.
La miopia è caratterizzata principalmente dall’allungamento del bulbo oculare; un aumento di 1 mm della lunghezza assiale corrisponde approssimativamente a una miopizzazione di 3 D. Il controllo dell’allungamento assiale è l’obiettivo primario della gestione della miopia, e la variazione della lunghezza assiale è considerata l’endpoint più importante nella valutazione dell’efficacia della terapia RLRL 1).
Le principali complicanze associate alla miopia includono il distacco della retina (aumento del rischio del 30% per ogni -1 D), la degenerazione maculare miopica (aumento del 58%) e il glaucoma ad angolo aperto (aumento del 20%) 6). La terapia RLRL è considerata un intervento preventivo per ridurre questi rischi a lungo termine.
Nei bambini di origine asiatica, la prevalenza della miopia è particolarmente elevata e, se non trattata, il rischio di complicanze gravi come distacco di retina e degenerazione maculare miopica aumenta significativamente. Si stima che per ogni aumento di 1D della miopia, il rischio di distacco di retina aumenti del 30%, di degenerazione maculare miopica del 58%, di glaucoma ad angolo aperto del 20% e di cataratta sottocapsulare posteriore del 21% 6).
Poiché un allungamento di 1 mm dell’asse oculare corrisponde a circa 3D di miopia, il controllo dell’allungamento assiale è l’obiettivo principale della gestione della miopia. La meta-analisi di Haarman et al. (2020) 7) ha mostrato che il rischio di complicanze aumenta in modo esponenziale con la gravità della miopia, sottolineando l’importanza di un intervento precoce per migliorare la prognosi a lungo termine.
La terapia RLRL è una delle opzioni per il controllo della progressione della miopia, insieme all’ortocheratologia e alle gocce di atropina a bassa concentrazione, e le evidenze si sono accumulate rapidamente a partire dagli anni 2020. In Giappone, è stata introdotta come trattamento a pagamento in alcune strutture. La revisione sistematica di Yam et al. (2025) ha riassunto le evidenze di diversi interventi per il controllo della progressione della miopia, inclusa la terapia RLRL 5).
D’altra parte, Bullimore et al. (2021) hanno esaminato in dettaglio i rischi e i benefici della gestione generale della miopia, sottolineando che anche nella terapia RLRL esiste un rischio di fototossicità retinica in caso di deviazione dai parametri di irradiazione 6). La corretta gestione del dispositivo, l’intensità di irradiazione e il rispetto dei tempi di esposizione sono prerequisiti per un uso sicuro.
La terapia RLRL è un trattamento per il controllo della progressione della miopia che prevede l’irradiazione dell’occhio con luce rossa visibile nella banda 650-670 nm a bassa intensità (0,3-1 mW/cm²) per 3 minuti due volte al giorno. Si ritiene che aumenti lo spessore coroidale e inibisca l’allungamento assiale attraverso la fotobiomodulazione 3). Attualmente non è approvato in Giappone ed è un trattamento a pagamento, da utilizzare sotto la supervisione di uno specialista.
2. Principali sintomi e reperti clinici
Sezione intitolata “2. Principali sintomi e reperti clinici”Indicatori dell’efficacia terapeutica
Sezione intitolata “Indicatori dell’efficacia terapeutica”L’efficacia della terapia RLRL viene valutata mediante i seguenti indicatori oggettivi.
- Lunghezza assiale: misurata con un biometro ottico. Monitorare le variazioni prima e dopo il trattamento e ogni 6 mesi.
- Spessore coroidale: misurazione dello spessore coroidale sottofoveale (SFCT) mediante OCT. Dopo l’irradiazione RLRL si osserva un aumento dello spessore coroidale. Uno studio di follow-up di 2 anni di Dong et al. (2023) ha confermato l’aumento dello spessore coroidale 2).
- Equivalente sferico: valutazione oggettiva in condizioni di cicloplegia.
- Acuità visiva corretta: verifica della stabilità dell’acuità visiva corretta prima e dopo il trattamento.
Avvertenze per la valutazione della sicurezza
Sezione intitolata “Avvertenze per la valutazione della sicurezza”La terapia RLRL è a bassa intensità, quindi si ritiene che gli eventi avversi a breve termine siano rari, ma è necessario verificare regolarmente i seguenti punti.
- Rischio di tossicità retinica: un’intensità, una durata o una frequenza di irradiazione eccessive possono teoricamente causare danni alla retina6). Valutare gli strati retinici e coroideali con OCT come baseline prima del trattamento e confrontarli regolarmente.
- Cambiamenti dell’acuità visiva e della visione dei colori: verificare la presenza di diminuzione dell’acuità visiva o anomalie della visione dei colori durante il trattamento.
- Sintomi soggettivi: prestare attenzione a lamentele come abbagliamento, immagini residue o anomalie del campo visivo.
3. Cause e fattori di rischio
Sezione intitolata “3. Cause e fattori di rischio”Fattori di rischio per la progressione della miopia
Sezione intitolata “Fattori di rischio per la progressione della miopia”La progressione della miopia, oggetto della terapia RLRL, è influenzata dai seguenti fattori di rischio.
- Insorgenza giovanile (in particolare tra i 6 e i 12 anni)
- Genitori miopi (soprattutto se entrambi miopi)
- Lunghe ore di lavoro da vicino (oltre 3 ore al giorno)
- Scarsa attività all’aperto (meno di 1 ora al giorno)
- Etnia asiatica (la prevalenza più alta nell’Asia orientale)
- Secondo le previsioni di Holden et al. (2016), circa il 50% della popolazione mondiale sarà miope entro il 20508), aumentando l’importanza sociale di un intervento precoce.
4. Diagnosi e metodi di esame
Sezione intitolata “4. Diagnosi e metodi di esame”Valutazione prima dell’inizio del trattamento
Sezione intitolata “Valutazione prima dell’inizio del trattamento”Prima di iniziare la terapia RLRL, registrare il basale con i seguenti esami e verificare l’idoneità.
| Esame | Scopo | Principali punti di verifica |
|---|---|---|
| Esame refrattivo sotto cicloplegia | Valutazione oggettiva del grado di miopia | Equivalente sferico e astigmatismo |
| Misurazione della lunghezza assiale | Impostazione del basale e monitoraggio della progressione | Misurata con biometria ottica |
| Esame del fondo oculare | Stato retinico e coroidale pre-trattamento | Valutazione delle alterazioni miopiche elevate |
| OCT (macula e nervo ottico) | Impostazione dei valori di riferimento per la tossicità retinica | Spessore stratificato di retina e coroide |
| Esame con lampada a fessura | Esclusione di patologie del segmento anteriore | Infiammazione attiva/cataratta |
Per l’esame in cicloplegia, nei bambini piccoli è indispensabile l’instillazione di un farmaco cicloplegico (ad esempio Cicloplegina® 1%). Un esame soggettivo senza cicloplegia può portare a una sovrastima della gradazione miopica.
Monitoraggio durante il trattamento
Sezione intitolata “Monitoraggio durante il trattamento”Per verificare l’efficacia e la sicurezza del trattamento, si raccomanda il seguente programma.
| Periodo | Contenuto |
|---|---|
| Dopo 1 mese | Compliance ai colliri, verifica dei sintomi soggettivi, acuità visiva corretta |
| Ogni 3-6 mesi | Misurazione della lunghezza assiale, refrazione sotto cicloplegia, OCT (spessore coroidale, valutazione retinica) |
| Ogni anno | Esame del fondo oculare con dilatazione pupillare, OCT angiografia (opzionale) |
È essenziale registrare i valori basali con la refrazione sotto cicloplegia e la misurazione ottica della lunghezza assiale. Inoltre, documentare lo stato retinico e coroidale pre-trattamento con esame del fondo oculare e OCT, da utilizzare per il monitoraggio della sicurezza durante la terapia. In caso di sospetta miopia elevata, verificare anche la presenza di degenerazione o lacerazioni retiniche periferiche.
5. Trattamento standard
Sezione intitolata “5. Trattamento standard”Consenso informato e valutazione dell’idoneità prima del trattamento
Sezione intitolata “Consenso informato e valutazione dell’idoneità prima del trattamento”Di seguito sono riportati i punti fondamentali per la selezione dei pazienti candidati alla terapia RLRL.
Indicazioni raccomandate:
- 6-18 anni (la maggior parte degli studi ha coinvolto questa fascia d’età)
- Miopia sferica equivalente ≥ -0,5 D con progressione documentata
- Miopia confermata mediante esame sotto cicloplegia
- Ambiente in cui i genitori possano garantire una gestione adeguata
Situazioni da valutare con cautela:
- Casi con anamnesi o familiarità di malattie retiniche
- Malattie fotosensibili (xeroderma pigmentoso, fotosensibilità cutanea, ecc.)
- Uso di farmaci che aumentano la sensibilità alla luce
Situazioni in cui evitare l’uso:
- Malattia retinica attiva (degenerazione retinica, neovascolarizzazione, ecc.)
- Pazienti con diagnosi certa di fotosensibilità
Protocollo terapeutico
Sezione intitolata “Protocollo terapeutico”Di seguito sono riportati i parametri terapeutici standard adottati nei principali RCT.
| Parametro | Valore standard | Note |
|---|---|---|
| Lunghezza d’onda | 650 nm (luce visibile rossa) | Alcuni studi hanno utilizzato 670 nm |
| Intensità di irradiazione | 0,3–1 mW/cm² | Luce non coerente, non laser |
| Tempo di irradiazione | 3 minuti/seduta | 2 volte al giorno (mattina e sera) |
| Frequenza del trattamento | 5 giorni/settimana (solo giorni scolastici) | — |
| Durata del trattamento | 12-24 mesi o più | Necessità di mantenere l’effetto in corso |
Il dispositivo utilizzato è principalmente un apparecchio portatile specializzato di produzione cinese (Suneye, ecc.) impiegato nella ricerca. È progettato per l’auto-irradiazione a domicilio da parte del paziente, ma la configurazione iniziale e i controlli periodici devono essere effettuati da uno specialista.
Risultati degli RCT principali
Sezione intitolata “Risultati degli RCT principali”In uno RCT della durata di un anno condotto da Jiang et al. (2022), il gruppo RLRL ha mostrato una significativa inibizione dell’allungamento assiale di 0,10 mm/anno (gruppo di controllo 0,38 mm/anno)1). Anche nel follow-up di due anni di Dong et al. (2023), l’effetto inibitorio sull’allungamento assiale è persistito ed è stato confermato un aumento dello spessore coroidale2).
In uno RCT multicentrico di Zeng et al. (2023), la progressione dell’equivalente sferico a un anno è stata di -0,20 D nel gruppo di trattamento (gruppo di controllo -0,71 D), con un’inibizione della progressione miopica di circa il 72%4).
Confronto dell’efficacia tra terapia RLRL e altri metodi di controllo della progressione miopica:
| Intervento | Tasso di inibizione refrattiva | Tasso di inibizione assiale | Evidenze principali |
|---|---|---|---|
| Terapia RLRL | 72% (Zeng 2023) | 74% (Jiang 2022) | RCT multipli |
| Atropina a bassa concentrazione 0,05% | Fino al 67% | — | Studio LAMP |
| Ortocheratologia | — | 43% | Si 2015 meta-analisi |
| MiSight (lenti a contatto multifocali) | 59% | 52% | Chamberlain 2019 |
| Occhiali DIMS | 55-59% | 37-38% | RCT Lam 2020 |
Tuttavia, poiché il disegno dello studio, l’età dei soggetti e la durata del trattamento differiscono, è necessario prestare attenzione nel confronto diretto 5). Il collirio a bassa concentrazione di atropina (Rijusea® Mini 0,025%) è l’unico farmaco approvato in Giappone a dicembre 2024 9), e le lenti per occhiali per la gestione della miopia (come DIMS) 10) sono raccomandate anche dalle linee guida della Japanese Society of Myopia. La terapia RLRL sta emergendo come opzione da combinare con questi interventi approvati.
Rispetto ai dati dello studio RCT triennale su MiSight (lenti a contatto multifocali) 11), dello studio RCT biennale sugli occhiali DIMS 12), della meta-analisi sull’ortocheratologia 13) e dello studio RCT sulla combinazione ortocheratologia + atropina 14), il tasso di inibizione a breve termine della terapia RLRL è buono, ma la mancanza di dati oltre i 5 anni rappresenta la sfida più grande. La tendenza all’aumento della maculopatia miopica nei giapponesi, evidenziata dallo studio di Hisayama 15), conferma ulteriormente l’importanza medica degli interventi di gestione della miopia, inclusa la terapia RLRL.
Combinazione con altre terapie
Sezione intitolata “Combinazione con altre terapie”- RLRL + atropina a bassa concentrazione: Poiché i meccanismi d’azione sono diversi, ci si aspetta un effetto additivo o sinergico, ma la verifica tramite RCT su larga scala è in corso 5).
- RLRL + ortocheratologia: è stata riportata come combinazione scelta per casi di progressione rapida.
- Se la monoterapia è insufficiente, si considera la combinazione con altre terapie di controllo della progressione miopica.
Consenso informato
Sezione intitolata “Consenso informato”Ad aprile 2026, la terapia RLRL non è approvata né rimborsata in Giappone e viene fornita come trattamento a pagamento. È necessario spiegare adeguatamente quanto segue ai pazienti e ai tutori e ottenere il consenso.
- Che si tratta di un trattamento non approvato dalle autorità farmaceutiche in Giappone
- Che le attuali evidenze provengono principalmente da studi osservazionali di 1-2 anni e la sicurezza a lungo termine non è ancora stabilita
- Che esiste teoricamente un rischio di tossicità retinica in caso di deviazione dai parametri di irradiazione6)
- Che non si tratta di una «cura» della miopia, ma di un «controllo della progressione»
- È obbligatorio sottoporsi a regolari visite oculistiche e monitoraggio della sicurezza.
Ad aprile 2026, in Giappone la terapia RLRL non è approvata come farmaco né coperta dall’assicurazione sanitaria. Viene offerta come trattamento a pagamento in alcune cliniche oculistiche; è importante consultare uno specialista per verificare indicazioni, sicurezza e costi. Le gocce di atropina a bassa concentrazione (Rijusea® Mini 0,025%) sono state approvate a dicembre 2024 come primo farmaco giapponese per la progressione della miopia, rappresentando un’opzione coperta dall’assicurazione sanitaria.
Ruolo della RLRL nel meccanismo di controllo della progressione miopica
Sezione intitolata “Ruolo della RLRL nel meccanismo di controllo della progressione miopica”Mentre i principali interventi ottici per il controllo della progressione miopica (ortocheratologia, occhiali DIMS, lenti a contatto multifocali) condividono il meccanismo comune dell’ipotesi del defocus periferico miopico, la terapia RLRL agisce attraverso una via completamente diversa: attivazione mitocondriale tramite modulazione fotobiologica (PBM) → miglioramento del flusso sanguigno coroidale → ispessimento coroidale → inibizione dell’allungamento assiale. Questo diverso meccanismo d’azione porta all’aspettativa di un effetto sinergico in combinazione con altre terapie 3).
Inoltre, come caratteristica unica della terapia RLRL, è stata osservata una risposta fisiologica acuta con un immediato aumento dello spessore coroidale dopo il trattamento 2). Questa è una caratteristica non riscontrata in altre terapie di controllo della progressione miopica, e la misurazione dello spessore coroidale è considerata utile come indicatore dell’effetto immediato del trattamento.
6. Fisiopatologia e meccanismi dettagliati di insorgenza
Sezione intitolata “6. Fisiopatologia e meccanismi dettagliati di insorgenza”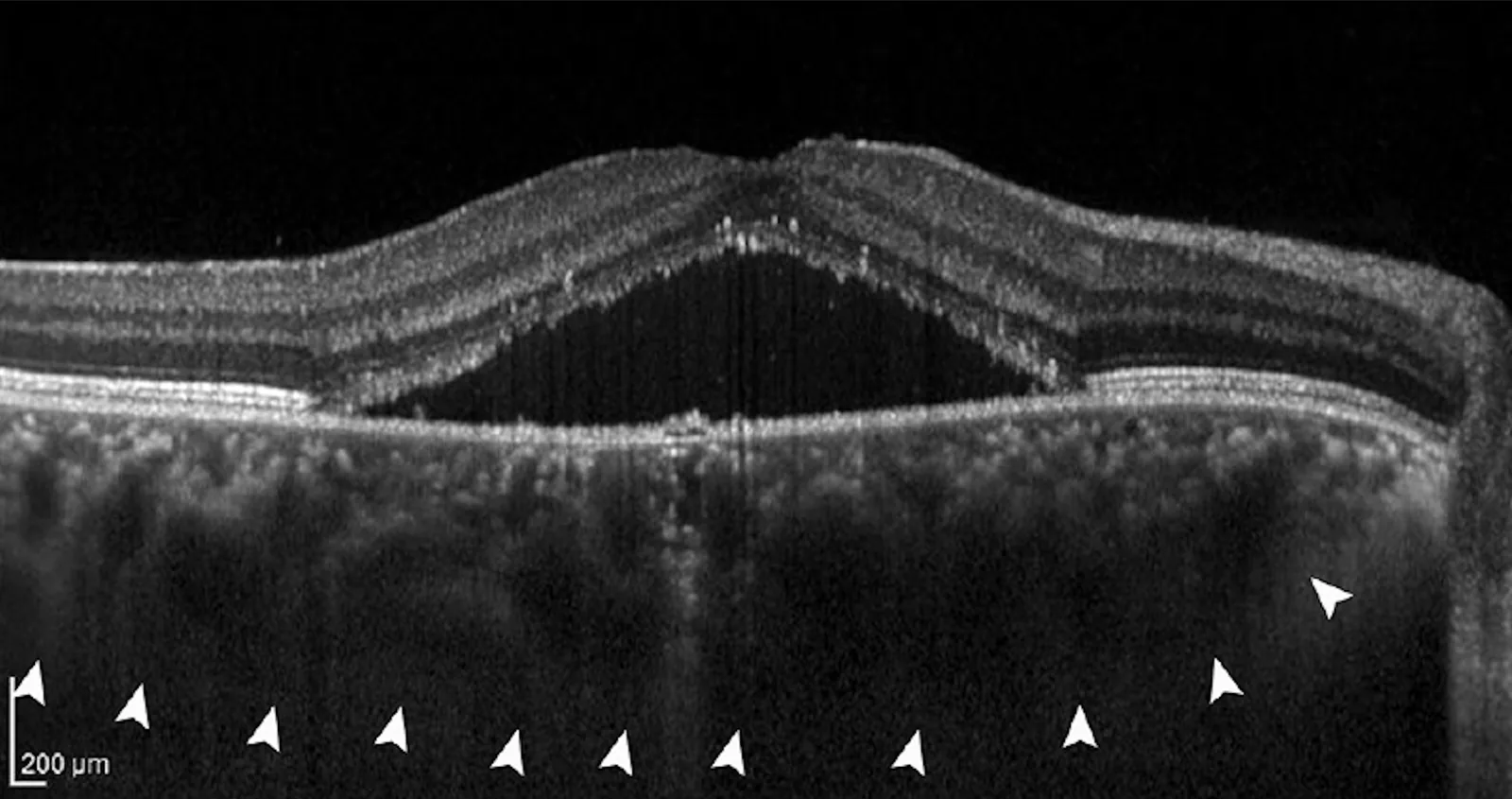
Modulazione fotobiologica (Photobiomodulation: PBM)
Sezione intitolata “Modulazione fotobiologica (Photobiomodulation: PBM)”Come meccanismo principale della terapia RLRL, viene proposta la modulazione fotobiologica (photobiomodulation: PBM) 3). La luce rossa nella banda 650-670 nm viene assorbita specificamente dal citocromo c ossidasi (Complesso IV) presente nei mitocondri cellulari, inducendo le seguenti risposte biologiche.
- Promozione della produzione di ATP
- Attivazione della segnalazione cellulare attraverso una moderata produzione di specie reattive dell’ossigeno (ROS)
- Vasodilatazione e aumento del flusso sanguigno tramite rilascio di ossido nitrico (NO)
- Miglioramento della circolazione coroidale e ispessimento
Aumento dello spessore coroidale e inibizione dell’allungamento assiale
Sezione intitolata “Aumento dello spessore coroidale e inibizione dell’allungamento assiale”Dopo l’irradiazione con RLRL è stato costantemente osservato un aumento dello spessore coroidale2)3). Si ritiene che l’aumento dello spessore coroidale influenzi la rigidità della parete oculare, contribuendo a inibire l’allungamento assiale. Un aumento dello spessore coroidale è stato riportato anche con l’ortocheratologia e l’atropina a bassa concentrazione, e si sta prestando attenzione alla possibilità che la coroide rappresenti una via comune per l’inibizione della progressione miopica.
Meccanismo di base della progressione miopica
Sezione intitolata “Meccanismo di base della progressione miopica”La progressione miopica è un processo biologico in cui la crescita oculare è regolata dalla trasmissione di segnali dalla retina alla sclera, e coinvolge i seguenti processi.
- Il defocus periferico ipermetropico funge da segnale di guida per l’allungamento assiale
- Il segnale di inibizione della crescita mediato dalla dopamina frena l’allungamento assiale
- Il rimodellamento della matrice extracellulare della sclera determina la lunghezza assiale
- L’ispessimento o l’assottigliamento della coroide rappresenta un biomarcatore delle variazioni della lunghezza assiale
La terapia RLRL interviene su questi segnali, frenando la crescita oculare a livello coroidale e sclerale, ma molti aspetti rimangono ancora da chiarire3). Il rischio quantitativo delle complicanze miopiche, come indicato dalla meta-analisi di Haarman et al. (2020), è ampiamente citato come base medica per l’intervento terapeutico7).
7. Ricerche recenti e prospettive future
Sezione intitolata “7. Ricerche recenti e prospettive future”Stabilire dati di efficacia e sicurezza a lungo termine
Sezione intitolata “Stabilire dati di efficacia e sicurezza a lungo termine”Gli attuali RCT principali hanno periodi di osservazione di 1-2 anni e i dati a lungo termine oltre 5 anni sono scarsi1)2). La persistenza dell’effetto dopo la sospensione del trattamento (effetto carry-over) non è ancora stabilita, e sono in corso studi che monitorano i cambiamenti nella velocità di progressione della miopia dopo la fine del trattamento.
Nello studio di follow-up a 2 anni di Dong et al. (2023), il gruppo trattato con RLRL ha mostrato una continua soppressione dell’allungamento assiale e un aumento dello spessore coroidale rispetto al gruppo di controllo, confermando il mantenimento dell’effetto con l’uso continuativo per 1 anno2). Tuttavia, poiché il disegno dello studio, i parametri di irradiazione e l’età dei soggetti differiscono tra gli studi, è necessaria cautela nel confronto diretto.
Quantificazione del rischio di tossicità retinica
Sezione intitolata “Quantificazione del rischio di tossicità retinica”Teoricamente esiste la possibilità che un’intensità, una durata o una frequenza di irradiazione eccessive causino danni alla retina. Nella valutazione rischio-beneficio della gestione della miopia di Bullimore et al. (2021), viene discusso l’equilibrio complessivo della sicurezza degli interventi ottici e farmacologici, inclusa la terapia RLRL, sottolineando l’importanza di una corretta gestione dei parametri6).
Sono in corso studi per stabilire i limiti di irradiazione sicuri e valutare il rischio. Nella pratica clinica, è necessario rispettare rigorosamente l’intensità di irradiazione (0,3-1 mW/cm²), la durata (3 minuti per sessione) e la frequenza (2 volte al giorno, 5 giorni a settimana), e verificare periodicamente la calibrazione del dispositivo.
Dal punto di vista della fototossicità, la quantità cumulativa di esposizione alla luce sui fotorecettori e sull’RPE è importante, e occorre prestare attenzione all’irradiazione che supera la dose raccomandata (in particolare l’uso deviante ad alta intensità e per lungo tempo). Come dimostra la meta-analisi delle complicanze della miopia di Haarman et al. (2020)7), è importante valutare individualmente il rapporto rischio-beneficio della terapia RLRL, presupponendo che una corretta gestione della miopia possa ridurre il rischio di complicanze gravi.
Confronto diretto con atropina a bassa concentrazione e ortocheratologia
Sezione intitolata “Confronto diretto con atropina a bassa concentrazione e ortocheratologia”Sono in corso studi clinici randomizzati che confrontano direttamente la terapia RLRL con l’ortocheratologia e l’atropina a bassa concentrazione. Si prevede di stabilire un protocollo personalizzato di gestione della miopia che tenga conto dei vantaggi e degli svantaggi di ciascuna terapia5).
Confronto delle caratteristiche dei tre principali interventi (RLRL, OK, atropina a bassa concentrazione):
| Intervento | Tasso di inibizione dell’asse oculare | Invasività | Comodità | Stato normativo in Giappone |
|---|---|---|---|---|
| Terapia RLRL | Circa 60-72% | Non invasivo | Eseguibile a casa | Non approvato (a pagamento) |
| Orthocheratologia | 30-50% | Contatto corneale presente | Uso notturno | Non approvato (a pagamento) |
| Atropina a bassa concentrazione 0,025% | Circa 62% | Collirio | Collirio prima di coricarsi | Approvato |
Previsione della progressione della miopia tramite IA
Sezione intitolata “Previsione della progressione della miopia tramite IA”Si sta sviluppando un modello che integra dati sulla lunghezza assiale, fattori di rischio e risposta al trattamento tramite IA per proporre strategie terapeutiche ottimali per ciascun paziente. Potrebbe essere applicato anche alla previsione della risposta alla terapia RLRL.
Tendenze verso l’approvazione nazionale
Sezione intitolata “Tendenze verso l’approvazione nazionale”Sulla base dell’accumulo di evidenze in Cina e Sud-est asiatico, potrebbero iniziare dialoghi con le autorità regolatorie anche in Giappone. Si attende con interesse l’attuazione di studi clinici randomizzati multicentrici nazionali e l’iter per l’approvazione farmaceutica. Con l’aumento globale della popolazione miope (Holden 2016: 4,9 miliardi entro il 20508)), la terapia RLRL si sta affermando come una delle opzioni per la gestione della miopia.
8. Riferimenti bibliografici
Sezione intitolata “8. Riferimenti bibliografici”- Jiang Y, Zhu Z, Tan X, et al. Effect of repeated low-level red-light therapy for myopia control in children: a multicenter randomized controlled trial. Ophthalmology. 2022;129:509-519.
- Dong J, Zhu Z, Xu H, et al. Myopia control effect of repeated low-level red-light therapy in Chinese children: a randomized, double-blind, controlled clinical trial. Ophthalmology. 2023;130:198-204.
- Wang W, Jiang Y, Zhu Z, et al. Chorioidal thickening as a potential therapeutic target in myopia management: a review of repeated low-level red light therapy. Surv Ophthalmol. 2023;68:1-12.
- Zeng J, Liu Y, Wang Z, et al. Efficacy of repeated low-level red-light stimulation on slowing myopia progression and ocular growth in children with myopia: a randomized controlled trial. Transl Vis Sci Technol. 2023;12:22.
- Yam JC, Zhang XJ, Zhang Y, et al. Interventions to reduce incidence and progression of myopia in children and adults. Prog Retin Eye Res. 2025.
- Bullimore MA, Ritchey ER, Shah S, et al. The risks and benefits of myopia control. Ophthalmology. 2021;128:1561-1579.
- Haarman AEG, Enthoven CA, Tideman JWL, et al. The complications of myopia: a review and meta-analysis. Invest Ophthalmol Vis Sci. 2020;61:49.
- Holden BA, Fricke TR, Wilson DA, et al. Global prevalence of myopia and high myopia and temporal trends from 2000 through 2050. Ophthalmology. 2016;123:1036-1042.
- 低濃度アトロピン点眼液を用いた近視進行抑制治療の治療指針作成委員会. 低濃度アトロピン点眼液を用いた近視進行抑制治療の手引き. 日眼会誌. 2025;129(10):851-854.
- 近視管理用眼鏡ガイドライン作成委員会. 近視管理用眼鏡(多分割レンズ)ガイドライン(第1版). 日眼会誌. 2025;129(10):855-860.
- Chamberlain P, Peixoto-de-Matos SC, Logan NS, et al. A 3-year randomized clinical trial of MiSight lenses for myopia control. Optom Vis Sci. 2019;96:556-567.
- Lam CSY, Tang WC, Tse DY, et al. Defocus incorporated multiple segments (DIMS) spectacle lenses slow myopia progression: a 2-year randomised clinical trial. Br J Ophthalmol. 2020;104:363-368.
- Si JK, Tang K, Bi HS, et al. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252-257.
- Kinoshita N, Konno Y, Hamada N, et al. Efficacy of combined orthokeratology and 0.01% atropine solution for slowing axial elongation in children with myopia: a 2-year randomized trial. Sci Rep. 2020;10:12750.
- Ueda E, Yasuda M, Fujiwara K, et al. Trends in the prevalence of myopia and myopic maculopathy in a Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2019;60:2781-2786.
