
درمان با نور قرمز (کاهش پیشرفت نزدیکبینی)
1. درمان با نور قرمز (کنترل پیشرفت نزدیکبینی) چیست؟
Section titled “1. درمان با نور قرمز (کنترل پیشرفت نزدیکبینی) چیست؟”درمان مکرر با نور قرمز با شدت کم (Repeated Low-Level Red Light Therapy: RLRL) یک روش درمانی غیرتهاجمی است که با تابش نور قرمز مرئی با طول موج مشخص (عمدتاً 650 تا 670 نانومتر) با شدت کم به چشم، از پیشرفت نزدیکبینی در کودکان جلوگیری میکند. پروتکل استاندارد شامل استفاده از یک دستگاه دستی مخصوص، جلسات 3 دقیقهای دو بار در روز، پنج روز در هفته است.
جایگاه درمان RLRL
Section titled “جایگاه درمان RLRL”درمان RLRL یک روش نسبتاً جدید برای کنترل پیشرفت نزدیکبینی است که شواهد آن از دهه ۲۰۲۰ به سرعت انباشته شده است. این روش به عنوان «گزینه چهارم» پس از سه درمان اصلی (قطره آتروپین با غلظت پایین، ارتوکراتولوژی و لنزهای تماسی چندکانونی) مورد توجه قرار گرفته است و بیشتر تحقیقات در شرق آسیا به ویژه چین انجام شده است.
نزدیکبینی عمدتاً ناشی از افزایش طول محور چشم است و هر ۱ میلیمتر افزایش طول محور معادل حدود ۳ دیوپتر نزدیکبینی است. مهار افزایش طول محور چشم مهمترین هدف مدیریت نزدیکبینی است و در ارزیابی اثربخشی درمان RLRL، تغییر طول محور چشم مهمترین نقطه پایانی محسوب میشود1).
عوارض عمده مرتبط با نزدیکبینی شامل جداشدگی شبکیه (افزایش ۳۰٪ خطر به ازای هر ۱- دیوپتر)، دژنراسیون ماکولای نزدیکبینی (افزایش ۵۸٪) و گلوکوم زاویه باز (افزایش ۲۰٪) است6). درمان RLRL به عنوان یک مداخله پیشگیرانه برای کاهش این خطرات بلندمدت در نظر گرفته میشود.
شیوع نزدیکبینی در کودکان آسیایی به ویژه بالا است و در صورت عدم درمان و پیشرفت به درجات بالا، خطر عوارض جدی مانند جداشدگی شبکیه و دژنراسیون ماکولای نزدیکبینی به طور قابل توجهی افزایش مییابد. تخمین زده میشود که به ازای هر ۱ دیوپتر افزایش نزدیکبینی، خطر جداشدگی شبکیه ۳۰٪، دژنراسیون ماکولای نزدیکبینی ۵۸٪، گلوکوم زاویه باز ۲۰٪ و آب مروارید زیرکپسولی خلفی ۲۱٪ افزایش مییابد6).
از آنجایی که افزایش ۱ میلیمتری طول محور چشم معادل حدود ۳ دیوپتر نزدیکبینی است، مهار افزایش طول محور مهمترین هدف مدیریت نزدیکبینی است. متاآنالیز Haarman و همکاران (۲۰۲۰) نشان میدهد که با افزایش شدت نزدیکبینی، خطر عوارض به صورت نمایی افزایش مییابد7) و مداخله در مراحل اولیه اهمیت زیادی در بهبود پیشآگهی بلندمدت دارد.
درمان RLRL به عنوان یکی از مداخلات کنترل پیشرفت نزدیکبینی در کنار ارتوکراتولوژی و قطره آتروپین با غلظت پایین، از دهه ۲۰۲۰ به سرعت شواهد خود را انباشته کرده است. در ژاپن نیز در برخی مراکز به عنوان درمان خودپرداخت معرفی شده است. مرور سیستماتیک Yam و همکاران (۲۰۲۵) شواهد مربوط به چندین مداخله کنترل پیشرفت نزدیکبینی از جمله RLRL را خلاصه کرده است5).
از سوی دیگر، Bullimore و همکاران (۲۰۲۱) به طور دقیق خطرات و مزایای کلی مدیریت نزدیکبینی را بررسی کرده و اشاره کردهاند که در درمان RLRL نیز در صورت انحراف از پارامترهای تابش، خطر سمیت نوری شبکیه وجود دارد6). رعایت مدیریت صحیح دستگاه، شدت تابش و مدت زمان تابش پیشنیاز استفاده ایمن است.
درمان RLRL یک درمان برای کاهش پیشرفت نزدیکبینی است که در آن نور قرمز مرئی در محدوده ۶۵۰ تا ۶۷۰ نانومتر با شدت کم (۰.۳ تا ۱ میلیوات بر سانتیمتر مربع) روزانه دو بار و هر بار به مدت ۳ دقیقه به چشم تابانده میشود. تصور میشود که این روش از طریق تعدیل زیستی نوری (photobiomodulation) ضخامت مشیمیه را افزایش داده و از افزایش طول محوری چشم جلوگیری میکند 3). در حال حاضر، این درمان در ژاپن تأیید نشده و به صورت خودپرداخت انجام میشود و باید تحت نظر پزشک متخصص استفاده شود.
۲. علائم اصلی و یافتههای بالینی
Section titled “۲. علائم اصلی و یافتههای بالینی”شاخصهای اثربخشی درمان
Section titled “شاخصهای اثربخشی درمان”اثربخشی درمان RLRL با استفاده از شاخصهای عینی زیر ارزیابی میشود:
- طول محوری چشم: اندازهگیری با دستگاه اندازهگیری طول محوری نوری. تغییرات قبل و بعد از درمان و هر ۶ ماه پیگیری میشود.
- ضخامت مشیمیه: اندازهگیری ضخامت مشیمیه زیر مرکزی (SFCT) با OCT. پس از تابش RLRL، افزایش ضخامت مشیمیه مشاهده میشود. در مطالعه پیگیری دو ساله Dong و همکاران (۲۰۲۳) افزایش ضخامت مشیمیه تأیید شد 2).
- معادل کروی عیب انکساری: ارزیابی عینی تحت فلج تطابقی.
- حدت بینایی اصلاحشده: تأیید پایداری حدت بینایی اصلاحشده قبل و بعد از درمان.
موارد احتیاط در ارزیابی ایمنی
Section titled “موارد احتیاط در ارزیابی ایمنی”درمان RLRL به دلیل شدت کم، عوارض جانبی کوتاهمدت کمی دارد، اما بررسی منظم موارد زیر ضروری است:
- خطر سمیت شبکیه: شدت، زمان و دفعات تابش بیش از حد میتواند از نظر تئوری باعث آسیب شبکیه شود 6). ارزیابی لایهای شبکیه و مشیمیه با OCT باید قبل از درمان به عنوان پایه ثبت و به طور منظم مقایسه شود.
- تغییرات بینایی و دید رنگی: بررسی وجود کاهش بینایی یا اختلال دید رنگی در طول درمان.
- علائم ذهنی: توجه به شکایاتی مانند خیرگی، پستصویر یا اختلال میدان بینایی.
۳. علل و عوامل خطر
Section titled “۳. علل و عوامل خطر”عوامل خطر پیشرفت نزدیکبینی
Section titled “عوامل خطر پیشرفت نزدیکبینی”عوامل خطر زیر در پیشرفت نزدیکبینی که هدف درمان RLRL است، نقش دارند.
- شروع در سنین پایین (به ویژه در سن ۶ تا ۱۲ سالگی)
- نزدیکبینی والدین (به ویژه هر دو والد)
- مدت زمان طولانی کار نزدیک (بیش از ۳ ساعت در روز)
- کمبود فعالیت در فضای باز (کمتر از ۱ ساعت در روز)
- نژاد آسیایی (شیوع در جمعیتهای آسیای شرقی بالاترین است)
- پیشبینی هولدن و همکاران (۲۰۱۶) نشان میدهد که تا سال ۲۰۵۰ حدود ۵۰٪ از جمعیت جهان نزدیکبین خواهند شد8) و اهمیت اجتماعی مداخله زودهنگام در حال افزایش است.
۴. تشخیص و روشهای آزمایش
Section titled “۴. تشخیص و روشهای آزمایش”ارزیابی قبل از شروع درمان
Section titled “ارزیابی قبل از شروع درمان”قبل از شروع درمان RLRL، آزمایشهای زیر برای ثبت خط پایه و تأیید اندیکاسیون انجام میشود.
| اقلام آزمایش | هدف | موارد اصلی تأیید |
|---|---|---|
| معاینه انکساری تحت سیکلوپلژی | ارزیابی عینی درجه نزدیکبینی | معادل کروی و میزان آستیگماتیسم |
| اندازهگیری طول محوری چشم | تعیین خط پایه و پایش پیشرفت | اندازهگیری با طولسنج محوری نوری |
| معاینه فوندوس | وضعیت شبکیه و مشیمیه قبل از درمان | بررسی تغییرات نزدیکبینی شدید |
| OCT (ماکولا و عصب بینایی) | تعیین مقادیر پایه برای سمیت شبکیه | ضخامت لایههای شبکیه و مشیمیه |
| معاینه با لامپ شکاف | رد بیماریهای بخش قدامی چشم | التهاب فعال و آب مروارید |
برای انجام معاینه تحت فلج تطابقی در کودکان خردسال، استفاده از قطرههای فلج کننده تطابق (مانند سایپلژین ۱٪) ضروری است. اگر تنها از معاینه ذهنی بدون فلج تطابقی استفاده شود، ممکن است درجه نزدیکبینی بیش از حد محاسبه شود.
پایش در طول درمان
Section titled “پایش در طول درمان”برای تأیید اثربخشی و ایمنی درمان، برنامه زمانی زیر توصیه میشود:
| زمان | اقدامات |
|---|---|
| ۱ ماه پس از شروع | بررسی پایبندی به قطرهها، علائم ذهنی، و حدت بینایی اصلاح شده |
| هر ۳ تا ۶ ماه | اندازهگیری طول محوری چشم، انکسار تحت فلج تطابقی، OCT (ارزیابی ضخامت مشیمیه و شبکیه) |
| هر سال | معاینه فوندوس با گشاد کردن مردمک، آنژیوگرافی OCT (اختیاری) |
ثبت مقادیر پایه با استفاده از معاینه انکساری تحت فلج تطابقی و اندازهگیری طول محوری چشم با روش نوری ضروری است. همچنین وضعیت شبکیه و مشیمیه قبل از درمان با معاینه فوندوس و OCT ثبت میشود تا در پایش ایمنی در طول درمان استفاده شود. در صورت مشکوک بودن به نزدیکبینی شدید، وجود دژنراسیون یا پارگی در شبکیه محیطی نیز بررسی میشود.
۵. روشهای استاندارد درمان
Section titled “۵. روشهای استاندارد درمان”رضایت آگاهانه و ارزیابی اندیکاسیون قبل از درمان
Section titled “رضایت آگاهانه و ارزیابی اندیکاسیون قبل از درمان”موارد اساسی برای انتخاب بیماران واجد شرایط درمان RLRL در زیر آورده شده است.
موارد توصیه شده:
- سن ۶ تا ۱۸ سال (بیشتر مطالعات این گروه سنی را هدف قرار دادهاند)
- نزدیکبینی کروی معادل ≥ ۰.۵- دیوپتر با پیشرفت تأیید شده
- نزدیکبینی تأیید شده با معاینه تحت سیکلوپلژی
- محیطی که والدین بتوانند مدیریت مناسب را انجام دهند
موقعیتهایی که باید با احتیاط تصمیمگیری شود:
- موارد با سابقه یا سابقه خانوادگی بیماری شبکیه
- بیماریهای حساس به نور (مانند خشکی پوست پیگمانته، حساسیت پوستی به نور)
- استفاده از داروهای حساس به نور
موقعیتهایی که باید از مصرف خودداری شود:
- بیماری فعال شبکیه (مانند دژنراسیون شبکیه، عروق جدید)
- بیماران با تشخیص قطعی حساسیت به نور
پروتکل درمان
Section titled “پروتکل درمان”پارامترهای استاندارد درمانی اتخاذ شده در کارآزماییهای بالینی تصادفی اصلی در زیر آورده شده است.
| پارامتر | مقدار استاندارد | توضیحات |
|---|---|---|
| طول موج | 650 نانومتر (نور مرئی قرمز) | در برخی مطالعات از 670 نانومتر استفاده شده است |
| شدت تابش | 0.3 تا 1 میلیوات بر سانتیمتر مربع | نور غیرهمدوس و غیرلیزری |
| مدت تابش | 3 دقیقه در هر جلسه | دو بار در روز (صبح و عصر) |
| تعداد جلسات درمانی | 5 روز در هفته (فقط روزهای مدرسه) | — |
| مدت درمان | ۱۲ تا ۲۴ ماه یا بیشتر | نیاز به حفظ اثر در طول درمان |
دستگاههای مورد استفاده عمدتاً دستگاههای دستی مخصوص ساخت چین (مانند Suneye) هستند که در تحقیقات به کار رفتهاند. این دستگاهها به گونهای طراحی شدهاند که بیمار بتواند در خانه از آنها استفاده کند، اما تنظیم اولیه و بررسی دورهای باید توسط پزشک متخصص انجام شود.
نتایج کارآزماییهای بالینی تصادفیسازی شده اصلی
Section titled “نتایج کارآزماییهای بالینی تصادفیسازی شده اصلی”در کارآزمایی بالینی تصادفیسازی شده یکساله توسط Jiang و همکاران (۲۰۲۲)، در گروه RLRL افزایش طول محوری چشم ۰.۱۰ میلیمتر در سال (در گروه کنترل ۰.۳۸ میلیمتر در سال) بود که نشاندهنده مهار قابل توجهی است1). پیگیری دو ساله توسط Dong و همکاران (۲۰۲۳) نیز نشان داد که اثر مهار افزایش طول محوری چشم پایدار بوده و ضخامت مشیمیه افزایش یافته است2).
در کارآزمایی بالینی تصادفیسازی شده چندمرکزی توسط Zeng و همکاران (۲۰۲۳)، پیشرفت معادل کروی در یک سال در گروه درمان ۰.۲۰- دیوپتر (در گروه کنترل ۰.۷۱- دیوپتر) بود که نشاندهنده مهار حدود ۷۲٪ از پیشرفت نزدیکبینی است4).
مقایسه اثربخشی درمان RLRL با سایر روشهای مهار پیشرفت نزدیکبینی:
| مداخله | میزان مهار تغییرات انکساری | میزان مهار افزایش طول محوری | شواهد اصلی |
|---|---|---|---|
| درمان RLRL | ۷۲٪ (Zeng 2023) | ۷۴٪ (Jiang 2022) | چندین کارآزمایی بالینی تصادفیسازی شده |
| آتروپین با غلظت پایین 0.05% | حداکثر 67% | — | مطالعه LAMP |
| اورتوکراتولوژی | — | 43% | متاآنالیز Si 2015 |
| MiSight (لنز تماسی چندکانونی) | 59% | 52% | Chamberlain 2019 |
| عینک DIMS | 55 تا 59% | 37 تا 38% | کارآزمایی بالینی تصادفی Lam 2020 |
با این حال، به دلیل تفاوت در طراحی مطالعه، سن شرکتکنندگان و مدت درمان، در مقایسه مستقیم باید احتیاط کرد 5). قطره آتروپین با غلظت پایین (Rijusea® Mini 0.025%) تنها داروی تأیید شده در ژاپن از دسامبر 2024 است 9) و لنزهای عینک مدیریت نزدیکبینی (مانند DIMS) 10) نیز توسط دستورالعمل انجمن نزدیکبینی ژاپن توصیه میشوند. درمان RLRL به عنوان گزینهای برای ترکیب با این مداخلات تأیید شده در نظر گرفته میشود.
در مقایسه با دادههای کارآزمایی بالینی تصادفیشده 3 ساله MiSight (لنز تماسی چندکانونی) 11)، کارآزمایی 2 ساله عینک DIMS 12)، متاآنالیز ارتوکراتولوژی 13) و کارآزمایی ترکیبی ارتوکراتولوژی + آتروپین 14)، نرخ مهار کوتاهمدت درمان RLRL مطلوب است، اما بزرگترین چالش عدم وجود دادههای بیش از 5 سال است. روند افزایش دژنراسیون ماکولای نزدیکبینی در ژاپنیها که توسط مطالعه Hisayama 15) نشان داده شده است، اهمیت پزشکی مداخلات مدیریت نزدیکبینی از جمله درمان RLRL را بیشتر تأیید میکند.
ترکیب با سایر درمانها
Section titled “ترکیب با سایر درمانها”- RLRL + آتروپین با غلظت پایین: از آنجایی که مکانیسم اثر این دو متفاوت است، اثر افزایشی یا همافزایی مورد انتظار است، اما تأیید آن در کارآزماییهای تصادفیشده در مقیاس بزرگ ادامه دارد 5).
- RLRL + ارتوکراتولوژی: به عنوان ترکیبی برای موارد پیشرفت سریع گزارش شده است.
- در صورت ناکافی بودن اثر درمان به تنهایی، ترکیب با سایر درمانهای مهار پیشرفت نزدیکبینی در نظر گرفته میشود.
رضایت آگاهانه
Section titled “رضایت آگاهانه”از آوریل 2026، درمان RLRL در ژاپن تأیید نشده و تحت پوشش بیمه نیست و به عنوان درمان خصوصی ارائه میشود. لازم است موارد زیر به طور کامل برای بیمار و والدین توضیح داده شود و رضایت کسب شود.
- این درمان در ژاپن تأیید نشده است.
- شواهد فعلی عمدتاً مبتنی بر مطالعات مشاهدهای 1 تا 2 ساله است و ایمنی طولانیمدت هنوز ثابت نشده است.
- از نظر تئوری، خطر سمیت شبکیه در صورت انحراف از پارامترهای تابش وجود دارد 6).
- این درمان «درمان» نزدیکبینی نیست، بلکه «مهار پیشرفت» است.
- مراجعه منظم به چشمپزشکی و پایش ایمنی ضروری است.
تا آوریل 2026، درمان RLRL در ژاپن تأییدیه دارویی و پوشش بیمهای ندارد. در برخی کلینیکهای چشمپزشکی به عنوان درمان خصوصی ارائه میشود و هنگام مراجعه، بررسی کافی در مورد اندیکاسیون، ایمنی و هزینه توسط متخصص ضروری است. قطره آتروپین با غلظت پایین (Rijusea® Mini 0.025%) به عنوان اولین داروی تأیید شده برای کنترل پیشرفت نزدیکبینی در دسامبر 2024 در ژاپن، یک گزینه درمانی تحت پوشش بیمه است.
جایگاه RLRL در مکانیسم مهار پیشرفت نزدیکبینی
Section titled “جایگاه RLRL در مکانیسم مهار پیشرفت نزدیکبینی”در حالی که مداخلات نوری اصلی برای مهار پیشرفت نزدیکبینی (ارتوکراتولوژی، عینک DIMS، لنزهای تماسی چندکانونی) بر اساس «فرضیه دسفوكوس محیطی میوپیک» عمل میکنند، درمان RLRL از طریق مسیر کاملاً متفاوتی شامل فعالسازی میتوکندری از طریق تعدیل نوری زیستی (PBM) → بهبود جریان خون مشیمیه → ضخیمشدن مشیمیه → مهار افزایش طول محوری چشم عمل میکند. این مکانیسم متفاوت منجر به انتظار اثر همافزایی در ترکیب با سایر درمانها شده است3).
همچنین، یکی از ویژگیهای منحصربهفرد درمان RLRL، مشاهده پاسخ فیزیولوژیک حاد به صورت افزایش فوری ضخامت مشیمیه پس از درمان است2). این ویژگی در سایر درمانهای مهار پیشرفت نزدیکبینی دیده نمیشود و اندازهگیری ضخامت مشیمیه به عنوان شاخص اثر فوری درمان مفید تلقی میشود.
6. پاتوفیزیولوژی و مکانیسم دقیق بروز بیماری
Section titled “6. پاتوفیزیولوژی و مکانیسم دقیق بروز بیماری”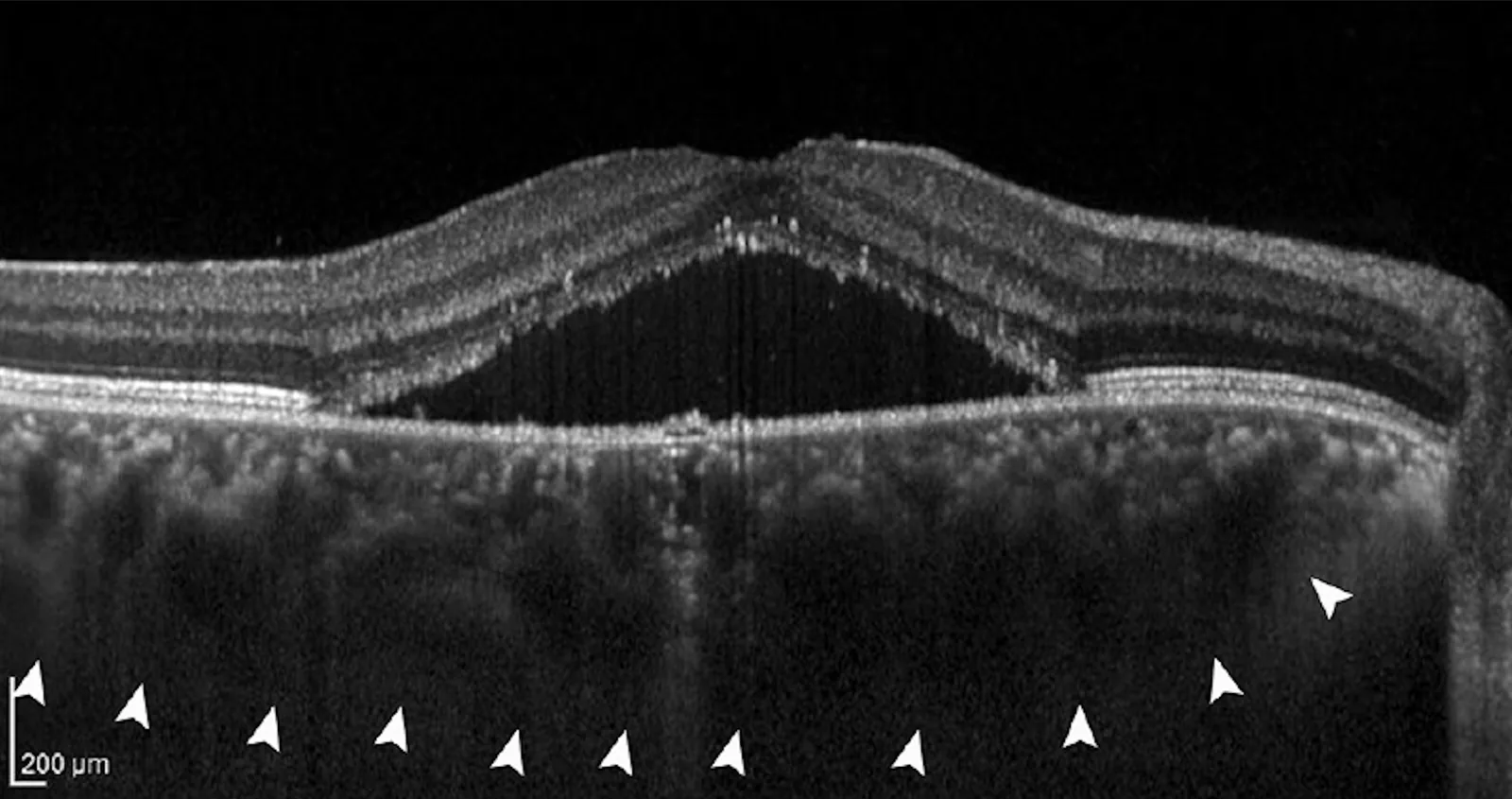
تعدیل نوری زیستی (Photobiomodulation: PBM)
Section titled “تعدیل نوری زیستی (Photobiomodulation: PBM)”مکانیسم اصلی درمان RLRL، تعدیل نوری زیستی (PBM) است3). نور قرمز در محدوده 650-670 نانومتر به طور اختصاصی توسط سیتوکروم اکسیداز (کمپلکس IV) در میتوکندری سلولها جذب شده و پاسخهای بیولوژیکی زیر را القا میکند:
- افزایش تولید ATP
- فعالسازی سیگنالهای سلولی از طریق تولید متعادل گونههای فعال اکسیژن (ROS)
- اتساع عروق و افزایش جریان خون از طریق آزادسازی نیتریک اکسید (NO)
- بهبود گردش خون مشیمیه و ضخیم شدن آن
افزایش ضخامت مشیمیه و مهار افزایش طول محوری چشم
Section titled “افزایش ضخامت مشیمیه و مهار افزایش طول محوری چشم”به طور مداوم مشاهده شده است که ضخامت مشیمیه پس از تابش RLRL افزایش مییابد2)3). تصور میشود که افزایش ضخامت مشیمیه بر سفتی دیواره چشم تأثیر گذاشته و به مهار افزایش طول محوری کمک میکند. افزایش ضخامت مشیمیه در ارتوکراتولوژی و آتروپین با غلظت پایین نیز گزارش شده است و توجه به این موضوع جلب شده است که مشیمیه ممکن است مسیر مشترکی برای مهار پیشرفت نزدیکبینی باشد.
مکانیسم اصلی پیشرفت نزدیکبینی
Section titled “مکانیسم اصلی پیشرفت نزدیکبینی”پیشرفت نزدیکبینی یک فرآیند بیولوژیکی است که در آن رشد چشم از طریق انتقال سیگنال از شبکیه به صلبیه تنظیم میشود و فرآیندهای زیر در آن نقش دارند.
- فوکوس پیرامونی هایپروپیک به عنوان سیگنال محرک افزایش طول محوری عمل میکند
- سیگنال مهار رشد از طریق دوپامین، افزایش طول محوری را مهار میکند
- بازسازی ماتریکس خارج سلولی صلبیه، طول محوری چشم را تعیین میکند
- ضخیم شدن یا نازک شدن مشیمیه به عنوان نشانگر زیستی تغییرات طول محوری عمل میکند
درمان RLRL با مداخله در این انتقال سیگنال، رشد چشم را در سطح مشیمیه و صلبیه مهار میکند، اما تصویر کامل هنوز تا حد زیادی ناشناخته است3). خطر کمی عوارض نزدیکبینی که توسط متاآنالیز Haarman و همکاران (2020) نشان داده شده است، به طور گسترده به عنوان مبنای پزشکی برای مداخله درمانی ذکر میشود7).
7. تحقیقات جدید و چشماندازهای آینده
Section titled “7. تحقیقات جدید و چشماندازهای آینده”ایجاد دادههای اثربخشی و ایمنی بلندمدت
Section titled “ایجاد دادههای اثربخشی و ایمنی بلندمدت”کارآزماییهای تصادفیسازی شده اصلی فعلی دوره پیگیری ۱ تا ۲ ساله دارند و دادههای بلندمدت بیش از ۵ سال محدود است 1)2). تداوم اثر پس از قطع درمان (اثر باقیمانده) نیز هنوز به اثبات نرسیده است و مطالعاتی برای پیگیری تغییرات سرعت پیشرفت نزدیکبینی پس از پایان درمان در حال انجام است.
در مطالعه پیگیری دو ساله Dong و همکاران (۲۰۲۳)، گروه درمان با RLRL در مقایسه با گروه کنترل، مهار مداوم افزایش طول محوری چشم و افزایش ضخامت مشیمیه را نشان داد و تداوم اثر با استفاده یک ساله تأیید شد 2). با این حال، به دلیل تفاوت در طراحی مطالعه، پارامترهای تابش و سن شرکتکنندگان بین مطالعات، مقایسه مستقیم نیازمند احتیاط است.
کمیسازی خطر سمیت شبکیه
Section titled “کمیسازی خطر سمیت شبکیه”از نظر تئوری، شدت، مدت و دفعات بیش از حد تابش میتواند باعث آسیب شبکیه شود. در ارزیابی خطر-فایده مدیریت نزدیکبینی توسط Bullimore و همکاران (۲۰۲۱)، تعادل ایمنی کلی مداخلات نوری و دارویی از جمله درمان RLRL مورد بحث قرار گرفته و بر اهمیت مدیریت مناسب پارامترها تأکید شده است 6).
مطالعاتی با هدف تعیین حد مجاز تابش ایمن و ارزیابی خطر در حال انجام است. در عمل بالینی، رعایت دقیق شدت تابش (۰.۳ تا ۱ میلیوات بر سانتیمتر مربع)، مدت تابش (۳ دقیقه در هر جلسه) و دفعات تابش (۲ بار در روز، ۵ روز در هفته) و کالیبراسیون منظم دستگاه ضروری است.
از نظر سمیت نوری، میزان تجمعی قرار گرفتن در معرض نور برای سلولهای بینایی و اپیتلیوم رنگدانه شبکیه مهم است و تابش بیش از حد توصیه شده (به ویژه استفاده نادرست با شدت بالا و مدت طولانی) نیازمند احتیاط است. همانطور که متاآنالیز عوارض نزدیکبینی توسط Haarman و همکاران (۲۰۲۰) نشان میدهد 7)، با فرض اینکه مدیریت مناسب نزدیکبینی میتواند خطر عوارض جدی را کاهش دهد، ارزیابی فردی خطر-فایده درمان RLRL مهم است.
مقایسه مستقیم با آتروپین با غلظت پایین و ارتوکراتولوژی
Section titled “مقایسه مستقیم با آتروپین با غلظت پایین و ارتوکراتولوژی”کارآزماییهای تصادفیسازی شده مقایسه مستقیم درمان RLRL با ارتوکراتولوژی و آتروپین با غلظت پایین در حال انجام است. انتظار میرود با در نظر گرفتن مزایا و معایب هر درمان، پروتکل مدیریت نزدیکبینی فردیسازی شده ایجاد شود 5).
مقایسه ویژگیهای سه مداخله اصلی (RLRL، ارتوکراتولوژی و آتروپین با غلظت پایین):
| مداخله | میزان مهار افزایش طول محوری | تهاجمی بودن | سهولت استفاده | وضعیت نظارتی در ژاپن |
|---|---|---|---|---|
| درمان RLRL | حدود ۶۰ تا ۷۲٪ | غیرتهاجمی | قابل انجام در منزل | تأیید نشده (خودپرداخت) |
| ارتوکراتولوژی | ۳۰ تا ۵۰٪ | تماس با قرنیه دارد | استفاده در شب | تأیید نشده (خودپرداخت) |
| آتروپین با غلظت پایین ۰٫۰۲۵٪ | حدود ۶۲٪ | قطره چشمی | قطره قبل از خواب | تأیید شده |
پیشبینی پیشرفت نزدیکبینی با استفاده از هوش مصنوعی
Section titled “پیشبینی پیشرفت نزدیکبینی با استفاده از هوش مصنوعی”مدلهایی در حال توسعه هستند که دادههای طول محوری چشم، عوامل خطر و پاسخ به درمان را با هوش مصنوعی تحلیل کرده و برای هر بیمار بهترین استراتژی درمانی را پیشنهاد میکنند. این مدلها ممکن است برای پیشبینی پاسخدهندگان به درمان RLRL نیز به کار روند.
روندهای مربوط به تأیید داخلی
Section titled “روندهای مربوط به تأیید داخلی”با انباشت شواهد در چین و جنوب شرق آسیا، احتمال دارد که گفتگو با نهادهای نظارتی در ژاپن نیز آغاز شود. اجرای کارآزماییهای بالینی تصادفی چندمرکزی داخلی و روند تأیید دارویی مورد توجه است. با توجه به افزایش جمعیت نزدیکبین در جهان (Holden 2016: ۴٫۹ میلیارد نفر تا سال ۲۰۵۰ 8))، درمان RLRL به عنوان یکی از گزینههای مدیریت نزدیکبینی مطرح میشود.
۸. منابع
Section titled “۸. منابع”- Jiang Y, Zhu Z, Tan X, et al. Effect of repeated low-level red-light therapy for myopia control in children: a multicenter randomized controlled trial. Ophthalmology. 2022;129:509-519.
- Dong J, Zhu Z, Xu H, et al. Myopia control effect of repeated low-level red-light therapy in Chinese children: a randomized, double-blind, controlled clinical trial. Ophthalmology. 2023;130:198-204.
- Wang W, Jiang Y, Zhu Z, et al. Chorioidal thickening as a potential therapeutic target in myopia management: a review of repeated low-level red light therapy. Surv Ophthalmol. 2023;68:1-12.
- Zeng J, Liu Y, Wang Z, et al. Efficacy of repeated low-level red-light stimulation on slowing myopia progression and ocular growth in children with myopia: a randomized controlled trial. Transl Vis Sci Technol. 2023;12:22.
- Yam JC, Zhang XJ, Zhang Y, et al. Interventions to reduce incidence and progression of myopia in children and adults. Prog Retin Eye Res. 2025.
- Bullimore MA, Ritchey ER, Shah S, et al. The risks and benefits of myopia control. Ophthalmology. 2021;128:1561-1579.
- Haarman AEG, Enthoven CA, Tideman JWL, et al. The complications of myopia: a review and meta-analysis. Invest Ophthalmol Vis Sci. 2020;61:49.
- Holden BA, Fricke TR, Wilson DA, et al. Global prevalence of myopia and high myopia and temporal trends from 2000 through 2050. Ophthalmology. 2016;123:1036-1042.
- 低濃度アトロピン点眼液を用いた近視進行抑制治療の治療指針作成委員会. 低濃度アトロピン点眼液を用いた近視進行抑制治療の手引き. 日眼会誌. 2025;129(10):851-854.
- 近視管理用眼鏡ガイドライン作成委員会. 近視管理用眼鏡(多分割レンズ)ガイドライン(第1版). 日眼会誌. 2025;129(10):855-860.
- Chamberlain P, Peixoto-de-Matos SC, Logan NS, et al. A 3-year randomized clinical trial of MiSight lenses for myopia control. Optom Vis Sci. 2019;96:556-567.
- Lam CSY, Tang WC, Tse DY, et al. Defocus incorporated multiple segments (DIMS) spectacle lenses slow myopia progression: a 2-year randomised clinical trial. Br J Ophthalmol. 2020;104:363-368.
- Si JK, Tang K, Bi HS, et al. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252-257.
- Kinoshita N, Konno Y, Hamada N, et al. Efficacy of combined orthokeratology and 0.01% atropine solution for slowing axial elongation in children with myopia: a 2-year randomized trial. Sci Rep. 2020;10:12750.
- Ueda E, Yasuda M, Fujiwara K, et al. Trends in the prevalence of myopia and myopic maculopathy in a Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2019;60:2781-2786.
