
Terapia com Luz Vermelha (Inibição da Progressão da Miopia)
1. O que é a Terapia com Luz Vermelha (Supressão da Progressão da Miopia)?
Seção intitulada “1. O que é a Terapia com Luz Vermelha (Supressão da Progressão da Miopia)?”A Terapia com Luz Vermelha de Baixa Intensidade Repetida (Repeated Low-Level Red Light Therapy: RLRL) é um tratamento não invasivo que suprime a progressão da miopia em crianças ao irradiar o olho com luz vermelha visível de comprimento de onda específico (principalmente 650-670 nm) em baixa intensidade. O protocolo padrão utiliza um dispositivo portátil dedicado, com sessões de 3 minutos duas vezes ao dia, 5 dias por semana.
Posicionamento da Terapia RLRL
Seção intitulada “Posicionamento da Terapia RLRL”A terapia RLRL é uma terapia relativamente nova para retardar a progressão da miopia, com evidências acumuladas rapidamente desde a década de 2020. É considerada a “quarta opção” após as três principais terapias convencionais (colírio de atropina em baixa concentração, ortoceratologia e lentes de contato multifocais), e a maioria das pesquisas é realizada no Leste Asiático, especialmente na China.
A miopia é causada principalmente pelo alongamento do eixo axial do olho, onde cada 1 mm de alongamento corresponde a aproximadamente 3 D de miopia. Suprimir o alongamento axial é o objetivo mais importante no gerenciamento da miopia, e a mudança no comprimento axial é o endpoint mais importante na avaliação da eficácia da terapia RLRL 1).
As principais complicações associadas à miopia incluem descolamento de retina (risco aumenta 30% por -1 D), degeneração macular miópica (aumenta 58%) e glaucoma de ângulo aberto (aumenta 20%) 6). A terapia RLRL é posicionada como uma intervenção preventiva para reduzir esses riscos de longo prazo.
Em crianças asiáticas, a prevalência de miopia é particularmente alta e, se não tratada e se tornar alta, o risco de complicações graves, como descolamento de retina e degeneração macular miópica, aumenta significativamente. Estima-se que cada aumento de 1 D aumenta o risco de descolamento de retina em 30%, degeneração macular miópica em 58%, glaucoma de ângulo aberto em 20% e catarata subcapsular posterior em 21% 6).
Como o alongamento axial de 1 mm corresponde a aproximadamente 3 D de miopia, suprimir o alongamento axial é o objetivo mais importante no gerenciamento da miopia. A meta-análise de Haarman et al. (2020) 7) mostrou que o risco de complicações aumenta exponencialmente com a gravidade da miopia, portanto, a intervenção em estágios leves tem grande significado na melhora do prognóstico de longo prazo.
A terapia RLRL é uma das intervenções para retardar a progressão da miopia, juntamente com a ortoceratologia e o colírio de atropina em baixa concentração, e as evidências têm se acumulado rapidamente desde a década de 2020. No Japão, foi introduzida em algumas instalações como tratamento particular. Na revisão sistemática de Yam et al. (2025), as evidências de várias intervenções para retardar a progressão da miopia, incluindo a terapia RLRL, foram resumidas 5).
Por outro lado, Bullimore et al. (2021) examinaram detalhadamente os riscos e benefícios do gerenciamento geral da miopia e apontaram que existe risco de fototoxicidade retiniana na terapia RLRL quando os parâmetros de irradiação se desviam 6). A adesão ao gerenciamento adequado do dispositivo, intensidade de irradiação e tempo de irradiação é pré-requisito para o uso seguro.
A terapia RLRL é um tratamento para inibir a progressão da miopia, que consiste em irradiar o olho com luz vermelha visível na faixa de 650-670 nm em baixa intensidade (0,3-1 mW/cm²) por 3 minutos, duas vezes ao dia. Acredita-se que aumente a espessura da coroide através da fotobiomodulação e iniba o alongamento axial 3). Atualmente, não é aprovado no Japão e é um serviço médico privado, utilizado sob supervisão de um especialista.
2. Principais Sintomas e Achados Clínicos
Seção intitulada “2. Principais Sintomas e Achados Clínicos”Indicadores de Eficácia do Tratamento
Seção intitulada “Indicadores de Eficácia do Tratamento”A eficácia da terapia RLRL é avaliada usando os seguintes indicadores objetivos:
- Comprimento axial: Medido por um dispositivo de medição de comprimento axial óptico. As alterações são acompanhadas antes e depois do tratamento e a cada 6 meses.
- Espessura da coroide: Medição da espessura da coroide subfoveal (SFCT) por OCT. Observa-se aumento da espessura da coroide após a irradiação com RLRL. Um estudo de acompanhamento de 2 anos por Dong et al. (2023) confirmou o aumento da espessura da coroide 2).
- Equivalente esférico: Avaliação objetiva sob cicloplegia.
- Acuidade visual corrigida: Confirmação da estabilidade da acuidade visual corrigida antes e depois do tratamento.
Notas sobre Avaliação de Segurança
Seção intitulada “Notas sobre Avaliação de Segurança”Embora a terapia RLRL seja de baixa intensidade e eventos adversos de curto prazo sejam raros, os seguintes pontos devem ser verificados regularmente:
- Risco de toxicidade retiniana: Intensidade, duração ou frequência excessivas de irradiação podem teoricamente causar lesão retiniana 6). A avaliação das camadas da retina e coroide por OCT deve ser registrada como linha de base antes do tratamento e comparada regularmente.
- Alterações na acuidade visual e visão de cores: Verificar a presença de diminuição da acuidade visual ou anormalidades na visão de cores durante o tratamento.
- Sintomas subjetivos: Atenção a queixas como ofuscamento, pós-imagem ou anormalidades no campo visual.
3. Causas e Fatores de Risco
Seção intitulada “3. Causas e Fatores de Risco”Fatores de Risco para Progressão da Miopia
Seção intitulada “Fatores de Risco para Progressão da Miopia”Os seguintes fatores de risco estão envolvidos na progressão da miopia, alvo do tratamento com RLRL:
- Início precoce (especialmente entre 6 e 12 anos de idade)
- Ambos os pais míopes (especialmente se ambos forem míopes)
- Longo tempo de trabalho de perto (mais de 3 horas por dia)
- Falta de tempo de atividade ao ar livre (menos de 1 hora por dia)
- Etnia asiática (maior prevalência entre asiáticos do Leste)
- A previsão de Holden et al. (2016) de que cerca de 50% da população mundial será míope em 20508) aumenta a importância social da intervenção precoce.
4. Diagnóstico e Métodos de Exame
Seção intitulada “4. Diagnóstico e Métodos de Exame”Avaliação Antes do Início do Tratamento
Seção intitulada “Avaliação Antes do Início do Tratamento”Antes de iniciar a terapia RLRL, registre a linha de base e confirme as indicações por meio dos seguintes exames:
| Item de Exame | Objetivo | Principais Pontos de Confirmação |
|---|---|---|
| Exame de refração sob cicloplegia | Avaliação objetiva do grau de miopia | Equivalente esférico e quantidade de astigmatismo |
| Medição do comprimento axial do olho | Estabelecimento da linha de base e monitoramento da progressão | Medido por biometria óptica |
| Exame de fundo de olho | Condição da retina e coroide antes do tratamento | Confirmação de alterações de miopia alta |
| OCT (mácula e nervo óptico) | Estabelecimento de valores de referência para toxicidade retiniana | Espessura das camadas da retina e coroide |
| Exame com lâmpada de fenda | Exclusão de doenças do segmento anterior | Inflamação ativa e catarata |
Para o exame sob cicloplegia, em crianças pequenas, é indispensável o uso de colírios cicloplégicos (como Cyplegin 1%). Se apenas o exame subjetivo for realizado sem cicloplegia, pode ser calculado um grau excessivo de miopia.
Monitoramento durante o tratamento
Seção intitulada “Monitoramento durante o tratamento”Para confirmar a eficácia e segurança do tratamento, recomenda-se o seguinte cronograma.
| Período | Conteúdo |
|---|---|
| 1 mês depois | Adesão ao colírio, confirmação de sintomas subjetivos, acuidade visual corrigida |
| A cada 3-6 meses | Medição do comprimento axial, refração sob cicloplegia, OCT (espessura coroidal, avaliação da retina) |
| A cada ano | Exame de fundo de olho com dilatação, OCT angiografia (opcional) |
É essencial registrar os valores basais com exame de refração sob cicloplegia e medição do comprimento axial óptico. Além disso, registre a condição da retina e coroide antes do tratamento com exame de fundo de olho e OCT, e utilize para monitoramento de segurança durante o tratamento. Se houver suspeita de miopia alta, verifique também a presença de degeneração ou rasgo retiniano periférico.
5. Métodos de tratamento padrão
Seção intitulada “5. Métodos de tratamento padrão”Consentimento informado e avaliação de adequação antes do tratamento
Seção intitulada “Consentimento informado e avaliação de adequação antes do tratamento”Abaixo estão os fundamentos para selecionar pacientes elegíveis para a terapia RLRL.
Indicações recomendadas:
- Idade de 6 a 18 anos (a maioria dos estudos incluiu essa faixa etária)
- Miopia esférica equivalente de −0,5 D ou mais com progressão confirmada
- Miopia confirmada sob exame com cicloplegia
- Ambiente onde os pais podem realizar o manejo adequado
Situações que requerem avaliação cuidadosa:
- Casos com histórico ou histórico familiar de doenças retinianas
- Doenças fotossensíveis (ex.: xeroderma pigmentoso, fotossensibilidade cutânea)
- Uso de medicamentos que causam fotossensibilidade
Situações a evitar:
- Doenças retinianas ativas (ex.: degeneração retiniana, neovascularização)
- Pacientes com diagnóstico confirmado de fotossensibilidade
Protocolo de Tratamento
Seção intitulada “Protocolo de Tratamento”Abaixo estão os parâmetros de tratamento padrão adotados nos principais RCTs.
| Parâmetro | Valor Padrão | Observações |
|---|---|---|
| Comprimento de onda | 650 nm (luz visível vermelha) | Alguns ensaios usam 670 nm |
| Intensidade de irradiação | 0,3–1 mW/cm² | Luz não coerente, não laser |
| Duração da irradiação | 3 min/sessão | 2 vezes ao dia (manhã e tarde) |
| Frequência do tratamento | 5 dias/semana (apenas dias letivos) | — |
| Duração do tratamento | 12 a 24 meses ou mais | Necessidade de manter o efeito contínuo |
Dispositivos portáteis dedicados fabricados na China (como Suneye) foram usados principalmente em pesquisas. Eles são projetados para que o paciente possa realizar a auto-irradiação em casa, mas a configuração inicial e as verificações periódicas são feitas por um especialista.
Resultados dos Principais Ensaios Clínicos Randomizados
Seção intitulada “Resultados dos Principais Ensaios Clínicos Randomizados”Em um ensaio clínico randomizado de um ano conduzido por Jiang et al. (2022), o grupo RLRL apresentou inibição significativa do alongamento axial de 0,10 mm/ano (grupo controle 0,38 mm/ano)1). O acompanhamento de dois anos por Dong et al. (2023) também confirmou o efeito sustentado de inibição do alongamento axial e aumento da espessura coroidal2).
O ensaio clínico randomizado multicêntrico de Zeng et al. (2023) mostrou progressão do equivalente esférico de um ano de −0,20 D no grupo de tratamento (grupo controle −0,71 D), inibindo a progressão da miopia em cerca de 72%4).
Comparação da Eficácia da Terapia RLRL com Outros Métodos de Inibição da Progressão da Miopia:
| Intervenção | Taxa de inibição refrativa | Taxa de inibição axial | Evidência principal |
|---|---|---|---|
| Terapia RLRL | 72% (Zeng 2023) | 74% (Jiang 2022) | Múltiplos ensaios clínicos randomizados |
| Atropina de baixa concentração 0,05% | Até 67% | — | Ensaio LAMP |
| Ortoceratologia | — | 43% | Meta-análise de Si 2015 |
| MiSight (lentes de contato multifocais) | 59% | 52% | Chamberlain 2019 |
| Óculos DIMS | 55-59% | 37-38% | Lam 2020 ECR |
No entanto, devido às diferenças no desenho do estudo, idade alvo e duração do tratamento, é necessário cuidado na comparação direta 5). O colírio de atropina em baixa concentração (Rijusea® Mini 0,025%) é o único medicamento aprovado no Japão em dezembro de 2024 9), e as lentes de óculos para gerenciamento da miopia (como DIMS) 10) também são recomendadas pelas diretrizes da Sociedade Japonesa de Miopia. A terapia RLRL está sendo posicionada como uma opção a ser combinada com essas intervenções aprovadas.
Comparado com dados do ensaio de 3 anos do MiSight (lentes de contato multifocais) 11), do ensaio de 2 anos dos óculos DIMS 12), da meta-análise de ortoceratologia 13) e do ensaio combinado de ortoceratologia + atropina 14), a taxa de inibição de curto prazo da terapia RLRL é boa, mas a ausência de dados além de 5 anos é o maior desafio. A tendência crescente de maculopatia miópica em japoneses, demonstrada pelo Estudo de Kumayama 15), apoia ainda mais a importância médica das intervenções de gerenciamento da miopia, incluindo a terapia RLRL.
Combinação com Outras Terapias
Seção intitulada “Combinação com Outras Terapias”- RLRL + Atropina em Baixa Concentração: Como os mecanismos de ação são diferentes, espera-se efeito aditivo ou sinérgico, mas a verificação por meio de grandes ensaios clínicos randomizados ainda está em andamento 5).
- RLRL + Ortoceratologia: Esta combinação é relatada para casos de progressão rápida.
- Quando a monoterapia é insuficiente, considere a combinação com outras terapias de inibição da progressão da miopia.
Consentimento Informado
Seção intitulada “Consentimento Informado”Em abril de 2026, a terapia RLRL não é aprovada regulatoriamente no Japão e não é coberta pelo seguro, sendo oferecida como tratamento particular. É necessário explicar o seguinte ao paciente e aos pais e obter consentimento.
- Que este tratamento não é aprovado regulatoriamente no Japão
- Que as evidências atuais são principalmente de estudos observacionais de 1 a 2 anos, e a segurança a longo prazo não está estabelecida
- Que existe risco teórico de toxicidade retiniana se os parâmetros de irradiação forem desviados 6)
- Que não é um tratamento para miopia, mas sim uma inibição da progressão
- Que são necessárias consultas oftalmológicas regulares e monitoramento de segurança
Em abril de 2026, a terapia RLRL não é aprovada regulatoriamente nem coberta pelo seguro no Japão. É oferecida como serviço particular em algumas clínicas oftalmológicas, sendo importante consultar um especialista sobre indicação, segurança e custo antes do tratamento. O colírio de atropina em baixa concentração (Rijusea® Mini 0,025%) é a primeira opção aprovada pelo seguro no Japão, aprovado em dezembro de 2024 como o primeiro medicamento nacional para inibição da progressão da miopia.
Papel do RLRL no mecanismo de inibição da progressão da miopia
Seção intitulada “Papel do RLRL no mecanismo de inibição da progressão da miopia”Enquanto as principais intervenções ópticas para inibição da progressão da miopia (ortoceratologia, óculos DIMS, lentes de contato multifocais) compartilham o mecanismo da “hipótese do desfoque periférico miópico”, a terapia RLRL atua por uma via completamente diferente: modulação fotobiológica (PBM) → ativação mitocondrial → melhora do fluxo sanguíneo coroidal → espessamento coroidal → inibição do alongamento axial. Essa diferença no mecanismo de ação leva à expectativa de efeito sinérgico quando combinada com outras terapias 3).
Além disso, uma característica única da terapia RLRL é a resposta fisiológica aguda de aumento imediato da espessura coroidal após o tratamento 2). Essa é uma característica não observada em outras terapias de inibição da progressão da miopia, tornando a medição da espessura coroidal útil como indicador imediato do efeito do tratamento.
6. Fisiopatologia e mecanismos detalhados de início
Seção intitulada “6. Fisiopatologia e mecanismos detalhados de início”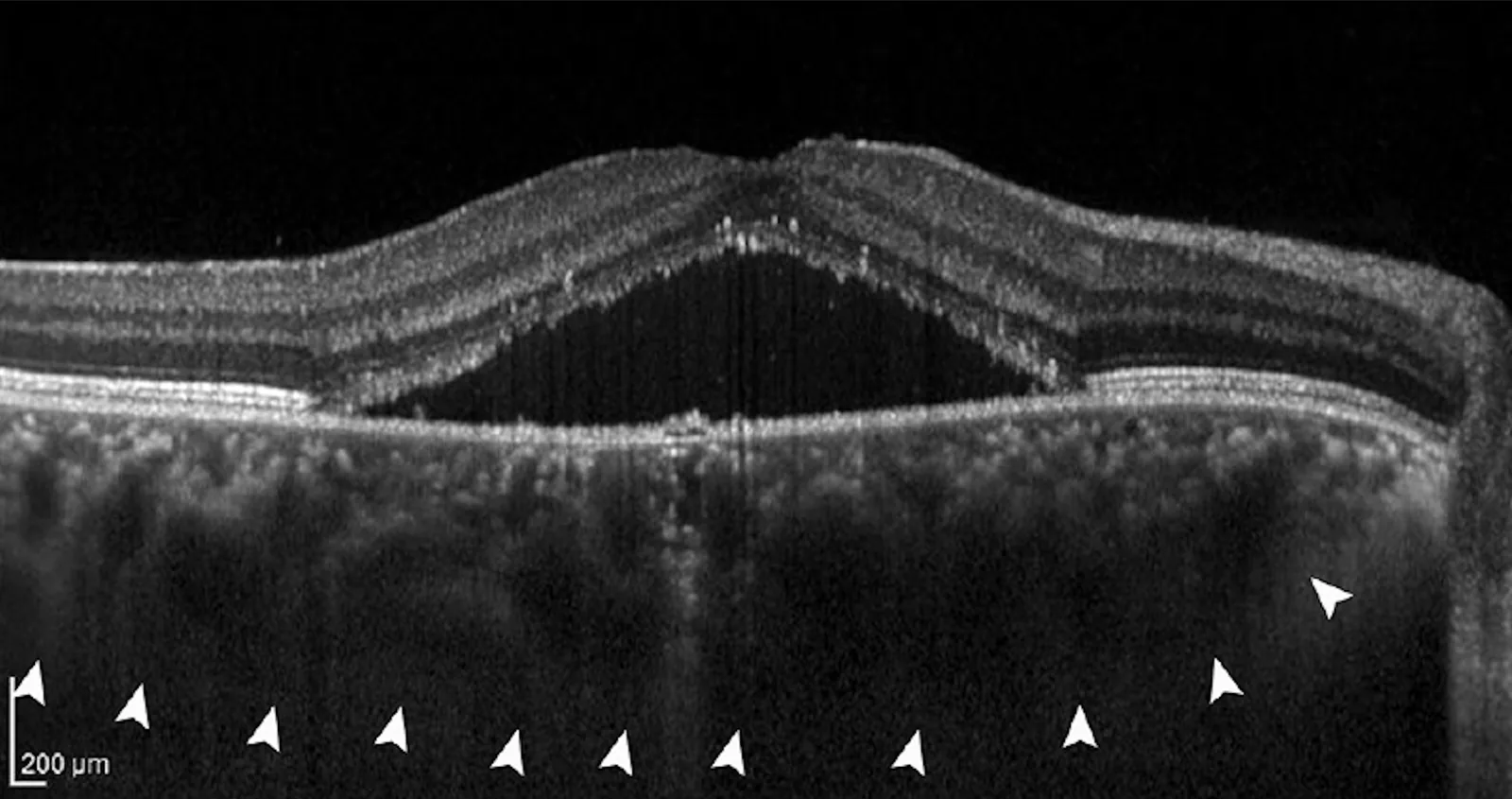
Modulação fotobiológica (Photobiomodulation: PBM)
Seção intitulada “Modulação fotobiológica (Photobiomodulation: PBM)”O principal mecanismo da terapia RLRL é a modulação fotobiológica (PBM) 3). A luz vermelha na faixa de 650-670 nm é especificamente absorvida pela citocromo c oxidase (Complexo IV) nas mitocôndrias intracelulares, induzindo as seguintes respostas biológicas:
- Aumento da produção de ATP
- Ativação da sinalização celular através da produção moderada de espécies reativas de oxigênio (ROS)
- Vasodilatação e aumento do fluxo sanguíneo pela liberação de óxido nítrico (NO)
- Melhora da circulação coroidal e espessamento da coroide
Aumento da espessura coroidal e inibição do alongamento axial
Seção intitulada “Aumento da espessura coroidal e inibição do alongamento axial”O aumento da espessura coroidal após a exposição ao RLRL tem sido consistentemente observado2)3). Acredita-se que o aumento da espessura coroidal afete a rigidez da parede ocular e contribua para a inibição do alongamento axial. O aumento da espessura coroidal também foi relatado com ortoceratologia e atropina em baixa concentração, chamando a atenção para a possibilidade de a coroide ser uma via comum na inibição da progressão da miopia.
Mecanismo básico da progressão da miopia
Seção intitulada “Mecanismo básico da progressão da miopia”A progressão da miopia é um processo biológico no qual o crescimento ocular é regulado pela transmissão de sinais da retina para a esclera, envolvendo os seguintes processos.
- O desfoco hiperópico periférico atua como sinal propulsor do alongamento axial
- Sinais inibitórios do crescimento mediados pela dopamina freiam o alongamento axial
- A remodelação da matriz extracelular da esclera determina o comprimento axial
- O espessamento ou afinamento da coroide serve como biomarcador da mudança no comprimento axial
A terapia RLRL intervém nessa transmissão de sinais e freia o crescimento ocular ao nível da coroide e esclera, mas o quadro completo ainda não é totalmente compreendido3). A meta-análise de Haarman et al. (2020) que mostra os riscos quantitativos das complicações da miopia é amplamente citada como base médica para a intervenção terapêutica7).
7. Pesquisas recentes e perspectivas futuras
Seção intitulada “7. Pesquisas recentes e perspectivas futuras”Estabelecimento de dados de eficácia e segurança a longo prazo
Seção intitulada “Estabelecimento de dados de eficácia e segurança a longo prazo”Os principais ensaios clínicos randomizados atuais têm período de observação de 1 a 2 anos, e dados de longo prazo acima de 5 anos são escassos 1)2). A persistência do efeito após a interrupção do tratamento (efeito carry-over) também não está estabelecida, e estudos estão em andamento para acompanhar as mudanças na velocidade de progressão da miopia após o término do tratamento.
No estudo de acompanhamento de 2 anos de Dong et al. (2023), o grupo de tratamento RLRL mostrou supressão contínua do alongamento axial e aumento da espessura coroidal em comparação com o grupo controle, com confirmação da eficácia do uso contínuo por 1 ano 2). No entanto, como o desenho do estudo, os parâmetros de irradiação e a idade dos participantes diferem entre os estudos, é necessário cuidado na comparação direta.
Quantificação do Risco de Toxicidade Retiniana
Seção intitulada “Quantificação do Risco de Toxicidade Retiniana”Teoricamente, existe a possibilidade de que intensidade, tempo ou frequência excessivos de irradiação causem danos à retina. Na avaliação de risco-benefício do manejo da miopia por Bullimore et al. (2021), o equilíbrio geral de segurança das intervenções ópticas e farmacológicas, incluindo a terapia RLRL, foi discutido, enfatizando a importância do gerenciamento adequado dos parâmetros 6).
Pesquisas estão sendo realizadas para estabelecer limites seguros de irradiação e avaliação de risco. Na prática clínica, é necessária adesão rigorosa à intensidade de irradiação (0,3-1 mW/cm²), tempo de irradiação (3 minutos/sessão) e frequência de irradiação (2 vezes ao dia, 5 dias por semana), juntamente com a calibração periódica do dispositivo.
Do ponto de vista da fototoxicidade, a exposição cumulativa à luz nos fotorreceptores e no EPR é importante, e deve-se ter cuidado ao exceder a dose recomendada (especialmente uso desviante de alta intensidade ou longa duração). Como mostrado na meta-análise de complicações da miopia por Haarman et al. (2020) 7), é importante avaliar individualmente o risco-benefício da terapia RLRL sob a premissa de que o manejo adequado da miopia pode reduzir o risco de complicações graves.
Comparação Direta com Atropina em Baixa Concentração e Ortoqueratologia
Seção intitulada “Comparação Direta com Atropina em Baixa Concentração e Ortoqueratologia”Ensaios clínicos randomizados comparando diretamente a terapia RLRL com ortoqueratologia e atropina em baixa concentração estão sendo realizados. Espera-se o estabelecimento de protocolos personalizados de manejo da miopia considerando as vantagens e desvantagens de cada terapia 5).
Comparação das características das três principais intervenções (RLRL, OK, atropina em baixa concentração):
| Intervenção | Taxa de supressão axial | Invasividade | Conveniência | Situação regulatória no Japão |
|---|---|---|---|---|
| Terapia RLRL | Cerca de 60-72% | Não invasivo | Pode ser realizado em casa | Não aprovado (pagamento próprio) |
| Ortoceratologia | 30-50% | Contato corneano | Uso noturno | Não aprovado (pagamento próprio) |
| Atropina de baixa concentração 0,025% | Cerca de 62% | Colírio | Colírio antes de dormir | Aprovado |
Predição da Progressão da Miopia com IA
Seção intitulada “Predição da Progressão da Miopia com IA”Está em desenvolvimento um modelo que integra dados de comprimento axial, fatores de risco e resposta ao tratamento com IA para propor estratégias terapêuticas ideais para cada paciente. Pode ser aplicado também para prever respondedores à terapia RLRL.
Tendências para Aprovação Nacional
Seção intitulada “Tendências para Aprovação Nacional”Com o acúmulo de evidências na China e Sudeste Asiático, é possível que se inicie um diálogo com as autoridades regulatórias no Japão. A atenção está voltada para a realização de ensaios clínicos randomizados multicêntricos nacionais e a aprovação regulatória. No contexto do aumento global da população míope (Holden 2016: 4,9 bilhões em 20508)), a terapia RLRL está se posicionando como uma opção no manejo da miopia.
8. Referências
Seção intitulada “8. Referências”- Jiang Y, Zhu Z, Tan X, et al. Effect of repeated low-level red-light therapy for myopia control in children: a multicenter randomized controlled trial. Ophthalmology. 2022;129:509-519.
- Dong J, Zhu Z, Xu H, et al. Myopia control effect of repeated low-level red-light therapy in Chinese children: a randomized, double-blind, controlled clinical trial. Ophthalmology. 2023;130:198-204.
- Wang W, Jiang Y, Zhu Z, et al. Chorioidal thickening as a potential therapeutic target in myopia management: a review of repeated low-level red light therapy. Surv Ophthalmol. 2023;68:1-12.
- Zeng J, Liu Y, Wang Z, et al. Efficacy of repeated low-level red-light stimulation on slowing myopia progression and ocular growth in children with myopia: a randomized controlled trial. Transl Vis Sci Technol. 2023;12:22.
- Yam JC, Zhang XJ, Zhang Y, et al. Interventions to reduce incidence and progression of myopia in children and adults. Prog Retin Eye Res. 2025.
- Bullimore MA, Ritchey ER, Shah S, et al. The risks and benefits of myopia control. Ophthalmology. 2021;128:1561-1579.
- Haarman AEG, Enthoven CA, Tideman JWL, et al. The complications of myopia: a review and meta-analysis. Invest Ophthalmol Vis Sci. 2020;61:49.
- Holden BA, Fricke TR, Wilson DA, et al. Global prevalence of myopia and high myopia and temporal trends from 2000 through 2050. Ophthalmology. 2016;123:1036-1042.
- 低濃度アトロピン点眼液を用いた近視進行抑制治療の治療指針作成委員会. 低濃度アトロピン点眼液を用いた近視進行抑制治療の手引き. 日眼会誌. 2025;129(10):851-854.
- 近視管理用眼鏡ガイドライン作成委員会. 近視管理用眼鏡(多分割レンズ)ガイドライン(第1版). 日眼会誌. 2025;129(10):855-860.
- Chamberlain P, Peixoto-de-Matos SC, Logan NS, et al. A 3-year randomized clinical trial of MiSight lenses for myopia control. Optom Vis Sci. 2019;96:556-567.
- Lam CSY, Tang WC, Tse DY, et al. Defocus incorporated multiple segments (DIMS) spectacle lenses slow myopia progression: a 2-year randomised clinical trial. Br J Ophthalmol. 2020;104:363-368.
- Si JK, Tang K, Bi HS, et al. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252-257.
- Kinoshita N, Konno Y, Hamada N, et al. Efficacy of combined orthokeratology and 0.01% atropine solution for slowing axial elongation in children with myopia: a 2-year randomized trial. Sci Rep. 2020;10:12750.
- Ueda E, Yasuda M, Fujiwara K, et al. Trends in the prevalence of myopia and myopic maculopathy in a Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2019;60:2781-2786.
