
การรักษาด้วยแสงสีแดง (ยับยั้งการลุกลามของสายตาสั้น)
1. การบำบัดด้วยแสงสีแดง (ยับยั้งการลุกลามของสายตาสั้น) คืออะไร?
หัวข้อที่มีชื่อว่า “1. การบำบัดด้วยแสงสีแดง (ยับยั้งการลุกลามของสายตาสั้น) คืออะไร?”การบำบัดด้วยแสงสีแดงความเข้มต่ำซ้ำๆ (Repeated Low-Level Red Light Therapy: RLRL) เป็นการรักษาแบบไม่รุกรานที่ยับยั้งการลุกลามของสายตาสั้นในเด็กโดยการฉายแสงสีแดงที่มองเห็นได้ที่มีความยาวคลื่นเฉพาะ (ส่วนใหญ่ 650-670 นาโนเมตร) ด้วยความเข้มต่ำไปยังดวงตา โปรโตคอลมาตรฐานใช้อุปกรณ์มือถือเฉพาะ โดยทำครั้งละ 3 นาที วันละ 2 ครั้ง สัปดาห์ละ 5 วัน
ตำแหน่งของการบำบัด RLRL
หัวข้อที่มีชื่อว่า “ตำแหน่งของการบำบัด RLRL”การบำบัดด้วย RLRL เป็นวิธีการรักษาที่ยับยั้งการลุกลามของสายตาสั้นที่ค่อนข้างใหม่ โดยมีหลักฐานสะสมอย่างรวดเร็วตั้งแต่ช่วงปี 2020 เป็นต้นมา ถือเป็น “ทางเลือกที่สี่” รองจากการรักษาหลักสามแบบดั้งเดิม (ยาหยอดอะโทรพีนความเข้มข้นต่ำ, ออร์โธเคราโทโลจี, และคอนแทคเลนส์มัลติโฟกัส) และงานวิจัยส่วนใหญ่ดำเนินการในเอเชียตะวันออก โดยเฉพาะในจีน
สายตาสั้นเกิดจากการยืดตัวของแกนลูกตาเป็นหลัก โดยการยืดตัว 1 มม. เทียบเท่ากับสายตาสั้นประมาณ 3 D การยับยั้งการยืดตัวของแกนลูกตาเป็นเป้าหมายที่สำคัญที่สุดในการจัดการสายตาสั้น และการเปลี่ยนแปลงความยาวแกนลูกตาเป็นจุดยุติที่สำคัญที่สุดในการประเมินประสิทธิภาพของการบำบัดด้วย RLRL 1)
ภาวะแทรกซ้อนหลักที่เกี่ยวข้องกับสายตาสั้น ได้แก่ จอประสาทตาลอก (ความเสี่ยงเพิ่มขึ้น 30% ต่อ -1 D), จุดรับภาพเสื่อมจากสายตาสั้น (เพิ่มขึ้น 58%), และต้อหินมุมเปิด (เพิ่มขึ้น 20%) 6) การบำบัดด้วย RLRL ถูกวางตำแหน่งให้เป็นการแทรกแซงเชิงป้องกันเพื่อลดความเสี่ยงระยะยาวเหล่านี้
ในเด็กเชื้อสายเอเชีย ความชุกของสายตาสั้นสูงเป็นพิเศษ และหากไม่ได้รับการรักษาจนกลายเป็นระดับสูง ความเสี่ยงของภาวะแทรกซ้อนร้ายแรง เช่น จอประสาทตาลอกและจุดรับภาพเสื่อมจากสายตาสั้นจะเพิ่มขึ้นอย่างมาก มีการประมาณว่าการเพิ่มขึ้น 1 D แต่ละครั้งจะเพิ่มความเสี่ยงของจอประสาทตาลอก 30%, จุดรับภาพเสื่อมจากสายตาสั้น 58%, ต้อหินมุมเปิด 20%, และต้อกระจกใต้แคปซูลหลัง 21% 6)
เนื่องจากการยืดตัวของแกนลูกตา 1 มม. เทียบเท่ากับสายตาสั้นประมาณ 3 D การยับยั้งการยืดตัวของแกนลูกตาจึงเป็นเป้าหมายที่สำคัญที่สุดในการจัดการสายตาสั้น การวิเคราะห์อภิมานโดย Haarman et al. (2020) 7) แสดงให้เห็นว่าความเสี่ยงของภาวะแทรกซ้อนเพิ่มขึ้นแบบทวีคูณตามความรุนแรงของสายตาสั้น ดังนั้นการแทรกแซงตั้งแต่ระยะไม่รุนแรงจึงมีความสำคัญอย่างยิ่งในการปรับปรุงการพยากรณ์โรคระยะยาว
การบำบัดด้วย RLRL เป็นหนึ่งในการแทรกแซงเพื่อยับยั้งการลุกลามของสายตาสั้นควบคู่ไปกับออร์โธเคราโทโลจีและยาหยอดอะโทรพีนความเข้มข้นต่ำ และหลักฐานได้สะสมอย่างรวดเร็วตั้งแต่ช่วงปี 2020 ในญี่ปุ่น ได้มีการนำมาใช้ในบางสถานพยาบาลในฐานะการรักษาแบบชำระเงินเอง ในการทบทวนอย่างเป็นระบบโดย Yam et al. (2025) ได้สรุปหลักฐานสำหรับการแทรกแซงยับยั้งการลุกลามของสายตาสั้นหลายวิธีรวมถึงการบำบัดด้วย RLRL 5)
ในทางกลับกัน Bullimore et al. (2021) ได้ตรวจสอบความเสี่ยงและประโยชน์ของการจัดการสายตาสั้นโดยทั่วไปอย่างละเอียด และชี้ให้เห็นว่ามีความเสี่ยงต่อพิษแสงต่อจอประสาทตาในการบำบัดด้วย RLRL เมื่อพารามิเตอร์การฉายรังสีเบี่ยงเบนไป 6) การปฏิบัติตามการจัดการอุปกรณ์ที่เหมาะสม ความเข้มของการฉายรังสี และระยะเวลาการฉายรังสีเป็นข้อกำหนดเบื้องต้นสำหรับการใช้งานอย่างปลอดภัย
การบำบัดด้วย RLRL เป็นการรักษาเพื่อยับยั้งการลุกลามของสายตาสั้น โดยการฉายแสงสีแดงที่มองเห็นได้ในช่วงความยาวคลื่น 650-670 นาโนเมตร ที่ความเข้มต่ำ (0.3-1 mW/cm²) เข้าสู่ดวงตา ครั้งละ 3 นาที วันละ 2 ครั้ง เชื่อกันว่าช่วยเพิ่มความหนาของคอรอยด์ผ่านกระบวนการโฟโตไบโอโมดูเลชัน (photobiomodulation) และยับยั้งการยืดตัวของแกนลูกตา 3) ปัจจุบันยังไม่ได้รับการอนุมัติในญี่ปุ่นและเป็นบริการทางการแพทย์แบบชำระเงินเอง ใช้ภายใต้การดูแลของผู้เชี่ยวชาญ
2. อาการหลักและผลการตรวจทางคลินิก
หัวข้อที่มีชื่อว่า “2. อาการหลักและผลการตรวจทางคลินิก”ตัวชี้วัดประสิทธิภาพการรักษา
หัวข้อที่มีชื่อว่า “ตัวชี้วัดประสิทธิภาพการรักษา”ประสิทธิภาพของการบำบัดด้วย RLRL ประเมินโดยใช้ตัวชี้วัดเชิงวัตถุวิสัยดังต่อไปนี้:
- ความยาวแกนลูกตา: วัดด้วยเครื่องวัดความยาวแกนลูกตาแบบใช้แสง ติดตามการเปลี่ยนแปลงก่อนและหลังการรักษา และทุก 6 เดือน
- ความหนาของคอรอยด์: วัดความหนาของคอรอยด์ใต้รอยบุ๋มจอตา (SFCT) ด้วย OCT พบว่าความหนาของคอรอยด์เพิ่มขึ้นหลังการฉายแสง RLRL การศึกษาติดตามผล 2 ปีโดย Dong et al. (2023) ยืนยันการเพิ่มขึ้นของความหนาคอรอยด์ 2)
- ค่าสายตาเอสเฟียริคอลสมมูล: การประเมินเชิงวัตถุวิสัยภายใต้การหยอดยาหยอดตาคลายกล้ามเนื้อปรับตา
- สายตาที่แก้ไขแล้ว: ยืนยันความคงที่ของสายตาที่แก้ไขแล้วก่อนและหลังการรักษา
ข้อควรระวังในการประเมินความปลอดภัย
หัวข้อที่มีชื่อว่า “ข้อควรระวังในการประเมินความปลอดภัย”แม้ว่าการบำบัดด้วย RLRL จะมีความเข้มต่ำและเหตุการณ์ไม่พึงประสงค์ระยะสั้นพบได้น้อย แต่จำเป็นต้องตรวจสอบประเด็นต่อไปนี้อย่างสม่ำเสมอ:
- ความเสี่ยงต่อพิษต่อจอตา: ความเข้ม ระยะเวลา หรือความถี่ในการฉายแสงที่มากเกินไปอาจทำให้เกิดการบาดเจ็บต่อจอตาได้ในทางทฤษฎี 6) ควรบันทึกการประเมินชั้นจอตาและคอรอยด์ด้วย OCT เป็นข้อมูลพื้นฐานก่อนการรักษาและเปรียบเทียบอย่างสม่ำเสมอ
- การเปลี่ยนแปลงของสายตาและการมองเห็นสี: ตรวจสอบว่ามีสายตาลดลงหรือความผิดปกติของการมองเห็นสีในระหว่างการรักษาหรือไม่
- อาการที่ผู้ป่วยรับรู้: ใส่ใจต่อข้อร้องเรียน เช่น อาการแสบตา ภาพติดตา หรือความผิดปกติของลานสายตา
3. สาเหตุและปัจจัยเสี่ยง
หัวข้อที่มีชื่อว่า “3. สาเหตุและปัจจัยเสี่ยง”ปัจจัยเสี่ยงต่อการลุกลามของสายตาสั้น
หัวข้อที่มีชื่อว่า “ปัจจัยเสี่ยงต่อการลุกลามของสายตาสั้น”ปัจจัยเสี่ยงต่อไปนี้เกี่ยวข้องกับการลุกลามของสายตาสั้นซึ่งเป็นเป้าหมายของการรักษาด้วย RLRL:
- การเริ่มต้นตั้งแต่อายุน้อย (โดยเฉพาะอายุ 6–12 ปี)
- พ่อแม่ทั้งสองคนสายตาสั้น (โดยเฉพาะถ้าทั้งคู่สายตาสั้น)
- ระยะเวลาทำงานระยะใกล้ที่ยาวนาน (มากกว่า 3 ชั่วโมงต่อวัน)
- ขาดเวลาทำกิจกรรมกลางแจ้ง (น้อยกว่า 1 ชั่วโมงต่อวัน)
- เชื้อชาติเอเชีย (ความชุกสูงสุดในกลุ่มเอเชียตะวันออก)
- การคาดการณ์ของ Holden et al. (2016) ว่าประมาณ 50% ของประชากรโลกจะสายตาสั้นภายในปี 20508) ทำให้ความสำคัญทางสังคมของการแทรกแซงตั้งแต่เนิ่นๆ เพิ่มขึ้น
4. การวินิจฉัยและวิธีการตรวจ
หัวข้อที่มีชื่อว่า “4. การวินิจฉัยและวิธีการตรวจ”การประเมินก่อนเริ่มการรักษา
หัวข้อที่มีชื่อว่า “การประเมินก่อนเริ่มการรักษา”ก่อนเริ่มการรักษาด้วย RLRL ให้บันทึกค่าพื้นฐานและยืนยันข้อบ่งชี้ผ่านการตรวจดังต่อไปนี้:
| รายการตรวจ | วัตถุประสงค์ | ประเด็นหลักที่ต้องยืนยัน |
|---|---|---|
| การตรวจวัดค่าสายตาภายใต้ยาหยอดตาขยายม่านตา | การประเมินระดับสายตาสั้นตามวัตถุวิสัย | ค่าสายตาเทียบเท่าทรงกลมและปริมาณสายตาเอียง |
| การวัดความยาวแกนลูกตา | การกำหนดค่าพื้นฐานและติดตามความคืบหน้า | วัดด้วยเครื่องวัดความยาวแกนลูกตาแบบใช้แสง |
| การตรวจอวัยวะภายในลูกตา | สภาพจอประสาทตาและคอรอยด์ก่อนการรักษา | ยืนยันการเปลี่ยนแปลงจากสายตาสั้นระดับสูง |
| OCT (จุดรับภาพและประสาทตา) | การกำหนดค่าอ้างอิงความเป็นพิษต่อจอประสาทตา | ความหนาของชั้นจอประสาทตาและคอรอยด์ |
| การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีดแสง | การแยกโรคของส่วนหน้าของลูกตา | การอักเสบที่ยังดำเนินอยู่และต้อกระจก |
สำหรับการตรวจภายใต้ฤทธิ์หยุดการปรับตา ในเด็กเล็ก การใช้ยาหยอดตาหยุดการปรับตา (เช่น Cyplegin 1%) เป็นสิ่งที่ขาดไม่ได้ หากทำการตรวจวัดสายตาแบบอัตนัยเพียงอย่างเดียวโดยไม่หยุดการปรับตา อาจคำนวณค่าระดับสายตาสั้นที่มากเกินไปได้
การติดตามระหว่างการรักษา
หัวข้อที่มีชื่อว่า “การติดตามระหว่างการรักษา”เพื่อยืนยันประสิทธิภาพและความปลอดภัยของการรักษา แนะนำให้ใช้ตารางเวลาดังต่อไปนี้
| ช่วงเวลา | เนื้อหา |
|---|---|
| หลังจาก 1 เดือน | การปฏิบัติตามการใช้ยาหยอดตา การยืนยันอาการ主观 การมองเห็นที่แก้ไขแล้ว |
| ทุก 3-6 เดือน | การวัดความยาวแกนตา การหาค่าสายตาภายใต้ฤทธิ์หยุดการปรับตา OCT (ความหนาคอรอยด์ การประเมินจอประสาทตา) |
| ทุกปี | การตรวจอวัยวะภายในตาด้วยการขยายม่านตา OCT angiography (ไม่บังคับ) |
การบันทึกค่าพื้นฐานด้วยการตรวจวัดค่าสายตาภายใต้ฤทธิ์หยุดการปรับตาและการวัดความยาวแกนตาด้วยแสงเป็นสิ่งจำเป็น นอกจากนี้ ให้บันทึกสภาพของจอประสาทตาและคอรอยด์ก่อนการรักษาด้วยการตรวจอวัยวะภายในตาและ OCT และใช้เพื่อติดตามความปลอดภัยระหว่างการรักษา หากสงสัยว่ามีสายตาสั้นระดับสูง ให้ตรวจสอบการเสื่อมหรือการฉีกขาดของจอประสาทตาส่วนปลายด้วย
5. วิธีการรักษามาตรฐาน
หัวข้อที่มีชื่อว่า “5. วิธีการรักษามาตรฐาน”การให้ข้อมูลและยินยอมก่อนการรักษาและการประเมินความเหมาะสม
หัวข้อที่มีชื่อว่า “การให้ข้อมูลและยินยอมก่อนการรักษาและการประเมินความเหมาะสม”ต่อไปนี้เป็นพื้นฐานในการเลือกผู้ป่วยที่เหมาะสมสำหรับการรักษาด้วย RLRL
ข้อบ่งชี้ที่แนะนำ:
- อายุ 6–18 ปี (การศึกษาส่วนใหญ่รวมกลุ่มอายุนี้)
- ค่าสายตาสั้นเทียบเท่าทรงกลม −0.5 D ขึ้นไป และมีการลุกลามที่ยืนยันแล้ว
- สายตาสั้นที่ยืนยันภายใต้การตรวจด้วยยาหยอดตาขยายม่านตา
- สภาพแวดล้อมที่ผู้ปกครองสามารถจัดการได้อย่างเหมาะสม
สถานการณ์ที่ควรพิจารณาอย่างรอบคอบ:
- กรณีที่มีประวัติหรือประวัติครอบครัวเป็นโรคจอประสาทตา
- โรคไวต่อแสง (เช่น ซีโรเดอร์มา พิกเมนโตซัม, ผิวหนังไวต่อแสง)
- การใช้ยาที่ทำให้เกิดอาการไวต่อแสง
สถานการณ์ที่ควรหลีกเลี่ยง:
- โรคจอประสาทตาที่กำลังดำเนินอยู่ (เช่น จอประสาทตาเสื่อม, หลอดเลือดใหม่)
- ผู้ป่วยที่ได้รับการวินิจฉัยแน่ชัดว่าไวต่อแสง
แนวทางการรักษา
หัวข้อที่มีชื่อว่า “แนวทางการรักษา”ต่อไปนี้เป็นพารามิเตอร์การรักษามาตรฐานที่ใช้ในการทดลองแบบสุ่มที่มีกลุ่มควบคุมหลัก
| พารามิเตอร์ | ค่ามาตรฐาน | หมายเหตุ |
|---|---|---|
| ความยาวคลื่น | 650 นาโนเมตร (แสงสีแดงที่มองเห็นได้) | การทดลองบางส่วนใช้ 670 นาโนเมตร |
| ความเข้มของการฉายแสง | 0.3–1 มิลลิวัตต์/ซม.² | แสงไม่ต่อเนื่องกัน ไม่ใช่เลเซอร์ |
| ระยะเวลาการฉายแสง | 3 นาที/ครั้ง | วันละ 2 ครั้ง (เช้าและเย็น) |
| ความถี่ในการรักษา | 5 วัน/สัปดาห์ (เฉพาะวันเรียน) | — |
| ระยะเวลาการรักษา | 12–24 เดือนขึ้นไป | จำเป็นต้องคงผลการรักษาอย่างต่อเนื่อง |
อุปกรณ์มือถือเฉพาะที่ผลิตในจีน (เช่น Suneye) ถูกใช้เป็นหลักในการวิจัย ออกแบบให้ผู้ป่วยสามารถฉายแสงด้วยตนเองที่บ้าน แต่การตั้งค่าเริ่มต้นและการตรวจติดตามเป็นระยะต้องทำโดยผู้เชี่ยวชาญ
ผลลัพธ์จากการทดลองทางคลินิกแบบสุ่มหลัก
หัวข้อที่มีชื่อว่า “ผลลัพธ์จากการทดลองทางคลินิกแบบสุ่มหลัก”ในการทดลองทางคลินิกแบบสุ่มระยะเวลา 1 ปีโดย Jiang et al. (2022) กลุ่ม RLRL แสดงการยับยั้งการยืดของแกนลูกตาอย่างมีนัยสำคัญที่ 0.10 มม./ปี (กลุ่มควบคุม 0.38 มม./ปี)1) การติดตามผล 2 ปีโดย Dong et al. (2023) ก็ยืนยันผลการยับยั้งการยืดของแกนลูกตาที่ยั่งยืนและการเพิ่มความหนาของคอรอยด์2)
การทดลองทางคลินิกแบบสุ่มหลายศูนย์โดย Zeng et al. (2023) แสดงให้เห็นว่าความก้าวหน้าของค่าสเฟียริคัลอิควิวาเลนต์ใน 1 ปีคือ −0.20 D ในกลุ่มรักษา (กลุ่มควบคุม −0.71 D) ซึ่งยับยั้งความก้าวหน้าของสายตาสั้นได้ประมาณ 72%4)
การเปรียบเทียบประสิทธิผลของการบำบัด RLRL กับวิธีการยับยั้งความก้าวหน้าของสายตาสั้นอื่นๆ:
| การแทรกแซง | อัตราการยับยั้งค่าสายตา | อัตราการยับยั้งความยาวแกนลูกตา | หลักฐานสำคัญ |
|---|---|---|---|
| การบำบัด RLRL | 72% (Zeng 2023) | 74% (Jiang 2022) | การทดลองทางคลินิกแบบสุ่มหลายรายการ |
| อะโทรพีนความเข้มข้นต่ำ 0.05% | สูงสุด 67% | — | การทดลอง LAMP |
| ออร์โธเคราโทโลจี (Orthokeratology) | — | 43% | การวิเคราะห์อภิมาน Si 2015 |
| MiSight (คอนแทคเลนส์หลายระยะ) | 59% | 52% | Chamberlain 2019 |
| แว่นตา DIMS | 55-59% | 37-38% | Lam 2020 การทดลองแบบสุ่มมีกลุ่มควบคุม |
อย่างไรก็ตาม เนื่องจากการออกแบบการทดลอง อายุเป้าหมาย และระยะเวลาการรักษาที่แตกต่างกัน จึงต้องใช้ความระมัดระวังในการเปรียบเทียบโดยตรง 5) ยาหยอดตาอะโทรพีนความเข้มข้นต่ำ (Rijusea® Mini 0.025%) เป็นยาชนิดเดียวที่ได้รับการอนุมัติในญี่ปุ่นในเดือนธันวาคม 2024 9) และเลนส์แว่นตาสำหรับจัดการสายตาสั้น (เช่น DIMS) 10) ก็ได้รับการแนะนำในแนวทางของสมาคมสายตาสั้นแห่งประเทศญี่ปุ่น การบำบัดด้วย RLRL กำลังถูกวางตำแหน่งเป็นทางเลือกที่สามารถใช้ร่วมกับการแทรกแซงที่ได้รับการอนุมัติเหล่านี้
เมื่อเปรียบเทียบกับข้อมูลจากการทดลอง MiSight (คอนแทคเลนส์มัลติโฟกัส) ระยะเวลา 3 ปี 11) การทดลองแว่นตา DIMS ระยะเวลา 2 ปี 12) การวิเคราะห์อภิมานของออร์โธเคราโทโลจี 13) และการทดลองแบบผสมผสานออร์โธเคราโทโลจี + อะโทรพีน 14) อัตราการยับยั้งระยะสั้นของการบำบัดด้วย RLRL อยู่ในเกณฑ์ดี แต่การไม่มีข้อมูลมากกว่า 5 ปีเป็นความท้าทายที่ใหญ่ที่สุด แนวโน้มที่เพิ่มขึ้นของจอประสาทตาเสื่อมจากสายตาสั้นในคนญี่ปุ่น ซึ่งแสดงโดยการศึกษา Kumayama 15) ยิ่งสนับสนุนความสำคัญทางการแพทย์ของการแทรกแซงการจัดการสายตาสั้นรวมถึงการบำบัดด้วย RLRL
การผสมผสานกับการบำบัดอื่นๆ
หัวข้อที่มีชื่อว่า “การผสมผสานกับการบำบัดอื่นๆ”- RLRL + อะโทรพีนความเข้มข้นต่ำ: เนื่องจากกลไกการออกฤทธิ์ต่างกัน คาดว่าจะมีผลเสริมหรือเสริมฤทธิ์กัน แต่การตรวจสอบผ่านการทดลองแบบสุ่มขนาดใหญ่ยังคงดำเนินอยู่ 5)
- RLRL + ออร์โธเคราโทโลจี: มีรายงานการใช้ร่วมกันนี้ในกรณีที่สายตาสั้นดำเนินไปอย่างรวดเร็ว
- เมื่อการรักษาเดี่ยวไม่ได้ผลเพียงพอ ควรพิจารณาผสมผสานกับการบำบัดยับยั้งการดำเนินของสายตาสั้นอื่นๆ
การยินยอมโดยได้รับข้อมูล
หัวข้อที่มีชื่อว่า “การยินยอมโดยได้รับข้อมูล”ณ เดือนเมษายน 2026 การบำบัดด้วย RLRL ยังไม่ได้รับการอนุมัติจากหน่วยงานกำกับดูแลในญี่ปุ่นและไม่ครอบคลุมโดยประกัน โดยให้บริการเป็นค่ารักษาพยาบาลส่วนตัว จำเป็นต้องอธิบายสิ่งต่อไปนี้ให้ผู้ป่วยและผู้ปกครองทราบอย่างเพียงพอและได้รับความยินยอม
- ว่าการรักษานี้ยังไม่ได้รับการอนุมัติจากหน่วยงานกำกับดูแลในญี่ปุ่น
- ว่าหลักฐานในปัจจุบันส่วนใหญ่มาจากการศึกษาเชิงสังเกตระยะเวลา 1-2 ปี และความปลอดภัยในระยะยาวยังไม่ได้รับการยืนยัน
- ว่ามีความเสี่ยงทางทฤษฎีต่อพิษต่อจอประสาทตาหากเบี่ยงเบนจากพารามิเตอร์การฉายแสง 6)
- ว่านี่ไม่ใช่การรักษาสายตาสั้น แต่เป็นการยับยั้งการดำเนินของสายตาสั้น
- ว่าจำเป็นต้องตรวจตาเป็นประจำและติดตามความปลอดภัย
ณ เดือนเมษายน 2026 การรักษา RLRL ยังไม่ได้รับการอนุมัติตามกฎระเบียบและไม่ครอบคลุมโดยประกันในญี่ปุ่น มีให้บริการเป็นบริการแบบชำระเงินเองในคลินิกตาบางแห่ง และสิ่งสำคัญคือต้องปรึกษาผู้เชี่ยวชาญเกี่ยวกับข้อบ่งชี้ ความปลอดภัย และค่าใช้จ่ายก่อนการรักษา ยาหยอดตาอะโทรปีนความเข้มข้นต่ำ (Rijusea® Mini 0.025%) เป็นตัวเลือกแรกที่ได้รับการอนุมัติจากประกันในญี่ปุ่น โดยได้รับการอนุมัติในเดือนธันวาคม 2024 ซึ่งเป็นยาระงับการลุกลามของสายตาสั้นชนิดแรกในประเทศ
บทบาทของ RLRL ในกลไกการยับยั้งการลุกลามของสายตาสั้น
หัวข้อที่มีชื่อว่า “บทบาทของ RLRL ในกลไกการยับยั้งการลุกลามของสายตาสั้น”ในขณะที่การแทรกแซงทางแสงหลักสำหรับการยับยั้งการลุกลามของสายตาสั้น (ออร์โธเคราโทโลจี, แว่นตา DIMS, คอนแทคเลนส์มัลติโฟกัส) มีกลไกร่วมกันคือ “สมมติฐานการเบลอรอบนอกแบบสายตาสั้น” การรักษา RLRL ทำงานผ่านวิถีทางที่แตกต่างอย่างสิ้นเชิง: การปรับเปลี่ยนทางชีวภาพด้วยแสง (PBM) → การกระตุ้นไมโตคอนเดรีย → การปรับปรุงการไหลเวียนเลือดคอรอยด์ → การหนาตัวของคอรอยด์ → การยับยั้งการยืดของแกนลูกตา ความแตกต่างของกลไกการออกฤทธิ์นี้นำไปสู่ความคาดหวังของผลเสริมฤทธิ์เมื่อรวมกับการรักษาอื่นๆ 3)
นอกจากนี้ ลักษณะเฉพาะของการรักษา RLRL คือการตอบสนองทางสรีรวิทยาเฉียบพลันโดยความหนาของคอรอยด์เพิ่มขึ้นทันทีหลังการรักษา 2) นี่เป็นลักษณะที่ไม่พบในการรักษายับยั้งการลุกลามของสายตาสั้นอื่นๆ ทำให้การวัดความหนาของคอรอยด์มีประโยชน์เป็นตัวบ่งชี้ผลการรักษาทันที
6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด
หัวข้อที่มีชื่อว่า “6. พยาธิสรีรวิทยาและกลไกการเกิดโรคโดยละเอียด”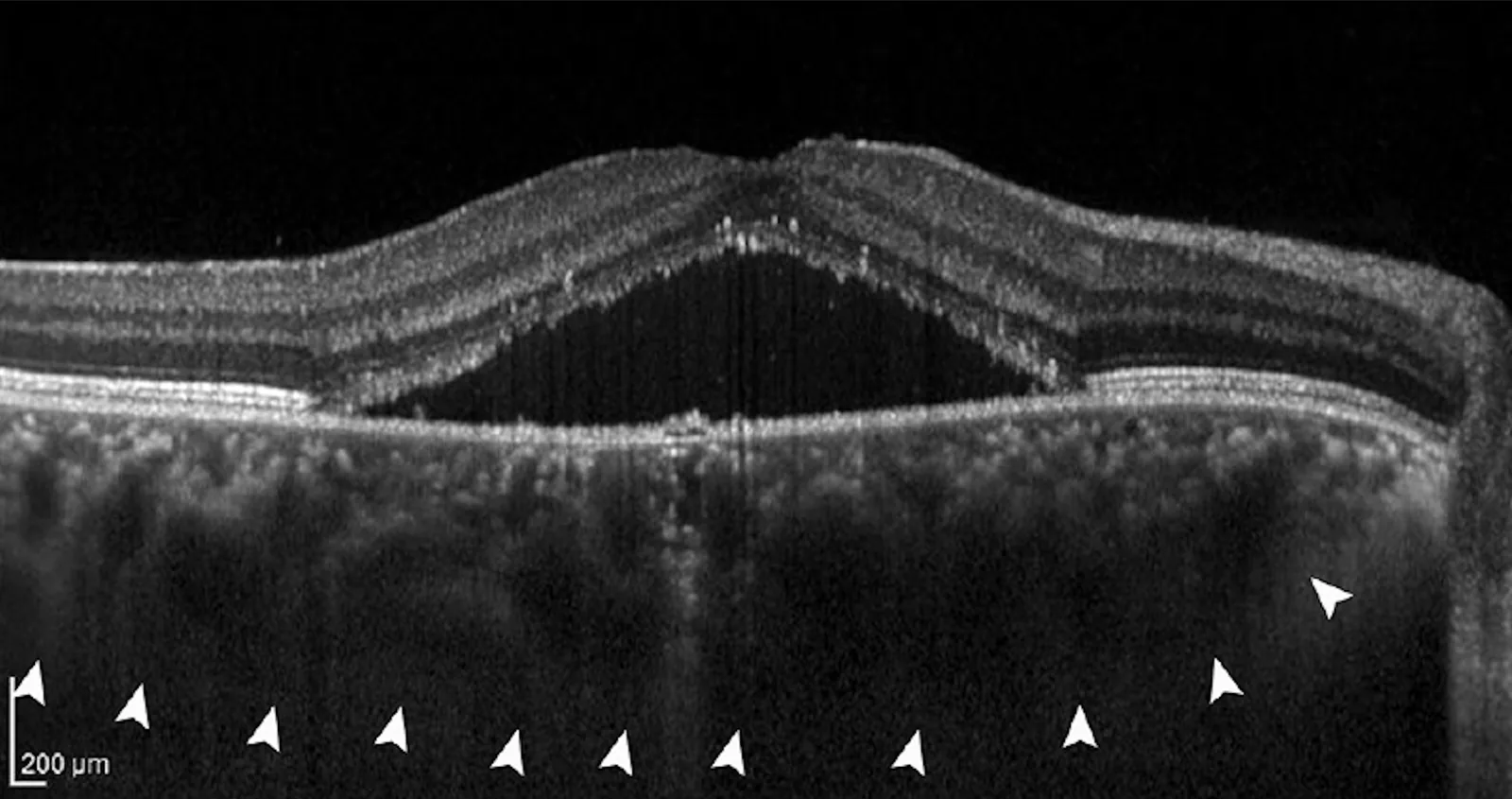
การปรับเปลี่ยนทางชีวภาพด้วยแสง (Photobiomodulation: PBM)
หัวข้อที่มีชื่อว่า “การปรับเปลี่ยนทางชีวภาพด้วยแสง (Photobiomodulation: PBM)”กลไกหลักของการรักษา RLRL คือการปรับเปลี่ยนทางชีวภาพด้วยแสง (PBM) 3) แสงสีแดงในช่วง 650-670 นาโนเมตรถูกดูดซับโดยเฉพาะโดยไซโตโครม ซี ออกซิเดส (Complex IV) ในไมโตคอนเดรียภายในเซลล์ ทำให้เกิดการตอบสนองทางชีวภาพดังต่อไปนี้:
- การเพิ่มการผลิต ATP
- การกระตุ้นสัญญาณเซลล์ผ่านการผลิตออกซิเจนชนิดปฏิกิริยา (ROS) ในระดับปานกลาง
- การขยายหลอดเลือดและการเพิ่มการไหลเวียนของเลือดผ่านการปล่อยไนตริกออกไซด์ (NO)
- การปรับปรุงการไหลเวียนของคอรอยด์และการหนาตัวของคอรอยด์
การเพิ่มความหนาของคอรอยด์และการยับยั้งการยืดของแกนลูกตา
หัวข้อที่มีชื่อว่า “การเพิ่มความหนาของคอรอยด์และการยับยั้งการยืดของแกนลูกตา”พบว่าความหนาของคอรอยด์เพิ่มขึ้นอย่างสม่ำเสมอหลังการฉายแสง RLRL2)3) เชื่อว่าการเพิ่มความหนาของคอรอยด์ส่งผลต่อความแข็งของผนังลูกตาและช่วยยับยั้งการยืดของแกนลูกตา นอกจากนี้ยังมีรายงานการเพิ่มความหนาของคอรอยด์ร่วมกับการจัดทรงกระจกตา (orthokeratology) และอะโทรพีนความเข้มข้นต่ำ ซึ่งทำให้สนใจว่าคอรอยด์อาจเป็นเส้นทางร่วมในการยับยั้งการลุกลามของสายตาสั้น
กลไกพื้นฐานของการลุกลามของสายตาสั้น
หัวข้อที่มีชื่อว่า “กลไกพื้นฐานของการลุกลามของสายตาสั้น”การลุกลามของสายตาสั้นเป็นกระบวนการทางชีวภาพที่การเจริญเติบโตของลูกตาถูกควบคุมผ่านการส่งสัญญาณจากจอประสาทตาไปยังตาขาว ซึ่งเกี่ยวข้องกับกระบวนการต่อไปนี้
- การเบนโฟกัสแบบสายตายาวส่วนปลาย (peripheral hyperopic defocus) ทำหน้าที่เป็นสัญญาณขับเคลื่อนการยืดของแกนลูกตา
- สัญญาณยับยั้งการเจริญเติบโตผ่านโดปามีนจะชะลอการยืดของแกนลูกตา
- การปรับโครงสร้างเมทริกซ์นอกเซลล์ของตาขาวเป็นตัวกำหนดความยาวแกนลูกตา
- การหนาหรือบางลงของคอรอยด์กลายเป็นตัวบ่งชี้ทางชีวภาพของการเปลี่ยนแปลงความยาวแกนลูกตา
การบำบัดด้วย RLRL เข้าไปแทรกแซงการส่งสัญญาณเหล่านี้และชะลอการเจริญเติบโตของลูกตาในระดับคอรอยด์และตาขาว แต่ภาพรวมยังไม่เป็นที่เข้าใจอย่างสมบูรณ์3) การวิเคราะห์อภิมานของ Haarman et al. (2020) ที่แสดงความเสี่ยงเชิงปริมาณของภาวะแทรกซ้อนจากสายตาสั้นถูกอ้างอิงอย่างกว้างขวางเป็นพื้นฐานทางการแพทย์สำหรับการแทรกแซงการรักษา7)
7. งานวิจัยล่าสุดและแนวโน้มในอนาคต
หัวข้อที่มีชื่อว่า “7. งานวิจัยล่าสุดและแนวโน้มในอนาคต”การสร้างข้อมูลประสิทธิภาพและความปลอดภัยในระยะยาว
หัวข้อที่มีชื่อว่า “การสร้างข้อมูลประสิทธิภาพและความปลอดภัยในระยะยาว”การทดลองแบบสุ่มที่มีกลุ่มควบคุมหลักในปัจจุบันมีระยะเวลาสังเกตการณ์ 1-2 ปี และข้อมูลระยะยาวมากกว่า 5 ปีมีน้อย 1)2) ความคงอยู่ของผลหลังหยุดการรักษา (ผล carry-over) ยังไม่เป็นที่แน่ชัด และกำลังมีการศึกษาวิจัยเพื่อติดตามการเปลี่ยนแปลงของความเร็วการลุกลามของสายตาสั้นหลังสิ้นสุดการรักษา
ในการศึกษาติดตามผล 2 ปีโดย Dong et al. (2023) กลุ่มที่ได้รับการรักษาด้วย RLRL แสดงการยับยั้งการยืดตัวของแกนลูกตาอย่างต่อเนื่องและความหนาของคอรอยด์เพิ่มขึ้นเมื่อเทียบกับกลุ่มควบคุม โดยยืนยันประสิทธิภาพของการใช้ต่อเนื่องเป็นเวลา 1 ปี 2) อย่างไรก็ตาม เนื่องจากการออกแบบการศึกษา พารามิเตอร์การฉายรังสี และอายุของอาสาสมัครแตกต่างกันระหว่างการทดลอง จึงต้องใช้ความระมัดระวังในการเปรียบเทียบโดยตรง
การหาปริมาณความเสี่ยงต่อพิษของจอประสาทตา
หัวข้อที่มีชื่อว่า “การหาปริมาณความเสี่ยงต่อพิษของจอประสาทตา”ในทางทฤษฎี มีความเป็นไปได้ที่ความเข้มข้น เวลา หรือความถี่ของการฉายรังสีที่มากเกินไปอาจทำให้เกิดการบาดเจ็บของจอประสาทตา ในการประเมินความเสี่ยง-ผลประโยชน์ของการจัดการสายตาสั้นโดย Bullimore et al. (2021) ได้มีการอภิปรายถึงความสมดุลด้านความปลอดภัยโดยรวมของการแทรกแซงทางแสงและเภสัชวิทยารวมถึงการบำบัดด้วย RLRL โดยเน้นย้ำถึงความสำคัญของการจัดการพารามิเตอร์ที่เหมาะสม 6)
กำลังมีการวิจัยเพื่อกำหนดขีดจำกัดการฉายรังสีที่ปลอดภัยและการประเมินความเสี่ยง ในทางปฏิบัติทางคลินิก จำเป็นต้องปฏิบัติตามความเข้มข้นของการฉายรังสี (0.3-1 mW/cm²) เวลาฉายรังสี (3 นาที/ครั้ง) และความถี่ในการฉายรังสี (2 ครั้ง/วัน 5 วัน/สัปดาห์) อย่างเคร่งครัด พร้อมกับการสอบเทียบอุปกรณ์เป็นระยะ
จากมุมมองของพิษจากแสง การสะสมของแสงที่เซลล์รับแสงและ RPE มีความสำคัญ และต้องใช้ความระมัดระวังเมื่อเกินปริมาณที่แนะนำ (โดยเฉพาะการใช้ที่เบี่ยงเบนไปในความเข้มสูงหรือระยะเวลานาน) ดังที่การวิเคราะห์อภิมานของภาวะแทรกซ้อนของสายตาสั้นโดย Haarman et al. (2020) ชี้ให้เห็น 7) สิ่งสำคัญคือต้องประเมินความเสี่ยง-ผลประโยชน์ของการบำบัดด้วย RLRL เป็นรายบุคคลภายใต้สมมติฐานที่ว่าการจัดการสายตาสั้นที่เหมาะสมสามารถลดความเสี่ยงของภาวะแทรกซ้อนร้ายแรงได้
การเปรียบเทียบโดยตรงกับ Atropine ความเข้มข้นต่ำและ Orthokeratology
หัวข้อที่มีชื่อว่า “การเปรียบเทียบโดยตรงกับ Atropine ความเข้มข้นต่ำและ Orthokeratology”กำลังมีการทดลองแบบสุ่มที่มีกลุ่มควบคุมเพื่อเปรียบเทียบโดยตรงระหว่างการบำบัดด้วย RLRL กับ orthokeratology และ atropine ความเข้มข้นต่ำ คาดว่าจะมีการกำหนดโปรโตคอลการจัดการสายตาสั้นเฉพาะบุคคลโดยพิจารณาถึงข้อดีและข้อเสียของการบำบัดแต่ละแบบ 5)
การเปรียบเทียบลักษณะของการแทรกแซงหลักสามประการ (RLRL, OK, atropine ความเข้มข้นต่ำ):
| การแทรกแซง | อัตราการยับยั้งแกนลูกตา | การรุกราน | ความสะดวก | สถานะการควบคุมในญี่ปุ่น |
|---|---|---|---|---|
| การบำบัดด้วย RLRL | ประมาณ 60-72% | ไม่รุกราน | สามารถทำได้ที่บ้าน | ยังไม่ได้รับการอนุมัติ (จ่ายเอง) |
| ออร์โธเคราโทโลจี | 30-50% | สัมผัสกระจกตา | ใส่ตอนกลางคืน | ยังไม่ได้รับการรับรอง (จ่ายเอง) |
| อะโทรพีนความเข้มข้นต่ำ 0.025% | ประมาณ 62% | ยาหยอดตา | หยอดก่อนนอน | ได้รับการรับรองแล้ว |
การทำนายความก้าวหน้าของสายตาสั้นด้วย AI
หัวข้อที่มีชื่อว่า “การทำนายความก้าวหน้าของสายตาสั้นด้วย AI”กำลังมีการพัฒนาแบบจำลองที่บูรณาการข้อมูลความยาวแกนตา ปัจจัยเสี่ยง และการตอบสนองต่อการรักษาด้วย AI เพื่อเสนอแผนการรักษาที่เหมาะสมที่สุดสำหรับผู้ป่วยแต่ละราย อาจนำไปใช้ทำนายผู้ที่ตอบสนองต่อการรักษา RLRL ได้ด้วย
แนวโน้มการอนุมัติในประเทศ
หัวข้อที่มีชื่อว่า “แนวโน้มการอนุมัติในประเทศ”ด้วยการสะสมหลักฐานในจีนและเอเชียตะวันออกเฉียงใต้ อาจเริ่มมีการเจรจากับหน่วยงานกำกับดูแลในญี่ปุ่น ความสนใจมุ่งไปที่การดำเนินการทดลองแบบสุ่มมีกลุ่มควบคุมหลายศูนย์ในประเทศและการอนุมัติยา ท่ามกลางการเพิ่มขึ้นของประชากรสายตาสั้นทั่วโลก (Holden 2016: 4.9 พันล้านคนในปี 20508)) การรักษา RLRL กำลังถูกวางตำแหน่งเป็นหนึ่งในทางเลือกในการจัดการสายตาสั้น
8. เอกสารอ้างอิง
หัวข้อที่มีชื่อว่า “8. เอกสารอ้างอิง”- Jiang Y, Zhu Z, Tan X, et al. Effect of repeated low-level red-light therapy for myopia control in children: a multicenter randomized controlled trial. Ophthalmology. 2022;129:509-519.
- Dong J, Zhu Z, Xu H, et al. Myopia control effect of repeated low-level red-light therapy in Chinese children: a randomized, double-blind, controlled clinical trial. Ophthalmology. 2023;130:198-204.
- Wang W, Jiang Y, Zhu Z, et al. Chorioidal thickening as a potential therapeutic target in myopia management: a review of repeated low-level red light therapy. Surv Ophthalmol. 2023;68:1-12.
- Zeng J, Liu Y, Wang Z, et al. Efficacy of repeated low-level red-light stimulation on slowing myopia progression and ocular growth in children with myopia: a randomized controlled trial. Transl Vis Sci Technol. 2023;12:22.
- Yam JC, Zhang XJ, Zhang Y, et al. Interventions to reduce incidence and progression of myopia in children and adults. Prog Retin Eye Res. 2025.
- Bullimore MA, Ritchey ER, Shah S, et al. The risks and benefits of myopia control. Ophthalmology. 2021;128:1561-1579.
- Haarman AEG, Enthoven CA, Tideman JWL, et al. The complications of myopia: a review and meta-analysis. Invest Ophthalmol Vis Sci. 2020;61:49.
- Holden BA, Fricke TR, Wilson DA, et al. Global prevalence of myopia and high myopia and temporal trends from 2000 through 2050. Ophthalmology. 2016;123:1036-1042.
- 低濃度アトロピン点眼液を用いた近視進行抑制治療の治療指針作成委員会. 低濃度アトロピン点眼液を用いた近視進行抑制治療の手引き. 日眼会誌. 2025;129(10):851-854.
- 近視管理用眼鏡ガイドライン作成委員会. 近視管理用眼鏡(多分割レンズ)ガイドライン(第1版). 日眼会誌. 2025;129(10):855-860.
- Chamberlain P, Peixoto-de-Matos SC, Logan NS, et al. A 3-year randomized clinical trial of MiSight lenses for myopia control. Optom Vis Sci. 2019;96:556-567.
- Lam CSY, Tang WC, Tse DY, et al. Defocus incorporated multiple segments (DIMS) spectacle lenses slow myopia progression: a 2-year randomised clinical trial. Br J Ophthalmol. 2020;104:363-368.
- Si JK, Tang K, Bi HS, et al. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252-257.
- Kinoshita N, Konno Y, Hamada N, et al. Efficacy of combined orthokeratology and 0.01% atropine solution for slowing axial elongation in children with myopia: a 2-year randomized trial. Sci Rep. 2020;10:12750.
- Ueda E, Yasuda M, Fujiwara K, et al. Trends in the prevalence of myopia and myopic maculopathy in a Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2019;60:2781-2786.
