
红光治疗(近视进展控制)
1. 什么是红光治疗(近视控制)?
Section titled “1. 什么是红光治疗(近视控制)?”重复低强度红光疗法(RLRL)是一种非侵入性治疗方法,通过向眼睛照射特定波长(主要为650-670nm)的低强度红色可见光,抑制儿童近视进展。标准方案使用专用手持设备,每天两次、每次3分钟,每周5天。
RLRL疗法的定位
Section titled “RLRL疗法的定位”RLRL疗法是一种相对较新的近视进展控制疗法,自2020年代以来证据迅速积累。它作为传统三大疗法(低浓度阿托品滴眼液、角膜塑形镜和多焦点隐形眼镜)之后的“第四种选择”而受到关注,大多数研究在以中国为中心的东亚地区进行。
近视的主要病理是眼轴延长,眼轴每延长1毫米大约相当于近视增加3屈光度。抑制眼轴延长是近视管理的最重要目标,在评估RLRL疗法的有效性时,眼轴长度的变化是最重要的终点指标1)。
近视的主要并发症包括视网膜脱离(每−1D风险增加30%)、近视性黄斑变性(增加58%)和开角型青光眼(增加20%)6)。RLRL疗法被定位为降低这些长期风险的预防性干预措施。
在亚洲儿童中,近视患病率特别高,如果不治疗而发展为高度近视,视网膜脱离、近视性黄斑变性等严重并发症的风险会大幅增加。据估计,每增加1D近视,视网膜脱离风险增加30%,近视性黄斑变性增加58%,开角型青光眼增加20%,后囊下白内障增加21%6)。
由于眼轴每延长1毫米大约相当于近视增加3D,抑制眼轴延长是近视管理的最重要目标。Haarman等人(2020)的荟萃分析7)表明,近视程度越重,并发症风险呈指数级上升,因此在轻度阶段进行干预对改善长期预后具有重要意义。
RLRL疗法作为与角膜塑形镜和低浓度阿托品滴眼液并列的近视进展控制干预措施之一,自2020年代以来证据迅速积累。在日本,一些机构已将其作为自费治疗引入。Yam等人(2025)的系统评价总结了包括RLRL疗法在内的多种近视进展控制干预措施的证据5)。
另一方面,Bullimore等人(2021)详细探讨了近视管理的总体风险和收益,并指出RLRL疗法在照射参数偏离时存在视网膜光毒性风险6)。适当的设备管理以及遵守照射强度和照射时间是安全使用的前提。
RLRL疗法是一种近视进展抑制治疗,使用650-670nm波段的低强度(0.3-1 mW/cm²)红色可见光,每天两次,每次3分钟照射眼睛。它被认为通过光生物调节增加脉络膜厚度并抑制眼轴延长3)。目前在日本尚未获批,属于自费医疗,需在专科医生管理下使用。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”治疗效果指标
Section titled “治疗效果指标”RLRL疗法的有效性通过以下客观指标评估。
- 眼轴长度:使用光学眼轴长度测量仪测量。追踪治疗前及每6个月的变化。
- 脉络膜厚度:通过OCT测量中心凹下脉络膜厚度(SFCT)。RLRL照射后观察到脉络膜厚度增加。Dong等人(2023)的2年随访研究证实了脉络膜厚度增加2)。
- 等效球镜屈光度:在睫状肌麻痹下进行客观评估。
- 矫正视力:确认治疗前后矫正视力的稳定性。
安全性评估注意事项
Section titled “安全性评估注意事项”RLRL疗法强度低,短期不良事件较少,但需定期确认以下事项。
- 视网膜毒性风险:过度的照射强度、时间或频率理论上可能导致视网膜损伤6)。治疗前通过OCT记录视网膜和脉络膜的分层评估作为基线,并定期比较。
- 视力与色觉变化:确认治疗期间是否有视力下降或色觉异常。
- 主观症状:注意患者是否有眩光、后像或视野异常等主诉。
3. 原因与风险因素
Section titled “3. 原因与风险因素”近视进展的风险因素
Section titled “近视进展的风险因素”RLRL疗法治疗的近视进展涉及以下风险因素。
- 早发(尤其是6至12岁发病)
- 父母近视(特别是双方都近视)
- 近距离用眼时间长(每天超过3小时)
- 户外活动时间不足(每天少于1小时)
- 亚洲民族(东亚人群患病率最高)
- Holden等人(2016)预测,到2050年全球约50%的人口将近视8),早期干预的社会重要性日益增加。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”在开始RLRL治疗前,通过以下检查记录基线并确认适应症。
| 检查项目 | 目的 | 主要确认事项 |
|---|---|---|
| 睫状肌麻痹下屈光检查 | 客观评估近视度数 | 等效球镜度和散光量 |
| 眼轴长度测量 | 基线设定和进展监测 | 通过光学眼轴长度测量仪测量 |
| 眼底检查 | 治疗前视网膜和脉络膜状态 | 确认高度近视性变化 |
| OCT(黄斑和视神经) | 设定视网膜毒性的基准值 | 视网膜和脉络膜分层厚度 |
| 裂隙灯显微镜检查 | 排除眼前节疾病 | 活动性炎症和白内障 |
对于睫状肌麻痹检查,在幼儿中必须使用睫状肌麻痹剂(如1%环戊通滴眼液)。仅进行非睫状肌麻痹的主观验光可能会导致近视度数过高。
治疗中的监测
Section titled “治疗中的监测”为确认治疗效果和安全性,建议遵循以下时间表。
| 时间 | 内容 |
|---|---|
| 1个月后 | 滴眼药依从性、自觉症状确认、矫正视力 |
| 每3~6个月 | 眼轴长度测量、睫状肌麻痹下屈光、OCT(脉络膜厚度、视网膜评估) |
| 每年 | 散瞳眼底检查、OCT血管成像(可选) |
必须通过睫状肌麻痹下屈光检查和光学眼轴长度测量记录基线值。此外,通过眼底检查和OCT记录治疗前的视网膜和脉络膜状态,用于治疗中的安全性监测。如果怀疑高度近视,还需检查周边视网膜有无变性或裂孔。
5. 标准治疗方法
Section titled “5. 标准治疗方法”治疗前的知情同意和适应症评估
Section titled “治疗前的知情同意和适应症评估”选择RLRL疗法患者的基考虑因素如下。
推荐适应症:
需谨慎判断的情况:
- 有视网膜疾病既往史或家族史的病例
- 光敏性疾病(如着色性干皮病、皮肤光敏感等)
- 使用光敏药物时
应避免使用的情况:
- 活动性视网膜疾病(如视网膜变性、新生血管等)
- 确诊为光敏感的患者
主要RCT中采用的标准治疗参数如下所示。
| 参数 | 标准值 | 备注 |
|---|---|---|
| 波长 | 650 nm(红色可见光) | 部分试验使用670 nm |
| 照射强度 | 0.3~1 mW/cm² | 非相干光、非激光 |
| 照射时间 | 3分钟/次 | 每日两次(早晚) |
| 治疗频率 | 5天/周(仅上学日) | — |
| 治疗时长 | 12~24个月或以上 | 需要持续维持效果 |
使用的设备主要是中国制造的专用手持设备(如Suneye等),主要用于研究。患者可以在家中自行照射,但初始设置和定期检查由专科医生进行。
主要随机对照试验结果
Section titled “主要随机对照试验结果”Jiang等人(2022)为期1年的随机对照试验显示,RLRL组的眼轴延长为0.10毫米/年(对照组0.38毫米/年),显著抑制了眼轴增长1)。Dong等人(2023)的2年随访显示,眼轴延长抑制效果持续,并确认脉络膜厚度增加2)。
Zeng等人(2023)的多中心随机对照试验显示,1年等效球镜进展治疗组为−0.20 D(对照组−0.71 D),近视进展抑制约72%4)。
RLRL疗法与其他近视进展抑制方法的疗效比较:
| 干预措施 | 屈光抑制率 | 眼轴抑制率 | 主要证据 |
|---|---|---|---|
| RLRL疗法 | 72%(Zeng 2023) | 74%(Jiang 2022) | 多项随机对照试验 |
| 低浓度阿托品0.05% | 高达67% | — | LAMP试验 |
| 角膜塑形镜 | — | 43% | Si 2015荟萃分析 |
| MiSight(多焦点隐形眼镜) | 59% | 52% | Chamberlain 2019 |
| DIMS眼镜 | 55~59% | 37~38% | Lam 2020随机对照试验 |
然而,由于试验设计、目标年龄和治疗持续时间不同,直接比较需谨慎5)。低浓度阿托品滴眼液(Rijusea® Mini 0.025%)是2024年12月在日本唯一获批的药物9),近视管理眼镜片(如DIMS)10)也得到日本近视学会指南推荐。RLRL疗法正被定位为与这些已批准干预措施联合使用的选择。
与MiSight(多焦点CL)的3年RCT11)、DIMS眼镜的2年RCT12)、OK的荟萃分析13)以及OK+阿托品联合RCT14)的数据相比,RLRL疗法的短期抑制率良好,但最大挑战是尚缺乏5年以上的数据。久山町研究15)显示的日本人近视性黄斑病变增加趋势,进一步支持了包括RLRL疗法在内的近视管理干预的医学重要性。
与其他疗法联合
Section titled “与其他疗法联合”- RLRL + 低浓度阿托品:由于两者作用机制不同,预期有相加或协同效应,但大规模RCT的验证仍在进行中5)。
- RLRL + 角膜塑形镜:有报道用于快速进展病例的联合选择。
- 当单药治疗效果不足时,考虑与其他近视进展抑制疗法联合使用。
截至2026年4月,RLRL疗法在日本尚未获得药事批准和医保覆盖,作为自费诊疗提供。需要向患者和监护人充分说明以下内容并获得同意。
- 该疗法在日本未获药事批准。
- 目前的证据主要来自1-2年的观察性研究,长期安全性尚未确立。
- 理论上存在偏离照射参数时的视网膜毒性风险6)。
- 这是近视的“进展抑制”而非“治疗”。
- 必须定期进行眼科检查和安全性监测。
RLRL在近视进展控制机制中的定位
Section titled “RLRL在近视进展控制机制中的定位”近视进展控制的主要光学干预措施(角膜塑形镜、DIMS眼镜、多焦点隐形眼镜)的共同机制是“周边近视性离焦假说”,而RLRL疗法通过完全不同的途径发挥作用:光生物调节(PBM)→ 线粒体激活 → 脉络膜血流改善 → 脉络膜增厚 → 眼轴延长抑制。这种不同的作用机制有望与其他疗法联合产生协同效应3)。
此外,RLRL疗法的一个独特之处在于观察到治疗后脉络膜厚度立即增加的急性生理反应2)。这是其他近视进展控制疗法所没有的特征,因此脉络膜厚度的测量可作为治疗即时效果指标。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”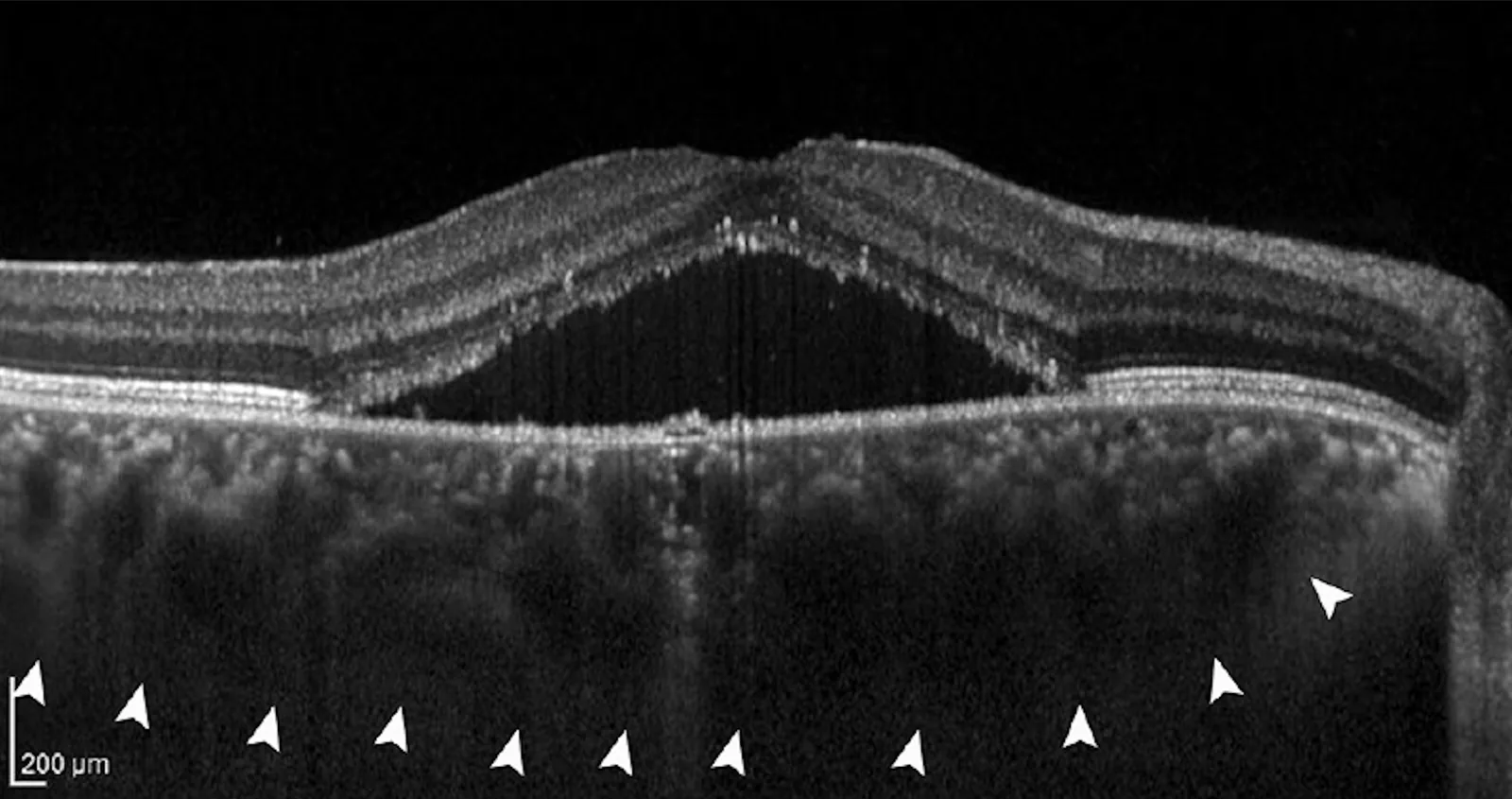
光生物调节(Photobiomodulation: PBM)
Section titled “光生物调节(Photobiomodulation: PBM)”RLRL疗法的主要机制被认为是光生物调节(PBM)3)。650-670nm波段的红光被线粒体中的细胞色素c氧化酶(复合物IV)特异性吸收,诱导以下生物反应。
- 促进ATP产生
- 通过适度产生活性氧(ROS)激活细胞信号
- 通过一氧化氮(NO)释放引起血管扩张和血流增加
- 改善脉络膜循环并使其增厚
脉络膜增厚与眼轴延长抑制
Section titled “脉络膜增厚与眼轴延长抑制”一致观察到RLRL照射后脉络膜厚度增加2)3)。脉络膜厚度的增加被认为会影响眼球壁的刚性,从而有助于抑制眼轴延长。角膜塑形镜和低浓度阿托品也报告了脉络膜厚度的增加,脉络膜作为近视进展控制的共同通路受到关注。
近视进展的基本机制
Section titled “近视进展的基本机制”近视进展是一个通过从视网膜到巩膜的信号传导调节眼球生长的生物学过程,涉及以下步骤:
- 周边远视性离焦作为眼轴延长的驱动信号
- 多巴胺介导的生长抑制信号制动眼轴延长
- 巩膜的细胞外基质重塑决定眼轴长度
- 脉络膜的增厚和变薄作为眼轴长度变化的生物标志物
RLRL疗法干预这些信号通路,在脉络膜和巩膜水平制动眼球生长,但全貌尚有许多未解之处3)。Haarman等人(2020)的荟萃分析显示的近视并发症定量风险被广泛引用为治疗干预的医学依据7)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”长期有效性和安全性数据的建立
Section titled “长期有效性和安全性数据的建立”目前主要的随机对照试验观察期为1-2年,5年以上的长期数据缺乏1)2)。治疗停止后的效果持续性(携带效应)也尚未确定,追踪治疗结束后近视进展速度变化的研究正在进行中。
Dong等人(2023)的2年随访研究显示,RLRL治疗组与对照组相比,持续抑制眼轴延长并增加脉络膜厚度,连续使用1年效果得以维持2)。但由于研究设计、照射参数和目标年龄在不同研究间存在差异,直接比较需谨慎。
视网膜毒性风险的量化
Section titled “视网膜毒性风险的量化”理论上,过度的照射强度、时间或频率可能导致视网膜损伤。Bullimore等人(2021)的近视管理风险-效益评估中,讨论了包括RLRL疗法在内的光学和药物干预的整体安全性平衡,强调了适当参数管理的重要性6)。
旨在设定安全照射限值和风险评估的研究正在进行。临床实践中,必须严格遵守照射强度(0.3-1 mW/cm²)、照射时间(3分钟/次)和照射频率(每天2次,每周5天),并定期校准设备。
从光毒性角度来看,光感受器和RPE的累积光暴露量很重要,需注意超过推荐量的照射(特别是高强度、长时间的超说明书使用)。正如Haarman等人(2020)的近视并发症荟萃分析所示7),在适当近视管理可降低严重并发症风险的前提下,个体化评估RLRL疗法的风险-效益至关重要。
与低浓度阿托品和角膜塑形镜的直接比较
Section titled “与低浓度阿托品和角膜塑形镜的直接比较”RLRL疗法与角膜塑形镜、低浓度阿托品的直接比较随机对照试验正在进行中。期待建立考虑各疗法优缺点的个性化近视管理方案5)。
三大干预措施(RLRL、OK、低浓度阿托品)的特性比较:
| 干预措施 | 眼轴抑制率 | 侵入性 | 便利性 | 日本监管状态 |
|---|---|---|---|---|
| RLRL疗法 | 约60-72% | 非侵入性 | 可在家进行 | 未批准(自费) |
| 角膜塑形镜 | 30–50% | 接触角膜 | 夜间佩戴 | 未批准(自费) |
| 低浓度阿托品0.025% | 约62% | 滴眼液 | 睡前滴眼 | 已批准 |
利用人工智能预测近视进展
Section titled “利用人工智能预测近视进展”利用人工智能整合分析眼轴长度数据、风险因素和治疗反应,为每位患者提出最佳治疗策略的模型正在开发中。该技术也可能应用于预测RLRL疗法的应答者。
国内批准动向
Section titled “国内批准动向”随着中国和东南亚地区证据的积累,日本可能与监管机构开始对话。国内多中心随机对照试验的实施和药物审批进展备受关注。在全球近视人口增加的背景下(Holden 2016:2050年达49亿人8)),RLRL疗法正逐渐成为近视管理的选择之一。
8. 参考文献
Section titled “8. 参考文献”- Jiang Y, Zhu Z, Tan X, et al. Effect of repeated low-level red-light therapy for myopia control in children: a multicenter randomized controlled trial. Ophthalmology. 2022;129:509-519.
- Dong J, Zhu Z, Xu H, et al. Myopia control effect of repeated low-level red-light therapy in Chinese children: a randomized, double-blind, controlled clinical trial. Ophthalmology. 2023;130:198-204.
- Wang W, Jiang Y, Zhu Z, et al. Chorioidal thickening as a potential therapeutic target in myopia management: a review of repeated low-level red light therapy. Surv Ophthalmol. 2023;68:1-12.
- Zeng J, Liu Y, Wang Z, et al. Efficacy of repeated low-level red-light stimulation on slowing myopia progression and ocular growth in children with myopia: a randomized controlled trial. Transl Vis Sci Technol. 2023;12:22.
- Yam JC, Zhang XJ, Zhang Y, et al. Interventions to reduce incidence and progression of myopia in children and adults. Prog Retin Eye Res. 2025.
- Bullimore MA, Ritchey ER, Shah S, et al. The risks and benefits of myopia control. Ophthalmology. 2021;128:1561-1579.
- Haarman AEG, Enthoven CA, Tideman JWL, et al. The complications of myopia: a review and meta-analysis. Invest Ophthalmol Vis Sci. 2020;61:49.
- Holden BA, Fricke TR, Wilson DA, et al. Global prevalence of myopia and high myopia and temporal trends from 2000 through 2050. Ophthalmology. 2016;123:1036-1042.
- 低濃度アトロピン点眼液を用いた近視進行抑制治療の治療指針作成委員会. 低濃度アトロピン点眼液を用いた近視進行抑制治療の手引き. 日眼会誌. 2025;129(10):851-854.
- 近視管理用眼鏡ガイドライン作成委員会. 近視管理用眼鏡(多分割レンズ)ガイドライン(第1版). 日眼会誌. 2025;129(10):855-860.
- Chamberlain P, Peixoto-de-Matos SC, Logan NS, et al. A 3-year randomized clinical trial of MiSight lenses for myopia control. Optom Vis Sci. 2019;96:556-567.
- Lam CSY, Tang WC, Tse DY, et al. Defocus incorporated multiple segments (DIMS) spectacle lenses slow myopia progression: a 2-year randomised clinical trial. Br J Ophthalmol. 2020;104:363-368.
- Si JK, Tang K, Bi HS, et al. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252-257.
- Kinoshita N, Konno Y, Hamada N, et al. Efficacy of combined orthokeratology and 0.01% atropine solution for slowing axial elongation in children with myopia: a 2-year randomized trial. Sci Rep. 2020;10:12750.
- Ueda E, Yasuda M, Fujiwara K, et al. Trends in the prevalence of myopia and myopic maculopathy in a Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2019;60:2781-2786.
