
Traitement par lumière rouge (freination de la progression de la myopie)
1. Qu’est-ce que la thérapie par lumière rouge (ralentissement de la progression de la myopie) ?
Section intitulée « 1. Qu’est-ce que la thérapie par lumière rouge (ralentissement de la progression de la myopie) ? »La thérapie par lumière rouge de faible intensité répétée (Repeated Low-Level Red Light Therapy : RLRL) est une méthode non invasive qui consiste à exposer l’œil à une lumière rouge visible de longueur d’onde spécifique (principalement 650 à 670 nm) à faible intensité pour ralentir la progression de la myopie chez l’enfant. Le protocole standard utilise un appareil portable dédié, avec des séances de 3 minutes deux fois par jour, cinq jours par semaine.
Place de la thérapie RLRL
Section intitulée « Place de la thérapie RLRL »La thérapie RLRL est une méthode relativement nouvelle de ralentissement de la progression de la myopie, dont les preuves se sont accumulées rapidement à partir des années 2020. Elle est considérée comme la « quatrième option » après les trois principales thérapies conventionnelles (collyre à l’atropine faible dose, orthokératologie, lentilles de contact multifocales), et la plupart des recherches sont menées en Asie de l’Est, principalement en Chine.
La myopie est principalement due à l’allongement de l’axe oculaire : un allongement de 1 mm correspond à environ 3 D de myopie. La suppression de l’allongement axial est l’objectif le plus important de la gestion de la myopie, et le changement de la longueur axiale est le critère d’évaluation principal de l’efficacité de la thérapie RLRL 1).
Les principales complications associées à la myopie comprennent le décollement de la rétine (risque augmenté de 30 % par dioptrie de myopie), la dégénérescence maculaire myopique (augmentation de 58 %) et le glaucome à angle ouvert (augmentation de 20 %) 6). La thérapie RLRL est considérée comme une intervention préventive pour réduire ces risques à long terme.
Chez les enfants asiatiques, la prévalence de la myopie est particulièrement élevée, et si elle n’est pas traitée, elle augmente considérablement le risque de complications graves telles que le décollement de la rétine et la dégénérescence maculaire myopique. On estime que pour chaque augmentation de 1D de la myopie, le risque de décollement de la rétine augmente de 30 %, celui de la dégénérescence maculaire myopique de 58 %, celui du glaucome à angle ouvert de 20 % et celui de la cataracte sous-capsulaire postérieure de 21 % 6).
Étant donné qu’un allongement de 1 mm de la longueur axiale correspond à environ 3D de myopie, la suppression de l’allongement axial est l’objectif le plus important de la gestion de la myopie. La méta-analyse de Haarman et al. (2020) 7) a montré que le risque de complications augmente de façon exponentielle avec la sévérité de la myopie, ce qui souligne l’importance d’une intervention précoce pour améliorer le pronostic à long terme.
La thérapie RLRL est l’une des interventions de contrôle de la progression de la myopie, aux côtés de l’orthokératologie et des gouttes d’atropine à faible concentration, et les preuves se sont accumulées rapidement depuis les années 2020. Au Japon, elle est introduite comme traitement privé dans certains établissements. La revue systématique de Yam et al. (2025) résume les preuves de plusieurs interventions de contrôle de la progression de la myopie, y compris la thérapie RLRL 5).
D’autre part, Bullimore et al. (2021) ont examiné en détail les risques et les avantages de la gestion de la myopie en général, et ont souligné que la thérapie RLRL comporte un risque de phototoxicité rétinienne en cas de déviation des paramètres d’irradiation 6). Une gestion appropriée de l’appareil, le respect de l’intensité et de la durée d’irradiation sont des conditions préalables à une utilisation sûre.
La thérapie RLRL est un traitement de freination de la progression de la myopie qui consiste à exposer l’œil à une lumière rouge visible de 650 à 670 nm à faible intensité (0,3 à 1 mW/cm²) deux fois par jour pendant 3 minutes. On pense qu’elle augmente l’épaisseur de la choroïde via la photobiomodulation et inhibe l’allongement axial 3). Actuellement, il s’agit d’un traitement non approuvé au Japon, pratiqué en médecine privée, et utilisé sous la supervision d’un spécialiste.
2. Principaux symptômes et signes cliniques
Section intitulée « 2. Principaux symptômes et signes cliniques »Indicateurs de l’efficacité du traitement
Section intitulée « Indicateurs de l’efficacité du traitement »L’efficacité de la thérapie RLRL est évaluée à l’aide des indicateurs objectifs suivants.
- Longueur axiale : mesurée par un appareil de mesure optique de la longueur axiale. Suivi des changements avant et après le traitement, tous les 6 mois.
- Épaisseur de la choroïde : mesure de l’épaisseur choroïdienne sous-fovéale (SFCT) par OCT. Une augmentation de l’épaisseur choroïdienne est observée après l’irradiation RLRL. L’étude de suivi sur 2 ans de Dong et al. (2023) a confirmé une augmentation de l’épaisseur choroïdienne 2).
- Équivalent sphérique : évaluation objective sous cycloplégie.
- Acuité visuelle corrigée : confirmation de la stabilité de l’acuité visuelle corrigée avant et après le traitement.
Précautions d’évaluation de la sécurité
Section intitulée « Précautions d’évaluation de la sécurité »Le traitement RLRL étant de faible intensité, les effets indésirables à court terme sont considérés comme rares, mais les points suivants doivent être vérifiés régulièrement.
- Risque de toxicité rétinienne : une intensité, une durée ou une fréquence d’irradiation excessive peut théoriquement provoquer des lésions rétiniennes6). Une évaluation stratifiée de la rétine et de la choroïde par OCT doit être enregistrée comme référence avant le traitement et comparée régulièrement.
- Modifications de l’acuité visuelle et de la vision des couleurs : vérifier la présence d’une baisse de l’acuité visuelle ou d’anomalies de la vision des couleurs pendant le traitement.
- Symptômes subjectifs : prêter attention aux plaintes telles que l’éblouissement, les images rémanentes ou les anomalies du champ visuel.
3. Causes et facteurs de risque
Section intitulée « 3. Causes et facteurs de risque »Facteurs de risque de progression de la myopie
Section intitulée « Facteurs de risque de progression de la myopie »La progression de la myopie, cible du traitement RLRL, implique les facteurs de risque suivants.
- Apparition précoce (notamment entre 6 et 12 ans)
- Parents myopes (surtout si les deux le sont)
- Temps prolongé passé en vision de près (plus de 3 heures par jour)
- Temps insuffisant passé en extérieur (moins d’une heure par jour)
- Ethnie asiatique (prévalence la plus élevée en Asie de l’Est)
- Selon les prévisions de Holden et al. (2016), environ 50 % de la population mondiale serait myope d’ici 20508), ce qui souligne l’importance sociale croissante d’une intervention précoce.
4. Diagnostic et méthodes d’examen
Section intitulée « 4. Diagnostic et méthodes d’examen »Évaluation avant le début du traitement
Section intitulée « Évaluation avant le début du traitement »Avant de commencer le traitement RLRL, effectuez les examens suivants pour enregistrer les valeurs de base et confirmer les indications.
| Examen | Objectif | Principaux points à vérifier |
|---|---|---|
| Réfraction sous cycloplégie | Évaluation objective du degré de myopie | Équivalent sphérique et cylindre |
| Mesure de la longueur axiale | Définition de la ligne de base et suivi de la progression | Mesurée par biométrie optique |
| Examen du fond d’œil | État rétinien et choroïdien avant traitement | Vérification des modifications myopiques sévères |
| OCT (macula et nerf optique) | Établissement des valeurs de référence pour la toxicité rétinienne | Épaisseur des couches rétiniennes et choroïdiennes |
| Examen à la lampe à fente | Exclusion des pathologies du segment antérieur | Inflammation active / cataracte |
Pour l’examen sous cycloplégie, l’instillation d’un cycloplégique (par exemple, Cyclopentolate 1%) est indispensable chez les jeunes enfants. Un examen subjectif sans cycloplégie peut conduire à une surévaluation de la puissance myopique.
Surveillance pendant le traitement
Section intitulée « Surveillance pendant le traitement »Pour confirmer l’efficacité et la sécurité du traitement, le calendrier suivant est recommandé.
| Période | Contenu |
|---|---|
| 1 mois plus tard | Observance du collyre, vérification des symptômes subjectifs, acuité visuelle corrigée |
| Tous les 3 à 6 mois | Mesure de la longueur axiale, réfraction sous cycloplégie, OCT (épaisseur choroïdienne, évaluation rétinienne) |
| Tous les ans | Examen du fond d’œil sous dilatation, OCT-angiographie (optionnel) |
Il est essentiel d’enregistrer les valeurs de base par réfraction sous cycloplégie et mesure optique de la longueur axiale. De plus, l’état de la rétine et de la choroïde avant le traitement doit être documenté par un examen du fond d’œil et une OCT, afin d’être utilisé pour la surveillance de la sécurité pendant le traitement. En cas de suspicion de myopie forte, vérifiez également la présence de dégénérescence ou de déchirures rétiniennes périphériques.
5. Traitement standard
Section intitulée « 5. Traitement standard »Consentement éclairé et évaluation de l’indication avant le traitement
Section intitulée « Consentement éclairé et évaluation de l’indication avant le traitement »Les éléments de base pour la sélection des patients éligibles à la thérapie RLRL sont présentés ci-dessous.
Indications recommandées :
- 6 à 18 ans (la plupart des études portent sur cette tranche d’âge)
- Myopie sphérique équivalente ≥ −0,5 D avec progression confirmée
- Myopie confirmée par examen sous cycloplégie
- Environnement permettant aux parents d’assurer une gestion appropriée
Situations nécessitant une évaluation prudente:
- Antécédents personnels ou familiaux de maladie rétinienne
- Maladies de photosensibilité (xeroderma pigmentosum, photosensibilisation cutanée, etc.)
- Utilisation de médicaments photosensibilisants
Situations à éviter:
- Maladie rétinienne active (dégénérescence rétinienne, néovascularisation, etc.)
- Patient avec un diagnostic confirmé de photosensibilité
Protocole de traitement
Section intitulée « Protocole de traitement »Les paramètres de traitement standard adoptés dans les principaux essais cliniques randomisés sont présentés ci-dessous.
| Paramètre | Valeur standard | Remarques |
|---|---|---|
| Longueur d’onde | 650 nm (lumière visible rouge) | 670 nm utilisé dans certains essais |
| Intensité d’irradiation | 0,3 à 1 mW/cm² | Lumière non cohérente, non laser |
| Temps d’irradiation | 3 minutes/séance | 2 fois par jour (matin et soir) |
| Fréquence du traitement | 5 jours/semaine (jours d’école uniquement) | — |
| Durée du traitement | 12 à 24 mois ou plus | Maintien de l’effet nécessaire en continu |
L’appareil utilisé est principalement un dispositif portable spécialisé fabriqué en Chine (Suneye, etc.) qui a été utilisé dans la recherche. Il est conçu pour que les patients puissent effectuer une auto-irradiation à domicile, mais la configuration initiale et les contrôles réguliers sont effectués par un médecin spécialiste.
Résultats des principaux essais contrôlés randomisés
Section intitulée « Résultats des principaux essais contrôlés randomisés »Dans un essai contrôlé randomisé d’un an mené par Jiang et al. (2022), le groupe RLRL a montré une inhibition significative de l’allongement axial de 0,10 mm/an (groupe témoin 0,38 mm/an)1). Dans le suivi de deux ans de Dong et al. (2023), l’effet inhibiteur sur l’allongement axial s’est maintenu et une augmentation de l’épaisseur choroïdienne a été confirmée2).
Dans l’essai contrôlé randomisé multicentrique de Zeng et al. (2023), la progression de l’équivalent sphérique sur un an était de −0,20 D dans le groupe traité (groupe témoin −0,71 D), inhibant la progression de la myopie d’environ 72 %4).
Comparaison de l’efficacité de la thérapie RLRL avec d’autres méthodes de contrôle de la progression de la myopie :
| Intervention | Taux d’inhibition de la réfraction | Taux d’inhibition axiale | Principales preuves |
|---|---|---|---|
| Traitement RLRL | 72 % (Zeng 2023) | 74 % (Jiang 2022) | Plusieurs ECR |
| Atropine à faible concentration 0,05 % | Jusqu’à 67 % | — | Essai LAMP |
| Orthokératologie | — | 43 % | Si 2015 méta-analyse |
| MiSight (lentilles multifocales) | 59 % | 52 % | Chamberlain 2019 |
| Lunettes DIMS | 55 à 59% | 37 à 38% | Essai clinique randomisé Lam 2020 |
Cependant, comme les schémas d’étude, les âges cibles et les durées de traitement diffèrent, une comparaison directe nécessite de la prudence5). Les collyres à l’atropine à faible concentration (Rijusea® Mini 0,025 %) sont le seul médicament approuvé au Japon en décembre 20249), et les verres de lunettes pour la gestion de la myopie (DIMS, etc.)10) sont également recommandés par les directives de la Société japonaise de la myopie. La thérapie RLRL est en train d’être positionnée comme une option à combiner avec ces interventions approuvées.
En comparaison avec les données de l’essai clinique randomisé de 3 ans sur MiSight (lentilles de contact multifocales)11), de l’essai clinique randomisé de 2 ans sur les lunettes DIMS12), de la méta-analyse de l’orthokératologie13) et de l’essai clinique randomisé combinant orthokératologie et atropine14), le taux de contrôle à court terme de la thérapie RLRL est bon, mais l’absence de données sur plus de 5 ans constitue le plus grand défi. La tendance à l’augmentation de la maculopathie myopique chez les Japonais, mise en évidence par l’étude de Hisayama15), confirme davantage l’importance médicale des interventions de gestion de la myopie, y compris la thérapie RLRL.
Combinaison avec d’autres thérapies
Section intitulée « Combinaison avec d’autres thérapies »- RLRL + atropine à faible concentration : Comme leurs mécanismes d’action sont différents, un effet additif ou synergique est attendu, mais la validation par des essais cliniques randomisés à grande échelle se poursuit5).
- RLRL + orthokératologie : une combinaison rapportée pour les cas de progression rapide.
- En cas d’efficacité insuffisante en monothérapie, envisager une combinaison avec d’autres traitements de freination de la myopie.
Consentement éclairé
Section intitulée « Consentement éclairé »En avril 2026, la thérapie RLRL n’est ni approuvée ni remboursée au Japon ; elle est proposée en soins à titre privé. Il est nécessaire d’expliquer pleinement ce qui suit au patient et à ses parents et d’obtenir leur consentement.
- Il s’agit d’un traitement non approuvé au Japon.
- Les preuves actuelles proviennent principalement d’études observationnelles d’un à deux ans ; la sécurité à long terme n’est pas établie.
- Il existe un risque théorique de toxicité rétinienne en cas de déviation des paramètres d’irradiation6).
- Il s’agit d’un « freinage » de la progression de la myopie, et non d’un « traitement » curatif.
- Des visites ophtalmologiques régulières et un suivi de sécurité sont obligatoires.
En avril 2026, la thérapie RLRL n’est pas approuvée par les autorités réglementaires ni remboursée par l’assurance maladie au Japon. Elle est proposée comme service payant dans certaines cliniques ophtalmologiques. Lors de la consultation, il est important de vérifier auprès d’un spécialiste l’indication, la sécurité et le coût. Les gouttes ophtalmiques d’atropine à faible concentration (Rijusea® Mini 0,025 %) ont été approuvées en décembre 2024 comme premier médicament de contrôle de la progression de la myopie au Japon, et constituent une option de traitement remboursée.
Place de la RLRL dans le mécanisme de contrôle de la progression de la myopie
Section intitulée « Place de la RLRL dans le mécanisme de contrôle de la progression de la myopie »Les principales interventions optiques pour contrôler la progression de la myopie (orthokératologie, lunettes DIMS, lentilles de contact multifocales) partagent un mécanisme commun basé sur l’hypothèse du défocus myopique périphérique, tandis que la thérapie RLRL agit par une voie totalement différente : activation mitochondriale via la photobiomodulation (PBM), amélioration du flux sanguin choroïdien, épaississement choroïdien et inhibition de l’allongement axial. Ce mécanisme d’action distinct suscite l’espoir d’un effet synergique en combinaison avec d’autres thérapies 3).
De plus, une caractéristique unique de la thérapie RLRL est l’observation d’une réponse physiologique aiguë, avec une augmentation immédiate de l’épaisseur choroïdienne après le traitement 2). Cette particularité, absente dans les autres thérapies de contrôle de la myopie, fait de la mesure de l’épaisseur choroïdienne un indicateur utile de l’effet immédiat du traitement.
6. Physiopathologie et mécanismes détaillés
Section intitulée « 6. Physiopathologie et mécanismes détaillés »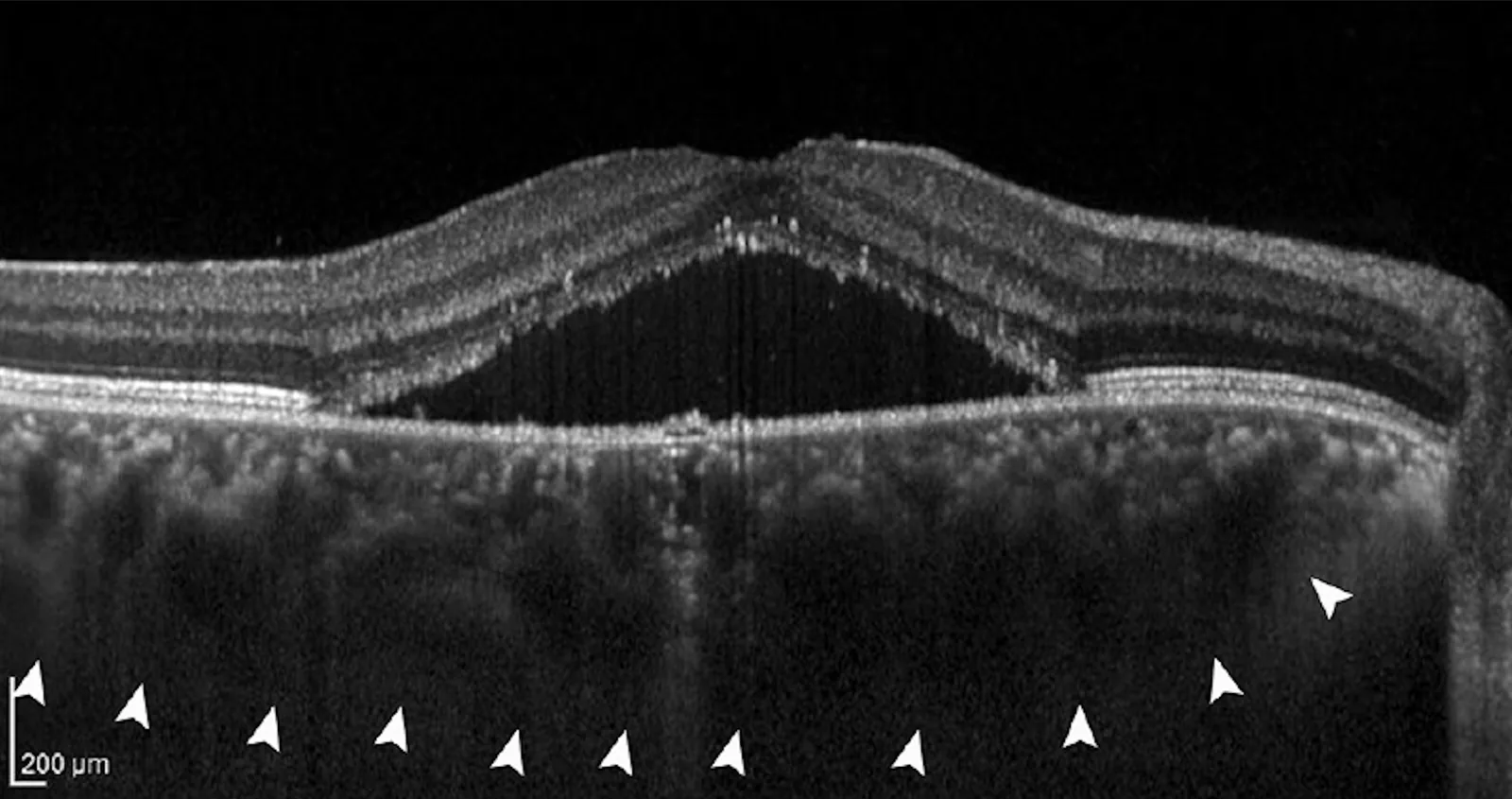
Photobiomodulation (PBM)
Section intitulée « Photobiomodulation (PBM) »Le mécanisme principal de la thérapie RLRL est la photobiomodulation (PBM) 3). La lumière rouge dans la bande de 650 à 670 nm est spécifiquement absorbée par la cytochrome c oxydase (Complexe IV) présente dans les mitochondries cellulaires, induisant les réponses biologiques suivantes.
- Promotion de la production d’ATP
- Activation de la signalisation cellulaire par une production modérée d’espèces réactives de l’oxygène (ROS)
- Vasodilatation et augmentation du flux sanguin par libération d’oxyde nitrique (NO)
- Amélioration de la circulation et épaississement de la choroïde
Épaississement choroïdien et inhibition de l’allongement axial
Section intitulée « Épaississement choroïdien et inhibition de l’allongement axial »Une augmentation de l’épaisseur choroïdienne après irradiation RLRL a été systématiquement observée2)3). On pense que l’augmentation de l’épaisseur choroïdienne affecte la rigidité de la paroi oculaire et contribue à inhiber l’allongement axial. Une augmentation de l’épaisseur choroïdienne a également été rapportée avec l’orthokératologie et l’atropine à faible concentration, ce qui suggère que la choroïde pourrait être une voie commune dans l’inhibition de la progression de la myopie.
Mécanisme fondamental de la progression de la myopie
Section intitulée « Mécanisme fondamental de la progression de la myopie »La progression de la myopie est un processus biologique dans lequel la croissance oculaire est régulée par la transmission de signaux de la rétine à la sclère, impliquant les étapes suivantes.
- Le défocus hypermétropique périphérique est le signal moteur de l’allongement axial
- Le signal inhibiteur de croissance médié par la dopamine freine l’allongement axial
- Le remodelage de la matrice extracellulaire de la sclère détermine la longueur axiale
- L’épaississement ou l’amincissement de la choroïde est un biomarqueur des changements de longueur axiale
La thérapie RLRL intervient dans ces voies de signalisation et freine la croissance oculaire au niveau de la choroïde et de la sclère, mais une grande partie reste inexpliquée 3). Le risque quantitatif des complications de la myopie, tel que présenté par la méta-analyse de Haarman et al. (2020), est largement cité comme base médicale pour l’intervention thérapeutique 7).
7. Recherches récentes et perspectives futures
Section intitulée « 7. Recherches récentes et perspectives futures »Établissement de données de sécurité et d’efficacité à long terme
Section intitulée « Établissement de données de sécurité et d’efficacité à long terme »Les principaux essais contrôlés randomisés actuels ont une période d’observation de 1 à 2 ans, et les données à long terme de plus de 5 ans sont rares1)2). La persistance de l’effet après l’arrêt du traitement (effet de report) n’est pas encore établie, et des études sont en cours pour suivre l’évolution de la vitesse de progression de la myopie après la fin du traitement.
Dans l’étude de suivi de 2 ans de Dong et al. (2023), le groupe traité par RLRL a montré une suppression continue de l’allongement axial et une augmentation de l’épaisseur choroïdienne par rapport au groupe témoin, confirmant le maintien de l’effet après un an d’utilisation continue2). Cependant, comme les conceptions d’étude, les paramètres d’irradiation et les âges des sujets diffèrent entre les études, une comparaison directe nécessite de la prudence.
Quantification du risque de toxicité rétinienne
Section intitulée « Quantification du risque de toxicité rétinienne »Il existe théoriquement un risque de lésion rétinienne en cas d’intensité, de durée ou de fréquence d’irradiation excessives. Dans l’évaluation des risques et bénéfices de la gestion de la myopie par Bullimore et al. (2021), l’équilibre global de sécurité des interventions optiques et pharmacologiques, y compris la thérapie RLRL, est discuté, soulignant l’importance d’une gestion appropriée des paramètres6).
Des études sont menées pour définir les limites d’irradiation sécuritaires et évaluer les risques. En pratique clinique, il est nécessaire de respecter strictement l’intensité d’irradiation (0,3 à 1 mW/cm²), la durée d’irradiation (3 minutes par séance) et la fréquence d’irradiation (2 fois par jour, 5 jours par semaine), et de vérifier régulièrement l’étalonnage de l’appareil.
Du point de vue de la phototoxicité, l’exposition lumineuse cumulative aux photorécepteurs et à l’EPR est importante, et une attention particulière est nécessaire en cas d’irradiation dépassant la dose recommandée (notamment une utilisation abusive de haute intensité et de longue durée). Comme le montre la méta-analyse des complications de la myopie de Haarman et al. (2020)7), il est important d’évaluer individuellement le rapport risque-bénéfice de la thérapie RLRL, en partant du principe qu’une gestion appropriée de la myopie peut réduire le risque de complications graves.
Comparaison directe avec l’atropine à faible concentration et l’orthokératologie
Section intitulée « Comparaison directe avec l’atropine à faible concentration et l’orthokératologie »Des essais contrôlés randomisés comparant directement la thérapie RLRL à l’orthokératologie et à l’atropine à faible concentration sont en cours. On espère établir un protocole personnalisé de gestion de la myopie tenant compte des avantages et des inconvénients de chaque thérapie5).
Comparaison des caractéristiques des trois principales interventions (RLRL, OK, atropine à faible concentration) :
| Intervention | Taux de suppression de l’axe oculaire | Invasivité | Commodité | Statut réglementaire au Japon |
|---|---|---|---|---|
| Thérapie RLRL | Environ 60 à 72 % | Non invasif | Réalisable à domicile | Non approuvé (à titre privé) |
| Orthokératologie | 30 à 50 % | Contact cornéen présent | Port nocturne | Non approuvé (à titre privé) |
| Atropine à faible concentration 0,025 % | Environ 62 % | Instillation | Instillation avant le coucher | Approuvé |
Prédiction de la progression de la myopie à l’aide de l’IA
Section intitulée « Prédiction de la progression de la myopie à l’aide de l’IA »Le développement de modèles qui intègrent les données de longueur axiale, les facteurs de risque et la réponse au traitement via l’IA pour proposer des stratégies thérapeutiques optimales pour chaque patient progresse. Cela pourrait également être appliqué à la prédiction des répondeurs à la thérapie RLRL.
Tendances vers l’approbation nationale
Section intitulée « Tendances vers l’approbation nationale »Suite à l’accumulation de preuves en Chine et en Asie du Sud-Est, des dialogues avec les autorités réglementaires pourraient être initiés au Japon. L’attention se porte sur la réalisation d’essais contrôlés randomisés multicentriques nationaux et sur les démarches en vue de l’approbation réglementaire. Dans le contexte de l’augmentation mondiale de la population myope (Holden 2016 : 4,9 milliards de personnes en 20508)), la thérapie RLRL est en train de s’imposer comme une option de gestion de la myopie.
8. Références
Section intitulée « 8. Références »- Jiang Y, Zhu Z, Tan X, et al. Effect of repeated low-level red-light therapy for myopia control in children: a multicenter randomized controlled trial. Ophthalmology. 2022;129:509-519.
- Dong J, Zhu Z, Xu H, et al. Myopia control effect of repeated low-level red-light therapy in Chinese children: a randomized, double-blind, controlled clinical trial. Ophthalmology. 2023;130:198-204.
- Wang W, Jiang Y, Zhu Z, et al. Chorioidal thickening as a potential therapeutic target in myopia management: a review of repeated low-level red light therapy. Surv Ophthalmol. 2023;68:1-12.
- Zeng J, Liu Y, Wang Z, et al. Efficacy of repeated low-level red-light stimulation on slowing myopia progression and ocular growth in children with myopia: a randomized controlled trial. Transl Vis Sci Technol. 2023;12:22.
- Yam JC, Zhang XJ, Zhang Y, et al. Interventions to reduce incidence and progression of myopia in children and adults. Prog Retin Eye Res. 2025.
- Bullimore MA, Ritchey ER, Shah S, et al. The risks and benefits of myopia control. Ophthalmology. 2021;128:1561-1579.
- Haarman AEG, Enthoven CA, Tideman JWL, et al. The complications of myopia: a review and meta-analysis. Invest Ophthalmol Vis Sci. 2020;61:49.
- Holden BA, Fricke TR, Wilson DA, et al. Global prevalence of myopia and high myopia and temporal trends from 2000 through 2050. Ophthalmology. 2016;123:1036-1042.
- 低濃度アトロピン点眼液を用いた近視進行抑制治療の治療指針作成委員会. 低濃度アトロピン点眼液を用いた近視進行抑制治療の手引き. 日眼会誌. 2025;129(10):851-854.
- 近視管理用眼鏡ガイドライン作成委員会. 近視管理用眼鏡(多分割レンズ)ガイドライン(第1版). 日眼会誌. 2025;129(10):855-860.
- Chamberlain P, Peixoto-de-Matos SC, Logan NS, et al. A 3-year randomized clinical trial of MiSight lenses for myopia control. Optom Vis Sci. 2019;96:556-567.
- Lam CSY, Tang WC, Tse DY, et al. Defocus incorporated multiple segments (DIMS) spectacle lenses slow myopia progression: a 2-year randomised clinical trial. Br J Ophthalmol. 2020;104:363-368.
- Si JK, Tang K, Bi HS, et al. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252-257.
- Kinoshita N, Konno Y, Hamada N, et al. Efficacy of combined orthokeratology and 0.01% atropine solution for slowing axial elongation in children with myopia: a 2-year randomized trial. Sci Rep. 2020;10:12750.
- Ueda E, Yasuda M, Fujiwara K, et al. Trends in the prevalence of myopia and myopic maculopathy in a Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2019;60:2781-2786.
