
Rotlichttherapie (Myopieprogression)
1. Was ist die Rotlichttherapie (Myopieprogression-Kontrolle)?
Abschnitt betitelt „1. Was ist die Rotlichttherapie (Myopieprogression-Kontrolle)?“Die wiederholte niedrigintensive Rotlichttherapie (Repeated Low-Level Red Light Therapy: RLRL) ist eine nicht-invasive Behandlungsmethode, bei der rotes sichtbares Licht einer bestimmten Wellenlänge (hauptsächlich 650–670 nm) mit geringer Intensität auf das Auge gestrahlt wird, um das Fortschreiten der Myopie bei Kindern zu kontrollieren. Das Standardprotokoll verwendet ein spezielles Handgerät mit Sitzungen von 3 Minuten zweimal täglich an 5 Tagen pro Woche.
Stellung der RLRL-Therapie
Abschnitt betitelt „Stellung der RLRL-Therapie“Die RLRL-Therapie ist eine relativ neue Myopieprogression-Kontrolltherapie, bei der seit den 2020er Jahren rasch Evidenz gesammelt wurde. Sie gilt als „vierte Option“ nach den drei etablierten Haupttherapien (niedrig dosiertes Atropin, Orthokeratologie, multifokale Kontaktlinsen) und wird hauptsächlich in Ostasien, insbesondere in China, erforscht.
Myopie wird hauptsächlich durch eine Verlängerung der Augenachse verursacht, wobei eine Verlängerung um 1 mm etwa einer Myopisierung von 3 D entspricht. Die Hemmung der axialen Verlängerung ist das wichtigste Ziel des Myopiemanagements, und die Veränderung der Augenachse ist der wichtigste Endpunkt bei der Bewertung der Wirksamkeit der RLRL-Therapie 1).
Zu den wichtigsten Komplikationen der Myopie gehören Netzhautablösung (30 % Risikoerhöhung pro −1 D), myope Makuladegeneration (58 % Erhöhung) und Offenwinkelglaukom (20 % Erhöhung) 6). Die RLRL-Therapie wird als präventive Intervention zur Reduzierung dieser Langzeitrisiken angesehen.
Bei asiatischen Kindern ist die Myopie-Prävalenz besonders hoch, und wenn sie unbehandelt fortschreitet, steigt das Risiko schwerwiegender Komplikationen wie Netzhautablösung und myoper Makuladegeneration erheblich. Für die wichtigsten myopiebedingten Komplikationen wird pro 1D-Zunahme ein Risikoanstieg von 30 % für Netzhautablösung, 58 % für myope Makuladegeneration, 20 % für Offenwinkelglaukom und 21 % für hintere subkapsuläre Katarakt geschätzt 6).
Da eine Verlängerung der axialen Augenlänge um 1 mm etwa einer Myopisierung von 3D entspricht, ist die Hemmung der axialen Verlängerung das wichtigste Ziel des Myopie-Managements. Die Metaanalyse von Haarman et al. (2020) 7) zeigt, dass das Komplikationsrisiko mit zunehmendem Myopiegrad exponentiell ansteigt, sodass ein Eingreifen in frühen Stadien für die Verbesserung der Langzeitprognose von großer Bedeutung ist.
Die RLRL-Therapie hat sich seit den 2020er Jahren als eine der Interventionen zur Myopieprogression-Hemmung neben Orthokeratologie und niedrig dosiertem Atropin schnell evidenzbasiert entwickelt. Auch in Japan wird sie in einigen Einrichtungen als Selbstzahlerleistung eingeführt. Der systematische Review von Yam et al. (2025) fasst die Evidenz mehrerer Interventionen zur Myopieprogression-Hemmung, einschließlich der RLRL-Therapie, zusammen 5).
Andererseits haben Bullimore et al. (2021) die Risiken und Vorteile des Myopie-Managements insgesamt detailliert untersucht und weisen darauf hin, dass bei Abweichung der Bestrahlungsparameter auch bei der RLRL-Therapie ein Risiko für retinale Phototoxizität besteht 6). Die Einhaltung geeigneter Geräteverwaltung, Bestrahlungsintensität und Bestrahlungsdauer ist Voraussetzung für eine sichere Anwendung.
Die RLRL-Therapie ist eine Behandlung zur Myopieprogression, bei der zweimal täglich für 3 Minuten rotes sichtbares Licht im Bereich von 650–670 nm mit geringer Intensität (0,3–1 mW/cm²) auf das Auge gestrahlt wird. Es wird angenommen, dass sie über Photobiomodulation die Aderhautdicke erhöht und die Augenachsenverlängerung hemmt 3). Derzeit ist sie in Japan nicht zugelassen und wird als Selbstzahlerleistung unter Aufsicht eines Facharztes durchgeführt.
2. Hauptsymptome und klinische Befunde
Abschnitt betitelt „2. Hauptsymptome und klinische Befunde“Indikatoren für die Behandlungswirkung
Abschnitt betitelt „Indikatoren für die Behandlungswirkung“Die Wirksamkeit der RLRL-Therapie wird anhand der folgenden objektiven Indikatoren bewertet.
- Achsenlänge: Messung mit einem optischen Achsenlängenmessgerät. Verlauf vor und nach der Behandlung sowie alle 6 Monate.
- Aderhautdicke: Messung der subfovealen Aderhautdicke (SFCT) mittels OCT. Nach RLRL-Bestrahlung wird eine Zunahme der Aderhautdicke beobachtet. In der 2-Jahres-Follow-up-Studie von Dong et al. (2023) wurde eine Zunahme der Aderhautdicke bestätigt 2).
- Sphärisches Äquivalent: Objektive Bewertung unter Zykloplegie.
- Korrigierte Sehschärfe: Überprüfung der Stabilität der korrigierten Sehschärfe vor und nach der Behandlung.
Hinweise zur Sicherheitsbewertung
Abschnitt betitelt „Hinweise zur Sicherheitsbewertung“Die RLRL-Therapie gilt als niedrigintensiv, daher werden kurzfristige unerwünschte Ereignisse als selten angesehen. Dennoch sollten die folgenden Punkte regelmäßig überprüft werden.
- Risiko einer Netzhauttoxizität: Übermäßige Bestrahlungsstärke, -dauer oder -häufigkeit kann theoretisch Netzhautschäden verursachen6). Eine OCT-basierte Schichtbeurteilung der Netzhaut und Aderhaut sollte vor der Behandlung als Ausgangswert dokumentiert und regelmäßig verglichen werden.
- Veränderungen von Sehschärfe und Farbsehen: Überprüfen Sie während der Behandlung auf Verschlechterung der Sehschärfe oder Farbsehstörungen.
- Subjektive Symptome: Achten Sie auf Beschwerden wie Blendung, Nachbilder oder Gesichtsfeldauffälligkeiten.
3. Ursachen und Risikofaktoren
Abschnitt betitelt „3. Ursachen und Risikofaktoren“Risikofaktoren für das Fortschreiten der Myopie
Abschnitt betitelt „Risikofaktoren für das Fortschreiten der Myopie“Das Fortschreiten der Myopie, das mit der RLRL-Therapie behandelt wird, wird durch folgende Risikofaktoren beeinflusst.
- Frühes Erkrankungsalter (insbesondere im Alter von 6–12 Jahren)
- Eltern mit Kurzsichtigkeit (insbesondere beide Elternteile)
- Lange Zeit für Naharbeit (mehr als 3 Stunden pro Tag)
- Mangel an Aktivitäten im Freien (weniger als 1 Stunde pro Tag)
- Asiatische Ethnie (höchste Prävalenz bei Ostasiaten)
- Holden et al. (2016) prognostizieren, dass bis 2050 etwa 50% der Weltbevölkerung kurzsichtig sein werden8), was die gesellschaftliche Bedeutung einer frühzeitigen Intervention unterstreicht.
4. Diagnose und Untersuchungsmethoden
Abschnitt betitelt „4. Diagnose und Untersuchungsmethoden“Beurteilung vor Behandlungsbeginn
Abschnitt betitelt „Beurteilung vor Behandlungsbeginn“Vor Beginn der RLRL-Therapie sollten die folgenden Untersuchungen durchgeführt werden, um die Ausgangswerte zu dokumentieren und die Indikation zu bestätigen.
| Untersuchungsparameter | Ziel | Wichtige Prüfpunkte |
|---|---|---|
| Refraktionsbestimmung unter Zykloplegie | Objektive Erfassung des Myopiegrades | Sphärisches Äquivalent, Astigmatismus |
| Messung der Achsenlänge | Basislinienbestimmung und Verlaufsüberwachung | Messung mittels optischer Achsenlängenbestimmung |
| Fundusuntersuchung | Netzhaut- und Aderhautzustand vor Behandlung | Überprüfung auf hochmyope Veränderungen |
| OCT (Makula und Sehnerv) | Festlegung des Referenzwerts für Netzhauttoxizität | Schichtdicke von Netzhaut und Aderhaut |
| Spaltlampenuntersuchung | Ausschluss von Erkrankungen des vorderen Augenabschnitts | Aktive Entzündung / Katarakt |
Bei der Untersuchung unter Zykloplegie ist bei Kleinkindern die Anwendung von Zykloplegika (z. B. Cyclopentolat 1%) unerlässlich. Eine rein subjektive Untersuchung ohne Zykloplegie kann zu einer übermäßigen Myopiekorrektur führen.
Überwachung während der Behandlung
Abschnitt betitelt „Überwachung während der Behandlung“Zur Überprüfung der Wirksamkeit und Sicherheit wird folgender Zeitplan empfohlen.
| Zeitpunkt | Inhalt |
|---|---|
| Nach 1 Monat | Einhaltung der Augentropfen, subjektive Symptome, korrigierte Sehschärfe |
| Alle 3–6 Monate | Messung der Achsenlänge, Refraktion unter Zykloplegie, OCT (Aderhautdicke, Netzhautbeurteilung) |
| Jährlich | Funduskopie in Mydriasis, OCT-Angiographie (optional) |
Eine Refraktionsbestimmung unter Zykloplegie und eine optische Biometrie zur Messung der Achsenlänge sind zur Erfassung der Ausgangswerte obligatorisch. Zudem sollten der Netzhaut- und Aderhautzustand vor der Behandlung mittels Funduskopie und OCT dokumentiert werden, um die Sicherheit während der Therapie zu überwachen. Bei Verdacht auf hohe Myopie ist auch auf periphere Netzhautdegenerationen oder -foramina zu achten.
5. Standardbehandlung
Abschnitt betitelt „5. Standardbehandlung“Informierte Einwilligung und Indikationsbewertung vor der Behandlung
Abschnitt betitelt „Informierte Einwilligung und Indikationsbewertung vor der Behandlung“Nachfolgend sind die grundlegenden Punkte bei der Auswahl von Patienten für die RLRL-Therapie aufgeführt.
Empfohlene Indikationen:
- 6–18 Jahre (die meisten Studien umfassen diese Altersgruppe)
- Äquivalente sphärische Myopie von −0,5 D oder mehr mit nachgewiesener Progression
- Myopie, bestätigt durch Untersuchung unter Zykloplegie
- Umgebung, in der die Eltern eine angemessene Betreuung gewährleisten können
Situationen, die mit Vorsicht beurteilt werden sollten:
- Fälle mit Vorgeschichte oder Familienanamnese von Netzhauterkrankungen
- Lichtempfindlichkeitserkrankungen (z. B. Xeroderma pigmentosum, Photosensitivität der Haut)
- Bei Einnahme von lichtempfindlichen Medikamenten
Situationen, in denen die Anwendung vermieden werden sollte:
- Aktive Netzhauterkrankungen (z. B. Netzhautdegeneration, Neovaskularisation)
- Patienten mit gesicherter Diagnose einer Lichtüberempfindlichkeit
Behandlungsprotokoll
Abschnitt betitelt „Behandlungsprotokoll“Die in den wichtigsten RCTs verwendeten Standardbehandlungsparameter sind unten aufgeführt.
| Parameter | Standardwert | Anmerkungen |
|---|---|---|
| Wellenlänge | 650 nm (rotes sichtbares Licht) | Einige Studien verwenden 670 nm |
| Bestrahlungsstärke | 0,3–1 mW/cm² | Inkohärentes Licht, kein Laser |
| Bestrahlungszeit | 3 Minuten/Sitzung | 2-mal täglich (morgens und abends) |
| Behandlungsfrequenz | 5 Tage/Woche (nur an Schultagen) | — |
| Behandlungsdauer | 12–24 Monate oder länger | Fortlaufende Aufrechterhaltung der Wirkung erforderlich |
Das verwendete Gerät ist ein spezielles Handgerät aus China (z. B. Suneye), das hauptsächlich in Studien eingesetzt wurde. Es ist für die Selbstanwendung durch den Patienten zu Hause konzipiert, jedoch müssen die Ersteinstellung und regelmäßige Kontrollen durch einen Facharzt erfolgen.
Ergebnisse der wichtigsten RCTs
Abschnitt betitelt „Ergebnisse der wichtigsten RCTs“In einer einjährigen RCT von Jiang et al. (2022) zeigte die RLRL-Gruppe eine signifikante Hemmung der axialen Verlängerung um 0,10 mm/Jahr (Kontrollgruppe 0,38 mm/Jahr) 1). Auch in der zweijährigen Nachbeobachtung von Dong et al. (2023) blieb der Effekt der axialen Verlängerungshemmung bestehen, und es wurde eine Zunahme der Aderhautdicke festgestellt 2).
In der multizentrischen RCT von Zeng et al. (2023) betrug der äquivalente sphärische Fortschritt nach einem Jahr −0,20 D in der Behandlungsgruppe (Kontrollgruppe −0,71 D), was einer Hemmung der Myopieprogression um etwa 72 % entspricht 4).
Vergleich der RLRL-Therapie mit anderen Methoden zur Myopieprogressionhemmung:
| Intervention | Refraktionshemmrate | Axiale Hemmrate | Wichtigste Evidenz |
|---|---|---|---|
| RLRL-Therapie | 72 % (Zeng 2023) | 74 % (Jiang 2022) | Mehrere RCTs |
| Niedrig dosiertes Atropin 0,05 % | Bis zu 67 % | — | LAMP-Studie |
| Orthokeratologie | — | 43% | Si 2015 Metaanalyse |
| MiSight (Multifokale CL) | 59% | 52% | Chamberlain 2019 |
| DIMS-Brille | 55–59 % | 37–38 % | Lam 2020 RCT |
Allerdings ist bei einem direkten Vergleich Vorsicht geboten, da sich Studiendesign, Altersgruppe und Behandlungsdauer unterscheiden 5). Niedrig dosierte Atropin-Augentropfen (Rijusea® Mini 0,025 %) sind das einzige in Japan im Dezember 2024 zugelassene Medikament 9), und Brillengläser zur Myopiekontrolle (z. B. DIMS) 10) werden auch in den Leitlinien der Japanischen Gesellschaft für Myopie empfohlen. Die RLRL-Therapie wird zunehmend als Option in Kombination mit diesen zugelassenen Interventionen betrachtet.
Im Vergleich zu Daten aus der 3-jährigen RCT mit MiSight (multifokale Kontaktlinsen) 11), der 2-jährigen RCT mit DIMS-Brillen 12), der Metaanalyse von Orthokeratologie 13) und der RCT mit Orthokeratologie plus Atropin 14) zeigt die RLRL-Therapie eine gute kurzfristige Progressionshemmung, jedoch fehlen noch Daten über 5 Jahre hinaus – dies ist die größte Herausforderung. Die zunehmende Tendenz myoper Makulopathie bei Japanern, wie die Hisayama-Studie 15) zeigt, unterstreicht die medizinische Bedeutung von Myopie-Management-Interventionen einschließlich der RLRL-Therapie weiter.
Kombination mit anderen Therapien
Abschnitt betitelt „Kombination mit anderen Therapien“- RLRL + niedrig dosiertes Atropin: Da die Wirkmechanismen unterschiedlich sind, werden additive oder synergistische Effekte erwartet, jedoch laufen noch groß angelegte RCTs zur Überprüfung 5).
- RLRL + Orthokeratologie: Wird als Kombination für schnell fortschreitende Fälle berichtet.
- Wenn die Monotherapie nicht ausreichend wirksam ist, sollte eine Kombination mit anderen Myopieprogressionstherapien in Betracht gezogen werden.
Informierte Einwilligung
Abschnitt betitelt „Informierte Einwilligung“Stand April 2026 ist die RLRL-Therapie in Japan nicht als Arzneimittel zugelassen und nicht von der Krankenkasse erstattungsfähig; sie wird als Selbstzahlerleistung angeboten. Es ist erforderlich, den Patienten und Erziehungsberechtigten Folgendes ausreichend zu erklären und ihre Einwilligung einzuholen.
- Dass es sich um eine in Japan nicht zugelassene Behandlung handelt
- Dass die derzeitige Evidenz hauptsächlich auf Beobachtungsstudien von 1–2 Jahren basiert und die Langzeitsicherheit nicht etabliert ist
- Dass theoretisch ein Risiko einer Netzhauttoxizität bei Abweichung von den Bestrahlungsparametern besteht6)
- Dass es sich nicht um eine „Behandlung“ der Myopie, sondern um eine „Progressionsverzögerung“ handelt
- Regelmäßige augenärztliche Kontrollen und Sicherheitsüberwachung sind zwingend erforderlich.
Stand April 2026 ist die RLRL-Therapie in Japan weder arzneimittelrechtlich zugelassen noch von der Krankenversicherung abgedeckt. Sie wird in einigen augenärztlichen Kliniken als Selbstzahlerleistung angeboten. Vor einem Besuch ist es wichtig, mit einem Facharzt die Indikation, Sicherheit und Kosten ausreichend zu klären. Niedrig dosierte Atropin-Augentropfen (Rijusea® Mini 0,025 %) wurden im Dezember 2024 als erstes Medikament zur Myopieprogression in Japan zugelassen und sind eine Option im Rahmen der Krankenversicherung.
Stellung von RLRL im Mechanismus der Myopieprogression-Hemmung
Abschnitt betitelt „Stellung von RLRL im Mechanismus der Myopieprogression-Hemmung“Während die wichtigsten optischen Interventionen zur Myopieprogression-Hemmung (Orthokeratologie, DIMS-Brillengläser, multifokale Kontaktlinsen) auf der gemeinsamen Hypothese des peripheren myopischen Defokus basieren, wirkt die RLRL-Therapie über einen völlig anderen Weg: photobiologische Modulation (PBM) → Mitochondrienaktivierung → Verbesserung der Aderhautdurchblutung → Aderhautverdickung → Hemmung der axialen Verlängerung. Dieser unterschiedliche Wirkmechanismus führt zur Erwartung synergistischer Effekte in Kombination mit anderen Therapien 3).
Ein weiteres Alleinstellungsmerkmal der RLRL-Therapie ist die Beobachtung einer akuten physiologischen Reaktion, bei der die Aderhautdicke unmittelbar nach der Behandlung zunimmt 2). Dies ist ein Merkmal, das bei anderen Therapien zur Myopieprogression-Hemmung nicht zu finden ist, und die Messung der Aderhautdicke gilt als nützlicher Indikator für die unmittelbare Wirkung der Behandlung.
6. Pathophysiologie und detaillierter Pathomechanismus
Abschnitt betitelt „6. Pathophysiologie und detaillierter Pathomechanismus“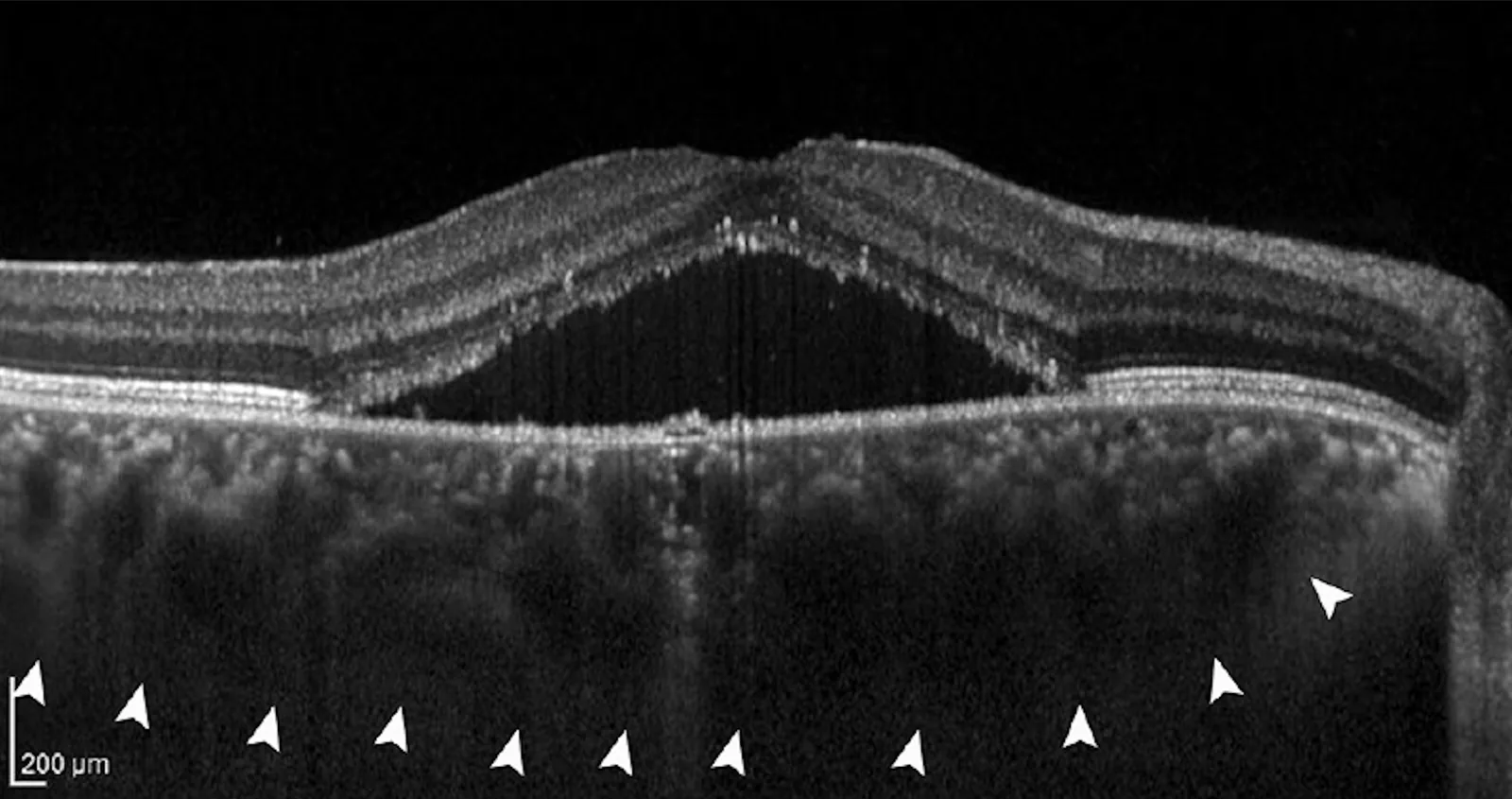
Photobiomodulation (PBM)
Abschnitt betitelt „Photobiomodulation (PBM)“Als Hauptmechanismus der RLRL-Therapie wird die Photobiomodulation (PBM) vorgeschlagen 3). Rotes Licht im Bereich von 650–670 nm wird spezifisch von der Cytochrom-c-Oxidase (Komplex IV) in den Mitochondrien der Zellen absorbiert und induziert die folgenden biologischen Reaktionen.
- Förderung der ATP-Produktion
- Aktivierung von Zellsignalen durch moderate Produktion reaktiver Sauerstoffspezies (ROS)
- Gefäßerweiterung und erhöhte Durchblutung durch Freisetzung von Stickstoffmonoxid (NO)
- Verbesserung der Durchblutung und Verdickung der Aderhaut
Verdickung der Aderhaut und Hemmung der Augenachsenverlängerung
Abschnitt betitelt „Verdickung der Aderhaut und Hemmung der Augenachsenverlängerung“Nach RLRL-Bestrahlung wurde durchgängig eine Zunahme der Aderhautdicke beobachtet2)3). Es wird angenommen, dass die Zunahme der Aderhautdicke die Steifigkeit der Augenwand beeinflusst und zur Hemmung der Augenachsenverlängerung beiträgt. Auch bei Orthokeratologie und niedrig dosiertem Atropin wurde eine Zunahme der Aderhautdicke berichtet, was darauf hindeutet, dass die Aderhaut ein gemeinsamer Signalweg bei der Hemmung des Myopiefortschritts sein könnte.
Grundlegender Mechanismus des Myopiefortschritts
Abschnitt betitelt „Grundlegender Mechanismus des Myopiefortschritts“Der Myopiefortschritt ist ein biologischer Prozess, bei dem das Augenwachstum durch Signalübertragung von der Netzhaut zur Lederhaut reguliert wird. Dabei sind folgende Schritte beteiligt.
- Periphere hyperope Defokussierung dient als treibendes Signal für die Verlängerung der Augenachse
- Dopaminvermittelte Wachstumshemmsignale bremsen die Verlängerung der Augenachse
- Die Umgestaltung der extrazellulären Matrix der Sklera bestimmt die Achsenlänge des Auges
- Verdickung und Verdünnung der Aderhaut dienen als Biomarker für Veränderungen der Augenachse
Die RLRL-Therapie greift in diese Signalwege ein und bremst das Augenwachstum auf der Ebene der Aderhaut und Sklera, jedoch sind die genauen Mechanismen noch weitgehend ungeklärt 3). Die von Haarman et al. (2020) in einer Metaanalyse aufgezeigten quantitativen Risiken von Myopie-Komplikationen werden häufig als medizinische Grundlage für therapeutische Interventionen zitiert 7).
7. Aktuelle Forschung und zukünftige Perspektiven
Abschnitt betitelt „7. Aktuelle Forschung und zukünftige Perspektiven“Etablierung von Langzeitdaten zu Wirksamkeit und Sicherheit
Abschnitt betitelt „Etablierung von Langzeitdaten zu Wirksamkeit und Sicherheit“Die derzeitigen wichtigsten RCTs haben einen Beobachtungszeitraum von 1–2 Jahren, und Langzeitdaten über 5 Jahre sind rar 1)2). Auch die Dauerhaftigkeit der Wirkung nach Behandlungsende (Carry-over-Effekt) ist noch nicht etabliert; es laufen Studien, die die Veränderung der Myopieprogression nach Therapieende verfolgen.
In der 2-Jahres-Follow-up-Studie von Dong et al. (2023) zeigte die RLRL-Behandlungsgruppe im Vergleich zur Kontrollgruppe eine anhaltende Hemmung der axialen Verlängerung und eine Zunahme der Aderhautdicke, wobei die Wirkung bei einjähriger kontinuierlicher Anwendung erhalten blieb 2). Allerdings unterscheiden sich Studiendesign, Bestrahlungsparameter und Altersgruppen zwischen den Studien, sodass ein direkter Vergleich mit Vorsicht zu interpretieren ist.
Quantifizierung des Netzhauttoxizitätsrisikos
Abschnitt betitelt „Quantifizierung des Netzhauttoxizitätsrisikos“Theoretisch besteht die Möglichkeit, dass übermäßige Bestrahlungsintensität, -dauer oder -häufigkeit Netzhautschäden verursachen. In der Risiko-Nutzen-Bewertung des Myopiemanagements von Bullimore et al. (2021) wird die allgemeine Sicherheitsbalance optischer und pharmakologischer Interventionen einschließlich der RLRL-Therapie diskutiert, wobei die Bedeutung einer angemessenen Parameterkontrolle betont wird 6).
Es werden Studien zur Festlegung von Sicherheitsgrenzwerten für die Bestrahlung und zur Risikobewertung durchgeführt. In der klinischen Praxis müssen die Bestrahlungsintensität (0,3–1 mW/cm²), die Bestrahlungsdauer (3 Minuten/Sitzung) und die Bestrahlungshäufigkeit (2-mal täglich, 5 Tage/Woche) strikt eingehalten werden, und eine regelmäßige Kalibrierung der Geräte ist erforderlich.
Aus phototoxischer Sicht ist die kumulative Lichtexposition der Photorezeptoren und des RPE entscheidend, und eine über die empfohlenen Mengen hinausgehende Bestrahlung (insbesondere abweichende Anwendung mit hoher Intensität und langer Dauer) erfordert Vorsicht. Wie die Metaanalyse zu Myopie-Komplikationen von Haarman et al. (2020) zeigt 7), ist es wichtig, das Risiko-Nutzen-Verhältnis der RLRL-Therapie individuell zu bewerten, unter der Annahme, dass ein angemessenes Myopie-Management das Risiko schwerwiegender Komplikationen verringern kann.
Direkter Vergleich mit niedrig dosiertem Atropin und Orthokeratologie
Abschnitt betitelt „Direkter Vergleich mit niedrig dosiertem Atropin und Orthokeratologie“Es werden derzeit randomisierte kontrollierte Studien durchgeführt, die die RLRL-Therapie direkt mit Orthokeratologie und niedrig dosiertem Atropin vergleichen. Die Etablierung eines personalisierten Myopie-Management-Protokolls unter Berücksichtigung der Vor- und Nachteile jeder Therapie wird erwartet 5).
Vergleich der Eigenschaften der drei Hauptinterventionen (RLRL, OK, niedrig dosiertes Atropin):
| Intervention | Axiale Längenhemmrate | Invasivität | Bequemlichkeit | Regulatorischer Status in Japan |
|---|---|---|---|---|
| RLRL-Therapie | ca. 60–72% | nicht-invasiv | zu Hause durchführbar | nicht zugelassen (Selbstzahler) |
| Orthokeratologie | 30–50% | Kontakt mit der Hornhaut | nächtliches Tragen | nicht zugelassen (Selbstzahler) |
| Niedrig dosiertes Atropin 0,025% | ca. 62% | Augentropfen | Einnahme vor dem Schlafengehen | Zugelassen |
KI-gestützte Vorhersage der Myopieprogression
Abschnitt betitelt „KI-gestützte Vorhersage der Myopieprogression“Es werden Modelle entwickelt, die Augenlängendaten, Risikofaktoren und Behandlungsreaktionen mittels KI integriert analysieren, um für jeden Patienten die optimale Behandlungsstrategie vorzuschlagen. Dies könnte auch zur Vorhersage des Ansprechens auf die RLRL-Therapie eingesetzt werden.
Entwicklungen zur nationalen Zulassung
Abschnitt betitelt „Entwicklungen zur nationalen Zulassung“Angesichts der zunehmenden Evidenz aus China und Südostasien könnten auch in Japan Gespräche mit den Aufsichtsbehörden aufgenommen werden. Die Durchführung multizentrischer RCTs im Inland und die Entwicklung hin zur Arzneimittelzulassung werden mit Spannung erwartet. Vor dem Hintergrund der weltweit steigenden Kurzsichtigkeitsrate (Holden 2016: 4,9 Milliarden Menschen bis 2050 8)) etabliert sich die RLRL-Therapie zunehmend als eine Option für das Myopiemanagement.
8. Literaturverzeichnis
Abschnitt betitelt „8. Literaturverzeichnis“- Jiang Y, Zhu Z, Tan X, et al. Effect of repeated low-level red-light therapy for myopia control in children: a multicenter randomized controlled trial. Ophthalmology. 2022;129:509-519.
- Dong J, Zhu Z, Xu H, et al. Myopia control effect of repeated low-level red-light therapy in Chinese children: a randomized, double-blind, controlled clinical trial. Ophthalmology. 2023;130:198-204.
- Wang W, Jiang Y, Zhu Z, et al. Chorioidal thickening as a potential therapeutic target in myopia management: a review of repeated low-level red light therapy. Surv Ophthalmol. 2023;68:1-12.
- Zeng J, Liu Y, Wang Z, et al. Efficacy of repeated low-level red-light stimulation on slowing myopia progression and ocular growth in children with myopia: a randomized controlled trial. Transl Vis Sci Technol. 2023;12:22.
- Yam JC, Zhang XJ, Zhang Y, et al. Interventions to reduce incidence and progression of myopia in children and adults. Prog Retin Eye Res. 2025.
- Bullimore MA, Ritchey ER, Shah S, et al. The risks and benefits of myopia control. Ophthalmology. 2021;128:1561-1579.
- Haarman AEG, Enthoven CA, Tideman JWL, et al. The complications of myopia: a review and meta-analysis. Invest Ophthalmol Vis Sci. 2020;61:49.
- Holden BA, Fricke TR, Wilson DA, et al. Global prevalence of myopia and high myopia and temporal trends from 2000 through 2050. Ophthalmology. 2016;123:1036-1042.
- 低濃度アトロピン点眼液を用いた近視進行抑制治療の治療指針作成委員会. 低濃度アトロピン点眼液を用いた近視進行抑制治療の手引き. 日眼会誌. 2025;129(10):851-854.
- 近視管理用眼鏡ガイドライン作成委員会. 近視管理用眼鏡(多分割レンズ)ガイドライン(第1版). 日眼会誌. 2025;129(10):855-860.
- Chamberlain P, Peixoto-de-Matos SC, Logan NS, et al. A 3-year randomized clinical trial of MiSight lenses for myopia control. Optom Vis Sci. 2019;96:556-567.
- Lam CSY, Tang WC, Tse DY, et al. Defocus incorporated multiple segments (DIMS) spectacle lenses slow myopia progression: a 2-year randomised clinical trial. Br J Ophthalmol. 2020;104:363-368.
- Si JK, Tang K, Bi HS, et al. Orthokeratology for myopia control: a meta-analysis. Optom Vis Sci. 2015;92:252-257.
- Kinoshita N, Konno Y, Hamada N, et al. Efficacy of combined orthokeratology and 0.01% atropine solution for slowing axial elongation in children with myopia: a 2-year randomized trial. Sci Rep. 2020;10:12750.
- Ueda E, Yasuda M, Fujiwara K, et al. Trends in the prevalence of myopia and myopic maculopathy in a Japanese population: the Hisayama Study. Invest Ophthalmol Vis Sci. 2019;60:2781-2786.
