CNGA3
الكروموسوم: 2q11.2
الوظيفة: الوحدة الفرعية ألفا لقناة CNG
التكرار: حوالي 25-50% من الحالات1)2)
نمط الطفرة: الطفرات المغلوطة هي السائدة. المجال الغشائي S4 هو نقطة ساخنة
التوزيع الجغرافي: في الشرق الأوسط والصين، CNGA3 يمثل أكثر من 80%

عمى الألوان الكامل (أكروماتوبسيا؛ ACHM) هو مرض وراثي نادر يصيب شبكية العين في كلتا العينين، حيث تفقد جميع أنواع الخلايا المخروطية الثلاثة وظيفتها. يُعرف أيضًا باسم “عمى الألوان القضيبي” أو “عمى الألوان التام” 1).
يُقدر معدل الانتشار عالميًا بحوالي 1 من كل 30,000 شخص 1). يتبع نمط وراثة جسمي متنحي، ولا يصاحبه تشوهات جهازية، ومتوسط العمر المتوقع طبيعي.
هناك نوعان من ACHM: كامل وغير كامل. في النوع الكامل، تغيب وظيفة المخاريط تمامًا، بينما في النوع غير الكامل، يحتفظ نوع واحد على الأقل من المخاريط ببعض الوظائف، وتكون حدة البصر حوالي 20/40 إلى 20/120، ويكون رهاب الضوء والرأرأة خفيفين 2).
الجينات المسببة هي ستة (CNGA3، CNGB3، GNAT2، PDE6C، PDE6H، ATF6)، ويمكن تحديد الجين المسبب في أكثر من 90% من الحالات 1)2). يشكل جينا CNGA3 وCNGB3 معًا 80-90% من الحالات.
تجدر الإشارة إلى أن اضطرابات رؤية الألوان العامة (اضطرابات رؤية الألوان الخلقية) ناتجة عن خلل في واحد أو اثنين من الصبغات البصرية للمخاريط وتؤثر فقط على رؤية الألوان. في ACHM، لا تعمل جميع المخاريط، مما يختلف جوهريًا بوجود انخفاض الرؤية، الرأرأة، ورهاب الضوء.
هناك حالة معروفة باسم تأثير المؤسس في جزيرة بينجيلاب (ميكرونيزيا). بعد إعصار في القرن الثامن عشر، انخفض عدد السكان بشكل كبير، وانتشر طفرة CNGB3 (p.S435F) بين الناجين، ليصل معدل الانتشار إلى حوالي 10% ومعدل حامل المرض إلى حوالي 30%1)2).
اضطرابات رؤية الألوان الخلقية العامة ناتجة عن خلل في واحد أو اثنين من الصبغات البصرية للمخاريط وتؤثر فقط على رؤية الألوان، مع بقاء الرؤية ضمن المعدل الطبيعي. في عمى الألوان الكلي، تفتقر وظيفة جميع المخاريط الثلاثة، مما يؤدي إلى فقدان رؤية الألوان بالإضافة إلى انخفاض الرؤية (حوالي 0.1 أو أقل)، الرأرأة، رهاب الضوء، وعمى النهار، وهذا يختلف جوهريًا.
تبدأ أعراض ACHM في الظهور خلال الأسابيع القليلة الأولى بعد الولادة.
استجابة حدقة متناقضة: انقباض أولي للحدقة في الظلام. علامة مميزة مهمة في تشخيص الأطفال.
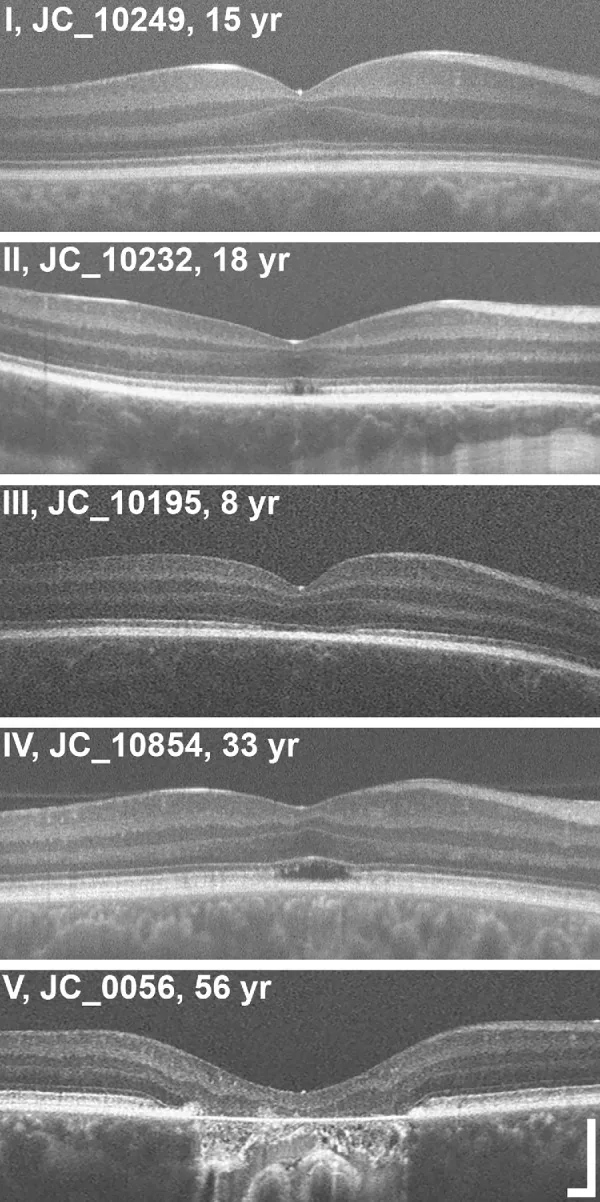
نتائج قاع العين: تبدو طبيعية تقريبًا في البداية. يُظهر تصوير الأوعية بالفلوريسين نتائج طبيعية تقريبًا. مع مرور الوقت، قد تحدث تغيرات رقشية وضمور في الظهارة الصباغية للشبكية. غالبًا ما يُلاحظ غياب المنعكس البقعي أو تنكس بقعي. في التصوير المقطعي التوافقي البصري، تكون الوصلة بين القطعة الداخلية والخارجية للمستقبلات الضوئية والمنطقة البينية غير منتظمة وغير واضحة.
نتائج تخطيط كهربية الشبكية: في تخطيط كهربية الشبكية تحت الإضاءة، تنخفض استجابة المخاريط بشكل كبير أو تختفي، بينما تكون استجابة العصي طبيعية أو شبه طبيعية في تخطيط كهربية الشبكية في الظلام1)2). في النمط GNAT2، تكون المخاريط الحساسة للطول الموجي القصير محفوظة بشكل أفضل مقارنة بالنمطين CNGA3/CNGB3.
نقص تنسج النقرة: يُلاحظ في 60-70% من حالات طفرات CNGA3/CNGB32).
التألق الذاتي لقاع العين: توجد أربعة أنماط: طبيعي، زيادة الإشارة المركزية، نقص الإشارة المركزية، حلقة مفرطة التألق مع نقص التألق المركزي2).
تقسيم التصوير المقطعي التوافقي البصري: تقييم التغيرات الهيكلية في الطبقات الخارجية للنقرة على خمس مراحل3).
| المرحلة | نتائج التصوير المقطعي التوافقي البصري |
|---|---|
| المرحلة 1 | الحفاظ على الطبقات الخارجية للشبكية (فرط انعكاس الغشاء المحدد الخارجي، تسطيح المنطقة الإهليلجية) |
| المرحلة 2 | تدمير المنطقة الإهليلجية |
| المرحلة 3 | ظهور فراغ بصري (optically empty space) |
| المرحلة 4 | فراغ بصري + تدمير جزئي للطبقة الظهارية الصباغية للشبكية (RPE) |
| المرحلة 5 | اختفاء الطبقة النووية الخارجية و/أو تدمير كامل للطبقة الظهارية الصباغية للشبكية (RPE) |
في دراسة متابعة لمدة 10 سنوات، على الرغم من استقرار أفضل حدة بصر مصححة (20/400 إلى 20/200)، تم تأكيد تقدم بنيوي في التصوير المقطعي التوافقي البصري (OCT) (توسع الفراغ البصري: العين اليمنى 246×59 ميكرومتر، العين اليسرى 326×53 ميكرومتر)3).
قد تظهر البؤر شديدة الانعكاس (hyperreflective foci) قبل أكثر من 3 سنوات من تغيرات المنطقة الإهليلجية (EZ)، مما يشير إلى إمكانية استخدامها كعلامات مبكرة لتقدم المرض3).
مقياس البصريات التكيفي الماسح بالليزر (AOSLO): يُظهر فسيفساء المخاريط مساحات مظلمة (dark space)، وزيادة في التباعد بين المخاريط، وانخفاض كثافة المخاريط. لا يوجد فرق كبير بين النوعين CNGA3 وCNGB3، بينما النوع GNAT2 يحافظ على المخاريط نسبيًا2).
اختبار رؤية الألوان: في لوحات إيشيهارا لرؤية الألوان، تكون جميع اللوحات غير قابلة للقراءة تقريبًا باستثناء لوحة العرض التوضيحي. في اختبار Panel D-15، يُظهر نمط أخطاء على المحور scotopic (بين deutan وtritan). في جهاز anomaloscope، يُظهر منحدرًا حادًا ولا يشمل نطاق التكافؤ اللوني الطبيعي.
غالبًا ما تظل أفضل حدة بصر مصححة مستقرة على المدى الطويل. من ناحية أخرى، قد يتطور التغير البنيوي (تدمير المنطقة الإهليلجية، توسع الفراغ البصري) بمرور الوقت في التقييم البنيوي بالتصوير المقطعي التوافقي البصري (OCT)3). من الخصائص حدوث انفصال بين الوظيفة والبنية، ومن المهم إجراء مراقبة منتظمة من خلال الفحوصات الدورية.
الوراثة جسمية متنحية. إذا كان كلا الوالدين حاملين (ناقلين)، فإن خطر إصابة الطفل بالمرض هو 25%1). غالبًا ما يحدث المرض لدى أطفال من أبوين أصحاء ظاهريًا، وفي كثير من الحالات لا يوجد تاريخ عائلي.
كما تم الإبلاغ عن نمط وراثة غير مندلية بسبب أحادية الوالدين الأبوية (UPD). في حالة تم فيها تكوين متماثل الزيجوت لـ CNGA3 c.778G>C (p.D260H) عن طريق UPD، لم يتم اكتشاف طفرة في الأم 6). هذه الأمثلة لها أهمية كبيرة في تقييم خطر التكرار في الاستشارة الوراثية.
CNGA3
الكروموسوم: 2q11.2
الوظيفة: الوحدة الفرعية ألفا لقناة CNG
التكرار: حوالي 25-50% من الحالات1)2)
نمط الطفرة: الطفرات المغلوطة هي السائدة. المجال الغشائي S4 هو نقطة ساخنة
التوزيع الجغرافي: في الشرق الأوسط والصين، CNGA3 يمثل أكثر من 80%
CNGB3
الكروموسوم: 8q21.3
الوظيفة: الوحدة الفرعية بيتا لقناة CNG
التكرار: حوالي 50% من الحالات1)2)
نمط الطفرة: الطفرات غير المغلوطة، الإزاحة الإطارية، والوصل هي السائدة. c.1148delC هي الطفرة الأكثر شيوعًا
التوزيع الجغرافي: في أوروبا وأمريكا، CNGB3 يمثل أكثر من 50%
جينات أخرى
GNAT2 (1p13.3): ترانسدوسين ألفا للمخاريط. حوالي 2%. خفيف نسبيًا مع الحفاظ على طبقة المستقبلات الضوئية 2)
PDE6C (10q23.33): الوحدة الفرعية ألفا لـ PDE المخروطية. نوع شديد مبكر الظهور 5)
PDE6H (12p12.3): الوحدة الفرعية جاما لـ PDE المخروطية. نادر جدًا 1)
ATF6 (1q23.3): عامل نسخ استجابة إجهاد الشبكة الإندوبلازمية. حوالي 2%. آلية لا تشارك مباشرة في نقل الضوء 1)2)
الأليل منخفض النفاذية: يحتفظ CNGB3 c.1208G>A (p.R403Q) بوظيفة جزئية، مما يؤدي إلى نمط ظاهري خفيف 2).
خصائص طفرة PDE6C: في 4 حالات تحمل طفرات جديدة (c.1670G>A، c.2192G>A)، لوحظت الثالوث (رأرأة، رهاب الضوء، ضعف رؤية الألوان) في جميع الحالات. أظهر تخطيط كهربية الشبكية اختفاء الرؤية النهارية ووميض 30 هرتز مع رؤية ليلية طبيعية، وأظهرت الحالات متغايرة الزيجوت المركبة نمطًا ظاهريًا أكثر شدة 5).
وراثة ثنائية الجينات: توجد حالات نادرة تحمل طفرات في كل من CNGA3 وCNGB3 1).
نظرًا لأن عمى الألوان الكامل هو مرض جسمي متنحي، فإن الوالدين قد يكونان حاملين لنسخة واحدة من الجين المتحور (حاملين) دون ظهور أعراض، وتكون رؤية الألوان طبيعية. في حالة اجتماع حاملين، يكون احتمال إنجاب طفل يحمل نسختين من الطفرة والإصابة بالمرض 25% 1).
عند ملاحظة رأرأة ورهاب الضوء وضعف البصر خلال الأسابيع الأولى بعد الولادة، يلزم إجراء فحوصات شاملة مع الأخذ في الاعتبار احتمالية الإصابة بعمى الألوان الكامل. الفحص الجيني ضروري للتشخيص النهائي.
تخطيط كهربية الشبكية
الأهمية التشخيصية: المعيار الذهبي
نتائج النوع الكامل: اختفاء أو انخفاض شديد في استجابة المخاريط في تخطيط كهربية الشبكية تحت الإضاءة الساطعة. استجابة العصي طبيعية إلى شبه طبيعية في تخطيط كهربية الشبكية تحت الإضاءة الخافتة1)2)
نتائج النوع غير الكامل: يتم الكشف عن استجابة مخروطية ضعيفة تتوافق مع وظيفة المخاريط المتبقية
خصائص نوع GNAT2: الحفاظ النسبي على المخاريط S مقارنة بنوع CNGA3/CNGB3
التصوير المقطعي البصري (OCT)
الأهمية التشخيصية: المعيار القياسي لتقييم البنية
محتوى التقييم: تصنيف من 5 مراحل للطبقة الخارجية للنقرة، الكشف عن نقص تنسج النقرة2)3)
المتابعة: حتى مع الاستقرار الوظيفي، قد يحدث تقدم بنيوي، لذا فإن المراقبة الدورية مهمة
الفحوصات المساعدة: تقييم متعدد الوسائط يجمع بين FAF و AOSLO
الاختبار الجيني
الأهمية التشخيصية: ضروري للتشخيص النهائي
الطريقة: لوحة مستهدفة لـ 6 جينات (CNGA3/CNGB3/GNAT2/PDE6C/PDE6H/ATF6)2)
معدل الحل: يمكن تحديد الجين المسبب في أكثر من 90% من الحالات1)
المشاركة في التجارب السريرية: التشخيص الجزيئي إلزامي للمشاركة في التجارب السريرية للعلاج الجيني
من المهم التفريق بين ACHM والأمراض التي تظهر بصورة سريرية مشابهة2).
حالياً، لا يوجد علاج جذري معتمد لـ ACHM1)2). يركز العلاج على تخفيف الأعراض.
على الرغم من شيوع طول النظر، إلا أن هناك مجموعة واسعة من الأخطاء الانكسارية، لذا فإن التصحيح بالنظارات أو العدسات اللاصقة مهم لتحقيق أقصى حدة بصرية. في حالة وجود الحول، يُنظر في العلاج بالإغلاق أو الأتروبين.
العدسات الواقية من الضوء لتخفيف رهاب الضوء تحسن جودة الحياة اليومية بشكل كبير. وفقاً لبيانات استبيان للمرضى، فضل 96% المرشحات الرمادية على الحمراء، وفضل 74% المرشحات الرمادية في الهواء الطلق2). من المهم اختيار ما يناسب تفضيلات كل مريض وبيئة نشاطه.
يتم استخدام الوسائل والتقنيات التالية 3).
من الضروري تقديم شرح ودعم من قبل متخصصين حول خصائص الوراثة الجسدية المتنحية، وخطر التكرار، وأهمية التشخيص الجيني. يُوصى أيضًا بإجراء التشخيص الجيني استعدادًا للمشاركة في التجارب السريرية المستقبلية للعلاج الجيني.
في استطلاع للمرضى، فضل 96% المرشحات الرمادية على المرشحات الحمراء، وفضل 74% المرشحات الرمادية في الهواء الطلق 2). ومع ذلك، نظرًا للاختلافات الفردية، يُنصح بتجربة مرشحات مختلفة واختيار الأنسب لبيئة نشاطك بالتشاور مع طبيب العيون أو أخصائي رعاية ضعف البصر.
سلسلة نقل الإشارة الضوئية في الخلايا المخروطية الطبيعية هي كما يلي1).
طفرة CNGA3: تؤدي الطفرات المغلوطة إلى إعاقة طي البروتين ونقله داخل الخلايا ودمجه في الغشاء1)7). يشكل المجال عبر الغشائي S4 نقطة ساخنة للطفرات. تم الإبلاغ عن أكثر من 150 طفرة مغلوطة، و103 طفرات لم يتم تحديد إمراضيتها بعد، لكن التحليل الهيكلي الوظيفي ثلاثي الأبعاد أشار إلى أن 86.4% منها لها عواقب وظيفية مشابهة للطفرات الممرضة المعروفة7).
طفرة CNGB3: تؤدي الطفرات غير المنطقية والإزاحة الإطارية إلى إنتاج بروتين قناة مبتور أو فاقد للوظيفة1). في حالة نقص CNGB3، تبقى القنوات المتجانسة CNGA3، مما قد يحافظ على وظيفة مخروطية طفيفة.
طفرة ATF6: هو عامل نسخ يشارك في استجابة البروتين غير المطوي (UPR) في الشبكة الإندوبلازمية، ولا يشارك مباشرة في سلسلة نقل الإشارة الضوئية1)2). تختلف آلية المرض عن الجينات الأخرى، ولا يزال البحث جارياً لفهمها.
قناة CNG هي بنية رباعية (CNGA3 × 3 و CNGB3 × 1، وفي بعض التقارير 2:2)، وكل وحدة فرعية تحتوي على 6 مجالات عبر غشائية، ومجال ربط النوكليوتيدات الحلقية، ومنطقة رابط C، ومجال تشكيل المسام1).
يبدو أن التطور الرئيسي للمخاريط بعد الولادة وشكلها طبيعيان تقريباً، ويُعتقد أن التنكس يبدأ من مرحلة البلوغ المبكر. يُشارك تراكم cGMP في عملية التنكس، وقد أظهرت النماذج الحيوانية تطوراً أسرع في المناطق الغنية بالمخاريط S1).
تقليدياً، كان يُعتقد أن ACHM مرض غير تقدمي. ومع ذلك، أظهرت الملاحظات طويلة المدى باستخدام التصوير المقطعي التوافقي البصري (OCT) أنه على الرغم من استقرار أفضل حدة بصرية مصححة، إلا أن التغيرات الهيكلية (تدمير EZ، توسع الفجوات البصرية) تتقدم3). هذا الانفصال بين الوظيفة والبنية له أهمية كبيرة في تقييم نافذة العلاج للعلاج الجيني.
في منطقة خالية من العصي (منطقة كثيفة المخاريط) في النقرة، يكون فقدان المخاريط ملحوظًا، بينما في المنطقة المجاورة للنقرة، تعوض العصي الوظيفة من خلال المساهمة في النطاق EZ 3).
فيما يلي التجارب السريرية الرئيسية للعلاج الجيني الجارية أو المكتملة حتى عام 2024 1)2).
| رقم NCT | الجين المستهدف | الناقل | الحالة |
|---|---|---|---|
| NCT03001310 | CNGB3 | AAV8-hCARp.hCNGB3 | مكتمل |
| NCT02610582 | CNGA3 | AAV8-hG1.7-hCNGA3 | مكتمل |
| NCT03758404 | CNGA3 | rAAV8.hCNGA3 | قيد التجنيد |
| NCT02599922 | CNGB3 | AAV2tYF-PR1.7-hCNGB3 (AGTC-401) | جاري |
| NCT02935517 | CNGA3 | AAV2tYF-PR1.7-hCNGA3 (AGTC-402) | جاري |
في تجربة NCT03001310 (AAV8-hCARp.hCNGB3) شملت 11 بالغًا و12 طفلًا (إجمالي 23 شخصًا)، كانت السلامة ضمن الحدود المقبولة. لوحظ تحسن في رؤية الألوان لدى 6/23، وتحسن في رهاب الضوء لدى 11/20، وتحسن في جودة الحياة لدى 21/23. كما لوحظ اتجاه لزيادة الالتهاب داخل العين عند الجرعات العالية 2).
في تجربة AAV8.CNGA3 (RD-CURE)، تم إعطاء 9 أشخاص ثلاث جرعات (1×10¹⁰ إلى 1×10¹¹ vg/عين). أظهرت بيانات السنة الأولى والثالثة اتجاهًا لتحسن حدة البصر وحساسية التباين، لكنها لم تصل إلى دلالة إحصائية. كانت السلامة جيدة 1)2).
أجرى McKyton وآخرون (2021) رسم خرائط قشرية بالرنين المغناطيسي الوظيفي بعد حقن تحت الشبكية لـ AAV2tYF-PR1.7-hCNGA3 (NCT02935517) في شخصين بالغين مصابين بـ CNGA3-ACHM 4). أظهرت العين المعالجة تحملًا للضوء أكبر بخمس مرات مقارنة بالعين غير المعالجة (تحسن كبير في رهاب الضوء)، واكتسبت القدرة على اكتشاف اللون الأحمر، ولوحظ انخفاض في حجم مجال الاستقبال السكاني (pRF) مما يشير إلى تحسن الدقة المكانية. من ناحية أخرى، لم يُلاحظ تنشيط في المناطق القشرية الخاصة بالرؤية اللونية (مثل V4)، وبقي مخطط كهربية الشبكية لكامل المجال غير قادر على كشف استجابة المخاريط. أبلغ المرضى عن تحسن في الحياة اليومية مثل “زيادة الشعور بالأمان عند عبور الشارع”، و”عدم الحاجة إلى عدسة مكبرة”، و”عدم الحاجة إلى نظارات شمسية في الخارج”.
تم تأكيد استعادة الوظيفة بعد الاستبدال الجيني في عدة نماذج حيوانية 1)2).
أظهرت التجارب على الحيوانات أن العلاج في سن مبكرة أكثر فعالية فيما يتعلق بنافذة الوقت الفعالة للعلاج. كانت استجابة الفئران المسنة ضعيفة، لكن المعالجة المسبقة بـ CNTF (عامل التغذية العصبية الهدبية) مكنت من استعادة الوظيفة في الكلاب المسنة 1)2).
تجربة سريرية (NCT04041232) لفينيل بوتيرات الجلسرين (PBA) الذي يستهدف استجابة الإجهاد الشبكي الإندوبلازمي جارية حاليًا 2). يُعتبر هذا النهج بديلاً للاستبدال الجيني عن طريق تخفيف سوء الطي في الشبكة الإندوبلازمية.
التحديات الرئيسية للعلاج الجيني هي كما يلي 1)2)4).
حاليًا، نحن في مرحلة تجارب السلامة والفعالية من المرحلة I/II. تم الإبلاغ عن تقليل رهاب الضوء وتحسين بعض الحساسية للضوء، لكن لم يتم تحقيق استعادة كاملة لرؤية الألوان2)4). أظهرت التجارب على الحيوانات أن العلاج في سن مبكرة قد يكون فعالًا، لكن البيانات طويلة المدى لدى البشر لا تزال محدودة. من المهم متابعة تقدم البحث وتحديث المعلومات بانتظام مع الطبيب المعالج.