年龄相关性黄斑变性(AMD)

吸烟与眼病(年龄相关性黄斑变性和白内障的风险)
一目了然的要点
Section titled “一目了然的要点”1. 吸烟与眼病的关系
Section titled “1. 吸烟与眼病的关系”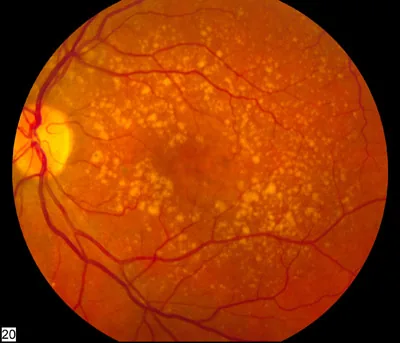
吸烟(烟草)已被确定为多种眼病的危险因素。特别是与年龄相关性黄斑变性(AMD)、白内障、干眼症、糖尿病视网膜病变、甲状腺眼病和Leber遗传性视神经病变的关联已得到科学证明。
烟草烟雾中含有超过4000种化学物质,其中的氰化物、镉、尼古丁和自由基会对眼组织造成多种损害。当前吸烟者患AMD的比值比为2.0~4.0(系统评价和荟萃分析)1),使其成为AMD中最强的可改变风险因素。对于核性白内障,吸烟20包年以上可使比值比升至约2.02)。
累积吸烟量(包年 = 每日吸烟支数 ÷ 20 × 吸烟年数)与眼病风险之间存在明确的剂量反应关系1)。戒烟后风险逐渐降低,但可能需要20年以上才能恢复到与非吸烟者相同的水平3),因此早期戒烟能带来最大益处。被动吸烟(二手烟暴露)与儿童和青少年过敏性疾病风险增加相关4)。
2. 与吸烟相关的眼病
Section titled “2. 与吸烟相关的眼病”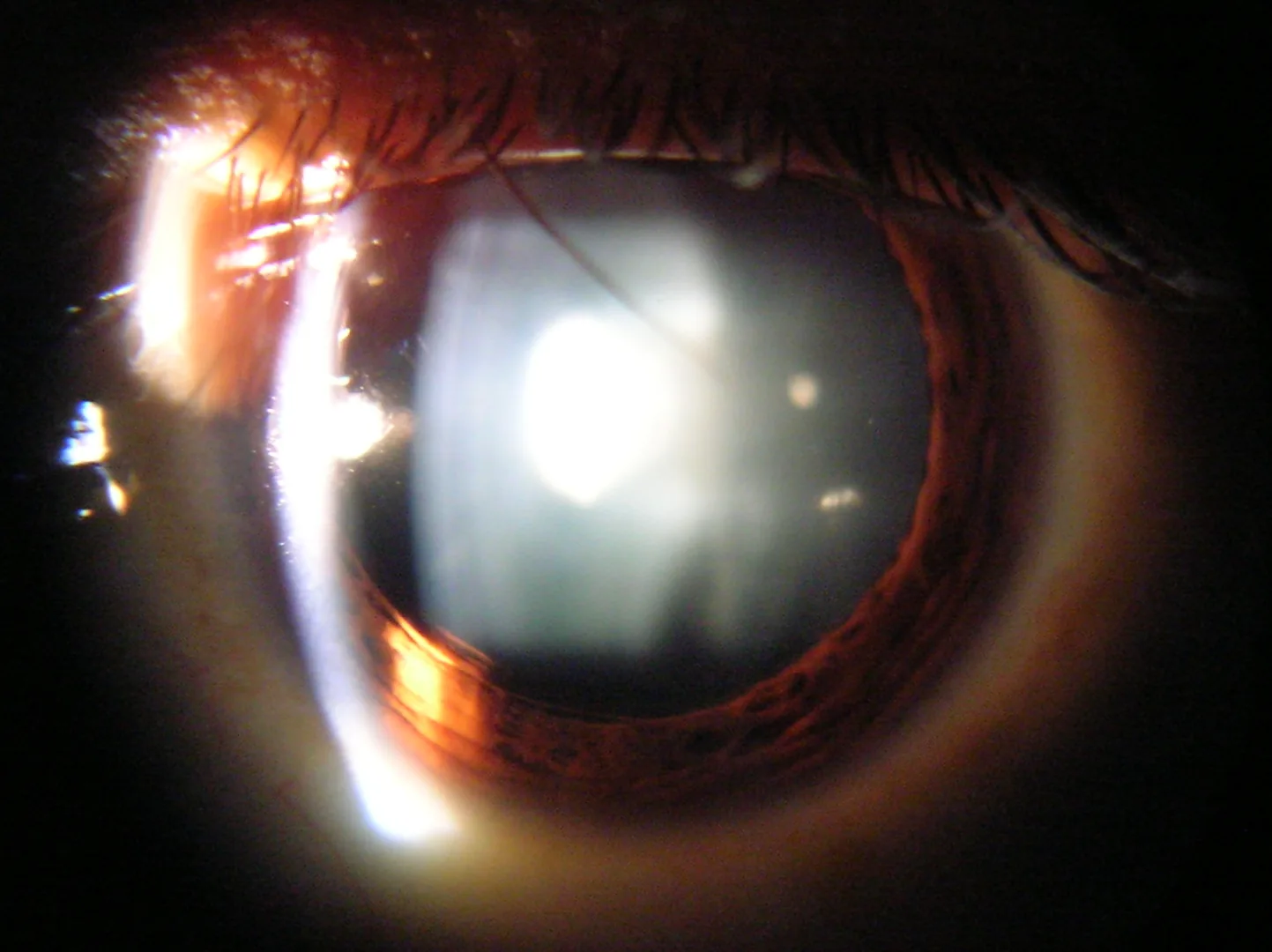
与吸烟相关的主要眼病可归纳为六种。
白内障
干眼症
直接有害作用:烟草烟雾直接损伤泪膜7)
杯细胞损伤:结膜杯细胞损伤导致黏液层变薄7)
被动吸烟环境可能增加过敏性疾病风险4)
甲状腺眼病(TED)
最强环境因素:吸烟是格雷夫斯眼病发生和加重的最强环境因素8)
发病风险:吸烟者TED发病OR约7.78)
放射性碘治疗后,吸烟者TED加重风险增加9)
糖尿病视网膜病变和Leber遗传性视神经病变
Section titled “糖尿病视网膜病变和Leber遗传性视神经病变”- 吸烟促进微血管损伤,这是其机制10)
- 增加糖尿病患者进展为增殖性视网膜病变的风险
- 在线粒体DNA突变携带者中,吸烟可诱发发病11)
- 吸烟加重线粒体功能障碍,增加发病风险11)
吸烟是Graves病患者发生甲状腺眼病(TED)的最强环境因素,使风险增加约7.7倍。戒烟已被证明可改善TED治疗效果,且吸烟者在放射性碘治疗后眼病恶化的风险也更高。在开始眼病治疗(类固醇、放射治疗、眼眶减压术)前进行戒烟指导,是最大化治疗效果的前提条件。
3. 流行病学数据
Section titled “3. 流行病学数据”吸烟对眼病的影响在人群水平上也很显著,是一个公共卫生问题。
| 疾病 | 风险增加(OR) | 备注 |
|---|---|---|
| AMD(总体) | 2.0~4.0 | 现吸烟者,荟萃分析1) |
| 渗出型AMD | 特别高 | 与包年呈剂量反应关系5) |
| 核性白内障 | 约2.0 | 20包年以上2) |
| 甲状腺眼病(TED) | 约7.7 | 格雷夫斯病患者8) |
| 糖尿病视网膜病变 | 增加 | 促进微血管损伤10) |
| LHON发病 | 诱因 | mtDNA突变携带者11) |
- 据估计,吸烟对AMD的人群归因危险度(PAR)约占25-30% 1)
- 大规模队列研究已证实吸烟者白内障手术风险显著增加 6)
- 有报告称,被动吸烟环境与儿童及青少年过敏性疾病风险增加有关 4)
- 关于电子烟(包括加热不燃烧烟草制品)对眼部影响的研究正在积累中 12),有待证据的确立
4. 诊断与筛查
Section titled “4. 诊断与筛查”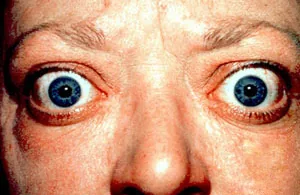
在眼科门诊,主动询问吸烟史非常重要。尤其是在AMD和甲状腺眼病的初诊问诊中,应将其作为必问项目。
吸烟史的量化:
- 计算包年数:每日吸烟支数 ÷ 20 × 吸烟年数
- 确认当前吸烟、已戒烟(戒烟年数)或不吸烟
- 同时评估被动吸烟环境(工作场所和家庭)
AMD高风险人群的应对:
- 对于有吸烟史、家族史和单眼AMD的患者,建议定期进行眼底检查 5)
- OCT对于早期检测玻璃膜疣和视网膜色素上皮变化是有效的
- 对于单眼发病病例,应缩短对侧眼的随访间隔。
甲状腺眼病患者的处理:
- 每次就诊时必须确认吸烟状况 8)
- 戒烟指导是开始治疗前的先决条件。
- 对于接受放射性碘治疗的吸烟者,应事先充分说明眼病加重的可能性 9)
- 术前问诊应包括吸烟史。
- 对于重度干眼症患者,问诊时应确认吸烟史和被动吸烟环境 7)
5. 戒烟指导与预防
Section titled “5. 戒烟指导与预防”戒烟是对眼部疾病最重要且已证实的预防措施,眼科医生也应积极介入。
戒烟对各类疾病风险的降低:
| 疾病 | 戒烟效果 | 证据 |
|---|---|---|
| AMD | 戒烟后10~20年风险显著降低 3) | 前瞻性队列 |
| 白内障(核性) | 戒烟后风险降低已被证实2) | 荟萃分析 |
| 甲状腺眼病 | 戒烟可改善TED治疗效果8) | 干预研究 |
| 糖尿病视网膜病变 | 有助于抑制血管损伤进展10) | 队列研究 |
5A法(眼科应用)13):
- 询问(Ask):对所有患者询问吸烟史
- 建议(Advise):具体告知吸烟的眼病风险
- 评估(Assess):评估戒烟意愿
- 帮助(Assist):介绍戒烟辅助药物或戒烟门诊
- 安排(Arrange):安排随访就诊
药物疗法戒烟支持:
- 尼古丁替代疗法(NRT):尼古丁贴片(7/14/21mg)·尼古丁口香糖13)
- 伐尼克兰(畅沛):α4β2尼古丁受体部分激动剂。标准疗程为12周13)
- 与戒烟门诊合作:利用保险覆盖的12周戒烟治疗计划(5次就诊)14)
6. 病理生理学·详细发病机制
Section titled “6. 病理生理学·详细发病机制”吸烟损害眼组织的主要机制大致分为四类:氧化应激、直接毒性、免疫调节异常和血管损伤。
氧化应激与AMD:
- 据估计,每吸一口香烟烟雾会产生约10的15次方个自由基15)
- 在香烟烟雾暴露的小鼠中,已报道RPE氧化性DNA损伤、基底内褶丧失、空泡增加、Bruch膜增厚和RPE凋亡15)
- Nrf2调控抗氧化反应,衰老和吸烟相关的氧化应激会导致其反应下降,这是一个问题15)
- 补体因子H(CFH)基因多态性(Y402H)与吸烟的协同效应显著增加AMD风险5)
氰化物与核性白内障:
- 烟草烟雾中的氰化物破坏晶状体蛋白(晶状体蛋白)的二硫键
- 蛋白质聚集和不溶化发生,导致核性白内障
- 吸烟量达20包年或以上的吸烟者核混浊显著增加2)
尼古丁与血管损伤:
- 尼古丁刺激交感神经,引起血管收缩,降低视网膜血流10)
- 糖尿病患者中,已有的微血管损伤因吸烟而进一步加重10)
免疫调节异常与甲状腺眼病(TED):
- 吸烟引起的免疫调节异常促进TSH受体抗体(TRAb)产生增加8)
- 眼眶成纤维细胞活化和透明质酸产生增加导致眼眶组织增厚和眼球突出8)
对泪膜的影响与干眼症:
- 烟草烟雾中的有害化学物质使泪膜脂质层不稳定,导致蒸发过强型干眼症7)
- 它损害结膜杯状细胞,使黏液层变薄,降低泪膜稳定性7)
LHON与线粒体功能障碍:
- 在线粒体DNA突变(如11778G>A)携带者中,吸烟会加重已有的线粒体功能障碍,成为发病诱因11)
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”电子烟和加热不燃烧烟草制品对眼睛的影响:
- 评估电子烟和加热不燃烧烟草制品(如IQOS)对眼睛影响的流行病学研究正在积累12)
- 人们担心通过尼古丁和挥发性有机化合物途径对眼表产生影响
- 与传统烟草相比的风险评估目前尚未确立,因此需要谨慎态度
基因-环境相互作用:
戒烟干预与AMD进展抑制:
- 验证戒烟对抑制AMD发病和进展效果的前瞻性队列研究正在进行中
- 戒烟与AREDS补充剂(维生素C 500mg、维生素E 400IU、锌80mg、铜2mg、叶黄素10mg、玉米黄质2mg)的联合效果也正在评估中。
三手烟:
- 附着在墙壁、衣物和家具上的残留化学物质(三手烟)对眼表的影响正受到关注。
- 与儿童及吸烟者家属的眼表疾病之间的关联是未来的研究课题。
基于AI的眼底照片吸烟状态评估:
- 已有研究报道使用机器学习模型从眼底照片评估吸烟状态,有望应用于眼科筛查。
8. 参考文献
Section titled “8. 参考文献”- Chakravarthy U, Wong TY, Fletcher A, et al. Clinical risk factors for age-related macular degeneration: a systematic review and meta-analysis. BMC Ophthalmol. 2010;10:31.
- Ye J, He J, Wang C, et al. Smoking and risk of age-related cataract: a meta-analysis. Invest Ophthalmol Vis Sci. 2012;53(7):3885-3895.
- Khan JC, Thurlby DA, Shahid H, et al. Smoking and age related macular degeneration: the number of pack years of cigarette smoking is a major determinant of risk for both geographic atrophy and choroidal neovascularisation. Br J Ophthalmol. 2006;90(1):75-80.
- Saulyte J, Regueira C, Montes-Martinez A, Khudyakov P, Takkouche B. Active or passive exposure to tobacco smoking and allergic rhinitis, allergic dermatitis, and food allergy in adults and children: a systematic review and meta-analysis. PLoS Med. 2014;11(3):e1001611. PMCID: PMC3949681. doi:10.1371/journal.pmed.1001611.
- Seddon JM, George S, Rosner B. Cigarette smoking, fish consumption, omega-3 fatty acid intake, and associations with age-related macular degeneration: the US Twin Study of Age-Related Macular Degeneration. Arch Ophthalmol. 2006;124(7):995-1001.
- Kelly SP, Thornton J, Edwards R, et al. Smoking and cataract: review of causal association. J Cataract Refract Surg. 2005;31(12):2395-2404.
- Moss SE, Klein R, Klein BE. Prevalence of and risk factors for dry eye syndrome. Arch Ophthalmol. 2000;118(9):1264-1268.
- Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
- Bartalena L, Marcocci C, Tanda ML, et al. Cigarette smoking and treatment outcomes in Graves ophthalmopathy. Ann Intern Med. 1998;129(8):632-635.
- Cai J, Boulton M. The pathogenesis of diabetic retinopathy: old concepts and new questions. Eye (Lond). 2002;16(3):242-260.
- Kirkman MA, Yu-Wai-Man P, Korsten A, et al. Gene-environment interactions in Leber hereditary optic neuropathy. Brain. 2009;132(Pt 9):2317-2326.
- Mehra D, Galor A. Digital screen use and dry eye: a review. Asia Pac J Ophthalmol. 2020;9(6):491-497.
- Fiore MC, Jaén CR, Baker TB, et al. Treating tobacco use and dependence: 2008 update. Clinical practice guideline. Rockville, MD: U.S. Department of Health and Human Services; 2008.
- JCS Joint Working Group. Guidelines for smoking cessation (JCS 2010): digest version. Circ J. 2012;76(4):1024-1043.
- Cano M, Thimmalappula R, Fujihara M, et al. Cigarette smoking, oxidative stress, the anti-oxidant response through Nrf2 signaling, and age-related macular degeneration. Vision Res. 2010;50(7):652-664.
