加齢黄斑変性(AMD)

喫煙と眼疾患(加齢黄斑変性や白内障のリスク)(Smoking and Eye Diseases AMD and Cataract Risk)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 喫煙と眼疾患の関連とは
Section titled “1. 喫煙と眼疾患の関連とは”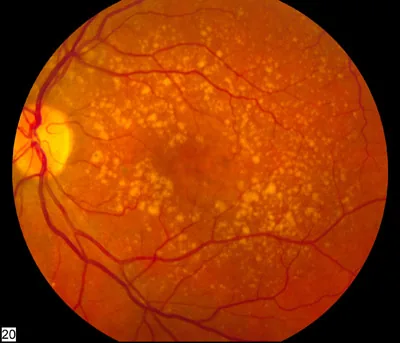
喫煙(タバコ)は複数の眼疾患のリスク因子として確立されている。特に加齢黄斑変性(AMD)・白内障・ドライアイ・糖尿病網膜症・甲状腺眼症・レーベル遺伝性視神経症との関連が科学的に証明されている。
タバコ煙には4,000種類以上の化学物質が含まれ、その中のシアン化物・カドミウム・ニコチン・フリーラジカルが眼組織に多彩な障害をもたらす。現喫煙者のAMD発症オッズ比は2.0〜4.0(システマティックレビュー・メタ解析)であり1)、AMDの修正可能リスク因子のなかで最も強力なものと位置づけられる。核白内障については、20 pack-year以上の喫煙でオッズ比が約2.0に上昇する2)。
累積喫煙量(pack-year = 1日喫煙本数(本)÷ 20 × 喫煙年数)と眼疾患リスクには明確な用量反応関係がある1)。禁煙後は徐々にリスクが低下するが、非喫煙者と同レベルに戻るまでには20年以上かかる場合があり3)、早期の禁煙が最大の恩恵をもたらす。受動喫煙(副流煙曝露)は小児・思春期のアレルギー疾患リスク上昇と関連する4)。
- 喫煙は加齢黄斑変性の最も重要な修正可能リスク因子である1)
- 核白内障リスクは20 pack-year以上でOR 約2.02)
- 禁煙後20年で非喫煙者に近いリスクに低下3)
- 受動喫煙もアレルギー疾患リスクを高める可能性がある4)
2. 喫煙と関連する眼疾患
Section titled “2. 喫煙と関連する眼疾患”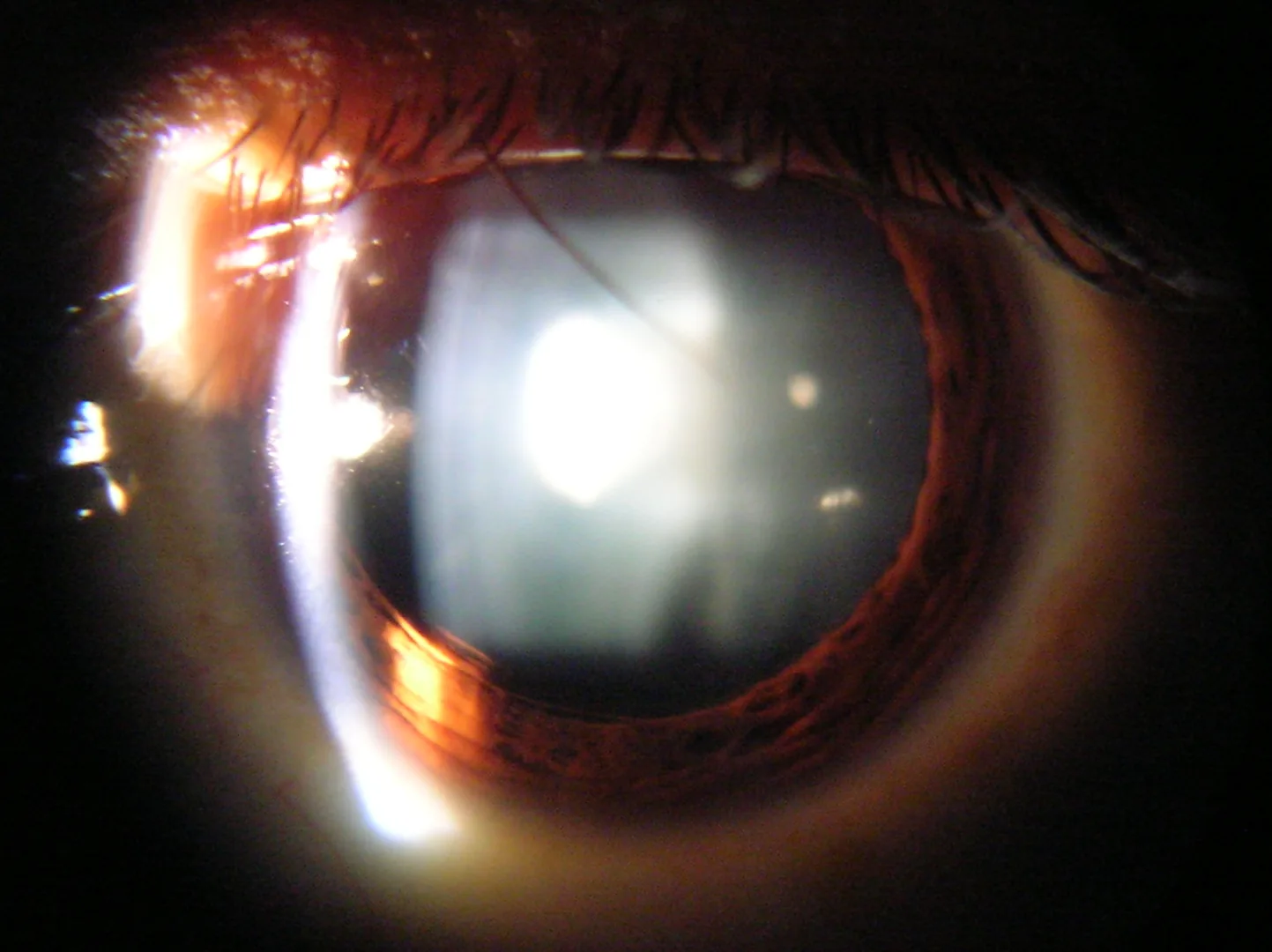
喫煙が関与する主な眼疾患は6種類に整理できる。
白内障
ドライアイ
直接的有害作用:タバコ煙が涙液層へ直接障害を与える7)
杯細胞障害:結膜杯細胞の障害による粘液層の菲薄化7)
受動喫煙環境ではアレルギー疾患リスクが高まる可能性がある4)
甲状腺眼症(TED)
最強の環境因子:喫煙はバセドウ病眼症の発症・重症化の最強環境因子8)
発症リスク:喫煙者のTED発症OR 約7.78)
放射性ヨウ素治療後のTED増悪リスクが喫煙者で上昇9)
糖尿病網膜症・レーベル遺伝性視神経症
Section titled “糖尿病網膜症・レーベル遺伝性視神経症”- 喫煙による微小血管障害の促進が機序となる10)
- 糖尿病患者での増殖網膜症進行リスクが増加する
レーベル遺伝性視神経症(LHON):
- ミトコンドリアDNA変異保有者において喫煙が発症の誘因となる11)
- 喫煙によるミトコンドリア機能障害の増悪が発症リスクを高める11)
3. 疫学データ
Section titled “3. 疫学データ”喫煙の眼疾患への影響は人口レベルでも大きく、公衆衛生上の課題である。
| 疾患 | リスク増加(OR) | 備考 |
|---|---|---|
| AMD(全体) | 2.0〜4.0 | 現喫煙者、メタ解析1) |
| 滲出型AMD | 特に高い | pack-yearと用量反応関係5) |
| 核白内障 | 約2.0 | 20 pack-year以上2) |
| 甲状腺眼症(TED) | 約7.7 | バセドウ病患者8) |
| 糖尿病網膜症 | 増加 | 微小血管障害促進10) |
| LHON発症 | 誘因 | mtDNA変異保有者11) |
- AMDの人口寄与危険割合(PAR)は喫煙が約25〜30%を占めるとの推計がある1)
- 喫煙者の白内障手術リスクは大規模コホート研究で有意な増加が確認されている6)
- 受動喫煙環境と小児・思春期のアレルギー疾患リスク増加が報告されている4)
- 電子タバコ(加熱式タバコを含む)については眼への影響の研究が蓄積しつつあり12)、エビデンスの確立が待たれる状況である
4. 診断とスクリーニング
Section titled “4. 診断とスクリーニング”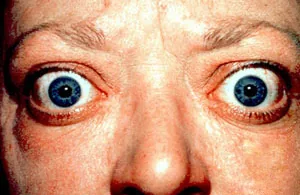
眼科外来では喫煙歴の積極的聴取が重要である。特にAMD・甲状腺眼症の初診問診においては必須の項目として位置づける。
喫煙歴の定量化:
- pack-year(パックイヤー)の算出:1日喫煙本数(本) ÷ 20 × 喫煙年数
- 現喫煙・禁煙(禁煙年数)・非喫煙の別を確認する
- 受動喫煙環境(職場・家庭)の評価も行う
AMD高リスク群への対応:
- 喫煙歴あり + 家族歴あり + 片眼AMD の患者は定期的な眼底検査を推奨する5)
- OCTによるドルーゼン・網膜色素上皮変化の早期検出が有効である
- 片眼発症例では対眼の経過観察間隔を短縮する
甲状腺眼症患者への対応:
- 喫煙状態の確認は診察時に必ず行う8)
- 禁煙指導は治療開始前の前提条件となる
- 放射性ヨウ素治療を行う喫煙者には眼症増悪の可能性を事前に十分説明する9)
白内障・ドライアイ患者への対応:
- 術前問診に喫煙歴を含める
- 重症ドライアイ患者の問診では喫煙歴・受動喫煙環境を確認する7)
5. 禁煙指導と予防
Section titled “5. 禁煙指導と予防”禁煙は眼疾患に対して最も重要かつ証明された予防策であり、眼科医も積極的に介入する役割がある。
禁煙による各疾患リスクの低下:
| 疾患 | 禁煙効果 | エビデンス |
|---|---|---|
| AMD | 禁煙後10〜20年でリスク有意低下3) | 前向きコホート |
| 白内障(核) | 禁煙後にリスク低下が認められる2) | メタ解析 |
| 甲状腺眼症 | 禁煙によりTED治療効果が改善8) | 介入研究 |
| 糖尿病網膜症 | 血管障害の進展抑制に寄与10) | コホート |
5A法(眼科での活用)13):
- Ask(尋ねる): 全患者に喫煙歴を問診する
- Advise(助言する): 喫煙の眼疾患リスクを具体的に伝える
- Assess(評価する): 禁煙意欲を評価する
- Assist(支援する): 禁煙補助薬・禁煙外来を紹介する
- Arrange(手配する): フォローアップの受診を設定する
薬物療法による禁煙支援:
- ニコチン代替療法(NRT):ニコチンパッチ(7/14/21mg)・ニコチンガム13)
- バレニクリン(チャンピックス):α4β2ニコチン受容体部分作動薬。12週間投与が標準13)
- 禁煙外来との連携:保険適用12週間の禁煙治療プログラム(5回の受診)を活用する14)
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”喫煙が眼組織を障害する主要メカニズムは、酸化ストレス・直接毒性・免疫調節異常・血管障害の4つに大別される。
酸化ストレスとAMD:
- タバコ煙1回の吸引で約10の15乗個のフリーラジカルが産生されると推定されている15)
- タバコ煙曝露マウスでは、RPEの酸化DNA損傷、基底陥入の喪失、空胞増加、Bruch膜肥厚、RPEアポトーシスが報告されている15)
- Nrf2は抗酸化応答を統括し、加齢や喫煙関連酸化ストレスで応答低下が問題となる15)
- 補体因子H(CFH)遺伝子多型(Y402H)と喫煙の相乗効果でAMDリスクが著しく増大する5)
シアン化物と核白内障:
- タバコ煙中のシアン化物が水晶体蛋白(クリスタリン)のジスルフィド結合を破壊する
- 蛋白質の凝集・不溶化が起こり、核白内障が生じる
- 20 pack-year以上の喫煙者で核混濁が顕著に増加する2)
ニコチンと血管障害:
- ニコチンが交感神経を刺激して血管収縮を引き起こし、網膜血流を低下させる10)
- 糖尿病患者では既存の微小血管障害が喫煙によりさらに増悪する10)
免疫調節異常と甲状腺眼症(TED):
- 喫煙による免疫調節異常がTSH受容体抗体(TRAb)の産生増加を促進する8)
- 眼窩線維芽細胞の活性化・ヒアルロン酸産生増加が眼窩組織の肥厚・眼球突出をもたらす8)
涙液層への影響とドライアイ:
- タバコ煙の有害化学物質が涙液層脂質層を不安定化し、蒸発亢進型ドライアイを引き起こす7)
- 結膜杯細胞を障害して粘液層を菲薄化させ、涙液の安定性が低下する7)
LHON とミトコンドリア障害:
- ミトコンドリアDNA変異(11778G>A 等)の保有者において、喫煙が既存のミトコンドリア機能障害を増悪させて発症誘因となる11)
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”電子タバコ・加熱式タバコの眼への影響:
- 電子タバコ(e-cigarette)および加熱式タバコ(IQOS等)の眼への影響を評価する疫学研究が蓄積しつつある12)
- ニコチン・揮発性有機化合物の経路を介した眼表面への影響が懸念されている
- 従来のタバコと比較したリスク評価は現時点では確立していないため、慎重な姿勢が必要である
遺伝子—環境相互作用:
禁煙介入とAMD進行抑制:
- 禁煙によるAMD発症抑制・進行抑制効果を検証する前向きコホート研究が進行中である
- 禁煙とAREDSサプリメント(ビタミンC 500mg・ビタミンE 400IU・亜鉛80mg・銅2mg・ルテイン10mg・ゼアキサンチン2mg)の組み合わせ効果の評価も行われている
三次喫煙(thirdhand smoke):
- 壁や衣服・家具に付着した残留化学物質(三次喫煙)の眼表面への影響が注目されている
- 小児や喫煙者の家族における眼表面障害との関連が今後の研究課題である
AIによる眼底写真からの喫煙状態推定:
- 機械学習モデルを用いて眼底写真から喫煙状態を推定する研究が報告されており、眼科スクリーニングへの応用が期待されている
8. 参考文献
Section titled “8. 参考文献”- Chakravarthy U, Wong TY, Fletcher A, et al. Clinical risk factors for age-related macular degeneration: a systematic review and meta-analysis. BMC Ophthalmol. 2010;10:31.
- Ye J, He J, Wang C, et al. Smoking and risk of age-related cataract: a meta-analysis. Invest Ophthalmol Vis Sci. 2012;53(7):3885-3895.
- Khan JC, Thurlby DA, Shahid H, et al. Smoking and age related macular degeneration: the number of pack years of cigarette smoking is a major determinant of risk for both geographic atrophy and choroidal neovascularisation. Br J Ophthalmol. 2006;90(1):75-80.
- Saulyte J, Regueira C, Montes-Martinez A, Khudyakov P, Takkouche B. Active or passive exposure to tobacco smoking and allergic rhinitis, allergic dermatitis, and food allergy in adults and children: a systematic review and meta-analysis. PLoS Med. 2014;11(3):e1001611. PMCID: PMC3949681. doi:10.1371/journal.pmed.1001611.
- Seddon JM, George S, Rosner B. Cigarette smoking, fish consumption, omega-3 fatty acid intake, and associations with age-related macular degeneration: the US Twin Study of Age-Related Macular Degeneration. Arch Ophthalmol. 2006;124(7):995-1001.
- Kelly SP, Thornton J, Edwards R, et al. Smoking and cataract: review of causal association. J Cataract Refract Surg. 2005;31(12):2395-2404.
- Moss SE, Klein R, Klein BE. Prevalence of and risk factors for dry eye syndrome. Arch Ophthalmol. 2000;118(9):1264-1268.
- Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
- Bartalena L, Marcocci C, Tanda ML, et al. Cigarette smoking and treatment outcomes in Graves ophthalmopathy. Ann Intern Med. 1998;129(8):632-635.
- Cai J, Boulton M. The pathogenesis of diabetic retinopathy: old concepts and new questions. Eye (Lond). 2002;16(3):242-260.
- Kirkman MA, Yu-Wai-Man P, Korsten A, et al. Gene-environment interactions in Leber hereditary optic neuropathy. Brain. 2009;132(Pt 9):2317-2326.
- Mehra D, Galor A. Digital screen use and dry eye: a review. Asia Pac J Ophthalmol. 2020;9(6):491-497.
- Fiore MC, Jaén CR, Baker TB, et al. Treating tobacco use and dependence: 2008 update. Clinical practice guideline. Rockville, MD: U.S. Department of Health and Human Services; 2008.
- JCS Joint Working Group. Guidelines for smoking cessation (JCS 2010): digest version. Circ J. 2012;76(4):1024-1043.
- Cano M, Thimmalappula R, Fujihara M, et al. Cigarette smoking, oxidative stress, the anti-oxidant response through Nrf2 signaling, and age-related macular degeneration. Vision Res. 2010;50(7):652-664.
