ルテイン・ゼアキサンチン

サプリメントと眼疾患(ルテイン・ゼアキサンチンなど)(Supplements and Eye Health Lutein Zeaxanthin)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. サプリメントと眼疾患の関連とは
Section titled “1. サプリメントと眼疾患の関連とは”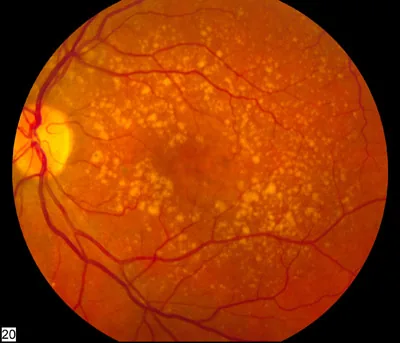
眼疾患の予防・進行抑制を目的として、栄養素・サプリメントの科学的根拠を検討する分野が注目されている。特に加齢黄斑変性(AMD)・白内障・ドライアイの3疾患について、大規模な無作為化比較試験(RCT)が実施されてきた。
最大のエビデンス源は米国国立眼科研究所(NEI)が主導したAREDS(Age-Related Eye Disease Study)である。1992〜2001年に実施されたAREDSは3,640例を対象とした大規模RCTであり1)、ビタミンC 500 mg・ビタミンE 400 IU・βカロチン15 mg・酸化亜鉛80 mgを組み合わせた「AREDS処方」を検証した。中等度以上のAMD(AREDSカテゴリ3・4)の患者においてAMD進行リスクが約25%低下することが示された1)。
2006〜2012年に実施されたAREDS2(4,203例)では2)、βカロチンをルテイン10 mg+ゼアキサンチン2 mg/日に置換した新処方の有効性・安全性が検証された。ルテイン・ゼアキサンチンへの置換はβカロチンと同等のAMD進行抑制効果を示しつつ2)、βカロチンに関連する喫煙者の肺癌リスク増加を回避できる点で現在の標準処方となっている。
重要な点として、AREDS/AREDS2処方は中等度以上のAMDを有する患者の進行抑制を対象としており、AMDのない一般人への発症予防効果は確立していない。サプリメントは眼科的管理の補助手段であり、定期的な眼科検査による早期発見・早期治療との組み合わせが基本となる。
2. 主要サプリメント成分と眼疾患
Section titled “2. 主要サプリメント成分と眼疾患”眼疾患に関連する主要なサプリメント成分は5種類に大別される。
ビタミンC・E
亜鉛
役割:抗酸化酵素(Cu/Zn-SOD・カタラーゼ等)の補因子として網膜色素上皮の代謝を支える1)。
AREDS処方用量:酸化亜鉛 80 mg/日(銅欠乏性貧血予防のため酸化銅 2 mg/日を併用)1)。
AREDS2での変更:25 mgへの減量が検討されたが、80 mg群と有意差がなかった2)。
オメガ3脂肪酸(EPA/DHA)
アントシアニン(ビルベリー等)
Section titled “アントシアニン(ビルベリー等)”ブルーベリー・ビルベリーに含まれるアントシアニンは、暗順応改善や網膜血流改善効果が基礎研究レベルで報告されている。ただし、RCTでの有効性エビデンスは限定的であり9)、現時点では診療において推奨できるエビデンスは不十分とされる。
AREDS・AREDS2処方の内容比較
Section titled “AREDS・AREDS2処方の内容比較”各処方成分の用量を以下に示す。
| 成分 | AREDS処方 | AREDS2処方 |
|---|---|---|
| ビタミンC | 500 mg/日 | 500 mg/日 |
| ビタミンE | 400 IU/日 | 400 IU/日 |
| βカロチン | 15 mg/日 | 除外(ルテイン/ゼアキサンチンに置換) |
| ルテイン | — | 10 mg/日 |
| ゼアキサンチン | — | 2 mg/日 |
| 酸化亜鉛 | 80 mg/日 | 80 mg/日(25 mgも検討) |
| 酸化銅 | 2 mg/日 | 2 mg/日 |
3. エビデンスの詳細
Section titled “3. エビデンスの詳細”AREDS研究の概要
Section titled “AREDS研究の概要”AREDS・AREDS2は眼科サプリメント研究の最高レベルのエビデンス源である。
AREDS(2001年報告)1):
- 対象:AREDSカテゴリ3(進行した一側性AMDまたは多数の中型ドルーゼン)・カテゴリ4(進行した両側性AMD)の3,640例
- 介入:ビタミンC 500 mg+ビタミンE 400 IU+βカロチン15 mg+酸化亜鉛80 mg/日
- 結果:AMD進行リスクを約25%低下(RR 0.75)。高リスク群での最大利益
AREDS2(2013年報告)2):
- 対象:4,203例(AMD患者)
- 主要変更:βカロチン→ルテイン10 mg+ゼアキサンチン2 mg/日への置換
- 結果:置換後もAMD進行抑制で非劣性を示した。喫煙既往者では滲出型AMD進行リスクがルテイン/ゼアキサンチン群でさらに低下
AREDS2の長期追跡(2022年、10年データ)10):
- ルテイン/ゼアキサンチン群では滲出型AMDへの進行リスクが長期的にさらに低下することが確認された
- 長期安全性の問題は認められなかった
主要臨床試験のまとめ
Section titled “主要臨床試験のまとめ”各試験の特徴を以下に示す。
| 試験名 | 対象 | 主要結果 |
|---|---|---|
| AREDS(2001) | AMD 3,640例 | AREDS処方でAMD進行リスク約25%低下1) |
| AREDS2(2013) | AMD 4,203例 | ルテイン/ゼアキサンチン置換で非劣性確認2) |
| AREDS2長期(2022) | AMD 4,203例 | 10年追跡でルテイン群の利益持続10) |
| DREAM(2018) | ドライアイ 535例 | オメガ3のドライアイ改善効果:プラセボと差なし7) |
白内障との関連
Section titled “白内障との関連”AREDS処方による白内障予防効果は確認されなかった1)。一方、複数の疫学研究においてルテイン・ゼアキサンチンの食事摂取量と核白内障リスクの間に逆相関が示されており5)、食事を通じた摂取が白内障発症のリスク低減につながる可能性が示唆されている。ただし、サプリメントとしての介入効果を証明する大規模RCTはまだない。
コクランレビュー(Mathew 2012、21 RCT)では、抗酸化ビタミン(A・C・E)・ルテイン・ゼアキサンチンのサプリメント補充は白内障の発症または進行を遅らせるという信頼性の高いエビデンスはないと結論している6)。
ドライアイとの関連
Section titled “ドライアイとの関連”DREAM試験(2018年)は、慢性ドライアイ患者535例を対象にオメガ3脂肪酸(EPA 2,000 mg+DHA 1,000 mg/日、12か月間)の有効性をオリーブ油プラセボと比較したRCTである。主要評価項目(OSDI[眼表面疾患指数]スコア)において両群間に有意差はなく7)、オメガ3サプリメントのドライアイへの有効性は否定的な結果となった。メタ解析(Giannaccare 2019)では一部の有効性が報告されているが11)、DREAM試験の質の高さからオメガ3サプリメントはドライアイの標準治療には含まれない。
4. 摂取の実際
Section titled “4. 摂取の実際”AREDS2処方の適応
Section titled “AREDS2処方の適応”- 対象:片眼に中等度以上のAMD(AREDSカテゴリ3・4)と診断されている患者2)
- 早期AMDへの効果は限定的:AREDSカテゴリ1・2(小型ドルーゼン)では有意な進行抑制効果は示されていない。不必要なサプリメント使用は過剰摂取リスクをもたらすため注意が必要
- 禁煙状態の確認:喫煙者にはβカロチンを含まないAREDS2処方を選択する
食事からの摂取
Section titled “食事からの摂取”
緑黄色野菜はルテイン・ゼアキサンチンの優れた供給源である4)。
- ほうれん草:ルテイン約12 mg/100 g、ゼアキサンチン約1.1 mg/100 g4)
- ケール:ルテイン約22 mg/100 g(食品中最高レベル)4)
- ブロッコリー:ルテイン約1.4 mg/100 g4)
- 卵黄:ルテイン・ゼアキサンチンの生物利用能が高い(野菜の3〜4倍)4)
魚(さば・さんま・いわし等)は週2回以上の摂取がEPA/DHA源として有用であり8)、疫学研究で魚摂取量とAMDリスク低下の関連が報告されている。
機能性表示食品制度
Section titled “機能性表示食品制度”サプリメントは医薬品ではなく、食品に分類される。消費者庁の機能性表示食品制度(2015年)により、一定の科学的根拠に基づいた機能性の表示が認められているが12)、医薬品のような有効性・安全性の国家による審査は受けていない。AREDS2処方成分に相当する製品を選ぶ際には、成分含有量を確認し、過剰摂取にならないよう注意する。
ほうれん草(約12 mg/100 g)・ケール(約22 mg/100 g)・ブロッコリーなどの緑黄色野菜がルテインの主要な食品源である4)。また、卵黄はルテイン含量は野菜ほど高くないが、脂溶性のため吸収効率が高い。食事から6〜10 mg/日のルテインを摂取することが目安とされる。緑黄色野菜を毎日積極的に食べることが、食事由来のルテイン摂取の基本となる。
5. 注意点・過剰摂取リスク
Section titled “5. 注意点・過剰摂取リスク”サプリメントは適切に使用しなければ副作用・リスクをもたらす。以下の点に注意が必要である。
βカロチンと喫煙者の肺癌リスク:
- ATBC研究(1994年)では喫煙男性29,133例へのβカロチン補充(20 mg/日)が肺癌発生率を18%増加させた13)
- CARET研究でも喫煙者・石綿曝露者でのβカロチン補充が肺癌リスクを増加
- AREDS2ではこの知見に基づきβカロチンをルテイン/ゼアキサンチンに置換した2)
- 喫煙者・禁煙後も喫煙歴のある人には、βカロチンを含むAREDS処方は使用しない
亜鉛の過剰摂取:
- AREDS処方の酸化亜鉛80 mg/日の長期使用時に銅欠乏性貧血が報告されている1)
- AREDS処方には酸化銅2 mgが銅欠乏対策として含まれているが、長期服用時は定期的な血液検査が推奨される
- 一般成人の亜鉛耐容上限量(日本人食事摂取基準2020年版):男性45 mg/日、女性35 mg/日
ビタミンEの大量摂取:
- Schürkら(2010年、メタ解析)においてビタミンE大量摂取と出血性脳卒中リスク増加の関連が示唆されている14)
- 高用量(400 IU/日)の長期使用については注意を要する
薬物との相互作用:
- ビタミンE・ω3脂肪酸は抗凝固作用を有し、ワルファリン等の抗凝固薬との相互作用に注意する
- 手術前は服用を中止するよう医師に相談する
AREDS処方に含まれるβカロチンは喫煙者の肺癌リスクを増加させるため、喫煙者・喫煙歴のある人には禁忌相当である13)。AREDS2処方ではβカロチンをルテイン/ゼアキサンチンに置換してこのリスクを回避している。また、酸化亜鉛80 mg/日の長期使用は銅欠乏性貧血を起こしうるため、処方には酸化銅2 mgが必ず含まれる1)。ビタミンEの高用量長期摂取は出血性脳卒中リスクとの関連が指摘されており14)、注意が必要である。
6. 病態生理学・抗酸化メカニズム
Section titled “6. 病態生理学・抗酸化メカニズム”酸化ストレスと眼疾患
Section titled “酸化ストレスと眼疾患”黄斑は光誘発性酸化ストレスのリスクが高い領域であり、紫外線・青色光により活性酸素種(ROS)が生じうる。酸化ストレスはAMDの発症・進行に関与する3)。
- ROS産生:光反応によるリポフシン(老廃物)の光酸化がRPE障害の主因となる
- ドルーゼン形成:RPEの処理能低下により細胞外マトリックスにリポタンパク質や補体が沈着する
- 滲出型AMDへの進行:酸化ストレスとRPE障害が補体活性化・VEGFシグナルを誘発し血管新生を起こす
黄斑色素の光保護作用
Section titled “黄斑色素の光保護作用”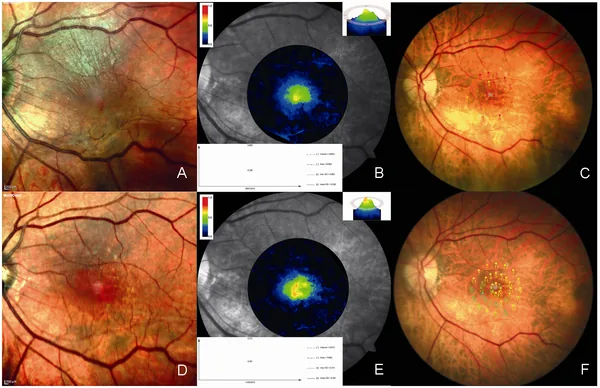
ルテイン・ゼアキサンチンは黄斑に選択的に蓄積し、黄斑色素光学密度(MPOD: Macular Pigment Optical Density)を形成する3)。
- 光フィルター機能:青色光(400〜500 nm)を選択的に吸収し、光受容体への到達を減衰させる
- 抗酸化機能:一重項酸素・ペルオキシラジカルを直接消去するROSスカベンジャーとして機能する
- meso-ゼアキサンチン:網膜内でルテインから酵素的に変換される第3の黄斑色素であり、黄斑中心部に最も高濃度で分布する3)
亜鉛の抗酸化酵素補因子としての役割
Section titled “亜鉛の抗酸化酵素補因子としての役割”亜鉛は抗酸化酵素Cu/Zn-SOD(銅・亜鉛スーパーオキシドジスムターゼ)の活性部位に必須の補因子として機能する1)。SODはROSの一種であるスーパーオキシドアニオンを無害な過酸化水素に変換する。また、カタラーゼ・グルタチオンペルオキシダーゼと連携して抗酸化防御系全体を維持する。RPEは視細胞から排出されたファゴソームを消化処理する高代謝組織であり、亜鉛の十分な供給は正常機能維持に重要である。
オメガ3脂肪酸の抗炎症作用
Section titled “オメガ3脂肪酸の抗炎症作用”DHA(ドコサヘキサエン酸)は網膜光受容体の外節膜に豊富に含まれるω3長鎖不飽和脂肪酸である。EPA(エイコサペンタエン酸)とともに、抗炎症性脂質メディエーターであるレゾルビン・プロテクチンの前駆体となる7)。これらのメディエーターは炎症収束を促進するが、RCTでのドライアイへの臨床効果は不十分とされる。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”AREDS2長期追跡データ(2022年)
Section titled “AREDS2長期追跡データ(2022年)”AREDS2の10年間の長期追跡データ(報告28: Chew 2022)では10)、ルテイン/ゼアキサンチン群は長期的に滲出型AMDへの進行リスクをさらに低下させることが確認された。また長期安全性の問題は認められず、喫煙者へのβカロチン非含有処方の有益性が改めて支持された。
黄斑色素光学密度(MPOD)のバイオマーカーとしての活用
Section titled “黄斑色素光学密度(MPOD)のバイオマーカーとしての活用”MPOD測定は黄斑内カロテノイド量の指標として研究されている3)。ヘテロクロマティックフリッカー法、共鳴ラマン分光、眼底自発蛍光などによる評価がサプリメント効果の客観的指標として検討されている。
遺伝子多型に基づく個別化栄養指導
Section titled “遺伝子多型に基づく個別化栄養指導”AMD感受性遺伝子(CFH Y402H・ARMS2 A69S)の多型によってAREDS処方の効果が異なる可能性が研究されている15)。CFH多型保有者では亜鉛への反応性が異なることが示唆されており15)、将来的には遺伝子プロファイルに基づいたサプリメント処方の個別化が実現する可能性がある。
腸内細菌叢とカロテノイド吸収
Section titled “腸内細菌叢とカロテノイド吸収”腸内細菌叢の組成がルテイン・ゼアキサンチンの吸収効率・血中濃度に影響することを示す基礎研究が蓄積されている。同じ食事・サプリメント摂取量でも個人間の血中ルテイン濃度に大きな差があることが知られており、腸内環境改善(プロバイオティクス等)との組み合わせによる吸収効率向上が探索されている。
ドライアイに対する栄養介入の継続研究
Section titled “ドライアイに対する栄養介入の継続研究”DREAM試験でオメガ3の効果は否定されたが7)、食事パターン全体(地中海食等)とドライアイリスクの関連についての研究が進んでいる11)。ポリフェノール・ビタミンDなど他の栄養素のドライアイへの関与も検討されており、新規RCTが実施されている。
8. 参考文献
Section titled “8. 参考文献”- Age-Related Eye Disease Study Research Group. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no. 8. Arch Ophthalmol. 2001;119(10):1417-1436.
- Age-Related Eye Disease Study 2 Research Group. Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013;309(19):2005-2015.
- Bernstein PS, Li B, Vachali PP, et al. Lutein, zeaxanthin, and meso-zeaxanthin: the basic and clinical science underlying carotenoid-based nutritional interventions against ocular disease. Prog Retin Eye Res. 2016;50:34-66.
- Perry A, Rasmussen H, Johnson EJ. Xanthophyll (lutein, zeaxanthin) content in fruits, vegetables and corn and egg products. J Food Compos Anal. 2009;22(1):9-15.
- Christen WG, Liu S, Glynn RJ, et al. Dietary carotenoids, vitamins C and E, and risk of cataract in women: a prospective study. Arch Ophthalmol. 2008;126(1):102-109.
- Mathew MC, Ervin AM, Tao J, et al. Antioxidant vitamin supplementation for preventing and slowing the progression of age-related cataract. Cochrane Database Syst Rev. 2012;(6):CD004567.
- Dry Eye Assessment and Management Study Research Group. n-3 Fatty acid supplementation for the treatment of dry eye disease. N Engl J Med. 2018;378(18):1681-1690.
- SanGiovanni JP, Chew EY, Clemons TE, et al. The relationship of dietary lipid intake and age-related macular degeneration in a case-control study: AREDS report no. 20. Arch Ophthalmol. 2007;125(5):671-679.
- Kalt W, Hanneken A, Milbury P, et al. Recent research on polyphenolics in vision and eye health. J Agric Food Chem. 2010;58(7):4001-4007.
- Chew EY, Clemons TE, Agrón E, et al. Long-term outcomes of adding lutein/zeaxanthin and ω-3 fatty acids to the AREDS supplements on age-related macular degeneration progression: AREDS2 report 28. JAMA Ophthalmol. 2022;140(7):692-698.
- Giannaccare G, Pellegrini M, Sebastiani S, et al. Efficacy of omega-3 fatty acid supplementation for treatment of dry eye disease: a meta-analysis of randomized clinical trials. Cornea. 2019;38(5):565-573.
- 消費者庁. 機能性表示食品制度の概要. 2015.
- Alpha-Tocopherol, Beta Carotene Cancer Prevention Study Group. The effect of vitamin E and beta carotene on the incidence of lung cancer and other cancers in male smokers. N Engl J Med. 1994;330(15):1029-1035.
- Schürks M, Glynn RJ, Rist PM, et al. Effects of vitamin E on stroke subtypes: meta-analysis of randomised controlled trials. BMJ. 2010;341:c5702.
- Seddon JM, Reynolds R, Yu Y, et al. Risk models for progression to advanced age-related macular degeneration using demographic, environmental, genetic, and ocular factors. Ophthalmology. 2011;118(11):2203-2211.
