ผลของสารอาหารและอาหารเสริม เช่น ลูทีน ซีแซนทีน วิตามินซี/อี สังกะสี และกรดไขมันโอเมก้า-3 ในการป้องกันและชะลอการดำเนินของจอประสาทตา เสื่อมตามอายุ (AMD ) ต้อกระจก และตาแห้ง ได้รับการศึกษาในการทดลองแบบสุ่มและมีกลุ่มควบคุมขนาดใหญ่
หลักฐานการชะลอการดำเนินของ AMD จาก AREDS (3,640 ราย) เป็นที่ยอมรับ 1) โดยสูตร AREDS (วิตามินซี/อี สังกะสี เบตาแคโรทีน) ลดความเสี่ยงของการดำเนินของ AMD ระดับปานกลางถึงรุนแรงลงประมาณ 25% 1)
ใน AREDS2 (4,203 ราย) เบตาแคโรทีนถูกแทนที่ด้วยลูทีน 10 มก. + ซีแซนทีน 2 มก./วัน ซึ่งให้ผลการยับยั้งการดำเนินโรคที่เทียบเท่า พร้อมหลีกเลี่ยงความเสี่ยงมะเร็งปอดในผู้สูบบุหรี่ 2)
ผลของกรดไขมันโอเมก้า-3 ในการปรับปรุงอาการตาแห้ง ไม่แตกต่างอย่างมีนัยสำคัญจากยาหลอกในการทดลอง DREAM (535 ราย) 7)
เบตาแคโรทีนเพิ่มความเสี่ยงมะเร็งปอดในผู้สูบบุหรี่ ดังนั้นสูตร AREDS ที่มีเบตาแคโรทีนจึงมีข้อห้ามในผู้สูบบุหรี่ 13)
ข้อบ่งชี้ของสูตร AREDS2 คือ AMD ระดับปานกลางถึงรุนแรงในตาข้างเดียว (ประเภท AREDS 3 หรือ 4) และยังไม่มีการพิสูจน์ผลในการป้องกันในประชากรทั่วไปก่อนเกิดโรค
อาหารเสริมเป็นเพียงวิธีการเสริม และควรใช้ร่วมกับการตรวจตาเป็นประจำ
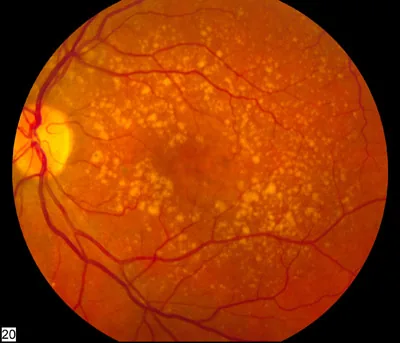
ภาพถ่ายจอประสาทตาของจอประสาทตาเสื่อมตามอายุ (AMD) ระดับปานกลาง (มีดรูเซนจำนวนมาก) National Eye Institute, National Institutes of Health. Intermediate age-related macular degeneration fundus photograph. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Intermediate_age_related_macular_degeneration.jpg. License: CC BY (Public Domain, U.S. federal government work).
ดรูเซน ขนาดกลางถึงใหญ่จำนวนมาก (คราบสีเหลืองขาว) กระจายในบริเวณจุดรับภาพ แสดงลักษณะภาพ
จอประสาทตา ทั่วไปของ
AMD ระดับปานกลาง ภาพนี้สอดคล้องกับลักษณะ
ดรูเซน ใน
AMD ระดับปานกลาง (ประเภท AREDS 3) ซึ่งเป็นหัวข้อของการศึกษา AREDS ที่กล่าวถึงในหัวข้อ “1. ความสัมพันธ์ระหว่าง
อาหารเสริมกับโรคตา ”
สาขาที่ศึกษาหลักฐานทางวิทยาศาสตร์ของสารอาหารและอาหารเสริมเพื่อป้องกันและชะลอการดำเนินของโรคตากำลังได้รับความสนใจ โดยเฉพาะอย่างยิ่งสำหรับสามโรค ได้แก่ จอประสาทตา เสื่อมตามอายุ (AMD ) ต้อกระจก และตาแห้ง ได้มีการทดลองแบบสุ่มและมีกลุ่มควบคุมขนาดใหญ่
แหล่งหลักฐานที่ใหญ่ที่สุดคือการศึกษาโรคตาที่เกี่ยวข้องกับอายุ (AREDS) ซึ่งนำโดยสถาบันตาแห่งชาติของสหรัฐอเมริกา (NEI) AREDS ดำเนินการระหว่างปี 1992 ถึง 2001 เป็นการทดลองแบบสุ่มและมีกลุ่มควบคุมขนาดใหญ่ใน 3,640 ราย 1) โดยทดสอบ “สูตร AREDS” ซึ่งรวมวิตามินซี 500 มก. วิตามินอี 400 IU เบตาแคโรทีน 15 มก. และซิงก์ออกไซด์ 80 มก. ผลลัพธ์แสดงให้เห็นว่าความเสี่ยงของการดำเนินของ AMD ลดลงประมาณ 25% ในผู้ป่วย AMD ระดับปานกลางถึงรุนแรง (ประเภท AREDS 3 หรือ 4) 1)
ในการศึกษา AREDS2 (4,203 ราย) ที่ดำเนินการระหว่างปี 2006 ถึง 2012 2) ได้มีการตรวจสอบประสิทธิภาพและความปลอดภัยของสูตรใหม่ที่แทนที่เบตาแคโรทีนด้วยลูทีน 10 มก. + ซีแซนทีน 2 มก./วัน การแทนที่ด้วยลูทีนและซีแซนทีนแสดงผลในการยับยั้งการดำเนินของ AMD เทียบเท่ากับเบตาแคโรทีน 2) ขณะเดียวกันก็หลีกเลี่ยงความเสี่ยงที่เพิ่มขึ้นของมะเร็งปอดในผู้สูบบุหรี่ที่เกี่ยวข้องกับเบตาแคโรทีน จึงกลายเป็นสูตรมาตรฐานในปัจจุบัน
จุดสำคัญคือ สูตร AREDS/AREDS2 มีวัตถุประสงค์เพื่อ ยับยั้งการดำเนินของโรคในผู้ป่วย AMD ระดับปานกลางถึงรุนแรง และยังไม่มีการพิสูจน์ผลในการป้องกันการเกิดโรคในคนทั่วไปที่ไม่มี AMD อาหารเสริมเป็นเครื่องมือช่วยในการจัดการทางจักษุวิทยา และการรวมกับการตรวจตาเป็นประจำเพื่อการตรวจพบและการรักษาตั้งแต่เนิ่นๆ เป็นพื้นฐาน
Q
อาหารเสริมสามารถป้องกันจอประสาทตาเสื่อมตามอายุได้หรือไม่?
A
สูตร AREDS มีหลักฐานที่ชัดเจนว่าลดความเสี่ยงของการดำเนินของ AMD ระดับปานกลางถึงรุนแรง (ประเภท AREDS 3 และ 4) ได้ประมาณ 25% 1) อย่างไรก็ตาม นี่คือ “การยับยั้งการดำเนินโรค” ไม่ใช่ผล “การป้องกันการเกิดโรค” ในคนที่มีสุขภาพดีที่ไม่มี AMD ยังไม่มีคำแนะนำทั่วไปสำหรับผู้ที่ไม่มีความเสี่ยงต่อ AMD และพิจารณาใช้สูตร AREDS2 ในผู้ป่วยที่ได้รับการยืนยันว่าเป็น AMD ระดับปานกลางถึงรุนแรง
ส่วนประกอบหลักของอาหารเสริมที่เกี่ยวข้องกับโรคตาสามารถจำแนกได้เป็น 5 ประเภท
ลูทีนและซีแซนทีน
บทบาท : ส่วนประกอบหลักของเม็ดสีจอประสาทตา (จอประสาทตา : บริเวณศูนย์กลางที่สำคัญที่สุดของอวัยวะภายในลูกตา) ทำหน้าที่เป็นตัวกรองดูดซับแสงสีน้ำเงิน และกำจัดอนุมูลอิสระ (ROS) เพื่อปกป้องจอตาจากความเสียหายจากออกซิเดชันที่เกิดจากแสง 3)
ขนาดยาในสูตร AREDS2 : ลูทีน 10 มก. + ซีแซนทีน 2 มก./วัน 2)
ความสัมพันธ์กับต้อกระจก : การศึกษาทางระบาดวิทยาแสดงให้เห็นความสัมพันธ์แบบผกผันระหว่างการบริโภคลูทีนและซีแซนทีนจากอาหารกับความเสี่ยงของต้อกระจก ชนิดนิวเคลียร์ 5)
วิตามินซีและอี
บทบาท : วิตามินต้านอนุมูลอิสระที่ละลายน้ำได้ (วิตามินซี) และละลายในไขมันได้ (วิตามินอี) ลดความเครียดออกซิเดชันในเยื่อบุผิวเม็ดสีจอตา (RPE )
ขนาดยาในสูตร AREDS : วิตามินซี 500 มก. + วิตามินอี 400 IU/วัน 1)
การป้องกันต้อกระจก : ผลการป้องกันต้อกระจก ของอาหารเสริมต้านอนุมูลอิสระสรุปว่า “ไม่ได้รับการยืนยัน” ในการทบทวนของ Cochrane (Mathew 2012) 6) การทดลอง AREDS ก็ไม่พบผลการป้องกันต้อกระจก อย่างมีนัยสำคัญ
สังกะสี
บทบาท : สนับสนุนการเผาผลาญของเยื่อบุผิวรงควัตถุจอประสาทตา ในฐานะโคแฟกเตอร์ของเอนไซม์ต้านอนุมูลอิสระ (เช่น Cu/Zn-SOD, catalase) 1) .
ขนาดยา AREDS : ซิงก์ออกไซด์ 80 มก./วัน (ร่วมกับคอปเปอร์ออกไซด์ 2 มก./วัน เพื่อป้องกันโรคโลหิตจางจากการขาดทองแดง) 1) .
การเปลี่ยนแปลงใน AREDS2 : มีการพิจารณาลดขนาดลงเหลือ 25 มก. แต่ไม่มีความแตกต่างอย่างมีนัยสำคัญเมื่อเทียบกับกลุ่ม 80 มก. 2) .
กรดไขมันโอเมก้า-3 (EPA/DHA)
AMD AMD 2) การศึกษาทางระบาดวิทยารายงานความสัมพันธ์ระหว่างการบริโภคปลากับความเสี่ยง AMD ที่ลดลง 8) .
ตาแห้ง ตาแห้ง เมื่อเทียบกับยาหลอกน้ำมันมะกอก 7) .
แอนโทไซยานินที่พบในบลูเบอร์รี่และบิลเบอร์รี่มีรายงานว่ามีผลในการปรับปรุงการปรับตัวในที่มืดและการไหลเวียนเลือดของจอประสาทตา ในระดับการวิจัยพื้นฐาน อย่างไรก็ตาม หลักฐานประสิทธิผลจากการทดลองแบบสุ่มมีจำกัด 9) และในปัจจุบัน หลักฐานยังไม่เพียงพอที่จะแนะนำให้ใช้ในทางคลินิก
ขนาดยาของแต่ละส่วนประกอบในสูตรแสดงไว้ด้านล่าง
ส่วนประกอบ สูตร AREDS สูตร AREDS2 วิตามินซี 500 มก./วัน 500 มก./วัน วิตามินอี 400 IU/วัน 400 IU/วัน เบตาแคโรทีน 15 มก./วัน ตัดออก (แทนที่ด้วยลูทีน/ซีแซนทีน) ลูทีน — 10 มก./วัน ซีแซนทีน — 2 มก./วัน ซิงก์ออกไซด์ 80 มก./วัน 80 มก./วัน (25 มก. อยู่ระหว่างการพิจารณา) คอปเปอร์ออกไซด์ 2 มก./วัน 2 มก./วัน
Q
ควรรับประทานอาหารเสริมลูทีนหรือไม่?
A
ในผู้ป่วยที่ได้รับการวินิจฉัยว่าเป็น AMD ระดับปานกลางถึงรุนแรง (ประเภท AREDS 3 และ 4) แนะนำให้รับประทานสูตร AREDS2 (ส่วนผสมของลูทีน 10 มก. + ซีแซนทีน 2 มก./วัน) 2) ในขณะที่ไม่มีคำแนะนำทั่วไปสำหรับผู้ที่มีสุขภาพดีไม่มีความเสี่ยงต่อ AMD โดยพื้นฐานแล้วควรได้รับจากการรับประทานผักใบเขียว เช่น ผักโขมและคะน้า สิ่งสำคัญคือต้องปรึกษาจักษุแพทย์ก่อนตัดสินใจ
AREDS และ AREDS2 เป็นแหล่งหลักฐานระดับสูงสุดในการวิจัยอาหารเสริมทางจักษุวิทยา
AREDS (รายงานปี 2001) 1) :
กลุ่มตัวอย่าง: 3,640 รายในประเภท AREDS 3 (AMD ข้างเดียวระยะลุกลามหรือดรูเซน ขนาดกลางหลายจุด) และประเภท 4 (AMD สองข้างระยะลุกลาม)
การแทรกแซง: วิตามินซี 500 มก. + วิตามินอี 400 IU + เบตาแคโรทีน 15 มก. + ซิงก์ออกไซด์ 80 มก./วัน
ผลลัพธ์: ความเสี่ยงในการลุกลามของ AMD ลดลงประมาณ 25% (RR 0.75) ประโยชน์สูงสุดในกลุ่มที่มีความเสี่ยงสูง
AREDS2 (รายงานปี 2013) 2) :
กลุ่มตัวอย่าง: 4,203 ราย (ผู้ป่วย AMD )
การเปลี่ยนแปลงหลัก: แทนที่เบตาแคโรทีนด้วยลูทีน 10 มก. + ซีแซนทีน 2 มก./วัน
ผลลัพธ์: แสดงให้เห็นว่าไม่ด้อยกว่าในการยับยั้งการดำเนินของ AMD หลังจากเปลี่ยนสูตร ในผู้ที่มีประวัติสูบบุหรี่ ความเสี่ยงของการดำเนินไปเป็น AMD ชนิดเปียกลดลงอีกในกลุ่มลูทีน/ซีแซนทีน
การติดตามระยะยาวของ AREDS2 (2022, ข้อมูล 10 ปี) 10) :
ยืนยันว่าความเสี่ยงของการดำเนินไปเป็น AMD ชนิดเปียกลดลงอีกในระยะยาวในกลุ่มลูทีน/ซีแซนทีน
ไม่พบปัญหาด้านความปลอดภัยในระยะยาว
ลักษณะของการทดลองแต่ละรายการแสดงไว้ด้านล่าง
ชื่อการทดลอง กลุ่มตัวอย่าง ผลลัพธ์หลัก AREDS (2001) ผู้ป่วย AMD 3,640 ราย ลดความเสี่ยงการดำเนินของ AMD ประมาณ 25% ด้วยสูตร AREDS1) AREDS2 (2013) ผู้ป่วย AMD 4,203 ราย ยืนยันความไม่ด้อยกว่าเมื่อเปลี่ยนเป็นลูทีน/ซีแซนทีน2) AREDS2 ระยะยาว (2022) ผู้ป่วย AMD 4,203 ราย ประโยชน์ของกลุ่มลูทีนคงอยู่หลังติดตามผล 10 ปี10) DREAM (2018) ผู้ป่วยตาแห้ง 535 ราย ผลของโอเมก้า 3 ต่อการปรับปรุงอาการตาแห้ง : ไม่แตกต่างจากยาหลอก7)
ไม่พบผลการป้องกันต้อกระจก ของสูตร AREDS1) ในทางกลับกัน การศึกษาทางระบาดวิทยาหลายชิ้นแสดงความสัมพันธ์ผกผันระหว่างการบริโภคลูทีนและซีแซนทีนจากอาหารกับความเสี่ยงของต้อกระจก ชนิดนิวเคลียร์5) ซึ่งบ่งชี้ว่าการได้รับผ่านอาหารอาจช่วยลดความเสี่ยงในการเกิดต้อกระจก อย่างไรก็ตาม ยังไม่มีการทดลองแบบสุ่มที่มีกลุ่มควบคุมขนาดใหญ่ที่พิสูจน์ผลของการแทรกแซงในรูปแบบอาหารเสริม
การทบทวนของ Cochrane (Mathew 2012, 21 RCT) สรุปว่าไม่มีหลักฐานที่เชื่อถือได้ว่าการเสริมวิตามินต้านอนุมูลอิสระ (A, C, E) ลูทีน และซีแซนทีน ชะลอการเกิดหรือการดำเนินของต้อกระจก 6)
การทดลอง DREAM (2018) เป็น RCT ในผู้ป่วยตาแห้ง เรื้อรัง 535 ราย เปรียบเทียบประสิทธิภาพของกรดไขมันโอเมก้า 3 (EPA 2,000 มก. + DHA 1,000 มก./วัน เป็นเวลา 12 เดือน) กับยาหลอกน้ำมันมะกอก ไม่มีความแตกต่างอย่างมีนัยสำคัญระหว่างสองกลุ่มในผลลัพธ์หลัก (คะแนน OSDI)7) ส่งผลให้ประสิทธิภาพของอาหารเสริมโอเมก้า 3 ต่อตาแห้ง เป็นลบ แม้ว่าการวิเคราะห์อภิมาน (Giannaccare 2019) จะรายงานประสิทธิภาพบางอย่าง11) แต่อาหารเสริมโอเมก้า 3 ไม่รวมอยู่ในการรักษามาตรฐานสำหรับตาแห้ง เนื่องจากคุณภาพสูงของการทดลอง DREAM
กลุ่มเป้าหมาย : ผู้ป่วยที่ได้รับการวินิจฉัยว่าเป็น AMD ระดับปานกลางถึงรุนแรงในตาข้างเดียว (ประเภท AREDS 3 และ 4)2) ผลจำกัดใน AMD ระยะเริ่มต้น : ไม่แสดงผลในการยับยั้งการดำเนินโรคอย่างมีนัยสำคัญในประเภท AREDS 1 และ 2 (ดรูเซน ขนาดเล็ก) ควรระวังการใช้ผลิตภัณฑ์เสริมอาหารที่ไม่จำเป็นเนื่องจากอาจมีความเสี่ยงจากการได้รับเกินขนาดยืนยันสถานะการสูบบุหรี่ : สำหรับผู้สูบบุหรี่ ให้เลือกสูตร AREDS2 ที่ไม่มีเบตาแคโรทีน
ใบผักโขม (ผักใบเขียวเข้มที่อุดมด้วยลูทีนและซีแซนทีน) Nillerdk. Spinach leaves (1 kg, separated from stems). Wikimedia Commons. 2008. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Spinach_leaves.jpg. License: CC BY 3.0.
ใบผักโขมที่เอาก้านออก มีลูทีนประมาณ 12 มก./100 กรัม เป็นแหล่งลูทีนและซีแซนทีนที่เป็นตัวแทน สอดคล้องกับการได้รับจากอาหารจากผักใบเขียวเข้มที่อุดมด้วยลูทีน (ผักโขม คะน้า) ที่กล่าวถึงในหัวข้อ “4. การได้รับจริง”
ผักใบเขียวเข้มเป็นแหล่งลูทีนและซีแซนทีนที่ดีเยี่ยม4)
ผักโขม : ลูทีนประมาณ 12 มก./100 กรัม, ซีแซนทีนประมาณ 1.1 มก./100 กรัม4) คะน้า : ลูทีนประมาณ 22 มก./100 กรัม (ระดับสูงที่สุดในบรรดาอาหาร)4) บรอกโคลี : ลูทีนประมาณ 1.4 มก./100 กรัม4) ไข่แดง : มีการดูดซึมลูทีนและซีแซนทีนสูง (มากกว่าผัก 3-4 เท่า)4)
ปลา (เช่น ปลาแมคเคอเรล ปลาซาบะ ปลาซาร์ดีน) มีประโยชน์เป็นแหล่ง EPA/DHA หากรับประทานสัปดาห์ละ 2 ครั้งขึ้นไป8) และการศึกษาทางระบาดวิทยารายงานความสัมพันธ์ระหว่างการบริโภคปลากับความเสี่ยง AMD ที่ลดลง
ลูทีนและซีแซนทีนเป็นสารอาหารสำคัญต่อสุขภาพดวงตา
รับประทานผักใบเขียวเข้มทุกวัน : ตั้งเป้ารับลูทีน 6-10 มก. ต่อวันจากผักโขม คะน้า บรอกโคลี ฯลฯ
รับประทานร่วมกับน้ำมันเพื่อเพิ่มการดูดซึม : เนื่องจากลูทีนละลายในไขมัน การผัดด้วยน้ำมันมะกอกหรือรับประทานกับน้ำสลัดจะช่วยเพิ่มประสิทธิภาพการดูดซึม
รับประทานปลาอย่างน้อยสัปดาห์ละ 2 ครั้ง : เพื่อเสริม EPA/DHA แนะนำให้รับประทานปลาที่มีไขมันสูง (ปลาแมคเคอเรล ปลาซาบะ) เป็นประจำ
ควรปรึกษาจักษุแพทย์ก่อนรับประทานอาหารเสริม : ก่อนรับประทานอาหารเสริมลูทีน ควรตรวจสภาพจอประสาทตา เสื่อมตามอายุ (AMD ) กับจักษุแพทย์และปรึกษาว่าจำเป็นต้องรับประทานจริงหรือไม่
อาหารเสริมไม่ใช่ยา แต่จัดเป็นอาหาร ภายใต้ระบบอาหารแสดงหน้าที่ทางสุขภาพ (พ.ศ. 2558) ของสำนักงานคณะกรรมการคุ้มครองผู้บริโภค อนุญาตให้แสดงหน้าที่ทางสุขภาพได้โดยมีหลักฐานทางวิทยาศาสตร์บางประการ 12) แต่ไม่ผ่านการตรวจสอบประสิทธิภาพและความปลอดภัยโดยรัฐเช่นเดียวกับยา เมื่อเลือกผลิตภัณฑ์ที่เทียบเท่าสูตร AREDS2 ควรตรวจสอบปริมาณส่วนประกอบและระวังไม่ให้ได้รับมากเกินไป
Q
อาหารชนิดใดที่มีลูทีนสูง?
A
ผักโขม (ประมาณ 12 มก./100 ก.), คะน้า (ประมาณ 22 มก./100 ก.), บรอกโคลี และผักใบเขียวเข้มและเหลืองอื่นๆ เป็นแหล่งอาหารหลักของลูทีน 4) ไข่แดงแม้จะมีลูทีนไม่สูงเท่าผัก แต่มีประสิทธิภาพการดูดซึมสูงเนื่องจากละลายในไขมัน แนะนำให้รับประทานลูทีนจากอาหาร 6–10 มก./วัน การรับประทานผักใบเขียวเข้มและเหลืองทุกวันเป็นพื้นฐานของการได้รับลูทีนจากอาหาร
หากใช้อาหารเสริมไม่ถูกต้อง อาจก่อให้เกิดผลข้างเคียงและความเสี่ยง ควรระวังประเด็นต่อไปนี้
เบตาแคโรทีนและความเสี่ยงมะเร็งปอดในผู้สูบบุหรี่ :
การศึกษา ATBC (1994) ในชายสูบบุหรี่ 29,133 คน พบว่าการเสริมเบตาแคโรทีน (20 มก./วัน) เพิ่มอุบัติการณ์มะเร็งปอด 18% 13)
การศึกษา CARET ก็พบความเสี่ยงมะเร็งปอดเพิ่มขึ้นในผู้สูบบุหรี่และผู้สัมผัสแร่ใยหินเมื่อเสริมเบตาแคโรทีน
จากข้อค้นพบนี้ AREDS2 จึงแทนที่เบตาแคโรทีนด้วยลูทีน/ซีแซนทีน 2)
ห้ามใช้สูตร AREDS ที่มีเบตาแคโรทีนในผู้สูบบุหรี่หรือผู้ที่เคยสูบบุหรี่ (แม้จะเลิกแล้ว)
การได้รับสังกะสีมากเกินไป :
มีรายงานภาวะโลหิตจางจากการขาดทองแดงเมื่อใช้สังกะสีออกไซด์ 80 มก./วัน ในสูตร AREDS เป็นเวลานาน 1)
สูตร AREDS มีคอปเปอร์ออกไซด์ 2 มก. เพื่อป้องกันการขาดทองแดง แต่แนะนำให้ตรวจเลือดเป็นระยะเมื่อใช้ในระยะยาว
ปริมาณสังกะสีสูงสุดที่ยอมรับได้สำหรับผู้ใหญ่ทั่วไป (ข้อกำหนดอาหารอ้างอิงของญี่ปุ่น 2020): ผู้ชาย 45 มก./วัน, ผู้หญิง 35 มก./วัน
การรับประทานวิตามินอีในปริมาณสูง:
Schürk และคณะ (2010, การวิเคราะห์อภิมาน) ชี้ให้เห็นความสัมพันธ์ระหว่างการรับประทานวิตามินอีปริมาณสูงกับความเสี่ยงที่เพิ่มขึ้นของโรคหลอดเลือดสมองแตก14)
ควรระมัดระวังการใช้ในขนาดสูง (400 IU/วัน) เป็นเวลานาน
ปฏิกิริยากับยา:
วิตามินอีและกรดไขมันโอเมก้า 3 มีฤทธิ์ต้านการแข็งตัวของเลือด ควรระวังปฏิกิริยากับยาต้านการแข็งตัวของเลือด เช่น วาร์ฟาริน
ปรึกษาแพทย์เกี่ยวกับการหยุดรับประทานก่อนการผ่าตัด
อาหารเสริมสำหรับดวงตาไม่ได้ “มาจากธรรมชาติและปลอดภัย” เสมอไป โปรดสังเกตประเด็นต่อไปนี้
ผู้สูบบุหรี่ควรหลีกเลี่ยงเบตาแคโรทีน: เบตาแคโรทีนเพิ่มความเสี่ยงมะเร็งปอดในผู้สูบบุหรี่ หากคุณสูบบุหรี่หรือมีประวัติสูบบุหรี่ ให้เลือกสูตร AREDS2 ที่มีลูทีน/ซีแซนทีน13)
ปฏิบัติตามปริมาณสังกะสี: การใช้ซิงก์ออกไซด์ 80 มก./วัน เป็นเวลานานอาจทำให้เกิดโรคโลหิตจางจากการขาดทองแดง ตรวจสอบให้แน่ใจว่าผลิตภัณฑ์ที่เทียบเท่าสูตร AREDS มีคอปเปอร์ออกไซด์ 2 มก.1)
ปฏิกิริยากับยา: วิตามินอีและกรดไขมันโอเมก้า 3 มีฤทธิ์ทำให้เลือดบางลง ควรปรึกษาแพทย์หากคุณกำลังรับประทานวาร์ฟาริน
ผลจำกัดใน AMD ระยะเริ่มต้น: ยังไม่พบผลในการชะลอการดำเนินโรคอย่างมีนัยสำคัญในประเภท AREDS 1 และ 2 (มีดรูเซน ขนาดเล็กเท่านั้น) การใช้อาหารเสริมโดยไม่จำเป็นนำมาซึ่งความเสี่ยงจากการได้รับมากเกินไป
Q
อาหารเสริมสำหรับดวงตามีผลข้างเคียงหรือไม่?
A
เบตาแคโรทีนในสูตร AREDS เพิ่มความเสี่ยงมะเร็งปอดในผู้สูบบุหรี่ ดังนั้นจึงห้ามใช้ในผู้สูบบุหรี่และผู้ที่มีประวัติสูบบุหรี่13) สูตร AREDS2 เปลี่ยนเบตาแคโรทีนเป็นลูทีน/ซีแซนทีนเพื่อหลีกเลี่ยงความเสี่ยงนี้ นอกจากนี้ การใช้ซิงก์ออกไซด์ 80 มก./วัน เป็นเวลานานอาจทำให้เกิดโรคโลหิตจางจากการขาดทองแดง ดังนั้นสูตรจึงมีคอปเปอร์ออกไซด์ 2 มก.1) การรับประทานวิตามินอีในปริมาณสูงเป็นเวลานานมีความสัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของโรคหลอดเลือดสมองแตก14) จึงต้องระมัดระวัง
จอประสาทตา ส่วนกลาง (macula) เป็นบริเวณที่มีความเสี่ยงสูงต่อภาวะเครียดออกซิเดชัน ที่เกิดจากแสง โดยรังสีอัลตราไวโอเลตและแสงสีฟ้าสามารถก่อให้เกิดอนุมูลอิสระ (ROS) ภาวะเครียดออกซิเดชัน มีส่วนเกี่ยวข้องกับการเกิดและการดำเนินของโรคจอประสาทตา เสื่อมตามอายุ (AMD ) 3)
การสร้าง ROS : การเกิดออกซิเดชันจากแสงของ lipofuscin (ของเสีย) จากปฏิกิริยาแสงเป็นสาเหตุหลักของความเสียหายต่อ RPE การเกิด drusen : ความสามารถในการประมวลผลของ RPE ที่ลดลงทำให้เกิดการสะสมของไลโปโปรตีนและคอมพลีเมนต์ ในเมทริกซ์นอกเซลล์การดำเนินไปสู่ AMD ชนิด渗出 : ภาวะเครียดออกซิเดชัน และความเสียหายของ RPE กระตุ้นการทำงานของคอมพลีเมนต์ และสัญญาณ VEGF ทำให้เกิดการสร้างเส้นเลือดใหม่
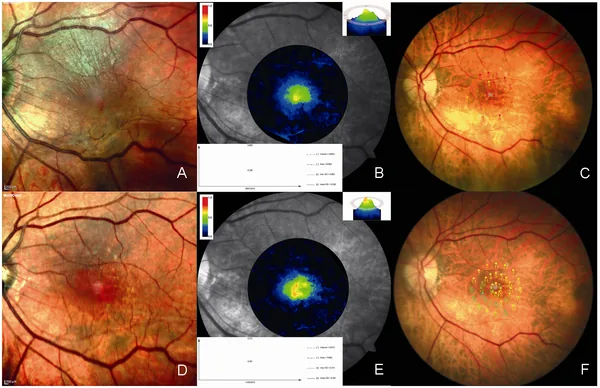
แผนที่สีเทียมของความหนาแน่นเชิงแสงของเม็ดสีจอประสาทตาส่วนกลาง (MPOD) (เปรียบเทียบก่อนและหลังการลอกเยื่อหุ้มชั้นในจอตา) Imanishi H, Takaoka M, Sonoda S, Oishi A, Yoshimura N. Multimodal imaging showing macular pigment optical density changes before and after
ERM peeling. PLOS ONE. 2018. Figure 1. DOI: 10.1371/journal.pone.0197034. License: CC BY 4.0.
แผนที่ที่แสดงความหนาแน่นเชิงแสงของเม็ดสีจอประสาทตา ส่วนกลาง (MPOD) ด้วยสีเทียม โดยแสดงการกระจายตัวของเม็ดสีที่มีความหนาแน่นสูง (โทนสีอบอุ่น) ที่ศูนย์กลางของ macula ซึ่งสอดคล้องกับหน้าที่ป้องกันแสงและต้านอนุมูลอิสระของ MPOD ที่เกิดจากลูทีนและซีแซนทีน ซึ่งกล่าวถึงในหัวข้อ “6. พยาธิสรีรวิทยาและกลไกต้านอนุมูลอิสระ”
ลูทีนและซีแซนทีนจะสะสมอย่างเฉพาะเจาะจงใน macula ก่อให้เกิดความหนาแน่นเชิงแสงของเม็ดสีจอประสาทตา ส่วนกลาง (MPOD) 3)
หน้าที่กรองแสง : ดูดซับแสงสีฟ้า (400-500 นาโนเมตร) อย่างเฉพาะเจาะจง และลดการเข้าถึงเซลล์รับแสง หน้าที่ต้านอนุมูลอิสระ : ทำหน้าที่เป็นตัวกำจัด ROS โดยตรงโดยการกำจัดออกซิเจน singlet และอนุมูล peroxylmeso-ซีแซนทีน : เม็ดสีจอประสาทตา ส่วนกลางชนิดที่สาม ซึ่งถูกเปลี่ยนจากลูทีนโดยเอนไซม์ภายในจอตา และพบในความเข้มข้นสูงสุดที่ศูนย์กลางของ macula 3)
สังกะสีทำหน้าที่เป็นโคแฟกเตอร์ที่จำเป็นในตำแหน่งเร่งของเอนไซม์ต้านอนุมูลอิสระ Cu/Zn-SOD (superoxide dismutase ที่มีทองแดงและสังกะสี) 1) SOD จะเปลี่ยนอนุมูล superoxide ซึ่งเป็น ROS ชนิดหนึ่ง ให้เป็นไฮโดรเจนเปอร์ออกไซด์ที่ไม่เป็นอันตราย นอกจากนี้ยังทำงานร่วมกับ catalase และ glutathione peroxidase เพื่อรักษาระบบป้องกันต้านอนุมูลอิสระโดยรวม RPE เป็นเนื้อเยื่อที่มีเมแทบอลิซึมสูงซึ่งย่อยสลายฟาโกโซมที่ถูกขับออกจากเซลล์รับแสง และการได้รับสังกะสีอย่างเพียงพอมีความสำคัญต่อการรักษาการทำงานปกติ
DHA (กรดโดโคซาเฮกซาอีโนอิก) เป็นกรดไขมันไม่อิ่มตัวเชิงซ้อนสายยาวโอเมก้า-3 ที่พบมากในเยื่อหุ้มส่วนนอกของเซลล์รับแสง จอประสาทตา ร่วมกับ EPA (กรดไอโคซาเพนตาอีโนอิก) เป็นสารตั้งต้นของสื่อกลางไขมันต้านการอักเสบ เช่น รีโซลวินและโปรเทกติน 7) สื่อกลางเหล่านี้ส่งเสริมการยุติการอักเสบ แต่ผลทางคลินิกต่อภาวะตาแห้ง ในการทดลองแบบสุ่มมีกลุ่มควบคุมถือว่าไม่เพียงพอ
เนื้อหาต่อไปนี้รวมถึงหัวข้อที่ยังอยู่ในระยะวิจัยหรืออยู่ระหว่างการพิจารณา รวมถึงเรื่องที่ยังไม่ได้รับการยอมรับให้รวมอยู่ในการรักษามาตรฐานในปัจจุบัน ดังนั้นจึงไม่แนะนำให้นำไปปฏิบัติโดยไม่ปรึกษาแพทย์
ในข้อมูลติดตามระยะยาว 10 ปีของ AREDS2 (รายงาน 28: Chew 2022) 10) กลุ่มลูทีน/ซีแซนทีนได้รับการยืนยันว่าช่วยลดความเสี่ยงของการลุกลามไปเป็น AMD ชนิด渗出ได้มากขึ้นในระยะยาว นอกจากนี้ไม่พบปัญหาด้านความปลอดภัยในระยะยาว และได้รับการสนับสนุนอีกครั้งถึงประโยชน์ของสูตรที่ไม่มีเบตาแคโรทีนสำหรับผู้สูบบุหรี่
การวัด MPOD กำลังถูกศึกษาเป็นตัวบ่งชี้ปริมาณแคโรทีนอยด์ในจอประสาทตา 3) วิธีการต่างๆ เช่น การกะพริบแบบต่างสี, สเปกโทรสโกปีรามานแบบเรโซแนนซ์ และการเรืองแสงอัตโนมัติของจอตา กำลังถูกประเมินเป็นตัวบ่งชี้วัตถุประสงค์ของผลของอาหารเสริม
กำลังศึกษาความเป็นไปได้ที่ผลของสูตร AREDS อาจแตกต่างกันตามความหลากหลายของยีนที่ไวต่อ AMD (CF H Y402H และ ARMS 2 A69S) 15) ผู้ที่มีความหลากหลายของ CF H ถูกเสนอว่ามีการตอบสนองต่อสังกะสีที่แตกต่างกัน 15) และในอนาคตอาจเป็นไปได้ที่จะปรับเปลี่ยนใบสั่งอาหารเสริมตามโปรไฟล์ทางพันธุกรรม
งานวิจัยพื้นฐานกำลังสะสมที่แสดงว่าองค์ประกอบของจุลินทรีย์ในลำไส้มีผลต่อประสิทธิภาพการดูดซึมและความเข้มข้นในเลือดของลูทีนและซีแซนทีน เป็นที่ทราบกันว่าแม้จะได้รับอาหารหรืออาหารเสริมในปริมาณเท่ากัน ความเข้มข้นของลูทีนในเลือดระหว่างบุคคลมีความแตกต่างกันมาก และกำลังมีการสำรวจการเพิ่มประสิทธิภาพการดูดซึมโดยการรวมกับการปรับปรุงสภาพแวดล้อมในลำไส้ (เช่น โปรไบโอติก)
แม้ว่าการทดลอง DREAM จะปฏิเสธผลของโอเมก้า-3 7) แต่การวิจัยเกี่ยวกับความสัมพันธ์ระหว่างรูปแบบการรับประทานอาหารโดยรวม (เช่น อาหารเมดิเตอร์เรเนียน) และความเสี่ยงต่อภาวะตาแห้ง กำลังดำเนินไป 11) บทบาทของสารอาหารอื่นๆ เช่น โพลีฟีนอลและวิตามินดีต่อภาวะตาแห้ง ก็กำลังถูกพิจารณา และกำลังมีการทดลองแบบสุ่มมีกลุ่มควบคุมใหม่ๆ
Age-Related Eye Disease Study Research Group. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no. 8. Arch Ophthalmol. 2001;119(10):1417-1436.
Age-Related Eye Disease Study 2 Research Group. Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013;309(19):2005-2015.
Bernstein PS, Li B, Vachali PP, et al. Lutein, zeaxanthin, and meso-zeaxanthin: the basic and clinical science underlying carotenoid-based nutritional interventions against ocular disease. Prog Retin Eye Res. 2016;50:34-66.
Perry A, Rasmussen H, Johnson EJ. Xanthophyll (lutein, zeaxanthin) content in fruits, vegetables and corn and egg products. J Food Compos Anal. 2009;22(1):9-15.
Christen WG, Liu S, Glynn RJ, et al. Dietary carotenoids, vitamins C and E, and risk of cataract in women: a prospective study. Arch Ophthalmol. 2008;126(1):102-109.
Mathew MC, Ervin AM, Tao J, et al. Antioxidant vitamin supplementation for preventing and slowing the progression of age-related cataract. Cochrane Database Syst Rev. 2012;(6):CD004567.
Dry Eye Assessment and Management Study Research Group. n-3 Fatty acid supplementation for the treatment of dry eye disease. N Engl J Med. 2018;378(18):1681-1690.
SanGiovanni JP, Chew EY, Clemons TE, et al. The relationship of dietary lipid intake and age-related macular degeneration in a case-control study: AREDS report no. 20. Arch Ophthalmol. 2007;125(5):671-679.
Kalt W, Hanneken A, Milbury P, et al. Recent research on polyphenolics in vision and eye health. J Agric Food Chem. 2010;58(7):4001-4007.
Chew EY, Clemons TE, Agrón E, et al. Long-term outcomes of adding lutein/zeaxanthin and ω-3 fatty acids to the AREDS supplements on age-related macular degeneration progression: AREDS2 report 28. JAMA Ophthalmol. 2022;140(7):692-698.
Giannaccare G, Pellegrini M, Sebastiani S, et al. Efficacy of omega-3 fatty acid supplementation for treatment of dry eye disease: a meta-analysis of randomized clinical trials. Cornea. 2019;38(5):565-573.
消費者庁. 機能性表示食品制度の概要. 2015.
Alpha-Tocopherol, Beta Carotene Cancer Prevention Study Group. The effect of vitamin E and beta carotene on the incidence of lung cancer and other cancers in male smokers. N Engl J Med. 1994;330(15):1029-1035.
Schürks M, Glynn RJ, Rist PM, et al. Effects of vitamin E on stroke subtypes: meta-analysis of randomised controlled trials. BMJ. 2010;341:c5702.
Seddon JM, Reynolds R, Yu Y, et al. Risk models for progression to advanced age-related macular degeneration using demographic, environmental, genetic, and ocular factors. Ophthalmology. 2011;118(11):2203-2211.