การสูบบุหรี่ (บุหรี่) เป็นปัจจัยเสี่ยงที่ได้รับการยืนยันสำหรับโรคตาหลายชนิด และมีความสัมพันธ์ที่พิสูจน์แล้วกับจอประสาทตา เสื่อมตามอายุ (AMD ), ต้อกระจก , ตาแห้ง , จอประสาทตาเสื่อมจากเบาหวาน , โรคตาจากต่อมไทรอยด์ (TED) และโรคเส้นประสาทตา ฝ่อจากพันธุกรรมลีเบอร์ (LHON )
อัตราส่วนออดส์ (OR) ของการเกิด AMD ในผู้ที่สูบบุหรี่ปัจจุบันอยู่ที่ 2.0–4.0 (การวิเคราะห์อภิมาน) 1) และถือเป็นปัจจัยเสี่ยงที่ปรับเปลี่ยนได้ที่สำคัญที่สุดสำหรับ AMD
ความเสี่ยงของต้อกระจก ชนิดนิวเคลียสเพิ่มขึ้นเป็น OR ประมาณ 2.0 ในผู้สูบบุหรี่ที่มีประวัติสูบมากกว่า 20 ซอง-ปี 2) และสาเหตุหลักคือการ变性ของโปรตีนเลนส์ตาเนื่องจากไซยาไนด์
การสูบบุหรี่เป็นปัจจัยสิ่งแวดล้อมที่แข็งแกร่งที่สุดที่เพิ่มความเสี่ยงของโรคตาจากต่อมไทรอยด์ (TED) ในผู้ป่วยโรคเกรฟส์ประมาณ 7.7 เท่า 8)
การสูบบุหรี่มือสอง (ควันข้างเคียง) อาจมีส่วนทำให้เกิดโรคภูมิแพ้และการอักเสบของผิวตา 4) งานวิจัยเกี่ยวกับผลของบุหรี่ไฟฟ้าต่อตาก็กำลังสะสมมากขึ้น 12)
การเลิกบุหรี่ช่วยลดความเสี่ยงของ AMD ลงอย่างมีนัยสำคัญในช่วง 10–20 ปี แต่การฟื้นตัวเต็มที่สู่ระดับของผู้ไม่สูบบุหรี่เป็นเรื่องยาก 3)
ในคลินิกจักษุ ควรสอบถามประวัติการสูบบุหรี่ (ซอง-ปี) ทุกครั้ง และให้คำแนะนำในการเลิกบุหรี่อย่างจริงจัง
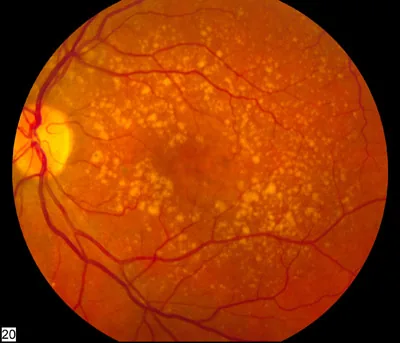
ภาพถ่ายจอประสาทตาของจอประสาทตาเสื่อมตามอายุระดับปานกลาง (ดรูเซนจุดภาพชัด) National Eye Institute, National Institutes of Health. Intermediate age-related macular degeneration fundus photograph. Reference #EDA2. Public Domain. Source ID: NIH-NEI-EDA2.
ภาพถ่ายจอประสาทตา ข้างขวาแสดงการสะสมของดรูเซน ชนิดนิ่มสีเหลืองอ่อนอย่างกว้างขวางที่จุดภาพชัด ซึ่งเป็นลักษณะของจอประสาทตา เสื่อมตามอายุระดับปานกลาง ภาพจอประสาทตา ทั่วไปของ AMD นี้สอดคล้องกับหัวข้อ “1. ความสัมพันธ์ระหว่างการสูบบุหรี่และโรคตา” ซึ่งการสูบบุหรี่เป็นปัจจัยเสี่ยงที่ใหญ่ที่สุด
การสูบบุหรี่ (บุหรี่) เป็นปัจจัยเสี่ยงที่ได้รับการยืนยันสำหรับโรคตาหลายชนิด ความสัมพันธ์กับจอประสาทตา เสื่อมตามอายุ (AMD ), ต้อกระจก , ตาแห้ง , จอประสาทตาเสื่อมจากเบาหวาน , โรคตาจากต่อมไทรอยด์ และโรคเส้นประสาทตา ฝ่อจากพันธุกรรมลีเบอร์ได้รับการพิสูจน์ทางวิทยาศาสตร์แล้ว
ควันบุหรี่มีสารเคมีมากกว่า 4,000 ชนิด โดยไซยาไนด์ แคดเมียม นิโคติน และอนุมูลอิสระในควันบุหรี่ก่อให้เกิดความเสียหายต่อเนื้อเยื่อตาหลายประการ อัตราส่วนออดส์ของการเกิดจอประสาทตา เสื่อมตามอายุ (AMD ) ในผู้ที่สูบบุหรี่ปัจจุบันอยู่ที่ 2.0–4.0 (การทบทวนวรรณกรรมอย่างเป็นระบบและการวิเคราะห์อภิมาน) 1) และถือเป็นปัจจัยเสี่ยงที่ปรับเปลี่ยนได้ที่รุนแรงที่สุดสำหรับ AMD สำหรับต้อกระจก นิวเคลียร์ การสูบบุหรี่ตั้งแต่ 20 แพ็ค-ปีขึ้นไปจะเพิ่มอัตราส่วนออดส์เป็นประมาณ 2.0 2)
มีความสัมพันธ์แบบขนาด-การตอบสนองที่ชัดเจนระหว่างปริมาณการสูบบุหรี่สะสม (แพ็ค-ปี = จำนวนบุหรี่ที่สูบต่อวัน ÷ 20 × จำนวนปีที่สูบ) กับความเสี่ยงของโรคตา 1) หลังจากเลิกสูบบุหรี่ ความเสี่ยงจะค่อยๆ ลดลง แต่อาจใช้เวลามากกว่า 20 ปีจึงจะกลับมาอยู่ในระดับเดียวกับผู้ไม่สูบบุหรี่ 3) ดังนั้นการเลิกสูบบุหรี่ตั้งแต่เนิ่นๆ จึงให้ประโยชน์สูงสุด การได้รับควันบุหรี่มือสองสัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของโรคภูมิแพ้ในเด็กและวัยรุ่น 4)
การสูบบุหรี่เป็นปัจจัยเสี่ยงที่ปรับเปลี่ยนได้ที่สำคัญที่สุดสำหรับจอประสาทตา เสื่อมตามอายุ 1)
ความเสี่ยงของต้อกระจก นิวเคลียร์เพิ่มขึ้นโดยมี OR ประมาณ 2.0 ที่ 20 แพ็ค-ปีขึ้นไป 2)
หลังจากเลิกสูบบุหรี่ 20 ปี ความเสี่ยงลดลงใกล้เคียงกับผู้ไม่สูบบุหรี่ 3)
การได้รับควันบุหรี่มือสองอาจเพิ่มความเสี่ยงของโรคภูมิแพ้ 4)
Q
การสูบบุหรี่ส่งผลต่อดวงตาอย่างไร?
A
การสูบบุหรี่เพิ่มความเสี่ยงของจอประสาทตา เสื่อมตามอายุ 2–4 เท่า และความเสี่ยงของต้อกระจก นิวเคลียร์ประมาณ 2 เท่า กลไกหลักคือสารออกซิแดนท์ ไซยาไนด์ และแคดเมียมในควันบุหรี่ทำลายเยื่อบุผิวรงควัตถุจอตาและโปรตีนในเลนส์ตา นอกจากนี้ยังเป็นปัจจัยที่ทำให้ตาแห้ง โรคตาจากต่อมไทรอยด์ (TED) และจอประสาทตาเสื่อมจากเบาหวาน แย่ลง โดยเฉพาะในผู้ป่วยโรคเกรฟส์ ความเสี่ยงของโรคตาสูงถึงประมาณ 7.7 เท่าของผู้ไม่สูบบุหรี่ การได้รับควันบุหรี่มือสองอาจเพิ่มความเสี่ยงของโรคตาได้เช่นกัน ดังนั้นการปรับปรุงสภาพแวดล้อมรอบข้างจึงสำคัญนอกเหนือจากตัวผู้ป่วยเอง
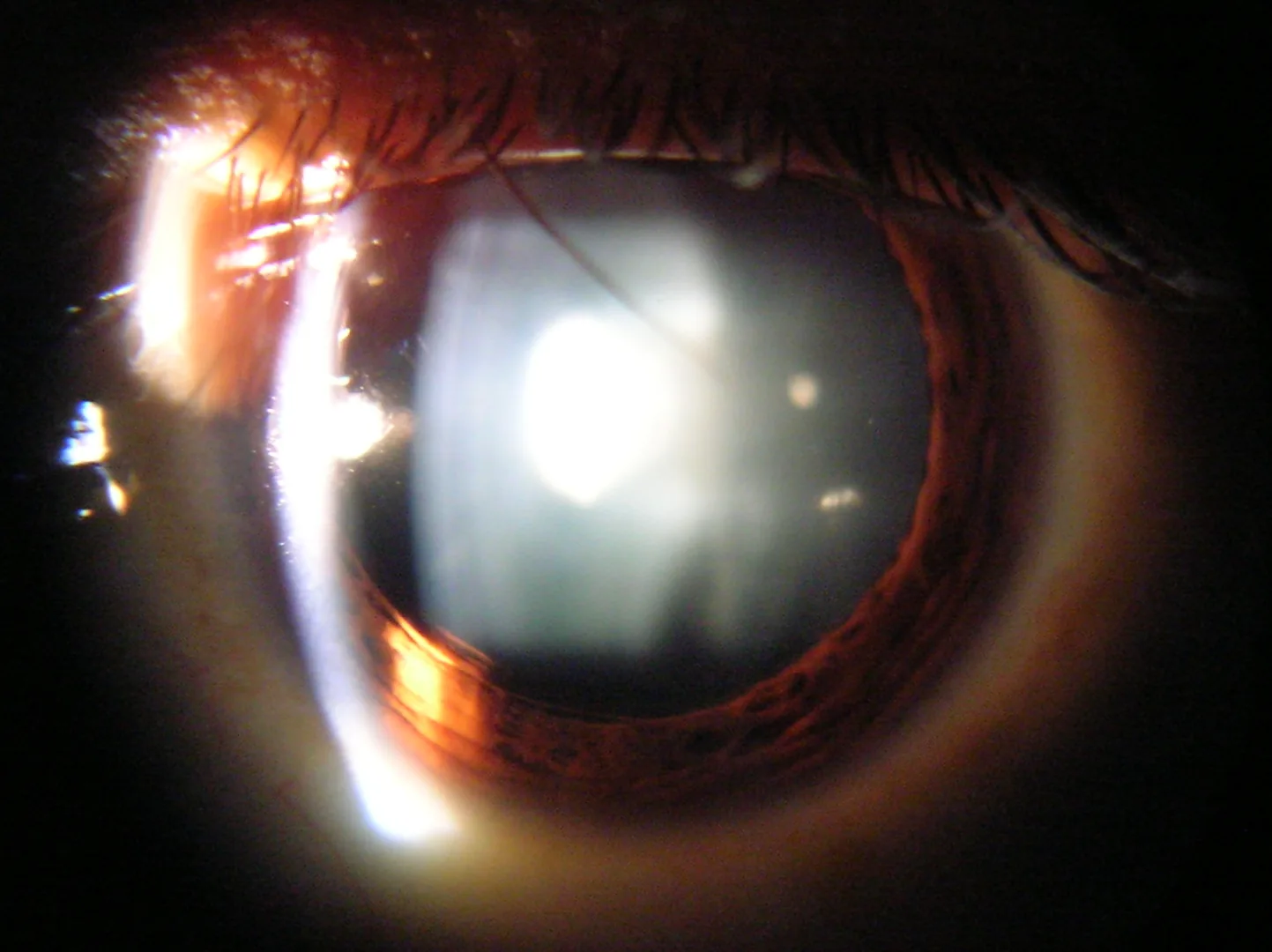
ภาพจากกล้องจุลทรรศน์กรีดแสงแสดงต้อกระจกนิวเคลียร์ (ความขุ่นของนิวเคลียสเลนส์) Rakesh Ahuja, MD. Slit lamp view of Cataract in Human Eye. Wikimedia Commons, 2005. License: CC BY-SA 3.0. Source ID: Wikimedia-Slit_lamp_view_of_Cataract_in_Human_Eye.
ภาพจากกล้องจุลทรรศน์กรีดแสงแสดงความขุ่นสีน้ำตาลเด่นชัดที่นิวเคลียสเลนส์ (
ต้อกระจก นิวเคลียร์) ซึ่งสอดคล้องกับ
ต้อกระจก นิวเคลียร์ที่เกิดจากไซยาไนด์เนื่องจากการสูบบุหรี่ที่กล่าวถึงในหัวข้อ “2. โรคตาที่เกี่ยวข้องกับการสูบบุหรี่”
โรคตาหลักที่เกี่ยวข้องกับการสูบบุหรี่สามารถจำแนกได้เป็น 6 ชนิด
จอประสาทตาเสื่อมตามอายุ (AMD)
ความเสี่ยงในการเกิดโรค : OR ของ AMD ในผู้สูบบุหรี่ปัจจุบัน 2.0–4.0 (การวิเคราะห์อภิมาน) 1)
ความสัมพันธ์ที่แน่นแฟ้นกับ AMD ชนิดมีน้ำซึม : โดยเฉพาะอย่างยิ่งสัมพันธ์อย่างมากกับ AMD ชนิดมีน้ำซึม (ชนิดเส้นเลือดใหม่) 5)
ความสัมพันธ์เชิงปริมาณ (dose-response) : ความสัมพันธ์เชิงบวกระหว่างปริมาณการสูบบุหรี่สะสม (pack-year) กับความเสี่ยง1)
ผลของการเลิกบุหรี่ : หลังจากเลิกบุหรี่ 20 ปี ความเสี่ยงลดลงใกล้เคียงกับผู้ไม่สูบบุหรี่3)
ต้อกระจก
ความเสี่ยงต้อกระจก ชนิดนิวเคลียร์ : ที่ 20 pack-year ขึ้นไป OR ประมาณ 2.02)
ยังมีรายงานความสัมพันธ์กับต้อกระจก ชนิดซับแคปซูลาร์ด้านหลัง 6)
กลไก : การทำลายพันธะไดซัลไฟด์ของโปรตีนในเลนส์โดยไซยาไนด์ทำให้เกิดต้อกระจก ชนิดนิวเคลียร์
ผลของการเลิกบุหรี่ : พบว่าความเสี่ยงลดลงหลังจากเลิกบุหรี่2)
ตาแห้ง
ผลเสียโดยตรง : ควันบุหรี่ทำลายชั้นน้ำตาโดยตรง7)
ความเสียหายต่อเซลล์ก๊อบเล็ต : ชั้นเมือกบางลงเนื่องจากความเสียหายต่อเซลล์ก๊อบเล็ตของเยื่อบุตา 7)
ในสภาพแวดล้อมที่ได้รับควันบุหรี่มือสอง ความเสี่ยงของโรคภูมิแพ้อาจเพิ่มขึ้น4)
โรคตาจากต่อมไทรอยด์ (TED)
ปัจจัยสิ่งแวดล้อมที่รุนแรงที่สุด : การสูบบุหรี่เป็นปัจจัยสิ่งแวดล้อมที่รุนแรงที่สุดในการเกิดและการทำให้รุนแรงขึ้นของโรคตาเกรฟส์ 8)
ความเสี่ยงในการเกิด : OR ของการเกิด TED ในผู้สูบบุหรี่ประมาณ 7.78)
หลังการรักษาด้วยไอโอดีนกัมมันตรังสี ความเสี่ยงของการทำให้ TED รุนแรงขึ้นเพิ่มขึ้นในผู้สูบบุหรี่9)
เบาหวานขึ้นจอตา :
การสูบบุหรี่เร่งให้เกิดความผิดปกติของหลอดเลือดขนาดเล็กเป็นกลไก 10)
เพิ่มความเสี่ยงของการลุกลามเป็นจอตางอกใหม่ในผู้ป่วยเบาหวาน
โรคเส้นประสาทตา ฝ่อจากพันธุกรรมแบบลีเบอร์ (LHON )
การสูบบุหรี่กระตุ้นให้เกิดโรคในผู้ที่มีการกลายพันธุ์ของดีเอ็นเอไมโตคอนเดรีย 11)
การสูบบุหรี่ทำให้การทำงานของไมโตคอนเดรียแย่ลง เพิ่มความเสี่ยงในการเกิดโรค 11)
Q
ความสัมพันธ์ระหว่างโรคตาจากต่อมไทรอยด์กับการสูบบุหรี่คืออะไร?
A
การสูบบุหรี่เป็นปัจจัยสิ่งแวดล้อมที่รุนแรงที่สุด เพิ่มความเสี่ยงของโรคตาจากต่อมไทรอยด์ (TED) ในผู้ป่วยเกรฟส์ประมาณ 7.7 เท่า การเลิกสูบบุหรี่ช่วยเพิ่มประสิทธิภาพการรักษา TED และความเสี่ยงที่โรคตาจะแย่ลงหลังการรักษาด้วยไอโอดีนกัมมันตรังสีก็สูงขึ้นในผู้สูบบุหรี่ การให้คำแนะนำให้เลิกสูบบุหรี่ก่อนเริ่มการรักษาโรคตา (สเตียรอยด์ การฉายรังสี การผ่าตัดลดเบ้าตา ) เป็นเงื่อนไขเบื้องต้นเพื่อเพิ่มประสิทธิภาพการรักษาสูงสุด
ผลกระทบของการสูบบุหรี่ต่อโรคตายังมีมากในระดับประชากร และเป็นความท้าทายด้านสาธารณสุข
โรค ความเสี่ยงที่เพิ่มขึ้น (OR) หมายเหตุ จอประสาทตา เสื่อมตามอายุ (โดยรวม)2.0–4.0 ผู้สูบบุหรี่ปัจจุบัน การวิเคราะห์อภิมาน 1) AMD ชนิด渗出 (Exudative AMD )สูงเป็นพิเศษ ความสัมพันธ์แบบขนาด-การตอบสนองกับ pack-year 5) ต้อกระจก ชนิดนิวเคลียร์ประมาณ 2.0 ≥20 pack-year 2) โรคเบ้าตา จากต่อมไทรอยด์ (TED) ประมาณ 7.7 ผู้ป่วยโรคเกรฟส์ 8) จอประสาทตาเสื่อมจากเบาหวาน เพิ่มขึ้น เร่งการเกิดโรคหลอดเลือดเล็ก 10) การเกิด LHON ปัจจัยกระตุ้น ผู้ที่มีการกลายพันธุ์ mtDNA 11)
ประมาณการว่าการสูบบุหรี่มีส่วนประมาณ 25-30% ของสัดส่วนความเสี่ยงที่เกิดจากประชากร (PAR) สำหรับโรค AMD 1)
ความเสี่ยงของการผ่าตัดต้อกระจก ในผู้สูบบุหรี่ได้รับการยืนยันว่าเพิ่มขึ้นอย่างมีนัยสำคัญในการศึกษา cohort ขนาดใหญ่ 6)
สภาพแวดล้อมที่ได้รับควันบุหรี่มือสองสัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของโรคภูมิแพ้ในเด็กและวัยรุ่น 4)
สำหรับบุหรี่ไฟฟ้า (รวมถึงบุหรี่แบบให้ความร้อน) งานวิจัยเกี่ยวกับผลกระทบต่อดวงตากำลังสะสมมากขึ้น 12) และยังคงรอการยืนยันหลักฐาน
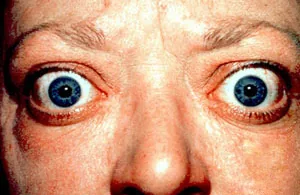
ตาโปนและการหดรั้งของเปลือกตาในโรคเกรฟส์ (โรคตาจากต่อมไทรอยด์) Jonathan Trobe, MD, University of Michigan Kellogg Eye Center. Proptosis and lid retraction from Graves’ Disease. Wikimedia Commons. License: CC BY 3.0. Source ID: Wikimedia-Proptosis_and_lid_retraction_from_Graves_Disease.
ภาพถ่ายภายนอกของโรคเกรฟส์ (โรคตาจากต่อมไทรอยด์ ) แสดงให้เห็นตาโปน (proptosis) ชัดเจนทั้งสองข้างและการหดรั้งของเปลือกตาบน สอดคล้องกับลักษณะทางคลินิกของโรคตาจากต่อมไทรอยด์ ซึ่งการสูบบุหรี่เพิ่มความเสี่ยงประมาณ 7.7 เท่า ดังที่กล่าวในหัวข้อ “4. การวินิจฉัยและการคัดกรอง”
ในคลินิกจักษุวิทยา การสอบถามประวัติการสูบบุหรี่อย่างจริงจังเป็นสิ่งสำคัญ โดยเฉพาะในการซักประวัติครั้งแรกสำหรับโรค AMD และโรคตาจากต่อมไทรอยด์ ควรถือเป็นรายการบังคับ
การหาปริมาณประวัติการสูบบุหรี่:
การคำนวณ pack-year: จำนวนบุหรี่ที่สูบต่อวัน ÷ 20 × จำนวนปีที่สูบบุหรี่
ยืนยันสถานะ: ปัจจุบันสูบ, เลิกสูบ (จำนวนปีที่เลิก), หรือไม่สูบ
ประเมินสภาพแวดล้อมที่ได้รับควันบุหรี่มือสอง (ที่ทำงานและที่บ้าน) ด้วย
การจัดการกลุ่มเสี่ยงสูงต่อโรค AMD :
ผู้ป่วยที่มีประวัติสูบบุหรี่ + ประวัติครอบครัว + AMD ข้างเดียว แนะนำให้ตรวจอวัยวะภายในตาเป็นประจำ 5)
การตรวจพบ drusen และการเปลี่ยนแปลงของ retinal pigment epithelium ตั้งแต่ระยะแรกด้วย OCT มีประสิทธิภาพ
ในกรณีที่เป็นตาเดียว ให้ลดระยะเวลาการติดตามตาอีกข้างลง
การดูแลผู้ป่วยโรคตาจากต่อมไทรอยด์ :
ต้องตรวจสอบสถานะการสูบบุหรี่ทุกครั้งเมื่อตรวจร่างกาย8)
การให้คำแนะนำให้เลิกบุหรี่เป็นเงื่อนไขเบื้องต้นก่อนเริ่มการรักษา
ในผู้สูบบุหรี่ที่ได้รับการรักษาด้วยไอโอดีนกัมมันตรังสี ต้องอธิบายล่วงหน้าอย่างเพียงพอถึงความเป็นไปได้ที่โรคตาจะแย่ลง9)
การดูแลผู้ป่วยต้อกระจก และตาแห้ง :
รวมประวัติการสูบบุหรี่ในการซักประวัติก่อนผ่าตัด
ในการซักประวัติผู้ป่วยตาแห้ง รุนแรง ให้ตรวจสอบประวัติการสูบบุหรี่และสภาพแวดล้อมที่ได้รับควันบุหรี่มือสอง7)
การเลิกบุหรี่เป็นมาตรการป้องกันที่สำคัญและได้รับการพิสูจน์แล้วมากที่สุดสำหรับโรคตา และจักษุแพทย์ก็มีบทบาทในการแทรกแซงอย่างจริงจัง
การลดความเสี่ยงของโรคต่างๆ หลังเลิกบุหรี่:
โรค ผลของการเลิกบุหรี่ หลักฐาน AMD ความเสี่ยงลดลงอย่างมีนัยสำคัญหลังเลิกบุหรี่ 10-20 ปี3) การศึกษาแบบไปข้างหน้า ต้อกระจก (นิวเคลียส)พบความเสี่ยงลดลงหลังเลิกสูบบุหรี่2) การวิเคราะห์อภิมาน โรคตาจากต่อมไทรอยด์ การเลิกสูบบุหรี่ช่วยเพิ่มประสิทธิภาพการรักษา TED8) การศึกษาแบบแทรกแซง จอประสาทตาเสื่อมจากเบาหวาน ช่วยยับยั้งการดำเนินของความผิดปกติของหลอดเลือด10) การศึกษาตามรุ่น
วิธี 5A (การใช้ในจักษุวิทยา) 13) :
ถาม : สอบถามประวัติการสูบบุหรี่ในผู้ป่วยทุกรายแนะนำ : บอกความเสี่ยงเฉพาะของโรคตาจากการสูบบุหรี่ประเมิน : ประเมินความตั้งใจเลิกบุหรี่ช่วยเหลือ : ส่งต่อเพื่อรับยาช่วยเลิกบุหรี่หรือคลินิกเลิกบุหรี่จัดเตรียม : นัดหมายติดตามผล
การสนับสนุนการเลิกบุหรี่ด้วยยา :
การบำบัดทดแทนนิโคติน (NRT): แผ่นแปะนิโคติน (7/14/21 มก.) และหมากฝรั่งนิโคติน13)
วาเรนิคลีน (Champix): ตัวกระตุ้นบางส่วนของตัวรับนิโคติน α4β2 การให้ยามาตรฐานเป็นเวลา 12 สัปดาห์13)
การประสานงานกับคลินิกเลิกบุหรี่: ใช้ประโยชน์จากโปรแกรมการรักษาเลิกบุหรี่ 12 สัปดาห์ (5 ครั้ง) ที่ครอบคลุมโดยประกัน14)
โปรดส่งข้อความต่อไปนี้ให้ผู้ป่วย
ข้อความถึงผู้ป่วย AMD หรือผู้ที่สงสัย : «หากคุณสูบบุหรี่วันละหนึ่งซอง ความเสี่ยงของจอประสาทตา เสื่อมตามอายุจะเพิ่มขึ้น 2 ถึง 4 เท่าเมื่อเทียบกับผู้ไม่สูบบุหรี่ การเลิกบุหรี่เป็นมาตรการป้องกันที่สำคัญที่สุด»
ข้อความถึงผู้ป่วยโรคตาจากต่อมไทรอยด์ : «หากผู้ป่วยโรคเกรฟส์ยังคงสูบบุหรี่ ความเสี่ยงในการเกิดโรคตาจะเพิ่มขึ้นมากกว่า 7 เท่า สามารถใช้ประกันสำหรับการรักษาเลิกบุหรี่ได้ ดังนั้นเราขอแนะนำให้ไปคลินิกเลิกบุหรี่»
สำหรับผู้ป่วยที่เลิกบุหรี่ได้ยาก : เขียนจดหมายส่งตัวไปคลินิกเลิกบุหรี่ และแจ้งว่าสามารถใช้แผ่นแปะนิโคตินและวาเรนิคลีนได้ หากการเลิกบุหรี่ทันทีโดยสมบูรณ์เป็นเรื่องยาก การเริ่มต้นด้วยการลดปริมาณการสูบบุหรี่ก็มีประโยชน์เช่นกัน
Q
การเลิกบุหรี่ช่วยลดความเสี่ยงของโรคตาหรือไม่?
A
การศึกษาแบบไปข้างหน้าแสดงให้เห็นว่าความเสี่ยงของ AMD ลดลงอย่างมีนัยสำคัญหลังจากเลิกบุหรี่ 10-20 ปี อย่างไรก็ตาม ความเสี่ยงไม่ได้กลับไปสู่ระดับของผู้ไม่สูบบุหรี่โดยสมบูรณ์ และยิ่งเลิกเร็วเท่าไร ผลก็ยิ่งมากขึ้นเท่านั้น การลดความเสี่ยงหลังเลิกบุหรี่ยังพบในต้อกระจก ชนิดนิวเคลียร์และโรคตาจากต่อมไทรอยด์ โดยเฉพาะอย่างยิ่งในระหว่างการรักษาโรคตาจากต่อมไทรอยด์ การเลิกบุหรี่ช่วยเพิ่มประสิทธิภาพของการรักษา จากมุมมองทางจักษุวิทยา การเลิกบุหรี่มีความสำคัญอย่างยิ่ง และควรสนับสนุนให้ใช้คลินิกเลิกบุหรี่ (ที่ครอบคลุมโดยประกัน) อย่างจริงจัง
กลไกหลักที่การสูบบุหรี่ทำลายเนื้อเยื่อตาแบ่งออกเป็นสี่ประเภท: ความเครียดออกซิเดชัน, ความเป็นพิษโดยตรง, ความผิดปกติของการควบคุมภูมิคุ้มกัน และความเสียหายของหลอดเลือด
ความเครียดออกซิเดชันและ AMD :
ประมาณว่าการสูดควันบุหรี่หนึ่งครั้งก่อให้เกิดอนุมูลอิสระประมาณ 10^15 ตัว15)
ในหนูที่ได้รับควันบุหรี่ มีรายงานความเสียหายของ DNA จากออกซิเดชันใน RPE การสูญเสียการบุ๋มฐาน การเพิ่มขึ้นของแวคิวโอล การหนาตัวของเยื่อบรูค และการตายแบบอะพอพโทซิส ของ RPE 15)
Nrf2 ควบคุมการตอบสนองต่อสารต้านอนุมูลอิสระ และการตอบสนองที่ลดลงกลายเป็นปัญหาในภาวะเครียดออกซิเดชัน ที่เกี่ยวข้องกับอายุและการสูบบุหรี่ 15)
ผลเสริมฤทธิ์ของความหลากหลายทางพันธุกรรมของยีนคอมพลีเมนต์ แฟกเตอร์ H (CF H) (Y402H) และการสูบบุหรี่เพิ่มความเสี่ยงของ AMD อย่างมีนัยสำคัญ 5)
ไซยาไนด์และต้อกระจก ชนิดนิวเคลียร์ :
ไซยาไนด์ในควันบุหรี่ทำลายพันธะไดซัลไฟด์ของโปรตีนเลนส์ (คริสตัลลิน)
เกิดการรวมตัวและการไม่ละลายของโปรตีน นำไปสู่ต้อกระจก ชนิดนิวเคลียร์
ความขุ่นของนิวเคลียสเพิ่มขึ้นอย่างมีนัยสำคัญในผู้สูบบุหรี่ที่มีประวัติ 20 pack-year ขึ้นไป 2)
นิโคตินและความผิดปกติของหลอดเลือด :
นิโคตินกระตุ้นระบบประสาทซิมพาเทติกทำให้เกิดการหดตัวของหลอดเลือด ลดการไหลเวียนเลือดในจอประสาทตา 10)
ในผู้ป่วยเบาหวาน โรคหลอดเลือดเล็กที่มีอยู่เดิมจะแย่ลงจากการสูบบุหรี่ 10)
ความผิดปกติของการควบคุมภูมิคุ้มกันและโรคตาต่อมไทรอยด์ (TED) :
ความผิดปกติของการควบคุมภูมิคุ้มกันจากการสูบบุหรี่ส่งเสริมการเพิ่มการผลิตแอนติบอดีต่อตัวรับ TSH (TRAb) 8)
การกระตุ้นไฟโบรบลาสต์ในเบ้าตา และการเพิ่มการผลิตกรดไฮยาลูโรนิกทำให้เนื้อเยื่อเบ้าตา หนาตัวและตาโปน 8)
ผลกระทบต่อชั้นฟิล์มน้ำตาและตาแห้ง :
สารเคมีอันตรายในควันบุหรี่ทำให้ชั้นไขมันของฟิล์มน้ำตาไม่เสถียร ทำให้เกิดตาแห้ง แบบระเหย 7)
ทำให้เซลล์กอบเล็ตของเยื่อบุตา ถูกทำลายและชั้นเมือกบางลง ส่งผลให้ความคงตัวของน้ำตาลดลง 7)
LHON และความผิดปกติของไมโทคอนเดรีย:
ในผู้ที่มีการกลายพันธุ์ของดีเอ็นเอไมโทคอนเดรีย (เช่น 11778G>A) การสูบบุหรี่จะทำให้ความผิดปกติของไมโทคอนเดรียที่มีอยู่แล้วแย่ลงและกลายเป็นปัจจัยกระตุ้นให้เกิดโรค 11)
เนื้อหาต่อไปนี้รวมถึงหัวข้อที่ยังอยู่ในขั้นตอนการวิจัยหรือยังเป็นที่ถกเถียง นำเสนอหลักฐานในปัจจุบันอย่างเป็นกลาง และไม่รับประกันประสิทธิผลของการแทรกแซงใดๆ
ผลกระทบของบุหรี่ไฟฟ้าและยาสูบแบบให้ความร้อนต่อดวงตา:
การศึกษาทางระบาดวิทยาที่ประเมินผลกระทบของบุหรี่ไฟฟ้าและยาสูบแบบให้ความร้อน (เช่น IQOS) ต่อดวงตากำลังสะสมมากขึ้น 12)
มีความกังวลเกี่ยวกับผลกระทบของนิโคตินและสารประกอบอินทรีย์ระเหยง่ายต่อผิวตาผ่านทางเดินต่างๆ
การประเมินความเสี่ยงเมื่อเทียบกับบุหรี่ทั่วไปยังไม่เป็นที่แน่ชัดในขณะนี้ จึงจำเป็นต้องมีท่าทีที่ระมัดระวัง
ปฏิสัมพันธ์ระหว่างยีนและสิ่งแวดล้อม:
ปฏิสัมพันธ์ระหว่างความหลากหลายทางพันธุกรรมของ CF H (Y402H) และ ARMS 2 (A69S) กับการสูบบุหรี่จะเพิ่มความเสี่ยงของ AMD มากขึ้น 5)
การวิจัยเกี่ยวกับการแทรกแซงการเลิกบุหรี่แบบเฉพาะบุคคลสำหรับผู้ที่มีความเสี่ยงทางพันธุกรรมสูงกำลังดำเนินไป
การแทรกแซงการเลิกบุหรี่และการยับยั้งการดำเนินของ AMD :
การศึกษาตามรุ่นไปข้างหน้ากำลังดำเนินการเพื่อตรวจสอบผลของการเลิกบุหรี่ในการยับยั้งการเกิดและการดำเนินของ AMD
กำลังมีการประเมินผลร่วมของการเลิกบุหรี่และอาหารเสริม AREDS (วิตามินซี 500 มก., วิตามินอี 400 IU, สังกะสี 80 มก., ทองแดง 2 มก., ลูทีน 10 มก., ซีแซนทีน 2 มก.)
ควันบุหรี่มือสาม (thirdhand smoke):
กำลังให้ความสนใจต่อผลกระทบของสารเคมีตกค้าง (ควันบุหรี่มือสาม) ที่ติดอยู่ตามผนัง เสื้อผ้า และเฟอร์นิเจอร์ต่อผิวตา
ความสัมพันธ์กับความผิดปกติของผิวตาในเด็กและครอบครัวของผู้สูบบุหรี่เป็นหัวข้อวิจัยในอนาคต
การประมาณสถานะการสูบบุหรี่จากภาพถ่ายจอประสาทตา ด้วย AI:
มีการรายงานการศึกษาโดยใช้แบบจำลองการเรียนรู้ของเครื่องเพื่อประมาณสถานะการสูบบุหรี่จากภาพถ่ายจอประสาทตา และคาดว่าจะนำไปประยุกต์ใช้ในการตรวจคัดกรองทางจักษุวิทยา
Chakravarthy U, Wong TY, Fletcher A, et al. Clinical risk factors for age-related macular degeneration: a systematic review and meta-analysis. BMC Ophthalmol. 2010;10:31.
Ye J, He J, Wang C, et al. Smoking and risk of age-related cataract: a meta-analysis. Invest Ophthalmol Vis Sci. 2012;53(7):3885-3895.
Khan JC, Thurlby DA, Shahid H, et al. Smoking and age related macular degeneration: the number of pack years of cigarette smoking is a major determinant of risk for both geographic atrophy and choroidal neovascularisation. Br J Ophthalmol. 2006;90(1):75-80.
Saulyte J, Regueira C, Montes-Martinez A, Khudyakov P, Takkouche B. Active or passive exposure to tobacco smoking and allergic rhinitis, allergic dermatitis, and food allergy in adults and children: a systematic review and meta-analysis. PLoS Med. 2014;11(3):e1001611. PMCI D: PMC3949681. doi:10.1371/journal.pmed.1001611.
Seddon JM, George S, Rosner B. Cigarette smoking, fish consumption, omega-3 fatty acid intake, and associations with age-related macular degeneration: the US Twin Study of Age-Related Macular Degeneration. Arch Ophthalmol. 2006;124(7):995-1001.
Kelly SP, Thornton J, Edwards R, et al. Smoking and cataract: review of causal association. J Cataract Refract Surg. 2005;31(12):2395-2404.
Moss SE, Klein R, Klein BE. Prevalence of and risk factors for dry eye syndrome. Arch Ophthalmol. 2000;118(9):1264-1268.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Bartalena L, Marcocci C, Tanda ML, et al. Cigarette smoking and treatment outcomes in Graves ophthalmopathy. Ann Intern Med. 1998;129(8):632-635.
Cai J, Boulton M. The pathogenesis of diabetic retinopathy: old concepts and new questions. Eye (Lond). 2002;16(3):242-260.
Kirkman MA, Yu-Wai-Man P, Korsten A, et al. Gene-environment interactions in Leber hereditary optic neuropathy. Brain. 2009;132(Pt 9):2317-2326.
Mehra D, Galor A. Digital screen use and dry eye: a review. Asia Pac J Ophthalmol. 2020;9(6):491-497.
Fiore MC, Jaén CR, Baker TB, et al. Treating tobacco use and dependence: 2008 update. Clinical practice guideline. Rockville, MD: U.S. Department of Health and Human Services; 2008.
JCS Joint Working Group. Guidelines for smoking cessation (JCS 2010): digest version. Circ J. 2012;76(4):1024-1043.
Cano M, Thimmalappula R, Fujihara M, et al. Cigarette smoking, oxidative stress, the anti-oxidant response through Nrf2 signaling, and age-related macular degeneration. Vision Res. 2010;50(7):652-664.