叶黄素和玉米黄质

补充剂与眼病(叶黄素、玉米黄质等)(Supplements and Eye Health Lutein Zeaxanthin)
一目了然的要点
Section titled “一目了然的要点”1. 补充剂与眼病的关系
Section titled “1. 补充剂与眼病的关系”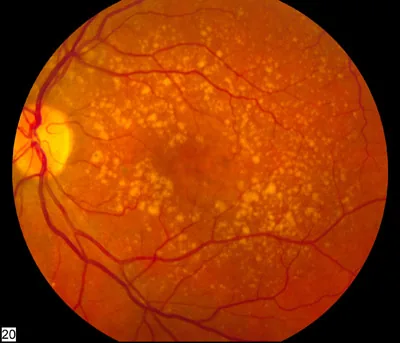
以预防和抑制眼病进展为目的,研究营养素和补充剂科学依据的领域正受到关注。特别是针对年龄相关性黄斑变性(AMD)、白内障和干眼症这三种疾病,已开展了大规模随机对照试验(RCT)。
最大的证据来源是美国国立眼科研究所(NEI)主导的AREDS(年龄相关性眼病研究)。AREDS于1992年至2001年进行,是一项涉及3,640名参与者的大规模RCT1),检验了结合维生素C 500 mg、维生素E 400 IU、β-胡萝卜素15 mg和氧化锌80 mg的“AREDS配方”。结果显示,中度及以上AMD(AREDS分类3和4)患者的AMD进展风险降低了约25%1)。
在2006年至2012年进行的AREDS2研究(4,203例)中2),验证了用叶黄素10 mg + 玉米黄质2 mg/日替代β-胡萝卜素的新处方的有效性和安全性。替代为叶黄素和玉米黄质显示出与β-胡萝卜素相当的AMD进展抑制效果2),同时避免了与β-胡萝卜素相关的吸烟者肺癌风险增加,因此成为目前的标准处方。
重要的是,AREDS/AREDS2处方针对的是中度至重度AMD患者的进展抑制,尚未确立对无AMD的一般人群的发病预防效果。补充剂是眼科管理的辅助手段,与定期眼科检查的早期发现和早期治疗相结合是基础。
2. 主要补充剂成分与眼病
Section titled “2. 主要补充剂成分与眼病”与眼病相关的主要补充剂成分大致可分为五类。
维生素C和E
锌
作用:作为抗氧化酶(Cu/Zn-SOD、过氧化氢酶等)的辅助因子,支持视网膜色素上皮的代谢1)。
AREDS配方剂量:氧化锌 80 mg/天(同时服用氧化铜 2 mg/天以预防铜缺乏性贫血)1)。
AREDS2中的变更:曾考虑减量至25 mg,但与80 mg组相比无显著差异2)。
Omega-3脂肪酸(EPA/DHA)
花青素(越橘等)
Section titled “花青素(越橘等)”蓝莓和越橘中含有的花青素在基础研究水平上已被报道具有改善暗适应和视网膜血流的作用。然而,RCT的有效性证据有限9),目前临床实践中尚不推荐使用。
AREDS与AREDS2配方内容比较
Section titled “AREDS与AREDS2配方内容比较”各配方成分的剂量如下所示。
| 成分 | AREDS配方 | AREDS2配方 |
|---|---|---|
| 维生素C | 500 mg/天 | 500 mg/天 |
| 维生素E | 400 IU/天 | 400 IU/天 |
| β-胡萝卜素 | 15 mg/天 | 排除(替换为叶黄素/玉米黄质) |
| 叶黄素 | — | 10 mg/天 |
| 玉米黄质 | — | 2 mg/天 |
| 氧化锌 | 80 mg/天 | 80 mg/天(25 mg也在考虑中) |
| 氧化铜 | 2毫克/天 | 2毫克/天 |
3. 证据详情
Section titled “3. 证据详情”AREDS研究概述
Section titled “AREDS研究概述”AREDS和AREDS2是眼科补充剂研究的最高级别证据来源。
AREDS(2001年报告)1):
- 对象:3,640例AREDS类别3(晚期单侧AMD或许多中型玻璃膜疣)或类别4(晚期双侧AMD)患者
- 干预:维生素C 500毫克+维生素E 400国际单位+β-胡萝卜素15毫克+氧化锌80毫克/天
- 结果:AMD进展风险降低约25%(相对风险0.75)。高风险组获益最大。
AREDS2(2013年报告)2):
- 对象:4,203例(AMD患者)
- 主要变更:用叶黄素10毫克+玉米黄质2毫克/天替代β-胡萝卜素
- 结果:替换后仍显示在延缓AMD进展方面非劣效。在有吸烟史的患者中,叶黄素/玉米黄质组渗出型AMD进展风险进一步降低。
AREDS2长期随访(2022年,10年数据)10):
- 叶黄素/玉米黄质组渗出型AMD进展风险长期进一步降低得到确认。
- 未发现长期安全性问题。
主要临床试验总结
Section titled “主要临床试验总结”各试验的特点如下所示。
| 试验名称 | 对象 | 主要结果 |
|---|---|---|
| AREDS(2001) | AMD 3,640例 | AREDS配方使AMD进展风险降低约25%1) |
| AREDS2(2013) | AMD 4,203例 | 叶黄素/玉米黄质替换确认非劣效2) |
| AREDS2长期研究(2022) | AMD 4,203例 | 10年随访显示叶黄素组持续获益10) |
| DREAM研究(2018) | 干眼 535例 | Omega-3改善干眼效果:与安慰剂无差异7) |
与白内障的关系
Section titled “与白内障的关系”AREDS配方未被证实能预防白内障1)。另一方面,多项流行病学研究显示,膳食中叶黄素和玉米黄质的摄入量与核性白内障风险呈负相关5),提示通过饮食摄入可能降低白内障发病风险。然而,尚无大规模随机对照试验证明补充剂的干预效果。
一项Cochrane系统评价(Mathew 2012,21项随机对照试验)得出结论,没有高质量证据表明补充抗氧化维生素(A、C、E)、叶黄素和玉米黄质能延缓白内障的发生或进展6)。
与干眼的关系
Section titled “与干眼的关系”DREAM试验(2018年)是一项随机对照试验,比较了Omega-3脂肪酸(EPA 2,000 mg + DHA 1,000 mg/天,持续12个月)与橄榄油安慰剂对535例慢性干眼患者的疗效。主要终点(OSDI评分)两组间无显著差异7),Omega-3补充剂对干眼的疗效为阴性。尽管一项荟萃分析(Giannaccare 2019)报告了部分疗效11),但由于DREAM试验的高质量,Omega-3补充剂未被纳入干眼的标准治疗。
4. 实际摄入
Section titled “4. 实际摄入”AREDS2配方的适应证
Section titled “AREDS2配方的适应证”- 目标人群:单眼中度至重度AMD(AREDS分类3和4)患者2)
- 对早期AMD效果有限:AREDS分类1和2(小玻璃膜疣)未显示显著的进展抑制效果。不必要的补充剂使用会带来过量摄入风险,因此需谨慎。
- 确认吸烟状态:对于吸烟者,选择不含β-胡萝卜素的AREDS2配方。

深绿色蔬菜是叶黄素和玉米黄质的优质来源4)。
- 菠菜:每100克含约12毫克叶黄素、约1.1毫克玉米黄质4)
- 羽衣甘蓝:每100克含约22毫克叶黄素(食物中最高水平)4)
- 西兰花:每100克含约1.4毫克叶黄素4)
- 蛋黄:叶黄素和玉米黄质的生物利用度高(是蔬菜的3至4倍)4)
鱼类(鲭鱼、秋刀鱼、沙丁鱼等)每周食用两次或以上可作为EPA/DHA的来源8),流行病学研究表明鱼类摄入量与AMD风险降低相关。
功能性标示食品制度
Section titled “功能性标示食品制度”补充剂不属于药品,而是归类为食品。根据日本消费者厅的功能性标示食品制度(2015年),允许基于一定科学证据标示功能性12),但并未像药品那样经过国家关于有效性和安全性的审查。在选择相当于AREDS2配方的产品时,请确认成分含量,并注意避免过量摄入。
菠菜(约12毫克/100克)、羽衣甘蓝(约22毫克/100克)、西兰花等黄绿色蔬菜是叶黄素的主要食物来源4)。蛋黄中叶黄素含量虽不如蔬菜高,但由于叶黄素是脂溶性的,吸收效率较高。建议每天从饮食中摄入6-10毫克的叶黄素。每天积极食用黄绿色蔬菜是从饮食中获取叶黄素的基础。
5. 注意事项与过量摄入风险
Section titled “5. 注意事项与过量摄入风险”如果补充剂使用不当,可能会带来副作用和风险。需要注意以下几点。
β-胡萝卜素与吸烟者的肺癌风险:
- ATBC研究(1994年)显示,对29,133名男性吸烟者补充β-胡萝卜素(20毫克/天)使肺癌发病率增加18%13)
- CARET研究也显示,在吸烟者和石棉暴露者中补充β-胡萝卜素会增加肺癌风险
- 基于这些发现,AREDS2用叶黄素/玉米黄质替代了β-胡萝卜素2)
- 吸烟者或曾有吸烟史(即使已戒烟)的人,不应使用含β-胡萝卜素的AREDS配方
过量摄入锌:
- 长期使用含氧化锌80毫克/天的AREDS配方时,有铜缺乏性贫血的报道1)
- AREDS配方中含有2毫克氧化铜以预防铜缺乏,但长期服用时建议定期进行血液检查。
- 一般成人锌的可耐受最高摄入量(日本2020年膳食摄入标准):男性45毫克/天,女性35毫克/天
大量摄入维生素E:
- Schürk等人(2010年,荟萃分析)提示大量摄入维生素E与出血性卒中风险增加相关14)
- 高剂量(400国际单位/天)长期使用需谨慎
药物相互作用:
- 维生素E和ω-3脂肪酸具有抗凝作用,需注意与华法林等抗凝药的相互作用
- 手术前应咨询医生是否停用
AREDS配方中的β-胡萝卜素会增加吸烟者患肺癌的风险,因此对吸烟者或有吸烟史者禁忌13)。AREDS2配方用叶黄素/玉米黄质替代β-胡萝卜素以避免此风险。此外,长期使用80毫克/天的氧化锌可能导致铜缺乏性贫血,因此配方中始终包含2毫克氧化铜1)。高剂量长期摄入维生素E与出血性卒中风险增加有关14),需谨慎。
6. 病理生理学与抗氧化机制
Section titled “6. 病理生理学与抗氧化机制”氧化应激与眼病
Section titled “氧化应激与眼病”黄斑是光诱导氧化应激的高风险区域,紫外线和蓝光可产生活性氧(ROS)。氧化应激参与AMD的发生和进展3)。
- ROS产生:光反应导致的脂褐素(废物)光氧化是RPE损伤的主要原因
- 玻璃膜疣形成:RPE处理能力下降导致脂蛋白和补体沉积在细胞外基质中
- 进展为渗出型AMD:氧化应激和RPE损伤诱导补体激活和VEGF信号,导致新生血管形成
黄斑色素的光保护作用
Section titled “黄斑色素的光保护作用”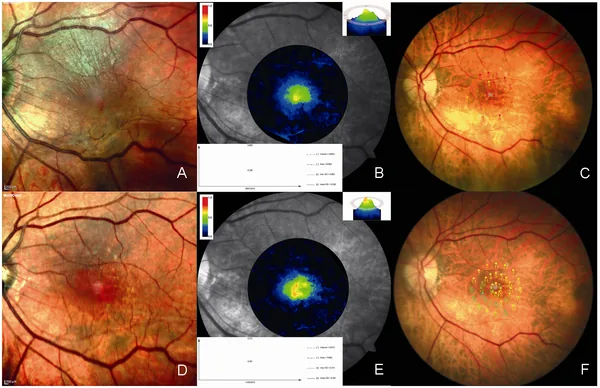
叶黄素和玉米黄质选择性积聚在黄斑,形成黄斑色素光密度(MPOD)3)。
- 光过滤功能:选择性吸收蓝光(400-500 nm),减少其到达光感受器
- 抗氧化功能:作为ROS清除剂,直接猝灭单线态氧和过氧自由基
- 内消旋玉米黄质:在视网膜内由叶黄素酶促转化而来的第三种黄斑色素,在黄斑中心凹浓度最高3)
锌作为抗氧化酶辅因子的作用
Section titled “锌作为抗氧化酶辅因子的作用”锌是抗氧化酶Cu/Zn-SOD(铜锌超氧化物歧化酶)活性位点必需的辅因子1)。SOD将一种ROS——超氧阴离子转化为无害的过氧化氢。它还与过氧化氢酶和谷胱甘肽过氧化物酶协同作用,维持整个抗氧化防御系统。RPE是一种高代谢组织,处理感光细胞脱落的吞噬体,充足的锌供应对维持其正常功能至关重要。
Omega-3脂肪酸的抗炎作用
Section titled “Omega-3脂肪酸的抗炎作用”DHA(二十二碳六烯酸)是视网膜光感受器外节膜中含量丰富的ω-3长链不饱和脂肪酸。它与EPA(二十碳五烯酸)一起,是抗炎脂质介质resolvin和protectin的前体7)。这些介质促进炎症消退,但RCT中对干眼的临床效果被认为不充分。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”AREDS2长期随访数据(2022年)
Section titled “AREDS2长期随访数据(2022年)”AREDS2的10年长期随访数据(报告28:Chew 2022)10)证实,叶黄素/玉米黄质组长期进一步降低了进展为渗出性AMD的风险。未发现长期安全性问题,并再次支持了吸烟者使用不含β-胡萝卜素配方的益处。
黄斑色素光密度(MPOD)作为生物标志物的应用
Section titled “黄斑色素光密度(MPOD)作为生物标志物的应用”MPOD测量作为黄斑内类胡萝卜素含量的指标正在研究中3)。异色闪烁光度法、共振拉曼光谱和眼底自发荧光等评估方法正在被探讨作为补充剂效果的客观指标。
基于基因多态性的个体化营养指导
Section titled “基于基因多态性的个体化营养指导”研究正在探索AREDS配方效果是否因AMD易感基因(CFH Y402H、ARMS2 A69S)的多态性而不同15)。有迹象表明,CFH多态性携带者对锌的反应性不同15),未来可能实现基于基因谱的个性化补充剂处方。
肠道菌群与类胡萝卜素吸收
Section titled “肠道菌群与类胡萝卜素吸收”积累的基础研究表明,肠道菌群的组成影响叶黄素和玉米黄质的吸收效率和血液浓度。已知即使饮食和补充剂摄入量相同,个体间血液叶黄素浓度也存在很大差异。正在探索通过改善肠道环境(如益生菌)来提高吸收效率。
干眼营养干预的持续研究
Section titled “干眼营养干预的持续研究”尽管DREAM试验否定了omega-3的效果7),但关于整体饮食模式(如地中海饮食)与干眼风险关联的研究正在进展中11)。多酚、维生素D等其他营养素对干眼的影响也在研究中,新的RCT正在进行。
8. 参考文献
Section titled “8. 参考文献”- Age-Related Eye Disease Study Research Group. A randomized, placebo-controlled, clinical trial of high-dose supplementation with vitamins C and E, beta carotene, and zinc for age-related macular degeneration and vision loss: AREDS report no. 8. Arch Ophthalmol. 2001;119(10):1417-1436.
- Age-Related Eye Disease Study 2 Research Group. Lutein + zeaxanthin and omega-3 fatty acids for age-related macular degeneration: the Age-Related Eye Disease Study 2 (AREDS2) randomized clinical trial. JAMA. 2013;309(19):2005-2015.
- Bernstein PS, Li B, Vachali PP, et al. Lutein, zeaxanthin, and meso-zeaxanthin: the basic and clinical science underlying carotenoid-based nutritional interventions against ocular disease. Prog Retin Eye Res. 2016;50:34-66.
- Perry A, Rasmussen H, Johnson EJ. Xanthophyll (lutein, zeaxanthin) content in fruits, vegetables and corn and egg products. J Food Compos Anal. 2009;22(1):9-15.
- Christen WG, Liu S, Glynn RJ, et al. Dietary carotenoids, vitamins C and E, and risk of cataract in women: a prospective study. Arch Ophthalmol. 2008;126(1):102-109.
- Mathew MC, Ervin AM, Tao J, et al. Antioxidant vitamin supplementation for preventing and slowing the progression of age-related cataract. Cochrane Database Syst Rev. 2012;(6):CD004567.
- Dry Eye Assessment and Management Study Research Group. n-3 Fatty acid supplementation for the treatment of dry eye disease. N Engl J Med. 2018;378(18):1681-1690.
- SanGiovanni JP, Chew EY, Clemons TE, et al. The relationship of dietary lipid intake and age-related macular degeneration in a case-control study: AREDS report no. 20. Arch Ophthalmol. 2007;125(5):671-679.
- Kalt W, Hanneken A, Milbury P, et al. Recent research on polyphenolics in vision and eye health. J Agric Food Chem. 2010;58(7):4001-4007.
- Chew EY, Clemons TE, Agrón E, et al. Long-term outcomes of adding lutein/zeaxanthin and ω-3 fatty acids to the AREDS supplements on age-related macular degeneration progression: AREDS2 report 28. JAMA Ophthalmol. 2022;140(7):692-698.
- Giannaccare G, Pellegrini M, Sebastiani S, et al. Efficacy of omega-3 fatty acid supplementation for treatment of dry eye disease: a meta-analysis of randomized clinical trials. Cornea. 2019;38(5):565-573.
- 消費者庁. 機能性表示食品制度の概要. 2015.
- Alpha-Tocopherol, Beta Carotene Cancer Prevention Study Group. The effect of vitamin E and beta carotene on the incidence of lung cancer and other cancers in male smokers. N Engl J Med. 1994;330(15):1029-1035.
- Schürks M, Glynn RJ, Rist PM, et al. Effects of vitamin E on stroke subtypes: meta-analysis of randomised controlled trials. BMJ. 2010;341:c5702.
- Seddon JM, Reynolds R, Yu Y, et al. Risk models for progression to advanced age-related macular degeneration using demographic, environmental, genetic, and ocular factors. Ophthalmology. 2011;118(11):2203-2211.
