ステロイド白内障(後囊下白内障)の所見
混濁パターン:視軸上の後囊直下に淡い点状混濁や空胞として発症する
進行様式:点状混濁が徐々に癒合し、境界明瞭で内部均一な皿状の後囊下混濁(PSC)となる
視機能障害の閾値:後囊下混濁の直径が2 mm以上になると視機能障害を生じ、手術が必要になることが多い
自覚症状:羞明(グレア)・霧視・視力低下が主体。PSCは瞳孔が縮小する明所で特に見えにくくなる特徴がある

ステロイド薬(糖質コルチコイド)の使用による眼の副作用として、後囊下白内障(posterior subcapsular cataract;PSC)と眼圧上昇(ステロイド緑内障)が代表的である。全身投与・点眼・吸入・外用薬いずれの投与経路でも生じうる。
後囊下白内障は薬物による水晶体混濁のなかで最も頻度が高い。いったん発症すると比較的短期間で高度の視力障害を生じる。
ステロイドによる眼圧上昇には個人差がある。正常眼に対してステロイド点眼を行った場合、約35%が中等度の眼圧上昇(6〜15 mmHg)を示し、約5%が高度の眼圧上昇(15 mmHg以上)を示す1)。開放隅角緑内障(POAG)患者ではhigh responder率が46〜92%と著しく高い1)。
吸入ステロイドによるPSCリスクについては、長期高用量使用でオッズ比(OR)1.3〜1.5の上昇が報告されている2)。経口ステロイドについても、長期使用で開放隅角緑内障のリスクが増加する3)。
全員が発症するわけではない。発症リスクは投与量・期間・個人の感受性により大きく異なる。眼圧上昇は約35%に中等度(6〜15 mmHg)、約5%に高度(15 mmHg以上)の上昇がみられる。後囊下白内障はプレドニゾロン換算10 mg/日以下では比較的まれであるが、大量投与を1年以上継続すると発症しやすくなる。長期使用が見込まれる場合は定期的な眼科受診が推奨される。

ステロイド薬による眼副作用は白内障と緑内障で異なる症状・所見を示す。
ステロイド白内障(後囊下白内障)の所見
混濁パターン:視軸上の後囊直下に淡い点状混濁や空胞として発症する
進行様式:点状混濁が徐々に癒合し、境界明瞭で内部均一な皿状の後囊下混濁(PSC)となる
視機能障害の閾値:後囊下混濁の直径が2 mm以上になると視機能障害を生じ、手術が必要になることが多い
自覚症状:羞明(グレア)・霧視・視力低下が主体。PSCは瞳孔が縮小する明所で特に見えにくくなる特徴がある
ステロイド緑内障の所見
眼圧上昇:通常21 mmHg以上に上昇する
眼圧上昇の持続:眼圧正常化までの期間は投与期間に比例する。トリアムシノロンによるものは9〜12か月間持続する
診断確定:ステロイドの中止により眼圧が正常化すれば診断が確定する
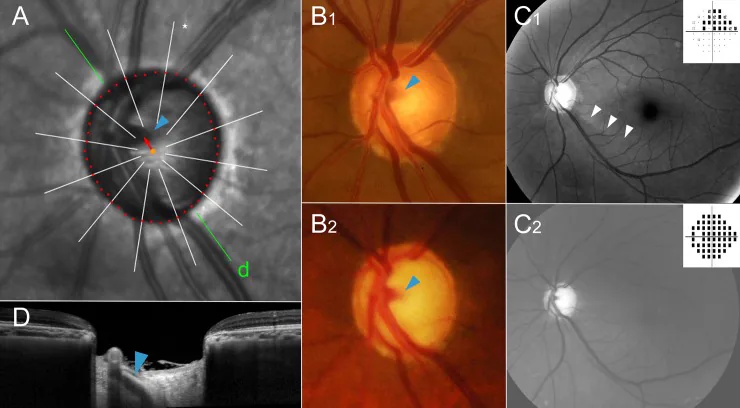
進行所見:眼圧上昇が持続すると緑内障性視野障害(弓状暗点・鼻側階段等)が生じる
後囊下の混濁により、明るい場所での羞明(まぶしさ)や霧視(かすみ)が生じやすい。PSCは視軸の後囊直下に生じるため、瞳孔が縮む昼間や明所で視力が低下しやすく、夜間より日中に見えにくいという特徴的な訴えがみられる。混濁の直径が2 mm以上になると、日常生活に支障を生じる程度の視機能障害が起こることが多い。
| 投与経路 | 主な薬剤・形態 | 眼副作用リスク |
|---|---|---|
| 全身投与(内服・静注) | プレドニゾロン等 | 最大。10 mg/日以上を1年以上で高リスク |
| 点眼・眼軟膏 | デキサメタゾン・フルオロメトロン等 | 眼圧上昇リスク高(薬剤力価に依存) |
| 結膜下・Tenon囊下注射 | トリアムシノロン等 | 眼局所での眼圧上昇 |
| 硝子体内注射 | トリアムシノロン・デキサメタゾンインプラント | 近年増加。眼圧上昇が約30%5) |
| 吸入 | 喘息治療薬 | 長期高用量でPSCリスク上昇(OR 1.3〜1.5)2) |
| 鼻スプレー・皮膚外用 | 各種ステロイド外用薬 | 稀だが長期使用で報告あり3) |
点眼での眼圧上昇作用は抗炎症作用に比例する。デキサメタゾン ≥ ベタメタゾン > フルオロメトロンの順に眼圧上昇作用が強く6)、用量依存性が認められる。
| 投与経路・薬剤 | 眼圧チェックのタイミング |
|---|---|
| ステロイド点眼(短期) | 開始後2〜4週4) |
| ステロイド点眼(長期) | 3か月ごと4) |
| トリアムシノロン硝子体内注射 | 1〜2週後、以後定期的に5) |
| デキサメタゾンインプラント | 1〜2週後、以後定期的に5) |
| 全身ステロイド長期投与 | 初回投与後1か月、以後3〜6か月ごと |
早ければ投与開始後1〜2週間で眼圧上昇を認めることがある。デキサメタゾンなどの強力なステロイドほど眼圧が上昇しやすく、定期的な眼圧チェックが必要である。投与開始後2〜4週での眼圧測定が推奨される。フルオロメトロンはデキサメタゾンやベタメタゾンと比較して眼圧上昇作用が弱く、眼圧上昇リスクの高い患者では代替薬として用いられる場合がある。
視軸上の後囊下に強い混濁が生じ、後囊下混濁の直径が2 mm以上になると視機能障害を生じ、手術が必要になることが多い。
第一段階:ステロイドの減量・中止
可能な限りステロイドの減量・中止を図る。原疾患(膠原病・腎移植等)の状況により困難なこともある。眼圧上昇リスクの低い代替薬(フルオロメトロン点眼等)への変更を検討する6)。
第二段階:眼圧降下薬による保存療法
視機能障害・眼圧レベルに応じて以下を適宜使用する:
トリアムシノロン残留の処置
硝子体内注射後に眼圧が持続上昇する場合は、硝子体内残留トリアムシノロンの除去(硝子体手術)、またはTenon囊下のトリアムシノロン塊の摘除が有効なこともある。
外科的治療
薬物コントロールが不良で視機能障害が進行しており、ステロイドの減量・中止による眼圧下降を待てない場合に手術を選択する。
ステロイドの中止により多くの場合眼圧は正常化する。ただしトリアムシノロン硝子体内注射後の眼圧上昇は9〜12か月持続することがある。長期間高眼圧が続いた場合、視神経・視野への障害は不可逆性となるため、早期対応が重要である。薬物治療で眼圧コントロールが不良な場合は線維柱帯切開術が有効であり、若年例では特に良好な成績が報告されている。
ステロイドは線維柱帯(房水の排出路)の細胞に直接作用し、複数の機序で房水流出抵抗を増大させる。
以上の機序は、原発開放隅角緑内障(POAG)のそれと類似しており、POAG患者がステロイドに対してhigh responderとなりやすい理由の一つと考えられている。
ステロイドによる水晶体障害は多因子性である。
小児でステロイド白内障が生じやすい理由は、成長期の水晶体上皮細胞がステロイドの作用を受けやすいためと考えられている。
Armaly MF. Statistical attributes of the steroid hypertensive response in the clinically normal eye. I. The demonstration of three levels of response. Invest Ophthalmol. 1965;4:187-197. PMID: 14283012.
Smeeth L, Boulis M, Hubbard R, et al. A population based case-control study of cataract and inhaled corticosteroids. Br J Ophthalmol. 2003;87(10):1247-1251.
Garbe E, LeLorier J, Boivin JF, et al. Risk of ocular hypertension or open-angle glaucoma in elderly patients on oral glucocorticoids. Lancet. 1997;350(9083):979-982.
Jones R 3rd, Rhee DJ. Corticosteroid-induced ocular hypertension and glaucoma: a brief review and update of the literature. Curr Opin Ophthalmol. 2006;17(2):163-167. doi:10.1097/01.icu.0000193079.55240.18.
Haller JA, Bandello F, Belfort R Jr, et al. Dexamethasone intravitreal implant in patients with macular edema related to branch or central retinal vein occlusion: twelve-month study results. Ophthalmology. 2011;118(12):2453-2460.
Cantrill HL, Palmberg PF, Zink HA, et al. Comparison of in vitro potency of corticosteroids with ability to raise intraocular pressure. Am J Ophthalmol. 1975;79(6):1012-1017.
Iwao K, Inatani M, Tanihara H. Success rates of trabeculotomy for steroid-induced glaucoma: a comparative, multicenter, retrospective cohort study. Am J Ophthalmol. 2011;151(6):1047-1056.
Clark AF, Wordinger RJ. The role of steroids in outflow resistance. Exp Eye Res. 2009;88(4):752-759.
Jobling AI, Augusteyn RC. What causes steroid cataracts? A review of steroid-induced posterior subcapsular cataracts. Clin Exp Optom. 2002;85(2):61-75.
Sundahl N, Bridelance J, Libert C, et al. Selective glucocorticoid receptor modulation: new directions with non-steroidal scaffolds. Pharmacol Ther. 2015;152:28-41.
Richter GM, Coleman AL. Minimally invasive glaucoma surgery: current status and future prospects. Clin Ophthalmol. 2016;10:189-206.
Jabs DA, Rosenbaum JT, Foster CS, et al. Guidelines for the use of immunosuppressive drugs in patients with ocular inflammatory disorders. Am J Ophthalmol. 2000;130(4):492-513.