Endogena
Via di infezione: Disseminazione ematogena da fungemia
Principali agenti patogeni: Candida albicans (più comune)
Frequenza: Più della metà di tutte le endoftalmiti endogene
Bilateralità: Presente in circa il 30% dei casi

L’endoftalmite fungina è una grave malattia oculare in cui i funghi infettano e proliferano nei fluidi intraoculari (umore vitreo e umore acqueo). A seconda della via di infezione, si classifica in due tipi: endogena (disseminazione ematogena) ed esogena (propagazione da chirurgia, trauma o cheratite).
Più della metà delle endoftalmiti endogene sono fungine e il 30% sono bilaterali. L’endoftalmite esogena è suddivisa in tre categorie: post-operatoria, post-traumatica e correlata a cheratite7). Rispetto all’endoftalmite batterica, la progressione è più lenta, con un peggioramento dei sintomi in giorni o settimane.
Endogena
Via di infezione: Disseminazione ematogena da fungemia
Principali agenti patogeni: Candida albicans (più comune)
Frequenza: Più della metà di tutte le endoftalmiti endogene
Bilateralità: Presente in circa il 30% dei casi
Esogena
Via di infezione: Propagazione da chirurgia, trauma o cheratite
Principali agenti patogeni: Genere Aspergillus (più comune)
Frequenza: Spesso unilaterale
Classificazione: Tre categorie: post-operatoria, post-traumatica e correlata a cheratite
I patogeni tipici sono le specie Candida e Aspergillus, ma sono in aumento anche le segnalazioni di specie rare. Sono state riportate Trichosporon (resistenza naturale agli echinocandine) 6), C. rugosa (meno dello 0,1% delle Candida non albicans) 3), Arthrographis kalrae 5) e Neoscytalidium dimidiatum 7).
Dopo la pandemia di COVID-19, sono stati segnalati consecutivamente casi di endoftalmite fungina innescata da immunosoppressione dovuta all’uso di steroidi 1, 9).
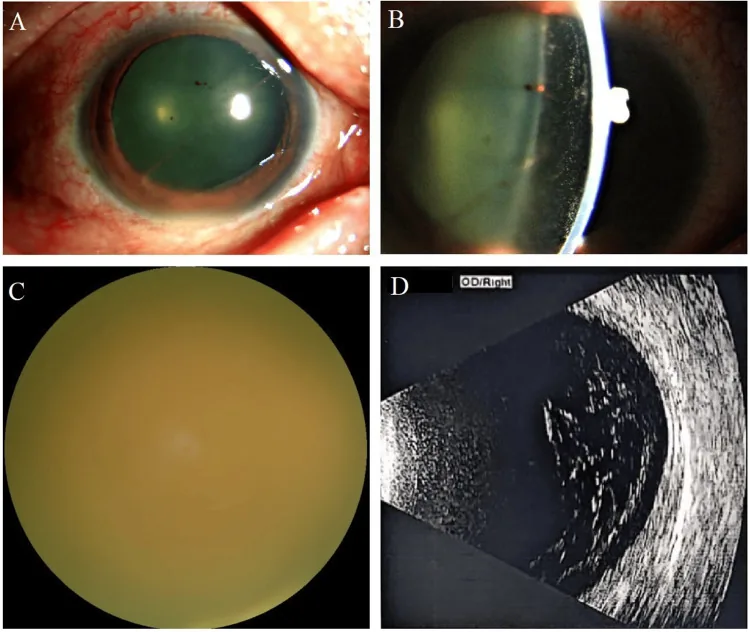
I sintomi iniziali comuni sono miodesopsie, visione offuscata e riduzione dell’acuità visiva. Nei casi avanzati possono comparire dolore oculare e arrossamento.
La velocità di progressione della malattia varia a seconda del patogeno.
Si osserva un infiltrato corioretinico giallo-biancastro cotonoso a bordi sfumati, prevalentemente al polo posteriore. Può essere associato a emorragie retiniche.
L’aspetto delle opacità vitreali è simile a quello delle uveiti non infettive come la sarcoidosi, e si riporta che fino al 50% dei casi precoci viene diagnosticato erroneamente2). Inoltre, ci sono casi in cui un’infezione fungina viene trascurata come vitreite ricorrente post-operatoria4). Per i dettagli, vedere la sezione «Diagnosi e metodi di esame».
I fattori di rischio differiscono tra forme endogene ed esogene. I principali fattori di rischio sono elencati di seguito.
| Classificazione | Principali fattori di rischio |
|---|---|
| Endogena | Nutrizione parenterale centrale, immunosoppressori, steroidi |
| Endogena | Trapianto d’organo, neutropenia, tumore maligno |
| Endogena | Diabete, lunga degenza in terapia intensiva |
| Esogena | Complicanze intraoperatorie, età avanzata, collirio steroideo |
| Esogeno | Ulcera corneale / uso improprio delle lenti a contatto |
In relazione al COVID-19, sono stati riportati casi di endoftalmite fungina indotta da immunosoppressione dovuta a ricovero prolungato e somministrazione di steroidi sistemici 1, 9). Altri fattori riportati includono chemioterapia per cancro al seno (leucopenia da docetaxel) 3), terapia immunosoppressiva (metotrexato + steroidi) 2), estensione di cheratite da scarsa igiene durante l’uso di lenti a contatto 5), colonizzazione fungina di IOL sotto forma di biofilm 6), infezione da funghi fitopatogeni a seguito di trauma vegetale 7) e scarso controllo del diabete 4, 8).
Sì. È stato riportato che gli steroidi sistemici usati nel trattamento del COVID-19 e i lunghi ricoveri in terapia intensiva causano immunosoppressione, che può scatenare endoftalmite fungina endogena 1, 9). In caso di alterazioni visive, è necessaria una tempestiva visita oculistica.
La coltura dei liquidi intraoculari è il gold standard. I campioni di vitreo hanno una maggiore resa diagnostica rispetto all’umore acqueo. Utilizzare agar Sabouraud e incubare sia a 37 °C che a temperatura ambiente per almeno due settimane.
Le emocolture sono positive solo in un terzo-metà dei casi endogeni; un risultato negativo non esclude l’endoftalmite.
Nella coltura di arricchimento, l’inoculazione del vitreo in flaconi per emocoltura ha mostrato una positività in media in 1,23 giorni 6).
Una volta identificato l’agente eziologico, è necessario eseguire un test di sensibilità agli antimicotici. Aspergillus terreus mostra un’alta resistenza (98%) all’amfotericina B (MIC 2 μg/mL)2). In un caso con sensibilità confermata di Trichosporon inkin al fluconazolo (MIC 2,0 μg/mL), la monoterapia con fluconazolo ha avuto successo6).
Sì. Anche nell’endoftalmite endogena, l’emocoltura è positiva solo in 1/3-1/2 dei casi. Anche il β-D-glucano può essere negativo3). La coltura diretta del liquido intraoculare o la PCR sono essenziali per una diagnosi definitiva.
Le caratteristiche dei principali antimicotici sono riportate di seguito.
| Farmaco | Via di somministrazione | Caratteristiche |
|---|---|---|
| Fluconazolo | EV o orale | Prima scelta per Candida |
| Voriconazolo | EV / orale | Efficace contro funghi filamentosi e Candida resistente |
| Amfotericina B | EV / intravitreale | Ampio spettro, penetrazione intraoculare limitata |
La durata del trattamento è solitamente di 4-6 settimane. Per Trichosporon inkin è stato riportato un caso di successo con fluconazolo per 16 settimane6).
Viene eseguita per la rimozione fisica della fonte infettiva (debulking), per facilitare la diffusione del farmaco e per il prelievo di campioni. È indicata nei seguenti casi:
Nei casi correlati a IOL, è importante la rimozione della IOL e del sacco capsulare contenente il biofilm5, 6).
Candida
Solo corioretinite : Azoli orali (fluconazolo, voriconazolo)
Con coinvolgimento vitreale : Aggiungere vitrectomia + iniezione intravitreale di antimicotico
Durata del trattamento : Generalmente 4-6 settimane
Aspergillus
Prima linea : Voriconazolo (A. terreus ha un tasso di resistenza all’amfotericina B del 98%)
Terapia locale : Vitrectomia + iniezione intravitreale di voriconazolo
Test di sensibilità : Obbligatorio (per confermare la resistenza)
Specie rare
Trichosporon: echinocandine inefficaci. Utilizzare dopo conferma della sensibilità al fluconazolo.
Altri: dopo identificazione con MALDI-TOF MS, scegliere in base ai test di sensibilità agli antimicotici.
In linea di principio, vanno evitati. Gli steroidi favoriscono la crescita fungina e rischiano di peggiorare rapidamente la condizione. È stato riportato un caso di endoftalmite da A. terreus che è peggiorata bruscamente dopo somministrazione di steroidi (desametasone intravitreale)2). È importante escludere un’infezione fungina prima di utilizzare colliri o iniezioni intravitreali di steroidi.
La progressione avviene per fasi: fungemia → colonizzazione della coroide e della retina → formazione di focolai infettivi → disseminazione nel vitreo → endoftalmite → panuveite → panoftalmite.
Koide et al. (2023) hanno riportato un caso di endoftalmite da C. rugosa e suggerito una via di ingresso nel corpo vitreo attraverso gli spazi di Virchow-Robin 3). C. rugosa è una specie rara (<0,1% dei Candida non albicans) ma può causare infezioni invasive in condizioni di immunosoppressione.
Kaderli Tamer et al. (2022) hanno riportato che, in un caso di endoftalmite insorta durante il trattamento per COVID-19, gli steroidi hanno potenziato la rottura della barriera emato-retinica, facilitando l’ingresso intraoculare del fungo 9).
Le specie di Trichosporon producono un antigene polisaccaridico capsulare (glucuronoxilomannano; GXM) che inibisce la fagocitosi da parte delle cellule fagocitarie, stabilendo così un’infezione invasiva 6). Questo meccanismo, insieme alla resistenza naturale agli echinocandine, è la causa principale della difficoltà di trattamento.
Come nuovo trattamento per l’endoftalmite fungina refrattaria, è stata riportata la tecnica di utilizzare povidone iodato allo 0,025% come liquido di irrigazione durante la vitrectomia.
Huang et al. (2024) hanno eseguito una vitrectomia con irrigazione di povidone iodato allo 0,025% in un caso di endoftalmite grave da Arthrographis kalrae 5). L’infezione, difficile da controllare con i farmaci antimicotici convenzionali, è stata domata da questo intervento. Il povidone iodato non possiede meccanismi di resistenza, risultando promettente per le infezioni fungine multiresistenti.
I breakpoint clinici (punti di taglio) per i farmaci antimicotici contro le specie di Trichosporon non sono ancora stati stabiliti 6). Attualmente, il trattamento è individualizzato in base ai risultati dei test di sensibilità ai farmaci di ciascuna struttura. Lo sviluppo di linee guida terapeutiche basate sull’evidenza rappresenta una sfida futura.