Endogen
Infektionsweg: Hämatogene Aussaat von einer Fungämie
Hauptverursacher: Candida albicans (am häufigsten)
Häufigkeit: Mehr als die Hälfte aller endogenen Endophthalmitiden
Beidseitigkeit: Bei etwa 30 % der Fälle

Die Pilzendophthalmitis ist eine schwere Augenerkrankung, bei der Pilze die intraokularen Flüssigkeiten (Glaskörper und Kammerwasser) infizieren und sich vermehren. Je nach Infektionsweg wird sie in zwei Typen eingeteilt: endogen (hämatogene Aussaat) und exogen (Ausbreitung von einer Operation, einem Trauma oder einer Keratitis).
Mehr als die Hälfte der endogenen Endophthalmitiden sind pilzbedingt, und 30 % sind beidseitig. Die exogene Endophthalmitis wird in drei Kategorien unterteilt: postoperativ, posttraumatisch und keratitisassoziiert7). Im Vergleich zur bakteriellen Endophthalmitis ist der Verlauf langsamer, mit einer Verschlechterung der Symptome über Tage bis Wochen.
Endogen
Infektionsweg: Hämatogene Aussaat von einer Fungämie
Hauptverursacher: Candida albicans (am häufigsten)
Häufigkeit: Mehr als die Hälfte aller endogenen Endophthalmitiden
Beidseitigkeit: Bei etwa 30 % der Fälle
Exogen
Infektionsweg: Ausbreitung von einer Operation, einem Trauma oder einer Keratitis
Hauptverursacher: Aspergillus-Arten (am häufigsten)
Häufigkeit: Oft einseitig
Klassifikation: Drei Kategorien: postoperativ, posttraumatisch und keratitisassoziiert
Die typischen Erreger sind Candida- und Aspergillus-Arten, aber auch Berichte über seltene Arten nehmen zu. Trichosporon (natürliche Resistenz gegen Echinocandine) 6), C. rugosa (weniger als 0,1 % der Non-albicans-Candida) 3), Arthrographis kalrae 5) und Neoscytalidium dimidiatum 7) wurden berichtet.
Nach der COVID-19-Pandemie wurden wiederholt Fälle von Pilz-Endophthalmitis berichtet, die durch eine Steroid-induzierte Immunsuppression ausgelöst wurden 1, 9).
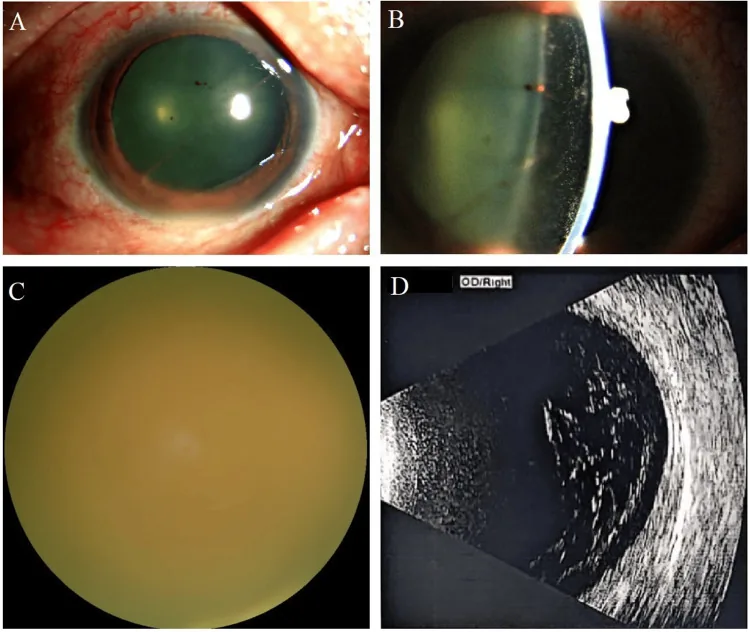
Häufige Anfangssymptome sind Mouches volantes, verschwommenes Sehen und Sehverschlechterung. In fortgeschrittenen Fällen können Augenschmerzen und Rötung auftreten.
Die Geschwindigkeit des Krankheitsverlaufs variiert je nach Erreger.
Es zeigt sich ein unscharf begrenztes, gelb-weißes, flockiges chorioretinales Infiltrat, hauptsächlich im hinteren Pol. Es kann mit Netzhautblutungen einhergehen.
Das Aussehen der Glaskörpertrübungen ähnelt dem einer nichtinfektiösen Uveitis wie Sarkoidose, und es wird berichtet, dass bis zu 50 % der frühen Fälle fehldiagnostiziert werden2). Zudem gibt es Fälle, in denen eine Pilzinfektion als postoperative rezidivierende Glaskörperentzündung übersehen wird4). Einzelheiten finden Sie im Abschnitt „Diagnose und Untersuchungsmethoden“.
Die Risikofaktoren unterscheiden sich zwischen endogenen und exogenen Formen. Die wichtigsten Risikofaktoren sind unten aufgeführt.
| Klassifikation | Hauptrisikofaktoren |
|---|---|
| Endogen | Zentrale Venenernährung, Immunsuppressiva, Steroide |
| Endogen | Organtransplantation, Neutropenie, bösartiger Tumor |
| Endogen | Diabetes, langer ICU-Aufenthalt |
| Exogen | Intraoperative Komplikationen, hohes Alter, Steroid-Augentropfen |
| Exogen | Hornhautgeschwür / unsachgemäße Verwendung von Kontaktlinsen |
Im Zusammenhang mit COVID-19 wurden Fälle von Pilz-Endophthalmitis berichtet, die durch Immunsuppression infolge langer Krankenhausaufenthalte und systemischer Steroidgabe ausgelöst wurden 1, 9). Weitere berichtete Faktoren sind Brustkrebs-Chemotherapie (Leukopenie durch Docetaxel) 3), Immunsuppression (Methotrexat + Steroide) 2), Ausbreitung einer Keratitis aufgrund schlechter Hygiene beim Tragen von Kontaktlinsen 5), Pilz-Biofilmbildung auf IOL 6), Infektion mit pflanzenpathogenen Pilzen durch Pflanzenverletzungen 7) und schlecht eingestellter Diabetes 4, 8).
Ja. Es wurde berichtet, dass systemische Steroide, die zur Behandlung von COVID-19 eingesetzt werden, und lange ICU-Aufenthalte zu Immunsuppression führen und eine endogene Pilz-Endophthalmitis auslösen können 1, 9). Bei Sehveränderungen ist eine sofortige augenärztliche Untersuchung erforderlich.
Die Kultur von Intraokularflüssigkeit ist der Goldstandard. Glaskörperproben haben eine höhere Diagnoserate als Kammerwasser. Verwenden Sie Sabouraud-Agar und inkubieren Sie sowohl bei 37 °C als auch bei Raumtemperatur für mindestens zwei Wochen.
Blutkulturen sind nur bei einem Drittel bis zur Hälfte der endogenen Fälle positiv; ein negatives Ergebnis schließt eine Endophthalmitis daher nicht aus.
Bei Anreicherungskultur wurde durch Inokulation von Glaskörperflüssigkeit in Blutkulturflaschen eine Positivität im Durchschnitt nach 1,23 Tagen berichtet 6).
Sobald der Erreger identifiziert ist, muss ein Antimykotika-Empfindlichkeitstest durchgeführt werden. Aspergillus terreus zeigt eine hohe Resistenzrate (98 %) gegen Amphotericin B (MHK 2 μg/mL)2). In einem Fall mit bestätigter Fluconazol-Empfindlichkeit von Trichosporon inkin (MHK 2,0 μg/mL) war eine alleinige Fluconazol-Therapie erfolgreich6).
Ja. Auch bei endogener Endophthalmitis ist die Blutkultur nur in 1/3 bis 1/2 der Fälle positiv. β-D-Glucan kann ebenfalls negativ sein3). Die direkte Kultur von Intraokularflüssigkeit oder PCR sind für die definitive Diagnose unerlässlich.
Die Eigenschaften der wichtigsten Antimykotika sind unten aufgeführt.
| Medikament | Verabreichungsweg | Eigenschaften |
|---|---|---|
| Fluconazol | i.v. oder oral | Mittel der ersten Wahl bei Candida |
| Voriconazol | i.v. / oral | Wirksam gegen Schimmelpilze und resistente Candida |
| Amphotericin B | i.v. / intravitreal | Breitspektrum, begrenzte intraokulare Penetration |
Die Behandlungsdauer beträgt in der Regel 4–6 Wochen. Bei Trichosporon inkin gibt es einen erfolgreichen Fall mit Fluconazol über 16 Wochen6).
Sie wird zur physikalischen Entfernung der Infektionsquelle (Debulking), zur Förderung der Medikamentenverteilung und zur Probenentnahme durchgeführt. Indiziert in folgenden Fällen:
Bei IOL-assoziierten Fällen ist die Entfernung der IOL und des Biofilm-haltigen Kapselsacks wichtig5, 6).
Candida
Nur Chorioretinitis : Orale Azole (Fluconazol, Voriconazol)
Mit Glaskörperbeteiligung : Zusätzlich Vitrektomie + intravitreale Antimykotika-Injektion
Behandlungsdauer : In der Regel 4–6 Wochen
Aspergillus
Erstlinientherapie : Voriconazol (A. terreus hat eine Amphotericin-B-Resistenzrate von 98%)
Lokale Therapie : Vitrektomie + intravitreale Voriconazol-Injektion
Empfindlichkeitstest : Obligatorisch (zur Bestätigung der Resistenz)
Seltene Erregerarten
Trichosporon: Echinocandine unwirksam. Nach Bestätigung der Fluconazol-Empfindlichkeit anwenden.
Sonstige: Nach Identifizierung mittels MALDI-TOF MS basierend auf Antimykotika-Empfindlichkeitstests auswählen.
Grundsätzlich sollten sie vermieden werden. Steroide fördern das Pilzwachstum und können den Zustand schnell verschlechtern. Es wurde ein Fall einer A. terreus-Endophthalmitis berichtet, die sich nach Gabe von Steroiden (intravitreales Dexamethason) rapide verschlechterte2). Vor der Anwendung von steroidhaltigen Augentropfen oder intravitrealen Injektionen ist es wichtig, eine Pilzinfektion auszuschließen.
Die fortschreitende Entwicklung verläuft stufenweise: Fungämie → Besiedlung der Aderhaut und Netzhaut → Bildung von Infektionsherden → Aussaat in den Glaskörper → Endophthalmitis → Panuveitis → Panophthalmitis.
Koide et al. (2023) berichteten über einen Fall von C. rugosa-Endophthalmitis und schlugen einen Eintrittsweg in den Glaskörper über die Virchow-Robin-Räume vor 3). C. rugosa ist eine seltene Spezies (<0,1 % der Non-albicans-Candida), kann aber bei Immunsuppression invasive Infektionen verursachen.
Kaderli Tamer et al. (2022) berichteten, dass bei einem Fall von Endophthalmitis während einer COVID-19-Behandlung Steroide die Zerstörung der Blut-Retina-Schranke verstärkten und das Eindringen des Pilzes in das Auge förderten 9).
Trichosporon-Arten produzieren ein Kapselpolysaccharid-Antigen (Glucuronoxylomannan; GXM), das die Phagozytose durch Fresszellen hemmt und so eine invasive Infektion etabliert 6). Dieser Mechanismus ist zusammen mit der natürlichen Resistenz gegen Echinocandine die Hauptursache für die schwierige Behandlung.
Als neuartige Behandlungsmethode für refraktäre Pilz-Endophthalmitis wurde die Verwendung von 0,025% Povidon-Iod als Spüllösung während der Vitrektomie berichtet.
Huang et al. (2024) führten bei einem Fall schwerer Endophthalmitis durch Arthrographis kalrae eine Vitrektomie mit 0,025% Povidon-Iod-Spülung durch 5). Die Infektion, die mit herkömmlichen Antimykotika schwer zu kontrollieren war, wurde durch diese Operation beherrscht. Povidon-Iod hat keinen Resistenzmechanismus und ist daher eine vielversprechende Option gegen multiresistente Pilze.
Die klinischen Breakpoints für Antimykotika gegen Trichosporon-Arten sind noch nicht etabliert 6). Derzeit erfolgt die Behandlung individuell basierend auf den Ergebnissen von Empfindlichkeitstests in den jeweiligen Einrichtungen. Die Entwicklung evidenzbasierter Behandlungsleitlinien ist eine zukünftige Herausforderung.