Léger
Position primaire du regard : pas de déviation verticale
En adduction : pas de déviation vers le bas (down shoot)
Élévation : limitée uniquement en adduction

Le syndrome de Brown est une forme de strabisme vertical caractérisée par une limitation ou une impossibilité d’élévation de l’œil en adduction, due à une anomalie du tendon du muscle oblique supérieur et de la trochlée. Il est également appelé syndrome de la gaine du tendon oblique supérieur. Il a été décrit pour la première fois en 1950 par le Dr Harold Whaley Brown 1).
La limitation de l’élévation en adduction est fondamentalement un problème mécanique : le tendon oblique supérieur ne peut pas glisser librement à travers la trochlée, ce qui rend le tendon rigide et inextensible.
Épidémiologie :
Génétique :
Des modes de transmission autosomique récessif ou autosomique dominant avec pénétrance réduite ont été rapportés1).
Les cas familiaux sont relativement rares, avec une incidence d’environ 1 pour 20 000 naissances. Des transmissions autosomique récessive ou autosomique dominante à pénétrance réduite ont été décrites1). La majorité des cas sont sporadiques.
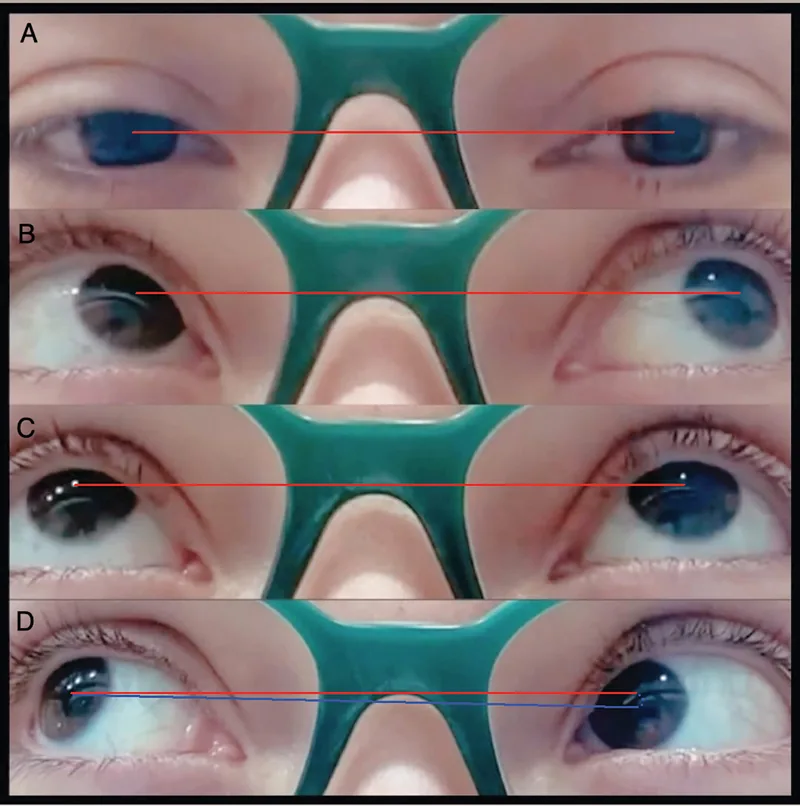
La limitation de l’élévation en adduction est le signe pathognomonique du syndrome de Brown.
Léger
Position primaire du regard : pas de déviation verticale
En adduction : pas de déviation vers le bas (down shoot)
Élévation : limitée uniquement en adduction
Modéré
Position primaire du regard : pas de déviation verticale
En adduction : déviation vers le bas (down shoot) présente
Élévation : limitation nette en adduction
Sévère
Position primaire du regard : hypotropie présente
En adduction : déviation vers le bas (down shoot) présente
Position anormale de la tête : inclinaison et rotation marquées de la tête
Les autres signes cliniques importants sont présentés ci-dessous1).
Le syndrome de Brown se divise en formes congénitale et acquise.
Voici une comparaison des causes.
| Classification | Causes principales |
|---|---|
| Congénital | Raccourcissement/perte d’élasticité du tendon, malformation de la trochlée, bande fibreuse |
| Acquis/inflammatoire | PR, arthrite juvénile idiopathique, LED, trochléite post-COVID-19 |
| Acquis/traumatique ou iatrogène | Fracture orbitaire, post-chirurgie, après cerclage scléral |
Congénital :
L’anomalie structurelle du complexe tendon-trochlée du muscle oblique supérieur est fondamentale 1). On observe un raccourcissement du tendon, une perte d’élasticité, une malformation de la trochlée, un nodule tendineux et une fibrose. Une explication récente propose la présence d’une bande fibreuse (fibrotic strand) prenant naissance dans la partie postérieure du tendon du muscle oblique supérieur jusqu’à la région trochléenne et ayant la même insertion 1). Une association avec les troubles congénitaux de l’innervation crânienne (CCDDs) a également été rapportée.
Un allongement de la distance ZT (distance entre l’anneau de Zinn et la trochlée) a été associé à l’apparition du syndrome de Brown. Chez 12 enfants normaux, la distance moyenne était de 37,1 ± 1 mm (35,8–38,7 mm), tandis qu’elle était allongée à 41,2 mm chez les patients atteints du syndrome de Brown 6).
Acquis :
Il a récemment été rapporté que la myasthénie grave oculaire peut se présenter avec des signes similaires au syndrome de Brown (anticorps anti-récepteur de l’acétylcholine positifs) 3), et doit être incluse dans le diagnostic différentiel.
Chez les adultes comme chez les enfants, l’apparition d’un syndrome de Brown dû à une trochléite après une infection à COVID-19 a été rapportée 5)8). L’IRM montre un gonflement de la gaine du tendon du muscle oblique supérieur et un rehaussement au gadolinium, et l’état s’améliore avec l’administration systémique de corticostéroïdes. Cela peut survenir même en l’absence de syndrome inflammatoire multisystémique.
Le diagnostic est un diagnostic clinique basé sur les antécédents et les signes cliniques1).
Principales méthodes d’examen :
Imagerie diagnostique :
Points clés du diagnostic différentiel :
| Maladie | FDT | Signes caractéristiques |
|---|---|---|
| Paralysie du muscle oblique inférieur | Négatif | Hyperaction du muscle oblique supérieur, strabisme en A |
| Paralysie du muscle élévateur double | Positif en adduction et abduction | Limitation de l’élévation dans toutes les directions |
| Fracture orbitaire | Positif en adduction et abduction | Antécédent de traumatisme / hypoesthésie sous-orbitaire |
| Myasthénie grave | Négatif (aspect restrictif) | Anticorps anti-AChR positifs3) |
L’interrogatoire sur les antécédents familiaux est également important, afin d’exclure un BS familial1).
Dans le syndrome de Brown congénital, la surveillance est le traitement de première intention. Une amélioration spontanée est observée chez 75 à 80 % des patients, et la règle est de ne pas se précipiter vers une intervention chirurgicale1).
Les corticostéroïdes sont efficaces dans le BS acquis inflammatoire.
La chirurgie est envisagée dans les cas suivants1) :
Allongement tendineux
Méthode de l’expandeur en silicone (méthode de Wright) : amélioration marquée dans 3 cas sur 4. Allongement du tendon SO de 10 mm.
Allongement par incision en Z : réalisé avec du fil Mersilene 5-0 dans un cas de BS bilatérale séquentielle. En cas de résultat insuffisant, conversion en ténectomie complète 6).
L’avantage est de réduire le risque de paralysie iatrogène du muscle oblique supérieur.
Ténectomie
Ténotomie/ténectomie du tendon SO : étude rétrospective de 38 cas, la plus efficace comme première intervention. Taux de disparition de l’AHP de 81,5 % 1).
Risque de paralysie iatrogène du muscle oblique supérieur par hypercorrection. Une surveillance postopératoire attentive est nécessaire.
Autres techniques chirurgicales
Allongement par division du tendon SO : amélioration significative de l’hypertropie et de la limitation de l’élévation dans 15 cas de BS sévère 1). Étude rétrospective de 20 cas : hypercorrection dans 2 cas (10 %).
Amincissement du tendon SO : efficace dans 21 yeux avec tendon SO épaissi 1).
Chirurgie de révision pour BS iatrogène : cas de libération du complexe SO par repositionnement du treillis en titane après ORIF de fracture orbitaire 4).
Dans les cas congénitaux, une amélioration spontanée est observée dans 75 à 80 % des cas, et la stratégie de base est une observation sans intervention chirurgicale urgente 1). Même dans les cas acquis idiopathiques, une rémission complète est rapportée dans 30 % des cas. Cependant, dans les cas graves (strabisme vers le bas en position primaire, position anormale marquée de la tête), une intervention chirurgicale est envisagée.
Une paralysie iatrogène du muscle oblique supérieur peut survenir après une ténotomie ou une résection du tendon du SO. L’allongement du tendon (méthode de l’expandeur en silicone, méthode de la Z-plastie) est considéré comme réduisant ce risque, et ces techniques sont de plus en plus privilégiées ces dernières années 1). Une surveillance attentive après la chirurgie est nécessaire.
Le dysfonctionnement du complexe tendon-trochlée du muscle oblique supérieur est le principal mécanisme du syndrome de Brown 1).
Contexte embryologique :
Les études de Sevel ont montré que le muscle oblique supérieur, le tendon et la trochlée se développent à partir d’un même tissu mésenchymateux 1). Cette observation explique l’évolution naturelle du BS congénital, qui s’améliore progressivement avec la croissance. Une association avec les troubles congénitaux de l’innervation crânienne (CCDDs) a également été suggérée, mais de nombreux cas ne présentent pas de limitation de l’abaissement en adduction, ce qui ne permet pas d’expliquer tous les cas 1).
Hypothèse de la bande fibreuse :
Une hypothèse récente propose l’existence d’une bande fibreuse (fibrotic strand) partant de la partie postérieure du tendon du SO jusqu’à la région trochléaire et ayant la même insertion que le tendon du SO 1). Les variations du site d’insertion pourraient expliquer non seulement la limitation typique de l’élévation en adduction, mais aussi des schémas atypiques de trouble de l’élévation.
Hypothèse de l’allongement de la distance ZT :
Il a été proposé que l’allongement de la distance ZT (distance entre l’anneau de Zinn et la trochlée) provoque un déplacement antérieur de la trochlée, augmentant la traction sur le tendon inversé du SO et entravant le télescopage 6). La distance ZT des patients (41,2 mm) était significativement plus longue que celle des enfants normaux (37,1 ± 1 mm).
Mécanismes liés au COVID-19 :
Les mécanismes possibles incluent l’invasion directe du virus dans les muscles squelettiques via le récepteur ACE2, ou une myotoxicité et une auto-immunité médiées par la libération de cytokines 5). L’apparition environ 3 semaines après l’infection est cohérente avec une réponse réactive.
Il a été récemment rapporté que la myasthénie grave oculaire peut présenter des signes similaires au BS 3). Un mécanisme par lequel le blocage des récepteurs AChR provoque des symptômes de type strabisme restrictif a été suggéré, et il est souligné la nécessité d’inclure la myasthénie grave dans le diagnostic différentiel chez les patients BS présentant un strabisme vertical.
Sur la base d’un rapport de BS intermittent et récurrent (cas d’un garçon de 5 ans ayant connu une rémission spontanée en un jour), deux nouvelles théories ont été proposées 7).
Shilo et al. (2022) ont proposé deux nouvelles théories : la “théorie de l’étirement” (l’étirement répété d’un tendon SO congénitalement court provoque un épaississement de la gaine tendineuse → ténosynovite sténosante) et la “théorie de l’évitement” (douleur aiguë → évitement des mouvements oculaires → réduction de l’étirement tendineux → rémission spontanée rapide) 7).
Concernant la relation entre la distance ZT et l’apparition du BS, des études prospectives supplémentaires sont attendues pour une validation plus poussée 6). Son utilisation comme indicateur prédictif de l’apparition du BS congénital est envisagée.