血管性病因
双侧PCA脑梗死:最常见病因。双侧大脑后动脉梗死导致枕叶广泛受损。
外伤或肿瘤后:可能在头部外伤、脑肿瘤或外科手术后发生。
心脏手术或脑血管造影:已知的医源性风险因素。
一氧化碳中毒或PRES:也可在中毒性或可逆性后部白质脑病综合征(PRES)中发生。顺铂等抗癌药物也是原因。

安东综合征(Anton Syndrome)是一种视觉病感缺失症(visual anosognosia),患者表现为皮质盲(cortical blindness),但自身并未意识到视力丧失,反而描述不存在的视觉体验。尽管患者是盲人,他们仍会进行虚构(confabulation),详细描述所见之物。
该病以奥地利神经学家加布里埃尔·安东(Gabriel Anton)的名字命名。安东报告了一例69岁患者,因双侧颞叶病变出现后天性病感缺失和耳聋。术语“anosognosia(病感缺失)”由约瑟夫·巴宾斯基(Joseph Babinski)创造,因此该病也被称为“安东-巴宾斯基综合征”。视觉病感缺失的最早描述可追溯到罗马时代的奴隶哈帕斯特(Harpaste),她否认自己失明,并抱怨房间太暗。
与夏尔·博内综合征的区别:需要注意,夏尔·博内综合征患者虽有视力障碍并出现幻视,但对自身视力障碍的洞察力得以保留,这与安东综合征有根本区别。
流行病学:中位年龄为55岁(范围6-96岁),无性别差异。最常见的原因是继发于脑血管意外(CVA),多见于有多种血管危险因素的老年人。大脑后动脉(PCA)卒中占所有卒中的5-10%。1) 1965年至2016年间,仅报告了28例安东-巴宾斯基综合征,极为罕见。2)
安东综合征是指皮质盲患者否认自己失明并进行虚构,缺乏自知力。而查尔斯·邦内综合征是视力障碍患者出现幻视,但仍保持对自身视力障碍的自知力。两者都以视觉障碍为背景,但在是否存在病感失认方面根本不同。
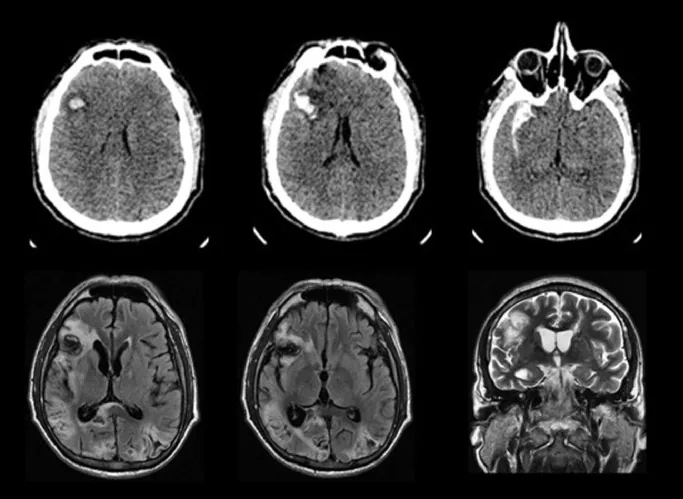
瞳孔对光反射的传入通路在外侧膝状体(LGB)之前就转向中脑顶盖前区,不经过枕叶(初级视皮层)。因此,即使枕叶受损,对光反射仍然保留。结合眼底检查正常,这是皮质盲的特征性表现。
安东综合征的主要病因和相关危险因素如下所示。
血管性病因
双侧PCA脑梗死:最常见病因。双侧大脑后动脉梗死导致枕叶广泛受损。
外伤或肿瘤后:可能在头部外伤、脑肿瘤或外科手术后发生。
心脏手术或脑血管造影:已知的医源性风险因素。
一氧化碳中毒或PRES:也可在中毒性或可逆性后部白质脑病综合征(PRES)中发生。顺铂等抗癌药物也是原因。
非血管性原因
MELAS:线粒体脑肌病。已报道在mt.3243A>G突变病例中发病。2)
MS加重、妊娠高血压脑病、产科出血:继发于多种全身性疾病。
感染性疾病:西尼罗病毒(WNV)脑炎、HIV相关PML等。3)
其他:肾上腺脑白质营养不良、中枢神经系统血管炎、蛛网膜下腔出血相关的缺血、Trousseau综合征中的双侧视放射病变等。
大脑后动脉(PCA)的解剖学特征:从基底动脉分支,近端(P1P2)供应深部结构(丘脑后部和中脑),远端(P3P4)供应枕叶皮质。P4段的损伤是视野缺损的主要原因。1) 枕叶皮质远离中心血管系统,结构上易受缺血影响。
临床诊断结合以下四点:虚构病史、视力丧失的临床证据、正常眼底检查结果以及枕叶损伤的影像学确认。
以下列出需要鉴别的疾病及鉴别要点。
| 疾病 | 鉴别要点 |
|---|---|
| 夏尔·博内综合征 | 存在幻视,洞察力保持(无病感失认) |
| 痴呆 | 认知性病感缺失及记忆障碍导致的虚构 |
| 韦尼克-科尔萨科夫综合征 | 硫胺素缺乏;即时记忆保留 |
| 诈病 | VEP证明中心视觉功能正常 |
| 心因性视觉障碍 | 眼球及对光反射无异常(与皮质盲相同),需要精神科评估 |
与心因性视觉障碍的鉴别尤为重要。双侧枕叶损伤导致的皮质盲在眼球上无异常发现,对光反射也保留,因此容易被误认为精神疾病或诈病。
安东综合征的治疗根据枕叶损伤的推定原因进行选择。病因治疗是基础。
抗血小板药物
阿司匹林:75~150毫克/日(A级)
氯吡格雷:75毫克/日(A级)
西洛他唑:200毫克/日(B级)
噻氯匹定:200毫克/日(B级)
其他预防性治疗
抗凝药:华法林等。适用于心源性栓塞(如心房颤动)引起的病例。
他汀类治疗:管理血脂异常和预防卒中复发。
危险因素管理:控制高血压、高血糖、血脂异常,戒烟。
对于脑卒中引起的病例,在发病4.5小时内可适用tPA(溶栓治疗)。1) 超过此时间,预防复发和康复成为治疗重点。时间越充裕,可挽救的神经细胞范围越大,因此出现症状时应立即急诊就医。
双侧广泛的枕叶(初级视觉皮层V1)损伤导致双侧同向偏盲,最终发展为皮质盲。枕叶皮质远离中心血管系统,结构上易受缺血影响。大脑后动脉远端(P3~P4)的梗死会阻断枕叶的血流。1)
视觉信息处理涉及腹侧通路(“what”通路:V4区,形态和颜色识别)和背侧通路(“where”通路:V5区,空间位置和运动识别)。部分皮层下纤维绕过V1直接连接V4和V5,因此即使V1广泛受损,这些通路仍可能发挥作用,从而保留色觉和运动感知。1) 这是Riddoch现象(能看到移动物体)的神经学基础。
关于盲视(blindsight)的机制,使用猕猴的研究报告了从LGBd到V2、V3、V4、V5/MT区、FST和LIP的直接投射通路,这可能解释无意识的视觉反应。
关于病感失认的机制存在多种假说。
| 假说 | 内容 | 依据 |
|---|---|---|
| 视觉皮层和联合皮层同时损伤 | 初级视觉皮层和视觉联合皮层同时受损,导致对自身状态缺乏洞察 | 枕叶广泛病变的临床表现 |
| 离断综合征 | 顶叶白质病变使视觉皮层与其他区域断开 | 伴有白质病变的病例中发病 |
| 与语言中枢的连接异常 | 受损的视觉皮层与功能正常的语言区域之间的连接中断,导致语言区域在没有视觉输入的情况下产生虚构回答。 | 虚构内容包含视觉细节。 |
目前,“与语言中枢的连接异常”假说最受支持。认为受损的视觉皮层向语言区域的反馈中断,导致语言区域产生“看见”的虚假报告。
最受支持的假说是“与语言中枢的连接异常”理论。枕叶损伤导致视觉皮层到语言区域的反馈回路中断,语言区域在没有视觉输入的情况下产生“看见”的虚构回答。这不是故意撒谎,而是脑回路损伤引起的神经学现象。
MELAS的机制:异常线粒体在小动脉内皮细胞和平滑肌细胞中积聚,导致毛细血管增生。癫痫发作引起神经血管单位快速能量耗竭,导致类似Todd麻痹的病理状态。Fryer假说提出癫痫发作是卒中样发作的触发因素。2)
WNV脑炎中血脑屏障(BBB)通过的机制:假设有三种途径:被动细胞运输、轴突运输和炎症诱导的BBB破坏。3)
Ziaul等人(2024)的病例报告指出,COVID-19患者缺血性卒中风险增加3.6倍,即使轻症COVID-19患者卒中风险也上升至约1%。1) 高炎症反应、高凝状态和医学严重程度被认为是血栓栓塞的易感因素。包括PCA在内的后循环卒中在疫情期间也存在延迟就诊的问题。
Ewida等人(2021)报告了一例MELAS合并安东-巴宾斯基综合征的病例,其MRI表现为DWI高信号且ADC等信号(与缺血性改变不一致)。2) 该表现不同于缺血性卒中的DWI改变(伴有ADC降低),被解释为癫痫发作导致的可逆性能量代谢障碍和血流动力学变化的组合。DWI表现的鉴别对MELAS治疗决策具有重要提示意义。
Srichawla(2022)报告称,干扰素α和含有WNV抗体的纯化免疫球蛋白制剂可能成为神经侵袭型WNV感染的未来治疗候选药物。3) 目前,对包括甲泼尼龙在内的现有药物反应不佳,尚无确定的治疗方法。超过80%的WNV感染无症状,但不到5%会进展为神经侵袭型,因此迫切需要建立治疗方法。